山羊胰腺腺泡细胞体外分离、纯化、培养和鉴定
2022-10-12张天西燕爱飞贺志雄谭支良
张天西 燕爱飞 杨 超 程 艳 贺志雄* 谭支良
(1.中国科学院亚热带农业生态研究所,亚热带农业生态过程重点实验室,畜禽养殖污染控制与资源化技术国家工程实验室,湖南省畜禽健康养殖工程技术研究中心,中国科学院亚热带农业生态研究所公共技术中心,长沙410125;2.中国科学院大学,北京100049)
反刍动物小肠内过瘤胃营养物质的消化受到胰腺外分泌功能的限制[1]。胰腺淀粉酶分泌不足可导致40%的过瘤胃淀粉消化不完全[2],表现出胰腺外分泌功能不足。开展胰腺腺泡细胞分离培养工作对于进一步从细胞分泌、配体结合、底物摄取、蛋白质合成或第二代信使等角度解析反刍动物胰腺外分泌功能不足机制,并建立可能的营养调控策略具有重要意义。
在细胞水平上对胰腺外分泌功能的探索始于20世纪70年代[3]。并已逐步建立了各类动物的胰腺腺泡细胞分离方法,包括人、猪、牛和鼠类等[4-7]。然而,目前尚未见山羊胰腺腺泡细胞的原代细胞分离和培养方法相关报道。且在已有的培养方法中,消化各动物胰腺腺泡细胞所使用的消化酶和消化时间各有不同,鉴定工作也鲜有报道。
胶原酶是在细胞解离工作中被广泛应用的消化酶,本试验主要评估不同浓度胶原酶Ⅳ和消化时间对山羊胰腺腺泡细胞的解离效果,优化山羊胰腺腺泡细胞原代培养方法,以期快速分离出足量且活性良好的胰腺腺泡细胞并稳定培养,为反刍动物胰腺外分泌功能的进一步研究奠定基础。
1 材料与方法
1.1 主要仪器及试剂
主要仪器包括:超净工作台(SW-CJ-2FD,苏州净化设备有限公司)、恒温摇床(KYC-100C,上海新苗医疗器械制造有限公司)、二氧化碳(CO2)培养箱(3111,Thermo Fisher公司,美国)、全自动细胞计数仪(Countess®Ⅱ FL,Thermo Fisher公司,美国)、倒置荧光显微镜(DMI3000B,Leica公司,德国)、激光扫描共聚焦显微镜(LSM880,Zesiss公司,德国)、共聚焦培养皿(BS-15-GJM,北京兰杰柯科技有限公司)等。
主要试剂包括:DMEM/F12培养基、胎牛血清(FBS)、无钙镁磷酸缓冲液(DPBS)、磷酸缓冲液(PBS)、0.25%胰蛋白酶消化液,均购自美国Gibco公司;胶原酶Ⅳ、重组人胰岛素、表皮生长因子(EGF),均购自德国Biofroxx公司;青链霉素混合液、庆大霉素、两性霉素b、均购自北京索莱宝科技有限公司;乙二醇双(2-氨基乙基醚)四乙酸(EGTA),购自北京凯诗源生物科技有限公司;兔抗羧肽酶A1(CPA1)(一抗),购自美国Proteintech公司;异硫氰酸荧光素(FITC)标记山羊抗兔免疫球蛋白G(IgG)(二抗),购自上海翊圣生物科技有限公司;通用固定液,购自武汉赛维尔生物科技有限公司;牛血清蛋白(BSA),购自北京伊塔生物科技有限公司;TritonX-100,购自美国Sigma公司;抗荧光淬灭剂[含染核试剂4’,6-二脒基-2-苯基吲哚(DAPI)],购自江苏碧云天生物研究所。
具体试剂配制如下:1)清洗液配制。向PBS(500 mL)中加入100×青链霉素混合液,使青链霉素混合液稀释成10×,文中称10×清洗液,将配制好的清洗液分装成实验室外用和内用2部分,外用部分用于屠宰取样时清洗胰腺组织,内用部分用于消化解离时对胰腺组织反复清洗。试验前配制,用前先预冷。2)转移液配制。向DMEM/F12培养基(50 mL)中加入100×青链霉素混合液,使青链霉素混合液稀释成10×,文中称10×转移液。取样完成后将胰腺组织置于转移液中运送至细胞培养室,转移液起保护作用。试验前配制,使用时全程置于冰上。3)培养基配制。用DMEM/F12培养基(500 mL)配制,在试验过程中需用青链霉素混合液浓度不同的2种培养基,原代培养需将青链霉素混合液稀释成10×,传代培养稀释成2×。此外还包含10%的FBS、10 μg/mL胰岛素、10 ng/mL EGF、2.5 μg/mL庆大霉素、2.5 μg/mL两性霉素b。试验前配制。4)消化液配制。运用DMEM/F12培养基将胶原酶Ⅳ配制成1.0和0.5 mg/mL 2个浓度的消化液,且都添加终浓度为0.001 mol/mL的EGTA。试验前配制,使用前37 ℃预热。5)抗体稀释。根据说明书用2%的BSA稀释。
1.2 试验动物
本研究的试验过程根据中国科学院亚热带农业生态研究所动物伦理委员会的指导进行。选取3月龄且健康状况良好的雌性湘东黑山羊进行屠宰,屠宰前禁食4 h以上。放血完毕后及时解剖暴露胰腺,在用预冷的10×清洗液不断冲洗的同时,迅速采取胰腺组织。适当剔除血管及筋膜,反复用10×清洗液清洗4~5遍后放入预先配制的10×转移液中,置于冰上及时带回实验室。
1.3 试验方法
1.3.1 消化酶的消化效率
在正式进行山羊胰腺腺泡细胞分离培养前,先探索适宜的消化时间、消化酶浓度及消化酶种类,以寻求更高的消化效率。运用1.0 mg/mL胶原酶Ⅳ作为山羊胰腺腺泡细胞消化解离的消化液,寻找在山羊胰腺组织上适宜的消化时间,设置15、20、25、30和35 min连续5个消化时间梯度;在得到适宜的消化时间后,进行1.0和0.5 mg/mL 2个浓度胶原酶Ⅳ消化液消化解离20 min后的比较;在验证过胶原酶Ⅳ的适宜浓度及消化时间后,用0.25%胰蛋白酶作为消化液来对比1.0 mg/mL的胶原酶Ⅳ。消化解离结束后进行总细胞计数及细胞活率检测。
具体操作步骤如下:1)预先用DMEM/F12配制50 mL浓度为1.0 mg/mL的胶原酶Ⅳ,配制10 mL浓度为0.5 mg/mL胶原酶Ⅳ及准备10 mL 0.25%胰蛋白酶。为得到更多的单细胞及减少细胞碎片,在3种消化液中添加EGTA,终浓度稀释至0.001 mol/mL。2)将取回的胰腺组织带回无菌细胞培养室,将胰腺组织从转移液中出。由于胰腺组织样品量有限,将采集的胰腺组织切分成1 g重量小块。3)将切分称重完的胰腺组织块置于超净工作台上。在10 cm培养皿中加适量10×清洗液,将组织块浸泡于其中,仔细剔除胰腺组织上多余的筋膜及脂肪组织。之后用清洗液重复清洗2~3遍,洗完后将每份胰腺组织剪切成1~3 mm3的小块,转移到15 mL离心管中再用清洗液清洗3~5遍。1 000 r/min离心2 min,去除多余液体。4)取5份清洗完的并剪碎的组织块各添加10 mL 1.0 mg/mL胶原酶Ⅳ消化液,用锡箔纸包裹离心管避光置于37 ℃、80 r/min的恒温摇床上消化。设置15、20、25、30和35 min消化时间梯度。5)每个消化时间节点结束后迅速加入5 mL含10% FBS的DMEM/F12终止消化,反复吹打之后1 000 r/min离心5 min弃上清。6)再添加5 mL含FBS的DMEM/F12混匀沉淀,用70 μm的细胞筛过滤收集细胞悬液,取每个离心管收集到的少量悬液在显微镜下观察消化状态,每个离心管取3个平行样用全自动细胞计数仪进行细胞活率检测和细胞计数。7)再取2份清洗完且剪碎的组织块置于15 mL无菌无酶离心管中,分别加入10 mL浓度为0.5 mg/mL胶原酶Ⅳ和10 mL 0.25%胰蛋白酶。用锡箔纸包裹避光置于37 ℃、80 r/min的恒温摇床上消化20 min。之后重复步骤5)和6)。
1.3.2 原代山羊胰腺腺泡细胞分离
具体操作步骤如下:1)将采集的胰腺组织块通过转移液运回细胞培养实验室。在无菌超净工作台上将胰腺组织取出,置于盛有清洗液的10 cm无菌培养皿中仔细剔除胰腺组织上多余的筋膜及脂肪组织。2)再用DPBS清洗3~5遍后将胰腺组织剪切成1~3 mm3的小块,使其能够被移液枪吸取。将剪好的胰腺组织块转移到15 mL无菌无酶离心管中,用含10×青链霉素的PBS反复冲洗5~6遍,最后1 000 r/min离心5 min弃上清。3)添加上述试验验证出的胶原酶Ⅳ 10 mL,用锡箔纸裹上离心管避光置于37 ℃、80 r/min的恒温摇床上消化20 min。4)消化结束后迅速加入5 mL含10% FBS的DMEM/F12终止消化,之后1 000 r/min离心5 min弃上清。5)添加5 mL含10% FBS、10×青链霉素混合液、2.5 μg/mL庆大霉素、2.5 μg/mL两性霉素、10 μg/mL胰岛素、10 ng/mL EGF的DMEM/F12混匀沉淀,用70 μm的细胞筛过滤收集细胞悬液。6)600×g、5 min离心,去上清,重悬接种到培养皿,调整接种密度为3×105个细胞/cm2,置于37 ℃、5% CO2饱和湿度的细胞培养箱中培养。1 d后观察贴壁及污染情况,若无问题则更换培养基继续培养。此后每天换1次液,整个过程中尽量避免剧烈晃动。
1.3.3 胰腺腺泡细胞的纯化及传代培养
在原代胰腺腺泡细胞传第1代时进行细胞纯化工作。采取差时消化、差速贴壁及细胞刮取等方法来对胰腺腺泡细胞进行纯化。
差时消化:利用细胞之间对消化酶的敏感性存在差异以及胰腺腺泡细胞的自身特性对胰腺腺泡细胞进行纯化。具体操作步骤如下:1)去除培养基后,静置2 min,用加2 mL PBS轻轻冲洗,会有一定量的细胞脱落。2)迅速收集脱落的细胞到15 mL无菌无酶离心管中,加2 mL含10% FBS的DMEM/F12,轻轻吹打后1 000 r/min离心5 min弃上清,用1 mL培养基重悬细胞后接种。3)向步骤1)培养皿清洗过的细胞中加入1.5 mL 0.25%胰蛋白酶消化液,摇晃铺平后静置2 min,不用放进培养箱。加3 mL含10% FBS的DMEM/F12终止消化,轻轻冲洗,将脱落的细胞收集到无菌离心管中轻轻吹打几下,1 000 r/min离心5 min弃上清,用1 mL培养基重悬细胞后接种。4)向未脱落的细胞中加1.5 mL 0.25%胰蛋白酶消化液,置于37 ℃、5% CO2饱和湿度的细胞培养箱中3 min;当细胞完全消化脱落时加3 mL含10% FBS的DMEM/F12终止消化。1 000 r/min离心5 min弃上清,用1 mL培养基重悬细胞后接种。
差速贴壁:根据各细胞间贴壁的时间存在差异来纯化得到胰腺腺泡细胞。具体操作步骤如下:1)结合上述差时消化接种的细胞,在接种后不同时间段观察贴壁情况。2)若在各时间点观察到有一定数量的贴壁细胞,则将悬液转移到新的培养皿继续贴壁,原培养皿加新的培养基继续培养。
细胞刮取:经过差时消化和差速贴壁处理后,会有形态比较均一的细胞成片生长。将形态均一、成簇生长的细胞用细胞刮子刮落,转移到新的培养皿继续培养。或者将除形态均一、成簇生长以外的细胞刮去,冲洗过后继续培养。
经过以上处理得到形态均一、纯度较高的胰腺腺泡细胞后进行传代培养,传代培养用含10% FBS、2×青链霉素混合液、2.5 μg/mL庆大霉素,2.5 μg/mL两性霉素、10 μg/mL胰岛素、10 ng/mL EGF的DMEM/F12培养基进行传代培养。同时进行胰腺腺泡细胞鉴定工作。
1.3.4 胰腺腺泡细胞的鉴定
利用免疫荧光技术对所培养的胰腺腺泡细进行鉴定。具体操作步骤如下:1)将纯化后的胰腺腺泡细胞接种到共聚焦小皿置于37 ℃、5% CO2饱和湿度细胞培养箱中培养。2)当细胞贴壁生长至70%以上时弃培养基,用1~2 mL PBS浸洗3次,每次3 min。3)添加1~2 mL常温的4%多聚甲醛后将培养皿置于4 ℃固定细胞30 min,固定结束后吸出多聚甲醛,缓慢加入PBS浸洗3次,每次5 min。4)配制0.2% TritonX-100(PBS配制)加1 mL至培养皿,室温下通透20 min。吸出0.2% TritonX-100,再用PBS浸洗3次,每次5 min。5)加入1 mL 2% FBS,室温下封闭1 h。封闭结束后吸出封闭液,切勿再次浸洗,向培养皿加入足量的一抗(CPA1稀释比例根据说明书,用2% BSA稀释),置于4 ℃过夜。6)次日取出培养皿,每孔加入1~2 mL PBS,浸洗3次,每次5 min,吸出PBS,加入足量的荧光二抗(FITC标记山羊抗兔IgG稀释比例根据说明书,用2% BSA稀释),室温下孵育1 h。7)加入2 mL PBS,浸洗3次,每次5 min,吸出PBS,加入抗荧光淬灭剂,共聚焦显微镜下观察拍照。
1.4 数据统计
细胞计数及细胞活率检测数据经Excel 2016进行初步整理后,采用SPSS 25.0软件的独立样本t检验进行统计学分析。试验结果以平均值和均值标准误表示。
2 结 果
2.1 消化酶消化效率对比
图1-a显示出各消化时间显微镜下观察得到的消化状态,发现细胞团的数量并不多,存在更多数量的单个细胞。随消化时间的增长,解离得到的细胞密度逐渐增加,但组织碎片也随之增多。图1-b显示随消化时间的逐步延长,消化得到的总细胞数从1.407×106个/mL逐步增长到5.262×106个/mL。图1-c显示细胞活率在消化20 min时达到91%,消化20 min后细胞活率逐渐降低,消化时间为35 min时细胞活率低至74%,为5个消化时间节点最低值。
图2显示了1.0和0.5 mg/mL 2个浓度胶原酶Ⅳ消化胰腺组织20 min后的比较结果。显微镜下观察消化状态见图2-a,结果显示0.5 mg/mL的胶原酶Ⅳ存在着比单个细胞数量还多的细胞碎片,且单个细胞数量也明显没有1.0 mg/mL的胶原酶Ⅳ充足。图2-b显示0.5 mg/mL的胶原酶Ⅳ消化得到的总细胞数为8.032×105个/mL,远低于1.0 mg/mL的胶原酶Ⅳ消化得到的总细胞数(2.275×106个/mL)。同时图2-c显示0.5 mg/mL胶原酶Ⅳ消化的细胞活率(83%)也低于1.0 mg/mL胶原酶Ⅳ消化的细胞活率(91%)。
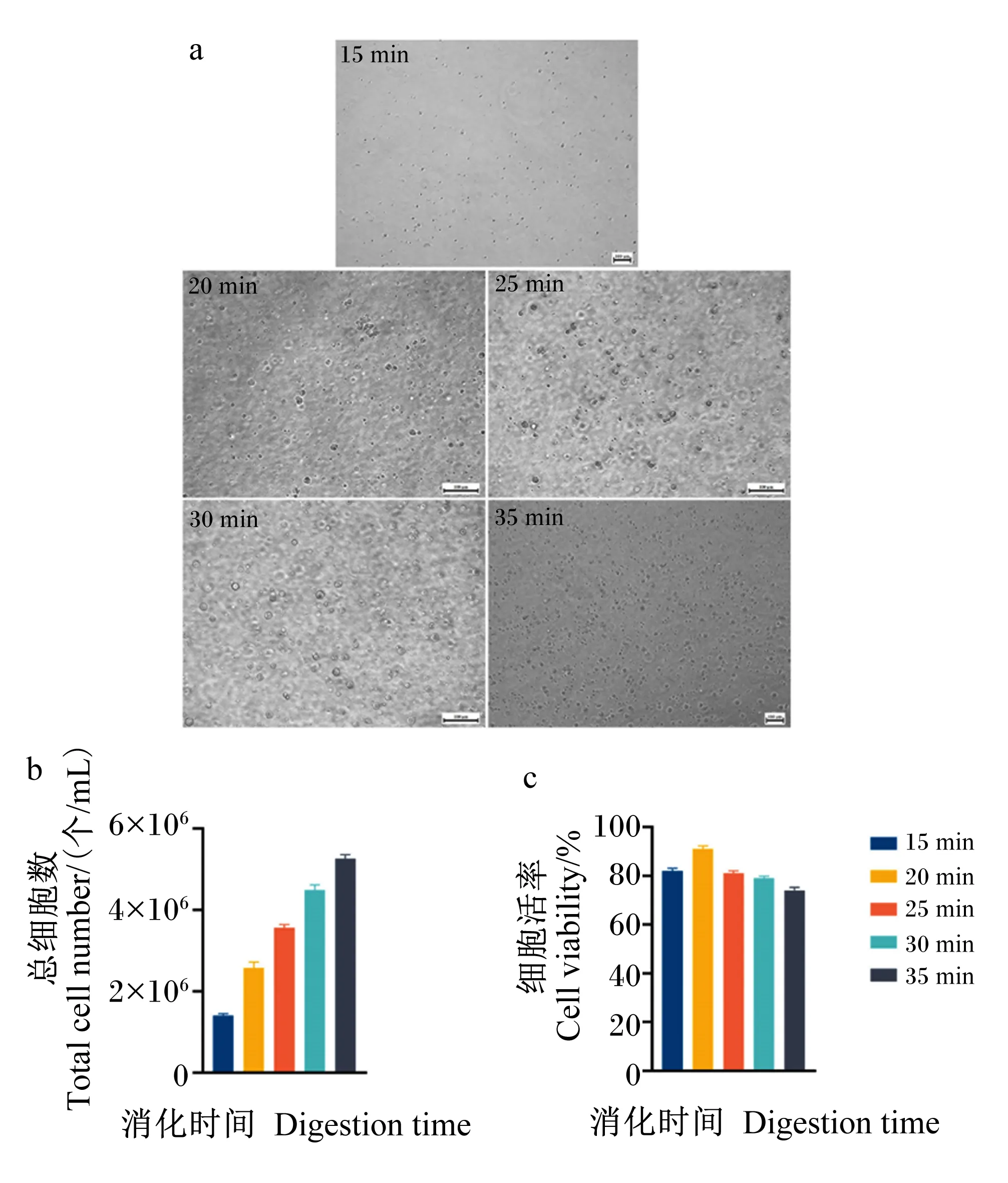
a:消化状态(100×);b:总细胞数;c:细胞活率。
图3-a显示胰蛋白酶虽有较少的细胞碎片,但消化得到的总细胞数及细胞活率均低于胶原酶Ⅳ。图3-b显示0.25%胰蛋白酶解离胰腺组织20 min得到的总细胞数低于1.0 mg/mL胶原酶Ⅳ消化得到的总细胞数。图3-c显示胰蛋白酶消化得到的细胞活率仅为80%,低于胶原酶Ⅳ消化得到的细胞活率(91%)。
2.2 山羊胰腺腺泡细胞的纯化及传代培养
在前述优化的消化酶浓度和消化时间基础上,我们进一步开展山羊胰腺腺泡细胞的纯化和传代培养。在1.0 mg/mL的胶原酶Ⅳ消化20 min后,用70 μm的细胞筛过滤收集细胞悬液,600 r/min多次离心后调整细胞悬液为3×105个细胞/cm2进行接种。接种后在显微镜下观察,图4-a显示细胞形态不均一,以成团成簇生长的细胞为主,杂细胞较多。因此我们开展了细胞纯化工作。

a:消化状态(100×);b:总细胞数;c:细胞活率。
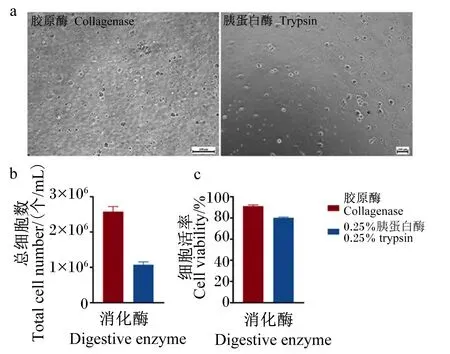
a:消化状态(100×);b:总细胞数;c:细胞活率。
pancreatic acinar cells
当原代细胞贴壁达90%以上后,我们通过差时消化、差速贴壁及细胞刮取等方法将原代细胞纯化后在进行传代培养。图4-b显示在纯化后,各时间节点的细胞形态明显更加均一,主要为成簇生长呈“鹅卵石”状的细胞。图4-c显示传代培养至第5代依然保持形态。

a:纯化前各时间点山羊胰腺腺泡细胞;b:纯化后各时间点山羊胰腺腺泡细胞;c:纯化后第5代山羊胰腺腺泡细胞。
2.3 山羊胰腺腺泡细胞鉴定
通过免疫荧光技术利用抗原抗体反应对山羊胰腺腺泡细胞进行鉴定。CPA1是胰腺腺泡细胞特异性表达的蛋白,因此我们选取CPA1作为目标蛋白。运用CPA1抗体作为一抗识别腺泡细胞中的CPA1,再用带荧光的二抗与一抗结合来显示CPA1蛋白。当目标蛋白、一抗和二抗结合在一起,在激光共聚焦显微镜下激发荧光才能显色呈阳性。若未显色则说明目标蛋白与抗体没有发生反应。据此,首先设置了不加一抗仅用二抗孵育的对照组(图5-a),结果没有激发绿色荧光,仅显示经染核试剂DAPI显色的蓝色细胞核部分,结果未显示阳性。当运用CPA1抗体对第1代细胞进行孵育,再与二抗结合时,细胞中的CPA1与CPA1抗体成功反应,激发绿色荧光,结果显示阳性(图5-b)。之后又对第5代细胞进性鉴定,同样显示出阳性(图5-c)。由此成功鉴定出本试验分离并纯化培养的细胞为山羊胰腺腺泡细胞。
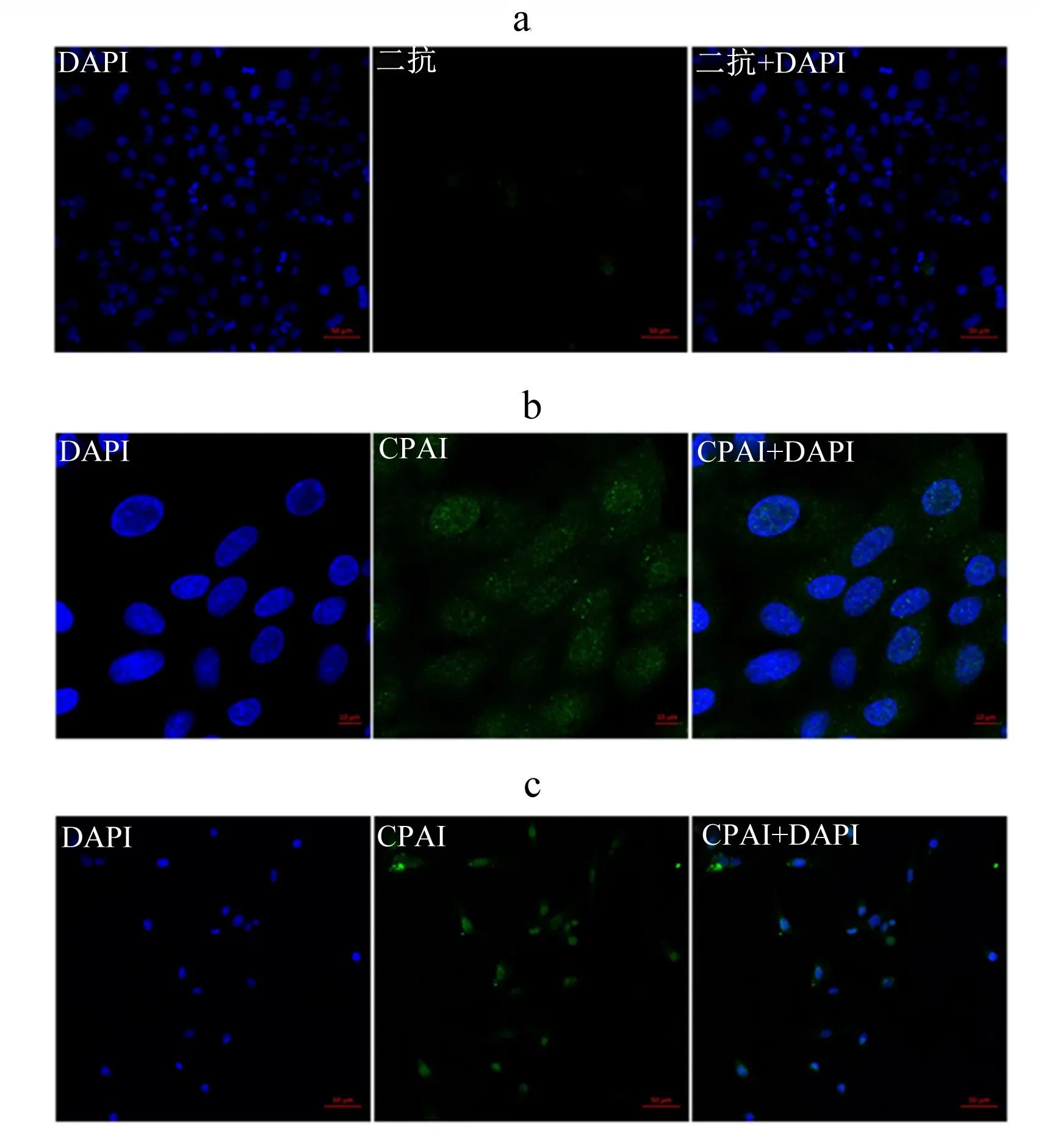
a:空白对照(100×);b:第1代细胞(200×);c:第5代细胞(100×)
3 讨 论
胰腺在各物种之间,以及各物种不同年龄阶段的生长发育、功能机理都有着极大地差异。因此现今依旧没有一个在各物种上能够稳定分离胰腺腺泡细胞原代培养的方法。当前在已经原代培养成功的胰腺腺泡上进行的研究也还存在着诸多疑问。例如,不同物种胰腺腺泡细胞上的胆囊收缩素(CCK)受体类型及分布存在差异,甚至于不具有CCK受体,且随着生长发育也有一定变化,然而,反刍动物随生长发育胰腺腺泡细胞上CCK受体图谱未见报道[8];胰腺腺泡细胞的自噬机制很大程度上影响着胰腺外分泌功能,然而,自噬的转录调控机制并未研究透彻[9];胰腺内分泌对胰腺外分泌影响的全部意义也尚不清楚[10];腺泡细胞内消化酶原提前激活的调控机制尚未得到统一解答[11];原代培养胰腺腺泡不能稳定传代等存在一系列疑问[7];原代培养的胰腺腺泡细胞进行细胞鉴定也鲜有报道。因此,山羊胰腺腺泡细胞分离培养方法的建立有助于对胰腺外分泌功能及其他生理机制在细胞水平上的研究。
在细胞分离的过程中能否得到数量足够且形态完整活性良好的腺泡细胞,取决于消化酶的类型的使用。胶原酶和胰蛋白酶在一般消化解离细胞的工作中较为常见。与胰蛋白酶相比,胶原酶具有温和的剪切力,胶原酶Ⅳ包含至少7种蛋白酶成分,能够更好地将组织块解离成单个细胞[12]。本试验还在消化液中运用了EGTA(一种钙离子螯合剂,能够破坏细胞间的连接而不影响细胞的完整性),这进一步使得分离得到的细胞为单个细胞[13]。
自1972年胰腺腺泡细胞运用胶原酶被首次分离成功后,由此在报道的腺泡细胞解离工作中胶原酶被更为广泛的使用[14]。但山羊的胰腺组织在消化解离的过程中可能与其他物种对消化液的要求有差异,因此胶原酶的消化时间及浓度需要验证,确定适宜的消化时间及浓度,以期得到良好的山羊胰腺腺泡细胞。在人胰腺腺泡细胞的分离试验中,研究人员运用0.8 mg/mL的胶原酶P消化人胰腺组织,但并没有描述清楚具体的消化时间[4]。在小鼠和猪的胰腺腺泡细胞分离工作中,分别运用了2 mg/mL胶原酶ⅠA消化30 min和2 mg/mL胶原酶Ⅱ消化40 min得到胰腺腺泡细胞[5-6]。Jayaveni等[7]运用1 mg/mL胶原酶Ⅲ将剪碎的牛胰腺组织消化15 min或更长时间进行牛胰腺腺泡细胞的分离培养。在上述试验中使用了不同类型的胶原酶,消化时间也各有差异,并且均没有介绍消化后的总细胞数和细胞活率等消化效率指标。因此在本试验中各指标需要进一步验证,运用1.0 mg/mL胶原酶Ⅳ作为消化液浓度,设置5个消化时间节点寻求适宜消化时间。由本试验结果可以看出,得到的总细胞数随着消化时间的延长逐渐增多。细胞活率在15 min时低于20 min,造成这样的原因可是是由于在消化前对胰腺组织进行机械剪切,造成组织块表面较多的损伤细胞。而20 min进一步消化出更多的未损伤细胞,所以20 min细胞活率高于15 min。而随着消化时间的延长细胞活率逐渐降低,这应该是消化过度造成的。因此选取总细胞数相对适宜、细胞活率较高的20 min进行后一步的试验,因为较高的细胞活率可避免接种后的污染风险。此外,在后期的试验中希望在较短的培养时间能得到足量的第1代贴壁细胞,因此需尤其注重得到的细胞具有较高活力,使解离得到的细胞具有较高的贴壁效率。
在验证适宜消化时间的过程中发现有细胞碎片的存在,因此尝试将消化液浓度降低,将1.0 mg/mL胶原酶Ⅳ降低到0.5 mg/mL,在消化20 min的情况下,结果显示细胞碎片确实少了许多,但单个细胞数量及细胞活率并不理想。在其他胰腺腺泡细胞的原代培养工作中,研究人员们同样也运用了1.0 mg/mL胶原酶,但胶原酶的类型不同[7]。由于胰腺自身的自噬、分泌消化酶等特异性,存在胰腺组织坏死及细胞损伤的情况[15],因此本试验并未尝试用低浓度的消化酶去延长消化时间,以得到更多的单个细胞。另外,胰腺腺泡细胞的自我损伤也是细胞分离难度较高、细胞生长不稳定的主要原因[11],因此消化酶浓度和消化时间的把控极为重要。
在各种细胞培养的工作中,0.25%胰蛋白酶常作为原代细胞解离的消化液来使用,但在胰腺组织上的运用较为少见,Guo等[16]运用胰蛋白酶冷消化法解离犊牛胰腺腺泡细胞,但其消化时间相对较长。在与1.0 mg/mL胶原酶Ⅳ对比的试验中我们发现,0.25%胰蛋白酶在同等条件下消化效率并不如胶原酶Ⅳ,虽说在显微镜下观察后发现0.25%胰蛋白酶消化得到的细胞碎片相对较少。但细胞碎片的问题经过多次摸索发现,在600 r/min离心5 min,重复2次可以有效清除细胞碎片的存在。
胰腺腺泡细胞虽然在胰腺组织中占比极高,但是在原代培养的过程中不免会分离出胰腺中的其他细胞,因此在培养过程中对分离的腺泡细胞进行了细胞纯化工作。分离的原代细胞主要依靠流式细胞术、差时消化、差速贴壁及细胞刮取等方法进行细胞纯化。但由于物种的原因,山羊胰腺腺泡细胞进行基因编辑存在极高的难度,另外就是抗体的缺乏,导致在工作中难以运用流式细胞术来纯化分离得到的山羊胰腺腺泡细胞。因此本试验运用了差时消化、差时贴壁、细胞刮取等方法相结合来对腺泡细胞进行纯化工作。这些手段相结合在保证成本的前提下,能够得到较为纯的细胞。虽说这3种方法主要依靠细胞形态来判断纯化得到的细胞,但本试验在之后进行了细胞的鉴定工作。由此也可验证纯化细胞工作的可行性。
鉴于胰腺腺泡细胞分泌消化酶的特殊性,在之前各物种培养原代腺泡细胞时都讨论了细胞存活时限[4-7]。早先原代培养的胰腺腺泡细胞存活时间比较短,随着消化酶、消化时间和培养基等影响因素的不断优化,目前胰腺腺泡细胞的培养时间大概在2周左右。但体外培养细胞所需的条件肯定是存在缺陷的,因此原代细胞应该总是处于一个应激的状态。近来也有报道,胰腺腺泡细胞极易化生为胰腺导管细胞[17],如果长时间培养可能会导致这样的情况发生。因此在本试验中,我们更期望得到与原组织更为接近的细胞。所以在细胞量足够的情况下更希望得到第1及第2代细胞。为保证细胞的活性,本试验在培养基中添加了EGF,同为防止腺泡细胞自身分泌消化酶的影响,在培养基中添加了10%的特级FBS。在这些条件的影响下,保证了本试验中胰腺腺泡细胞在第1代及第2代有了良好的完整性及活性。
在胰腺腺泡细胞分离成功后,由于考虑到胰腺腺泡细胞自身分泌胰蛋白酶可能造成其不容易贴壁,因此担心分离培养的细胞是否是预期得到的胰腺腺泡细胞。尽管胰腺腺泡细胞的分离培养已有过一些报道,但鉴定工作并不多见。鉴于原代培养的山羊胰腺腺泡细胞分离培养及鉴定工作鲜有报道,另外也为了验证纯化工作的可行性,因此展开了山羊胰腺腺泡细胞的鉴定工作。一开始试验效仿Jayaveni等[7]运用α-淀粉酶抗体来进行鉴定工作,但经过多次试验及调整并未显示阳性,分析可能是物种的原因造成的。因此决定选用其他抗体进行鉴定。CPA1是一种在胰腺腺泡细胞中产生的锌金属蛋白酶,在饮食蛋白C端支链和芳香族氨基酸的裂解过程中发挥作用,最早于1929年从牛胰腺提取物中鉴定出该酶[18]。在医学上,CPA1被确定为胰腺腺泡细胞癌的标志物,但在运用胰腺组织做免疫组化时,正常胰腺组织中的腺泡细胞也能被CPA1抗体染色呈阳性,且相较于胰蛋白酶等其他标志物具有更高的灵敏度[19-20]。受此启发,本试验运用CPA1抗体来进行山羊胰腺腺泡细胞的鉴定工作,这也是CPA1抗体首次运用于原代培养的胰腺腺泡细胞鉴定工作中。试验结果验证了胰腺腺泡细胞鉴定的可行性。
4 结 论
湘东黑山羊胰腺组织经1.0 mg/mL的胶原酶Ⅳ消化20 min,得到2.275×106个/mL总细胞数及91%的细胞活率,相同条件下消化效率优于0.5 mg/mL胶原酶Ⅳ和0.25%胰蛋白酶。采用差时消化、差速贴壁和细胞刮取等方法纯化原代细胞,得到活性良好且形态均一呈“鹅卵石”状的山羊胰腺腺泡细胞。纯化后的山羊胰腺腺泡细胞能够稳定传5代以上,且形态不发生改变。通过兔抗CPA1作为一抗对第1代及第5代山羊胰腺腺泡细胞进行鉴定,结果显示阳性。综上所述,本试验方法能够在短时间内成功分离并培养山羊胰腺腺泡细胞。
