感染性结石的解脲酶菌相关因素研究及治疗进展
2022-10-04李卫胜何文强靳潇潇杨雄
李卫胜 何文强 靳潇潇 杨雄
1.河南中医药大学泌尿外科,河南郑州 450003;2.河南中医药大学第一附属医院泌尿外科,河南郑州 450003
肾结石是泌尿外科多发性疾病之一,根据其发病原因可分为代谢性结石和感染性结石。感染性结石通常指磷酸铵镁结石,占肾结石的10%~15%。结石的主要成分是六水磷酸铵镁和碳酸磷灰石。在肾结石的发生、发展过程中生物膜反复包裹解脲酶菌,使抗菌药物难以杀死并清除细菌,常致患者发生复发性尿路感染,并引起相关并发症如肾周脓肿和脓胸等。目前对感染性结石发生机制的研究主要集中在体外细胞培养模型和大鼠模型,但两种模型均无法模拟正常尿流动力学特征或建立系统的肾脏感染性结石模型。本文通过对解脲酶菌引起感染性结石的相关因素及治疗进行分析,以期探讨新的研究方向及潜在的治疗靶点。
1 解脲酶菌引起感染性结石的相关因素及发病机制
1.1 尿路感染与感染性结石的关系分析
尿路感染(urinary tract infections,UTIs)和感染性结石具有显著相关性,可能存在因果关系或平行关系,但其具体机制仍不清楚。二者发病特点具有诸多相似之处,常因病原菌经尿道逆行感染膀胱、输尿管、肾脏所致,女性患病风险和发病率皆明显高于男性,且随着年龄的不断增加,男女患病比率降低。洪扬等使用不同计数的奇异变形杆菌建立大鼠肾脏感染性结石模型,只有10组大鼠形成感染性结石且均为膀胱结石,成石率为50%,试验组并无肾结石形成,提示宿主免疫对感染性结石的形成有抑制作用,其形成是一个复杂过程。细菌感染尿路却未形成结石,对感染性结石的预防、新治疗靶点的研究、指导感染性结石的药物治疗具有重要意义。然而细菌生物膜的形成及抗生素的广泛应用使泌尿系病原菌耐药性增加,造成临床治疗策略的进一步复杂化,因此迫切需要新的生物学研究方法及建立试验模型做为基础,对尿路感染与感染性结石进行深入研究,明确它们的关系并建立有效的试验模型是寻找新治疗靶点的关键。
1.2 解脲酶菌及其毒力因子
了解病原菌感染及致病机制是预防疾病发生的关键,因此对病原菌感染、定植及繁殖机制的研究在疾病的预防与治疗中意义重大。相关研究证实,感染性结石的形成以解脲酶菌感染尿路并产生脲酶为基础,造成尿路上皮细胞损伤,并分解尿素产生CO和NH,使尿液pH 升高进而产生铵和碳酸氢盐,最终形成鸟粪石(六水磷酸铵镁结石)与碳酸磷灰石。见图1。
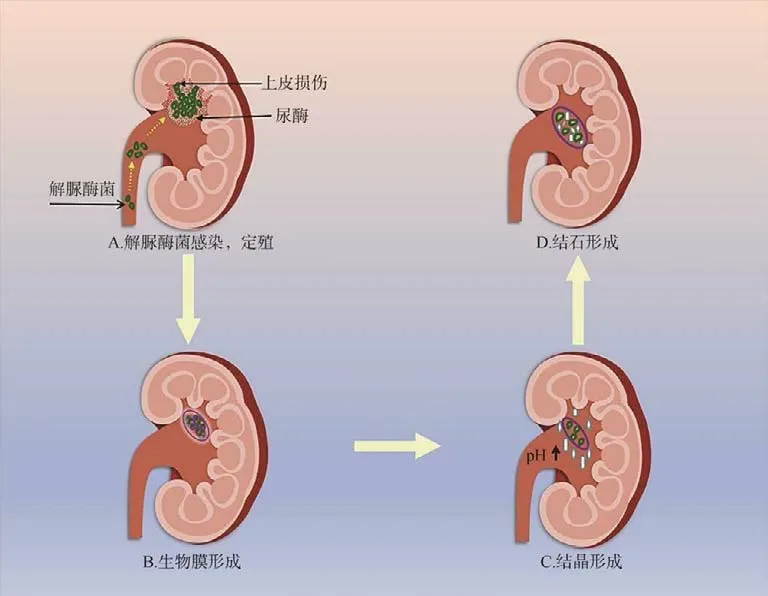
图1 感染性结石形成机制
苏晓伟等研究显示,94 例感染性结石中,感染大肠埃希菌49 例,感染奇异变形杆菌12 例,感染肺炎克雷伯菌6 例;211 例草酸钙结石患者中,感染大肠埃希菌103 例,感染粪肠球菌20 例,感染无乳链球菌12 例;60 例尿酸结石患者中,感染大肠埃希菌24 例,感染粪肠球菌8 例,感染肺炎克雷伯菌5 例。结论是感染性结石UTIs 例数、尿菌培养阳性例数明显高于其他组,感染性结石与UTIs 具有显著相关性,尿路致病性大肠埃希菌(uropathogenic Escherichia coli,UPEC)是尿路感染的主要致病菌。
王冠博等对患者中段尿、肾盂尿、结石进行细菌培养,发现尿与结石的细菌培养结果不具一致性,结石菌株并非以UPEC 为主,与Walton–Diaz等的研究结论一致。造成上述差异的具体原因尚不明确,结石嵌顿造成肾盂感染的尿液无法流入膀胱可能只是一种相关因素。感染性结石的形成过程极具复杂性,单纯尿培养无法准确反映结石内部及其周围的病原学特征,不能精准指导抗生素的使用。对结石及其周围尿液进行细菌培养并进行药敏试验更具临床意义,以此作为预防感染性结石形成、防止术后感染的临床用药显然更可靠。
细菌毒力因子是病原菌黏附于尿路上皮细胞发生尿路感染进而形成感染性结石的前提,与病原菌黏附、侵袭、抵抗或逃避宿主免疫、降低细菌药物敏感性密切相关,细菌毒力主要包括侵袭力和毒素。侵袭力是细菌在体内发生黏附、定植、扩散、抵抗或逃避宿主免疫的能力;黏附功能是后续过程发生的基础,因此在感染初期阶段抑制病原菌黏附可有效控制感染发展。黏附素是主要的黏附相关毒力因子,它可使病原菌与细胞或组织表面受体结合发生黏附,包括菌毛和非菌毛黏附素,以革兰阴性菌如UPEC、革兰阳性球菌如屎肠球菌最常见。研究表明,使用菌毛抗体干扰细菌感染早期的黏附阶段,抑制细菌–细菌或细菌–宿主之间的黏附,为疾病的预防与治疗提供了潜在靶点。相同种属菌群中不同亚型的细菌和菌毛使抗毒素疫苗与药物研发面临很大困难,如UPEC–Ⅰ型菌毛主要与膀胱上皮细胞上D–甘露糖受体结合,导致膀胱炎的发生,UPEC–P型菌毛结构和Ⅰ型菌毛相似,主要依靠菌毛顶端黏附分子PapG 与近段小管、远端小管上皮细胞受体相结合,引起上行性尿路感染及肾盂肾炎。Davis研究表明,宿主–细菌相互作用可促进毒力因子表达并抵抗宿主反应,使其他细菌受益,推测感染性结石的形成与此模式有直接相关性,即大肠埃希菌抵抗宿主时,其毒力因子的表达为其他解脲酶菌发挥生物学功能提供了有利条件,促进感染性结石的发生发展,仍需要相关实验验证。张肖肖等报道,毒力基因esp、gel、agg 的携带与肠球菌生物膜的形成密切相关,提示细菌毒力基因与生物膜的相关性,而生物膜在促进结石形成、增强细菌耐药性与毒力的同时,使感染性结石更易复发、治疗方向更加复杂,如何降低生物膜的形成可作为新治疗靶点,具体机制有待进一步研究。
1.3 细菌生物膜的形成
研究细菌生物膜的形成机制及生物学特点对指导临床规范使用抗生素,减少菌株多重耐药有重要意义。生物膜是细菌不可逆附着于实体表面、繁殖、分化并分泌一些多糖基质,将菌体包裹其中而形成的细菌聚集体膜状物,其形成与细菌抵抗宿主免疫、降低抗生素敏感性、慢性持续性及难治性感染等密切相关。被生物膜包裹其中的休眠菌和滞留菌是导致复发性感染的关键因素,因此感染性结石的易复发性与此有关。患尿路感染而不形成感染性结石的原因可能与细菌计数少、不能达到形成生物膜的计数或不能表达足够的毒力因子来逃避或抵抗宿主免疫、降低抗生素敏感性有关。不合理使用抗生素会增加菌株多重耐药性,且细菌多重耐药与生物膜形成呈正相关性,说明生物膜是不规范使用抗生素导致病原菌多重耐药的关键因素。病原菌对抗生素敏感性降低,机体发生反复感染等与生物膜形成密切相关:①细胞外基质使宿主免疫和抗生素无法穿透生物膜屏障杀死内部细菌;②生物膜可使细菌培养结果呈假阴性,失去临床指导意义;③生物膜反复包裹病原菌,为其躲避机体免疫与药物攻击提供了有利条件。另外,病原菌可通过基因调整产生多态性亚型,一旦宿主免疫功能下降或药物浓度降低,就会引起复发性感染或持续性感染。
2 感染性结石的治疗
感染性结石具有生长快、易复发的特点,若没有及时采取合理的治疗方案,患者可出现严重的并发症如肾衰竭,甚至导致死亡。感染性结石的治疗一般遵循3 个原则,即清除所有结石碎片、使用抗生素治疗感染、防止复发。治疗方法包括术前术后应用抗生素、外科及微创取石(如冲击波碎石术)、输尿管软镜、经皮肾镜取石术(percutaneous nephrolithotomy,PCNL)、残片处理(如解脲酶抑制剂的使用、结石溶解及尿液酸化等)。临床医师需综合考虑患者的具体情况制定合理的治疗方案,改善患者预后,防止疾病复发。
2.1 抗生素的应用
感染性结石常合并相关并发症如肾积脓、肾周脓肿等。行腔镜手术如激光腔镜碎石等治疗时,高灌注压、局部温度及肾盂内压升高等是感染性结石碎裂后内部细菌入血发生感染扩散、感染性休克的高危因素,这些高危因素增加了感染性结石的治疗复杂性,如何预防或降低并发症的发生,仍是一道难题。对感染性结石患者术前和术后积极抗感染治疗,可有效降低相关并发症,预防术后发生脓毒血症或发热,以达到满意的疗效。Sierra–Diaz等进行了一项前瞻性研究,对尿培养阳性的暴露组分别在术前、术后7d 给予抗生素治疗,非暴露组分别在术前8h、术后1h 经验性静脉注射抗生素,结果显示暴露组并发症占比大于非暴露组(27%16%),说明尿菌培养阳性是术后发热的主要危险因素,标准化治疗方案可降低手术相关并发症发生率。上述研究证明,抗生素可提高感染性结石治疗的安全性,术前使用敏感抗生素至尿菌培养阴性或尿白细胞下降,可降低术后患感染性并发症的风险及其发生率。目前对围手术期预防性应用抗生素的意见相对一致,但使用时间尚未达成统一。对于初始用药或感染较轻的患者可根据经验用药,应注意的是抗生素的使用要符合菌群特点,用药前需评估患者身体综合情况如肾功能等及安全性。相关研究表明,合理使用抗生素可有效降低生物膜形成、控制细菌多重耐药的发生及发展,因此抗生素的使用应参考最新指南,选择合适的种类、剂量及疗程,有针对性的进行用药。目前临床上采用抗生素治疗尿路感染,主要根据尿细菌培养与药敏试验结果用药。尿与结石细菌培养结果的差异性提示,结石及其周围细菌培养结果对抗生素的临床使用更具指导意义。
2.2 外科及微创取石术
2.2.1 体外冲击波碎石(extracorporeal shock wave lithotripsy,ESWL)与Mini–经皮肾镜取石术(mini–percutaneous nephrolithotomy,MPCNL)ESWL 是肾结石微创治疗的主要方式之一,具有操作简单、成本低等特点,常作为直径<10mm 的输尿管结石治疗首选,但ESWL 的初始结石清除率相对输尿管软镜、Mini–经皮肾镜取石较低。由于感染性结石多为鹿角样大结石,且结石内部有病原菌存在,采用ESWL 治疗时易形成输尿管石街,发生输尿管堵塞、压力升高、感染扩散等并发症,安全性较差,因此对鹿角样结石或感染性结石的治疗,不宜使用此方法。与ESWL 相比,MPCNL 结石清除率高达90%以上,适用于经ESWL、输尿管软镜碎石术治疗失败的患者,因此应用范围广泛,常作为复杂性、多发性肾结石、输尿管结石的首选治疗方案。李铁等的研究显示,尽管MPCNL 组与EWSL 组相比结石清除率更高(98%88%),但其并发症如感染、发热延迟出血等发生率也较高,且术后血清中与组织损伤相关的氧化应激指标内皮素–1(endothelin–1,ET–1)、血红蛋白加氧酶1(heme oxygenase–1,HO–1)、皮质醇(cortist,COR)、血管紧张素Ⅱ(angiotensinⅡ,Ang–Ⅱ)皆显著高于ESWL 组。另有研究表明,应用MPCNL 治疗上尿路结石时,需使用经皮穿刺高压泵灌注,此过程不但会升高肾内压,还可能造成肾损伤,使结石内部病原菌逆行性入血而引起患者脓毒血症的发生。因此输尿管软镜技术应运而生,给肾结石的治疗带来了新方案。
2.2.2 输尿管软镜 输尿管软镜、ESWL、MPCNL是泌尿外科微创治疗的主要方式,为直径2cm 以内结石的首选治疗方案。输尿管软镜联合激光治疗泌尿系结石的安全性高于传统术式,与ESWL 相比,具有适用范围广、微创、术后恢复快等优点;与MPCNL 相比,结石清除率虽无明显差异,但其并发症少,安全性更高。研究发现,输尿管软镜结石清除率受结石种类、数量、尿路复杂性等因素影响,联合负压吸引装置治疗尿路结石,可减少输尿管软镜激光碎石过程中温度及灌注压升高引起的并发症如细菌入血扩散,脓毒血症等,提高尿路结石治疗的安全性。
2.3 残片处理
完全清除结石碎片是防止术后疾病复发的关键,感染性结石的治疗更是如此,否则极易引起结石复发或肾绞痛、尿源性感染等并发症,因此除术中取净结石碎片外,术后残片的处理也极为重要,包括解脲酶抑制剂的使用、结石溶解及尿液酸化等。根据上述探讨推测,解脲酶抑制剂联合抗生素可有效提高感染性结石手术治疗的安全性,防止术后复发,降低并发症发生率等。
3 总结与展望
上述讨论表明,感染性结石的发生发展、预防和治疗、手术的预后与UTIs 及病原菌的种类密切相关,大肠埃希菌感染尿路可能是结石相关病原菌在泌尿系统生存与繁殖并形成结石的基础,尚需进一步实验证实。选用哪种方案治疗需综合考虑结石的类型、性质、直径、位置等,对于感染性结石或鹿角样结石的治疗应严格遵守相关治疗原则,且术前和术后均应使用抗生素,以增加治疗的安全性,降低发生并发症的风险。与抗生素治疗相比,毒力因子的抗毒素研究是一种新的治疗靶点研究方向,它只针对毒力因子产生作用,目的是将病原菌转化为无毒性细菌,不对细菌施加高选择压力,不杀死或抑制细菌生长,可有效降低细菌耐药性的产生,缓解抗生素治疗所带来的细菌耐药性压力。通过毒力因子抗体或干扰细菌毒力基因的表达阻碍生物膜形成是潜在的治疗靶点,如何建立系统的肾感染性结石实验模型和毒力因子研究模型仍是当前面临的研究难题。
