肠炎沙门氏菌SEF14菌毛研究进展
2013-09-10厚华艳朱春红朱国强
厚华艳,朱春红,孟 霞,朱国强*
(1.扬州大学兽医学院,江苏扬州 225009;2.江苏省家禽科学研究所,江苏扬州 225125)
肠炎沙门氏菌SEF14菌毛研究进展
厚华艳1,朱春红2,孟 霞1,朱国强1*
(1.扬州大学兽医学院,江苏扬州 225009;2.江苏省家禽科学研究所,江苏扬州 225125)
1 SEF14菌毛的发现
Feutrier等1986年首次在临床分离的一株人源肠炎沙门氏菌中发现一种菌毛(后来被称为SEF14菌毛),具有甘露糖敏感血凝反应(MSHA),形态上与肠杆菌科细菌的Ⅰ型菌毛难以分辨,蛋白质亚单位为14.4 kD,比伤寒沙门氏菌Ⅰ型菌毛亚单位(22.1 kD)小,N-末端18个氨基酸残基与大肠杆菌和伤寒沙门氏菌Ⅰ型菌毛同源[1]。Müller等在同一株人源肠炎沙门氏菌分离株上鉴定了甘露糖敏感且形态和生化特性上不同于之前报道的SEF14的典型Ⅰ型菌毛[2]。1990年Tahorns等通过单克隆抗体(MAb)介导方法在肠炎沙门氏菌表面鉴定出这一菌毛样结构,蛋白质亚单位为14.3 kD,直径小于5 nm,没有凝集红细胞能力[3]。目前已有的研究表明:SEF14蛋白亚基基因sefA主要分布于D血清型沙门氏菌中,但SEF14抗原只表达于都柏林沙门氏菌、肠炎沙门氏菌、莫斯科沙门氏菌和布利丹沙门氏菌菌体表面[4-5]。根据其凝集红细胞能力和形态大小的差异,而且与已经鉴定的其他菌毛蛋白没有同源性,所以不能够归于现有的沙门氏菌菌毛中任何一类[6]。
2 SEF14菌毛的分子生物学
sef基因操纵子位于一个小致病毒力岛,主要由sefA、sefB、sefC、sefD4个结构基因编码蛋白完成SEF14菌毛的合成和组装(图1),sefA编码主要蛋白亚基,sefB和sefC分别编码伴侣蛋白和推进蛋白,sefD编码菌毛的顶端粘附素,位于SEF14菌毛结构顶端[7-8]。sefB编码菌毛周质伴侣蛋白,与大肠杆菌菌毛周质伴侣蛋白同源,在周间隙中与菌毛蛋白亚基SEFA结合,避免其前体非活性聚集;SefC蛋白与大肠杆菌菌毛外膜蛋白同源,促使伴侣蛋白SefB与菌毛蛋白亚基或菌毛蛋白前体解离;sefR是紧连sefD的一个反向调节基因[9-11]。Clouthier和Edwards等认为sefABCD操纵子基因作为一个整体同时转录和翻译,在sefA上游有两个主要转录起始位点,sefBC的转录也要从sefA的启动子区起始,在sefA极性(polar)突变株中sefB、sefC和sefD均不能转录和表达[7-9]。如图2所示,在SEF14菌毛亚单位突变株△sefA中,亚单位SEFD能够以菌毛类似物表达于菌体表面(图2B),但在突变株△sefD中,亚单位SEFA则不能表达展呈于菌体表面(图2D),依此推测次要亚单位SEFD是通过主要亚单位SEFA结合伴侣蛋白和推进蛋白并成功通过细胞周间隙,表达于菌体表面,和亚单位SEFA组装成成熟SEF14菌毛。但sefA基因的极性突变株无任何亚单位表达于菌体表面(图2C)。SEF14菌毛是一个典型的经伴侣蛋白-推进蛋白途径分泌的蛋白。通常情况下,伴侣蛋白、推进蛋白两个辅助蛋白参与其中作用,菌毛蛋白结构亚单位在细胞周质中与伴侣蛋白结合以避免非活性形式的聚集或者被相关蛋白酶降解;然后在推进蛋白的作用下穿过外膜蛋白,表达于细菌表面并完成组装[12]。
朱春红等利用PCR扩增方法检测了18株鸡白痢沙门氏菌、11株肠炎沙门氏菌以及1株都柏林沙门氏菌标准株中sefA、sefD和sefR基因序列,结果表明以11株肠炎沙门氏菌及1株都柏林沙门氏菌染色体DNA为模板能够扩增sefA、sefD以及sefR基因,以18株鸡白痢沙门氏菌染色体DNA为模板能够扩增sefA基因,但只有分离于1980年之前的7株分离菌能够成功扩增sefD和sefR基因,而另11株1980年后分离菌PCR扩增sefD和sefR基因均为阴性。据此认为SEF14菌毛操纵子亚单位基因sefA、sefD以及调节基因sefR在不同沙门氏菌中的变异情况可能是SEF14菌毛局限性表达的原因之一[13]。

图1 肠炎沙门氏菌sef14基因结构图(Edwards,2000)Fig.1 Thesef14gene cluster ofS.enteritidis
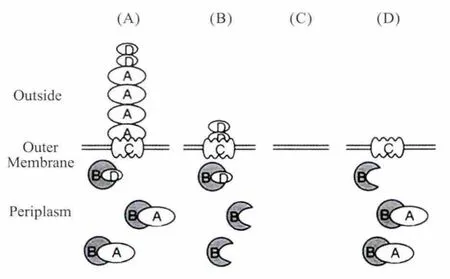
图2 肠炎沙门氏菌SEF14菌毛可能的分泌表达机制(Edwards,2000)Fig.2 Predicted export of SEF14 fimbriae subunits from periplasm in different mutants
3 SEF14菌毛的表达
sef基因操纵子的表达受细菌生长周期、环境因素、调控因子等多方面因素的调控。Walker等利用特异性检测SEF14菌毛的ELISA试验,研究4株不同的肠炎沙门氏菌在肉汤培养和平板培养条件下,SEF14菌毛表达的合适温度和pH条件,至少3个环境因素影响SEF14菌毛表达:温度、pH、细菌之间的关联性,在pH呈酸性,温度为37℃时,更利于SEF14菌毛表达[14]。sef基因操纵子表达还受调控因子RpoS的调控,但RpoS对sef操纵子的调控是直接的还是间接的目前还不确定[6]。本实验室优化肠炎沙门氏菌标准株50336 SEF14菌毛表达最佳条件为:接种标准株50336单菌落于TSB培养基中,25℃摇床培养24 h,次日按1∶100转接到新的TSB培养基中,20℃摇床培养 24 h,第 3 d按 1∶50转接到 CFA(pH6.0)培养基中,37℃静置培养50 h~60 h。此外还发现经萘啶酮酸诱导的缺失株△sefA与野生株相比,在20℃时生长极缓慢(未发表实验数据)。
4 SEF14菌毛致病性
菌毛在细菌和宿主细胞之间相互作用中发挥重要毒力作用[15]。特定菌毛在肠道细菌中的分布可能与其致病性有密切关系,如广泛分布于革兰氏阴性菌中的Ⅰ型菌毛,介导病原菌与宿主如咽喉部,肠道上皮或者膀胱上皮组织之间的黏附;但细菌中同时也存在着这样一类菌毛结构,他们限制性分布于某些特定的细菌,比如只在沙门氏菌中发现的质粒编码的菌毛结构(PEF),则介导沙门氏菌特异性黏附于宿主肠道的M细胞。SEF14菌毛有限分布于肠炎沙门氏菌和相近的D群沙门氏菌中[7]。
Edward等通过构建sefA和sefD突变株研究SEF14菌毛功能,sef操纵子极性突变株对小鼠毒力下降为1∶1 000倍,而sefA非极性突变株的毒力无明显变化,但sefD突变株毒力显著降低。表明SEF14菌毛次要亚单位黏附素sefD对于SEF14菌毛的毒力是必要的[7]。最新研究显示,野生株中sefD基因在42℃时转录被抑制,而缺失sefD基因的回补株中sefD基因的转录量为野生株的103倍,但回补株的生长却受到了抑制,野生株和缺失株感染鸡的血钙和产蛋量下降,但感染回补株的鸡这种现象。表明sefD基因突变株或者在鸡的高体温下抑制sefD基因表达的野生株均通过产生不同代谢物来促进肠炎沙门氏菌的毒力[16]。
Thorns等曾报道SEF14菌毛突变株与相应野生株相比更快被人中性粒细胞吞噬[17]。Edward等的研究显示,sefD突变株与野生株相比在小鼠腹腔巨噬细胞中的存活率下降,他认为SEF14菌毛能够使肠炎沙门氏菌在巨噬细胞中有效存活[7]。本实验室利用Red同源重组构建了SEF14菌毛突变株,并用野生株、突变株对肠上皮细胞系IPEC-J2和人结肠癌细胞系Caco-2进行了粘附实验,小鼠腹腔巨噬细胞吞噬作用和野生株以及相应突变株在小鼠腹腔巨噬细胞内的存活作用。初步结果表明野生株及相应突变株对上皮细胞及肠道细胞的粘附数量差异不显著,SEF14菌毛并不特异性介导肠炎沙门氏菌与肠上皮细胞的粘附作用,或者不是粘附的主要作用因子,小鼠腹腔巨噬细胞吞噬试验和存活试验结果表明:活化的小鼠腹腔巨噬细胞对突变株吞噬作用增强,借助SEF14菌毛的作用,肠炎沙门氏菌能更好的作用于巨噬细胞并在巨噬细胞中存活,利于其隐性感染和长期排毒(数据未发表)。
关于其在易感动物体内的致病力情况,Thorns报道SEF14菌毛突变株和野生株相比在肠道的定殖、对一日龄雏鸡、产蛋鸡及BALb/c小鼠的侵袭和系统性的传播差异不显著[17]。Rajasekara等证明,与野生株相比,SEF14菌毛突变株在其感染鸡的肝、脾中几乎分离不到感染菌[18]。Dibb-Fuller、Thorns和Ogunniyi等认为SEF14菌毛对侵袭作用没有影响[19-20]。有趣的是,Thiagarajan发现SEF14菌毛在鸡中与经卵巢传播有关[21]。也有人认为SEF14菌毛单个毒力因子在肠炎沙门氏菌致病性中并未发挥主要毒力作用,可能与其他毒力因子协同发挥作用,或者是感染的宿主不同,发挥作用也不同[16]。目前为止,关于SEF14菌毛的功能存在很大争议。
5 SEF14菌毛的潜在应用前景
研究表明肠炎沙门氏菌的鞭毛蛋白、孔蛋白、外膜蛋白、SEF14和SEF21菌毛蛋白均具有免疫原性,可以作为抗原免疫动物并提供有效的免疫保护作用[22]。以SEF14和SEF21菌毛作为抗原,脂质体为免疫佐剂,点眼法免疫家禽,能够产生系统性和粘膜免疫反应,在免疫家禽的肠道和血清中能够检测到抗体IgA和IgG,同时降低了肠炎沙门氏菌在肠道中的定殖和粪便中的排菌[23]。Lopes等重组表达肠炎沙门氏菌SEF14菌毛亚单位蛋白SEFA,并将其导入无致病性、无毒的大肠杆菌中,免疫1日龄鸡,产生抗SEFA蛋白的特异性免疫反应,可以在免疫家禽的肠道和胆汁中检测到抗SEFA的抗体IgA[24]。抗细菌感染的免疫保护作用通常是由多种抗原协同参与完成,单一抗原或抗原亚单位不能对宿主提供足够的保护。Aslanzadeh等的研究表明肠炎沙门氏菌SEF21、SEF17和SEF14菌毛的联合免疫可产生更好的免疫效果[25]。
目前,由肠炎沙门氏菌引起的食物中毒事件繁多,特别是西方发达国家,造成严重经济损失,大多是因为食用了肠炎沙门氏菌污染的肉蛋产品,因此快速、准确、特异性诊断肠炎沙门氏菌的方法尤为重要。鉴于SEF14菌毛免疫原性,将其制成颗粒抗原,用于检测抗肠炎沙门氏菌SEF14菌毛特异性抗体,在第二次乳胶凝集试验中根据鞭毛抗原上的特异位点可以将其与都柏林沙门氏菌区别开来[5,26]。该方法比较理想,但价格昂贵。此外,SEF14菌毛主要亚单位基因sefA主要分布于D群沙门氏菌中,根据sefA基因设计的PCR检测方法一定程度上可特异性检测D群沙门氏菌的感染[27]。Thorns等建立了SEF14-DAS ELISA能够将肠炎沙门氏菌感染与其他沙门氏菌如鸡白痢沙门氏菌、鼠伤寒沙门氏菌等的感染区分开[28]。
本实验室利用SEF14菌毛的限制性表达特性建立了肠炎沙门氏菌的特异性诊断方法:朱春红建立和优化了重组亚单位蛋白rSEFA介导的间接ELISA方法特异性检测肠炎沙门氏菌血清抗体。该间接ELISA具有较好的特异性,能特异性识别肠炎沙门氏菌和都柏林沙门氏菌感染血清,不能识别相近的鸡白痢沙门氏菌感染血清[29]。段晓丽利用制备的抗SEF14菌毛MAb建立了双抗体夹心间接ELISA方法。该方法以MAb作为捕获抗体包被酶标板,以抗SEF14菌毛的鸡血清为检测抗体,该双抗体夹心间接ELISA方法特异性更强,灵敏性更高,对肠炎沙门氏菌特异性抗体检测有潜在的应用前景[30]。
6 展 望
鉴于肠炎沙门氏菌SEF14菌毛的免疫原性和亚单位蛋白基因sefA的特异性分布,在建立新型诊断技术方面和未来研制基因工程疫苗方面具有广阔应用前景。目前为止,关于SEF14菌毛的致病机理和免疫机理存在很大争议,但随着分子生物学研究技术的不断发展,SEF14菌毛的结构和功能研究也在不断深入,相信在肠炎沙门氏菌感染特异性检测与预防控制方面定会发挥重要作用。
[1]Feutrier J,Kay W W,Trust T J.Purification and characterization of fimbriae fromSalmonella enteritidis[J].J Bacteriol,1986,168(1):221-227.
[2]Müller K H,Collinson S K,Trust T J,et al.Type 1 fimbriae ofSalmonella enteritidis[J].J Bacteriol,1991,173(15):4765-4772.
[3]Tahorns C J,Sojka M G,Chasey D.Detection of a novel Fimbrial structure on the surface ofSalmonella enteritidisby using a monoclonal antibody[J].J Clin Microbiol,1990,28:2409-2414.
[4]Turcotte C,Woodward M J.Cloning DNA nucleotide sequence and distriburion of the gene encoding SEF14,a fimbrial antigen ofSalmonella enteritidis[J].J Gen Microbicl,1993,139:1477-1485.
[5]Thorn C J,Soika M G,Mclaren I M,et al.Characterisation of monoclonal antibodies against a fimbrial structure ofSalmonella enteritidisand certain other serogroup DSalmonellaeand their application as serotyping regents[J].Res Vet Sci,1992,53(3):3000-3008.
[6]Edwards R A,Matlock B C,Heffernan B J,et al.Genomic analysis and growth-phase-dependent regulation of the SEF14 fimbriae ofSalmonella enterica serovar enteritidis[J].Microbiology,2001,147(10):2705-2711.
[7]Edward R A,Schifferli D M,Maloy S R.A role forSalmonella fimbriaein intraperitoneal infections[J].PNAS USA,2000,97(3):1258-1262.
[8]Clouthier S C,Collinson S K,Kay W W.Unique fimbriae-like structures encoded by sefD of the SEF14 fimbrial gene cluster ofSalmonella enteritidis[J].Mol Microbiol,1994,12:893-901.
[9]Clouthier S C,Müller K H,Doran J L,et al.Characterization of three fimbrial genes,sefABC,ofSalmonella enteritidis[J].J Bacteriol,1993,175(9):2523-2533.
[10]Hultgren S J,Normark S.Chaperone-assisted assembly and molecular architecture of adhesive pili[J].Annu Rev Microbiol,1992,45:383-415.
[11]Collighan R J,Woodward M J.The SEF14 fimbrial antigen ofSalmonellaenterica serovarenteritidisis encoded within a pathogenicity islet[J].Vet Microbiol,2001,80(3):235-245.
[12]Thorns C J.Salmonellafimbriae:novel antigens in the detection and control ofsalmonellainfections[J].Br Vet J,1995,151(6):643-658.
[13]朱春红,陆广富,陈雯雯,等.SEF14菌毛操纵子在肠炎沙门氏菌和D-群沙门氏菌的变异分析[J].微生物学报,2011,51(2):276-280.
[14]Walker S L,Sojka M,Dibb-Fuller M,et al.Effect of pH,temperature and surface contact on the elaboration of fimbriae and flagella bySalmonellaserotype enteritidis[J].J Med Microbiol,1999,48(3):253-261.
[15]Van der Woude M,Braaten B,Low D.Epigenetic phase variation of the pap operon inEscherichia coli[J].Trends Microbiol,1996,4:5-9.
[16]Rajashekara G,Munir S,Alexeyev M F,et al.Pathogenic role of SEF14,SEF17 and SEF21 fimbriae inSalmonella enterica serovar enteritidisinfection of chickens[J].Appl Enviro Microbiol,2000,66:1759-1763.
[17]Thorns C J,Turcotte C,Gemmell C G,et al.Studies into the role of the SEF14 fimbrial antigen in the pathogenesis ofSalmonella enteritidis[J].Microbial pathogenesis,1996,20:235-246.
[18]Thiagarajan D,Saeed M,Turek 1,et al.In vitroattachment and invasion ofchicken ovarian granulosa cells bySalmonella enteritidisphage type 8[J].Infect Immun,1996,64:5015-5021.
[19]Dibb-Fuller M P,Allen-Vercoe E,Thorns C J,et al.Fimbriaeand flagella-mediated association with and invasion of cultured epithelial cells bySalmonella enteritidis[J].Microbiology,1999,145(5):1023-1031.
[20]Ogunniyi A D,Kotlarski I,Morona R,et al.Role of SefA subunit protein of SEF14 fimbriae in the pathogenesis ofSalmonella enterica serovar enteritidis[J].Infect Immun,1997,65:708-717.
[21]Morales C A,Guard J,Sanchez-Ingunza R,et al.Virulence and metabolic characteristics ofSalmonella enterica serovar enteritidisstrains with different sefD variants in hens[J].Appl Enviro Microbiol,2012,78:6405-6412.
[22]Ochoa-Repáraz J,Sesma B,Alvarez M,et al.Humoral immune response in hens naturally infected withSalmonella enteritidisagainst outer membrane proteins and other surface structural antigens[J].Vet Res,2004,35(3):291-298.
[23]Li Wen-zhe,Watarai S,Iwasaki T,et al.Suppression ofSalmonella enterica serovar enteritidisexcretion by intraocular vaccination with fimbriae proteins incorporated in liposomes[J].Dev Comp Immunol,2004,28(1):29-38.
[24]Lopes V C,Velayudhan B T,Halvorson D A,et al.Preliminary evaluation of the use of thesefAfimbrial gene to elicit immune response againstSalmonella enterica serotype enteritidisin chickens[J].Avian Dis,2006,50(2):185-190.
[25]Aslanzadeh J,Paulissen L J.Adherence and pathogenesis ofSalmonella enteritidisin mice[J].Microbiol Immunol,1990,34(11):885-893.
[26]Rajashekara G,Munir S,Lamichhane C M,et al.Application of recombinantfimbrialprotein forthe specific detection ofSalmonella enteritidisinfection in poultry[J].Diagn Microbiol Infect Dis,1998,32(3):147-157.
[27]Woodward M J,Kirwan S E.Detection ofSalmonella enteritidisin eggs by the polymerase chain reactin[J].Vet Rec,1996,138:411-413.
[28]Thorns C J,Bell M M,Sojka M G,et al.Development and application of enzyme-linked immunosorbent assay for specific detection ofSalmonella enteritidisinfections in chickens based on antibodies to SEF14 fimbrial antigen[J].J Clin Microbiol,1996,34(4):792-797.
[29]朱春红,吴娟,代保英,等.肠炎沙门氏菌SEF14菌毛SEFA亚单位的克隆表达以及间接ELISA检测方法的建立[J].中国预防兽医学报,2010,32(1):44-48.
[30]段晓丽.基于SEF14菌毛的肠炎沙门氏菌特异性诊断方法的建立及应用[D].扬州:扬州大学,2012.
S852.61
B
1008-0589(2013)10-0855-04
10.3969/j.issn.1008-0589.2013.10.20
*Correspondingauthor
2012-02-16
国家自然科学基金(31101833、31101826、31270171);江苏省自然科学基金(SBK201122944);国家科技支撑计划(2012BAK17B10);教育部创新团队(IRT0978);江苏高校优势学科建设工程资助项目;扬州市农业科技攻关计划项目(YZ2011066)
厚华艳(1987-),女,内蒙古赤峰人,硕士研究生,主要从事病原微生物致病机理及免疫机理研究.
*通信作者:E-mail:yzgqzhu@hotmail.com;yzgqzhu@yzu.edu.cn
(本文编辑:赵晓岩)
