足月儿坏死性小肠结肠炎危险因素分析
2022-09-21程舒鹏陈名武潘家华
程舒鹏,陈名武,潘家华
新生儿坏死性小肠结肠炎(neonatal necrotizing enterocolitis,NEC)是一种新生儿期常见的严重的胃肠道疾病。在欧美国家,NEC的发病率为0.07%~0.10%,其中约90.0%为早产儿,足月儿约10.0%,可引起一系列严重并发症,且重度NEC有较高的致残率[1]。目前对早产儿NEC的研究较多,对足月儿NEC的研究相对较少,流行病学研究[2]表明,孕期口服药物、新生儿窒息、新生儿败血症、先天性心脏病(congenital heart disease,CHD)、胎膜早破(premature rupture of membrane,PROM)、宫内窘迫和母亲妊娠期高血压疾病等与足月儿NEC的发生高度相关。近来研究[3]表明,孕晚期羊水过少、妊娠期肝内胆汁淤积症(intrahepatic cholestasis of pregnancy,ICP)、新生儿胎粪吸入综合征(meconium aspiration syndrome,MAS)、新生儿休克和妊娠期糖尿病等也可能与足月儿NEC的发生相关。鉴于目前对足月儿中这些危险因素研究较少,且部分相关性不确定,该研究收集了中国科学技术大学附属第一医院新生儿科近5年来收治的NEC足月儿临床资料,以期为这些危险因素的研究提供最新的数据支持,并希望发现新的危险因素,为临床医师对足月NEC高危儿的防治提供新线索。
1 材料与方法
1.1 病例资料选取2016 年4月—2021年4月中国科学技术大学附属第一医院新生儿科住院的足月新生儿,胎龄≥37周,采用《实用新生儿学》第4版修正Bell分期诊断标准[4],Bell分期≥Ⅱ期。排除标准:合并遗传代谢病、先天性免疫缺陷病、消化道畸形、临床资料不全者。选取同期新生儿科的非NEC足月儿中,以个体1 ∶2匹配选择出生日期间隔<2月,胎龄差<1周,出生体质量差<100 g的足月儿为对照组。
1.2 资料选取
1.2.1一般情况 回顾性分析两组患儿的一般资料,包括胎龄、性别、出生日期、出生体质量、生产方式、发病日龄、出生地点和最终结局。
1.2.2危险因素定义 通过阅读文献选取以下NEC危险因素分析:① 晚发性羊水过少[5]:孕晚期( 28周以后),B超提示羊水指数(amniotic fluid index,AFI)≤5 cm者;② ICP[5]:无诱因的皮肤瘙痒及血清胆汁酸≥11 μmol/L,并排除其他能引起皮肤瘙痒及肝功能异常的疾病;③ MAS[4]:有明确的吸入胎粪污染的羊水病史(气管插管时声门处或气管内吸引物可见胎粪),生后不久出现呼吸窘迫,结合胸部X线改变;④ CHD[6]:依据心脏彩超结果诊断,且均有血流动力学改变者;⑤ 新生儿窒息[4]:1或者5 min Apgar评分≤7分,仍未建立有效自主呼吸,并排除其他引起低Apgar评分的病因;⑥ 新生儿败血症[4]:NEC发病前患儿有临床表现,血培养或脑脊液(或其他无菌腔液)培养阳性或临床诊断败血症成立;⑦ 妊娠期糖尿病[5]:孕期糖耐量检查异常,于正规医院确诊者;⑧ 新生儿休克[4]:新生儿休克的诊断及分度参考《实用新生儿学》,轻度为5分,中度为6~8分,重度为9~10分;⑨ 胎膜早破[5]:依据阴道窥器检查和阴道液pH值测定;⑩ 宫内窘迫[5]:依据胎心监护评分、羊水粪染、胎儿头皮血气分析pH<7.2;妊娠期高血压疾病[5]:包括妊娠期高血压、子痫前期、子痫、慢性高血压并发子痫前期及妊娠合并慢性高血压。

2 结果
2.1 一般情况共纳入NEC组43例,其中Ⅱ期34例,Ⅲ期9例,病例的纳入和排除流程见图1。对照组纳入86例,两组中纳入的CHD类型均包括房间隔缺损(atrial septal defect,ASD)和室间隔缺损(ventricular septal defect,VSD)。两组患儿胎龄、出生体质量、产妇年龄、性别、生产方式和出生地点等资料的差异无统计学意义 (P>0.05),见表1。
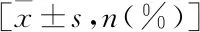
表1 NEC组和非NEC组的一般资料比较
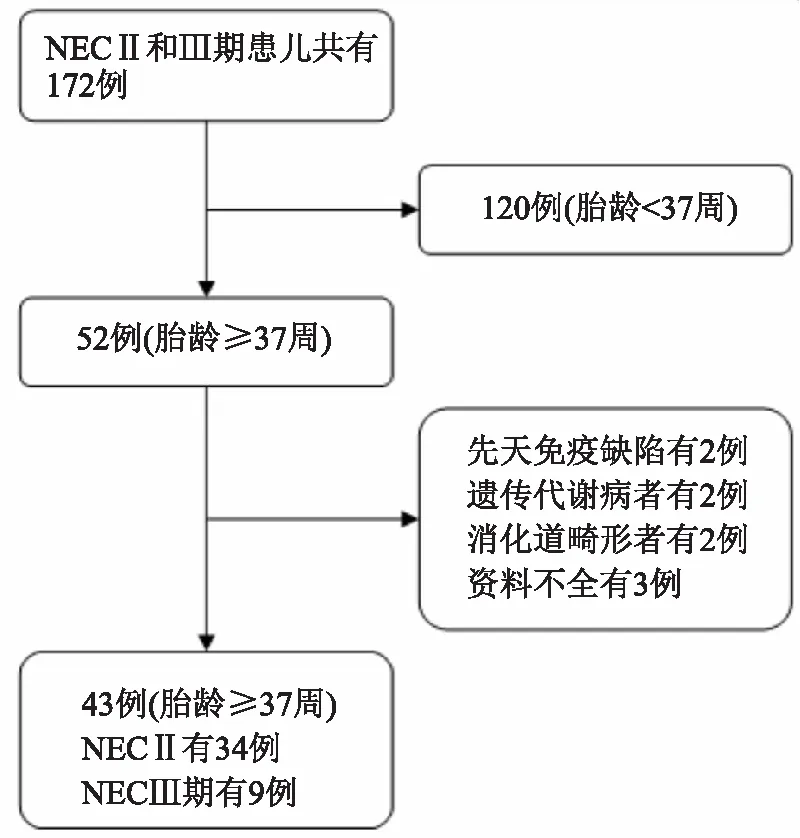
图1 NEC组患儿筛选流程图
2.2 NEC组发病日龄分布43例NEC足月儿发病在生后2~17 d,平均为6.3 d。
2.3 NEC治疗方案与结局NEC组患儿均行保守治疗(禁食、胃肠减压、应用抗生素等),其中9例肠穿孔并发腹膜炎,穿孔病变部位位于结肠7例、小肠2例,小儿外科行病变肠管切除+修补术。5例死亡,38例治疗好转后出院。
2.4 NEC发病危险因素的单因素分析晚发性羊水过少、MAS、CHD、新生儿窒息、新生儿败血症、新生儿休克、妊娠期糖尿病、胎膜早破、宫内窘迫和妊娠期高血压疾病发生率在NEC组和非NEC组间的差异有统计学意义(P<0.05),ICP发生率两组差异无统计学意义(P>0.05)。见表2。

表2 NEC发病危险因素的单因素分析[n(%)]
2.5 NEC发病危险因素的多因素分析将单因素分析有统计学意义的变量,纳入多因素Logistic回归模型,结果显示晚发性羊水过少、MAS、CHD、新生儿窒息、新生儿败血症、新生儿休克、妊娠期糖尿病、胎膜早破、宫内窘迫和妊娠期高血压疾病是NEC发生的危险因素。见表3。

表3 NEC危险因素的Logistic回归分析
3 讨论
本研究采用病例对照研究设计,分析了11项与足月儿NEC发生可能相关的危险因素,发现晚发性羊水过少、MAS、CHD、新生儿休克、妊娠期糖尿病、胎膜早破、新生儿败血症、新生儿窒息、宫内窘迫和妊娠期高血压疾病可显著增加足月儿NEC的发生风险。
本研究足月儿的平均发病日龄为6.3 d。Neu et al[1]发现足月儿NEC常发生在生后1周内,以便血症状最为多见,病情进展迅速时,出现腹胀、肠鸣音减弱后,很快出现便血、呕吐等较严重症状。
此外,本研究发现晚发性羊水过少可增加NEC的发病风险。Underwood et al[7]发现羊水是首先进入胎儿肠道内的液体,羊水含有氨基酸、蛋白质和干细胞等物质,这些营养物质可促进肠道细胞增殖分化,维持肠道免疫稳态并降低 NEC的发病率。早发性羊水过少发生在妊娠28周之前,比较少见,最常见的原因是胎儿畸形。晚发性羊水过少发生于妊娠28周之后,常见原因有胎膜早破、胎盘功能低下、胎儿宫内生长受限等[8]。结合本研究结果,提示晚发性羊水过少可能与NEC的发生有关。
MAS常见于足月儿或过期产儿,研究[9]表明,主要是由于胎粪机械性阻塞呼吸道所致,重者可出现呼吸衰竭,且中性粒细胞和促炎细胞因子的升高在该病的发病机制中发挥重要作用。在本研究中,MAS患儿肺组织产生的大量的细胞因子可能通过血液循环到达肠道,诱发肠道炎症反应并改变了肠道的保护屏障。此外,胎粪污染的羊水经消化道也可能直接诱发肠道免疫反应,从而增加NEC的风险。因此,该结果需开展前瞻性研究加以证实。
本研究再次支持,CHD和新生儿休克可增加足月儿NEC风险。Baxi et al[10]研究发现主要是此类患儿易出现体内血液分布异常,肠系膜血流供应减少,同时易产生大量的自由基,介导再灌注损伤。刘婧 等[11]研究发现,新生儿休克时,组织有效灌流量减少,在感染、缺氧等因素作用下,机体可能过多地释放多种炎症介质和细胞因子,诱发全身炎症反应综合征,使脏器组织产生损害,包括胃肠黏膜缺氧缺血、功能衰竭,甚至坏死等。另外,Stacey et al[12]研究认为,若孕母妊娠期血糖长期位于偏高水平,可能对胎儿肠道血流状态产生影响,肠道上皮细胞出现缺氧缺血性损伤,甚至变性、坏死,增加NEC的发病率,故妊娠期糖尿病可能与足月儿NEC的发生相关。
此外,本研究成果也支持新生儿窒息、宫内窘迫、妊娠期高血压疾病为足月儿NEC发生的危险因素[13-14]。Neu et al[13]研究表明,上述因素均可导致围生期缺氧缺血,改变了体内血流分布状态,肠系膜血供减少,肠道上皮细胞变性、坏死。此外,有研究[14]表明,胎膜早破时间>18 h,新生儿败血症的发生率明显增加,此时细菌在机体内大量增殖并产生毒素,并随血液循环系统到达肠道,在肠道产生大量细胞因子,导致机体促炎和抗炎信号失衡,损伤肠道屏障功能。
本研究同时纳入了ICP因素,研究[15]表明ICP可增加早产儿NEC发病风险,但未发现其对足月儿NEC 发病产生影响,可能与样本量较小以及部分孕妇口服降胆汁酸药物有关。因此,后期有必要开展前瞻性研究加以验证。
本研究是单中心回顾性研究,仅纳入了NEC≥Ⅱ期的足月儿,样本量较小,且信息来源于病案系统,存在一定的局限性,后续将扩大样本量多中心收集资料分析。
