1632例老年患者使用氨甲环酸注射剂的不良反应报告分析
2022-09-20闫峻峰吴承云邹林珂吴行伟成都市第五人民医院四川成都630四川省医学科学院四川省人民医院药学部四川成都6007电子科技大学医学院个体化药物治疗四川省重点实验室四川成都6007四川省药品不良反应监测中心四川成都6007
刘 静,闫峻峰,兰 姗,吴承云,边 原,邹林珂,吴行伟(.成都市第五人民医院,四川 成都 630;. 四川省医学科学院·四川省人民医院药学部,四川 成都 6007;3. 电子科技大学医学院,个体化药物治疗四川省重点实验室,四川 成都 6007;.四川省药品不良反应监测中心,四川 成都 6007)
氨甲环酸又名凝血酸,是一种人工合成的赖氨酸 类似物,因其止血效果显著,在临床常用于急慢性、局限性或全身性原发性纤维蛋白溶解亢进所致的各种出血[1]。随着该药的广泛应用,国内外陆续有氨甲环酸致药品不良反应(adverse drug reaction,ADR)的病例报道和综述,但鲜有系统研究。笔者通过检索四川省药品不良反应监测中心数据库,发现仅有2例氨甲环酸片剂所致老年患者ADR报告,故本研究着重探讨65岁及以上老年患者使用氨甲环酸注射剂所致ADR的特点和临床表现,以期为老年患者安全用药提供参考。
1 资料和方法
1.1 资料来源
从四川省药品不良反应监测中心数据库中提取2013年1月 – 2020年5月上报的65岁及以上老年患者使用氨甲环酸注射剂导致ADR的报告,药品包括氨甲环酸氯化钠注射液、氨甲环酸注射液、注射用氨甲环酸。纳入患者性别、年龄、用药名称、ADR等关键信息完整的报告进行分析。
1.2 方法
采用Excel软件记录纳入的ADR报告信息,包括患者年龄、性别、给药途径、剂型以及ADR累及系统/器官等,对同一报告累及多个系统/器官或涉及多种临床表现的,分别计算例次。使用SPSS软件对结果进行统计分析。
2 结果
2.1 ADR报告基本情况
共纳入ADR报告1632份,主要为氨甲环酸氯化钠注射液所致ADR报告(77.70%),1632份报告中,新的ADR报告315份(19.30%),严重ADR报告35份(2.14%),详见表1。
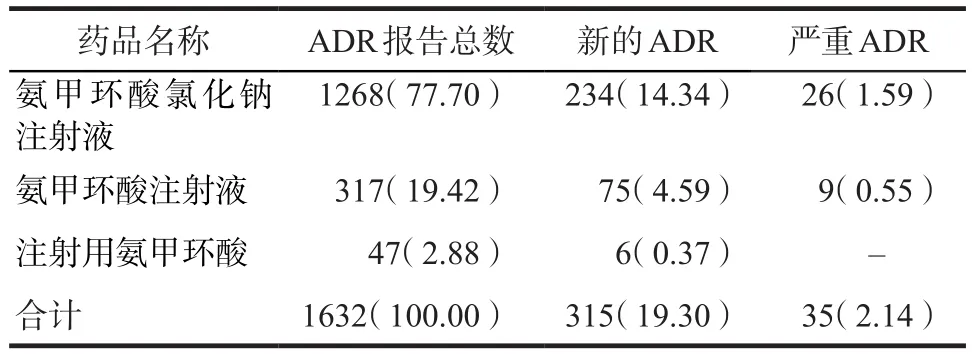
表1 ADR报告基本情况.份(%)Tab 1 Basic information of ADR reports. case(%)
2.2 患者基本信息
发生ADR的患者年龄以65 ~ 75岁最多(71.02%),显著高于其他年龄段(P< 0.05)。男性753例,女性879例,男女比例为0.86∶1,但患者性别无统计学差异(P> 0.05),详见表2。
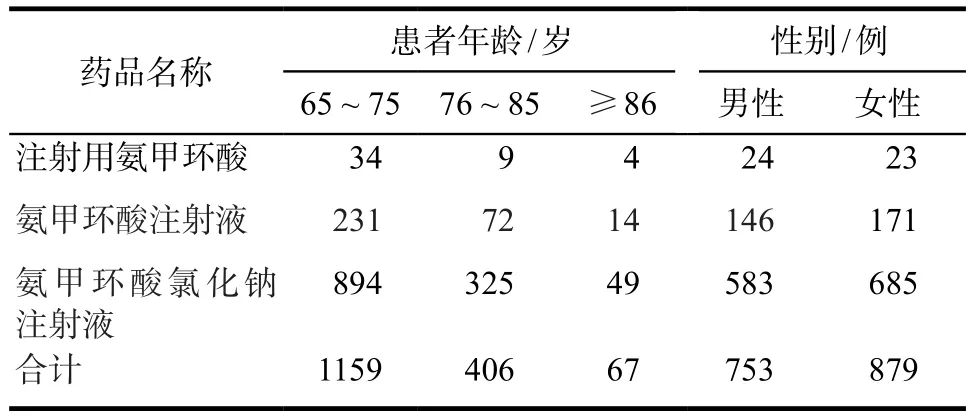
表2 患者基本信息Tab 2 Basic information of patients
2.3 药品信息及给药途径
1268例患者所用氨甲环酸氯化钠注射液为大容量注射液(100 mL),317例患者所用氨甲环酸注射液为小容量注射液(2 mL、5 mL、10 mL),47例患者所用注射用氨甲环酸为粉针剂(0.5 g、1.0 g);给药途径共3种,静脉滴注占比最多(1604份,98.28%),其次为静脉注射(26份,1.59%),2份报告给药途径为泵注。
2.4 药品销售额与ADR报告数量
通过药智网数据库查询3种药品销售情况(表3),发现氨甲环酸氯化钠注射液销售额远大于氨甲环酸注射液和注射用氨甲环酸,且ADR报告也多于氨甲环酸注射液和注射用氨甲环酸(表4);氨甲环酸注射液销售额小于注射用氨甲环酸,但收到的ADR报告数量却多于注射用氨甲环酸。
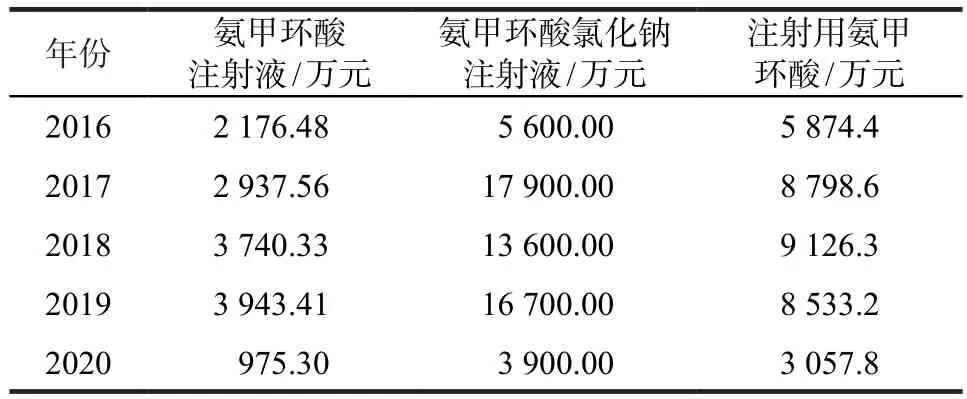
表3 3种药品的销售额Tab 3 Sales situation of three drugs
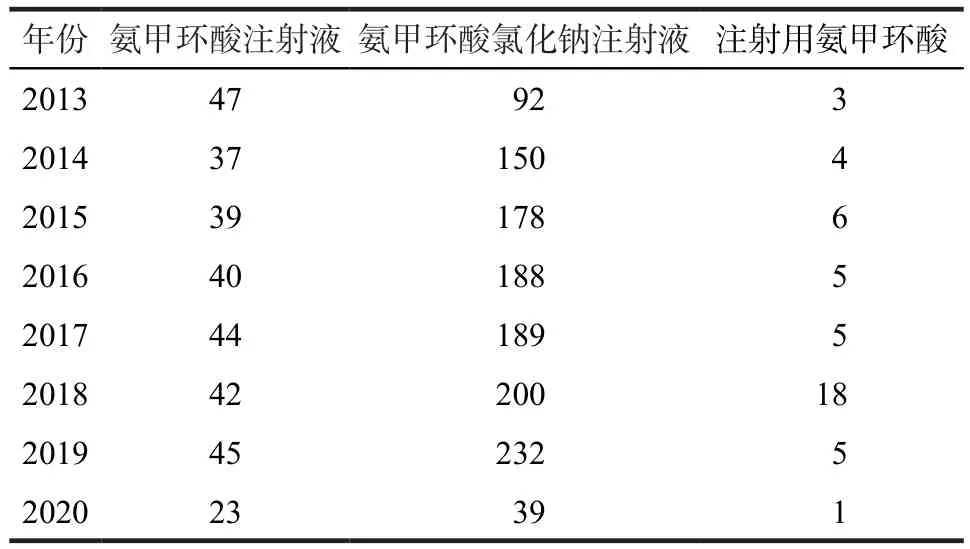
表4 3种药品的ADR报告数量.例Tab 4 Number of ADR reports of three drugs. case
2.5 ADR累及系统/器官及临床表现
1632份ADR报告中,氨甲环酸氯化钠注射液ADR累及14个系统/器官,氨甲环酸注射液ADR累及10个系统/器官,注射用氨甲环酸ADR累及7个系统/器官,3种药品在不同系统/器官的ADR发生率有一定差异。氨甲环酸注射剂累及系统/器官前10位如表5所示,听觉和前庭功能损害、泌尿系统损害、心率及心律紊乱ADR报告数各1份。
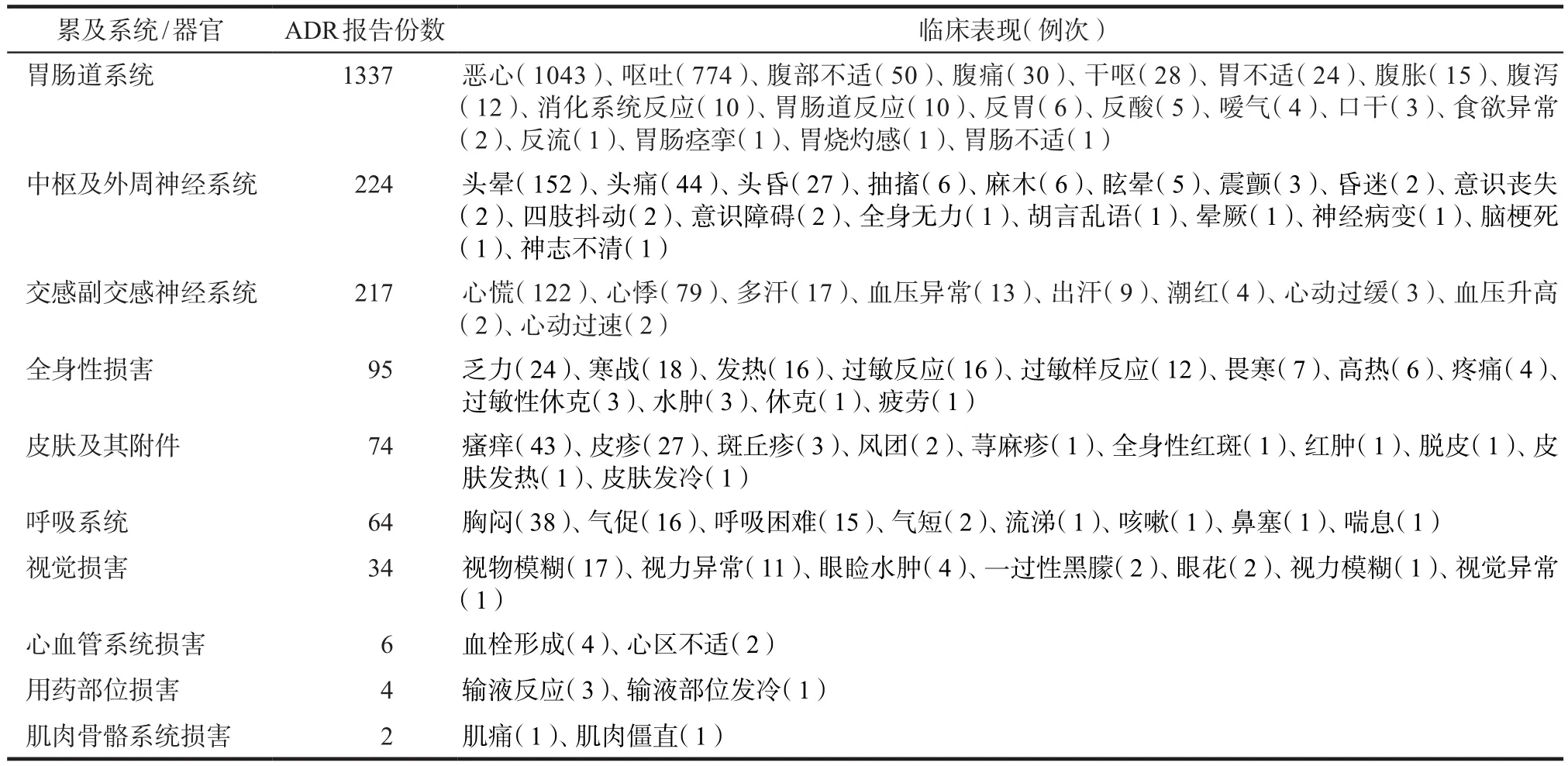
表5 ADR累及系统/器官及临床表现Tab 5 Systems/organs involed in ADR and clinical manifestations
2.6 新的ADR
1632份ADR报告中,新的ADR报告315份,其中氨甲环酸氯化钠注射液234份,氨甲环酸注射液75份,注射用氨甲环酸6份,新的ADR累及系统/器官见表6。
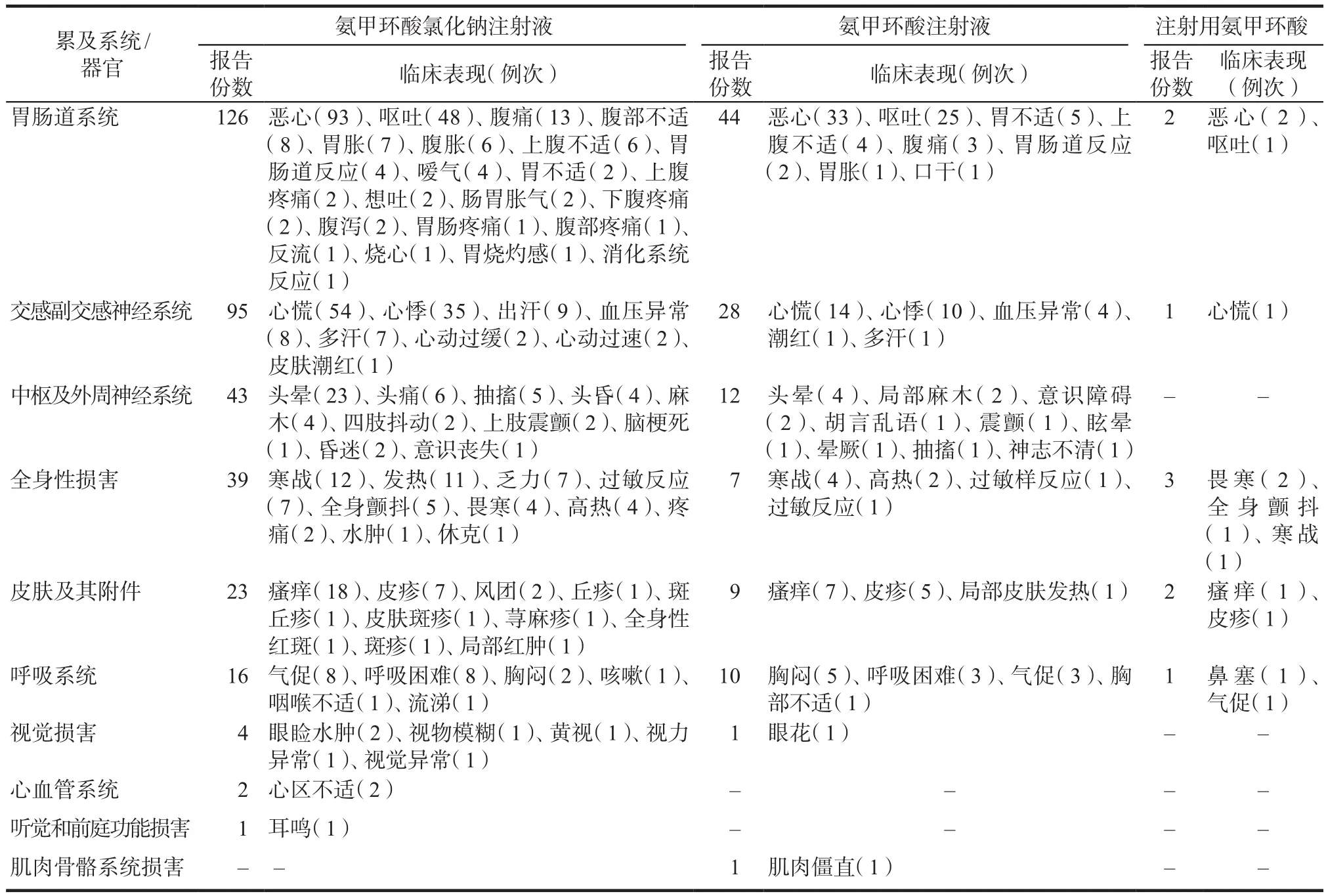
表6 新的ADR累及系统/器官及临床表现Tab 6 Systems/organs involed in new ADR and clinical manifestations
3 讨论
3.1 说明书中未提及的ADR
说明书中详细罗列了氨甲环酸注射剂致胃肠道系统、中枢及外周神经系统、视觉损害等系统/器官的ADR,提醒临床关注其ADR并及时应对,但仍有一些研究结果显示的ADR在说明书中并未提及。本研究中发现有患者存在过敏(样)反应及相关症状,相关文献也记载了氨甲环酸氯化钠注射液可致过敏反应或引起过敏性休克[2-3],氨甲环酸片剂说明书中提及了过敏反应症状,美国FDA氨甲环酸氯化钠注射液说明书中也提及氨甲环酸可能存在包括过敏反应在内的超敏反应[4-6]。美国FDA氨甲环酸氯化钠注射液说明书中提示该药可引起癫痫发作,包括局灶性和全身性癫痫。本研究中虽未有癫痫的不良反应报告,但有患者出现抽搐、震颤、四肢抖动的癫痫类症状,查询国内文献发现有氨甲环酸氯化钠注射液致四肢强直反应的报道[7-8],有文献[9]提到氨甲环酸相关性癫痫的危险因素包括高龄、女性以及应用高剂量氨甲环酸。新的ADR报告中患者出现的心慌、心悸等交感副交感神经系统损害并未在说明书中提及,但此系统的不良反应发生率位居前二,且查阅文献资料发现有心慌的不良反应出现[10-11],这提示说明书的警示内容可能不全,提示临床老年患者在用药时可能发生交感副交感神经系统损害。虽然说明书和文献中均未提到氨甲环酸可致肝胆系统损害,但本研究中发现有患者累及肝胆系统,这提示有肝功能损害的患者在使用氨甲环酸时可能加重肝损害。以上ADR提示现有说明书对临床使用警示作用可能不到位,需进一步研究补充,从而提醒医务人员在用药时做好预防措施,减少ADR的发生。
3.2 不同氨甲环酸注射剂ADR发生情况对比分析
氨甲环酸对热稳定,但易被酸、碱破坏,极易被氧化。药典中对于氨甲环酸原料药中Z-异构体杂质限度要求是不超过0.2%[12]。氨甲环酸属于离子敏感性药物,其注射剂在生产过程中的配液环节通常在不锈钢罐中进行。造成该药质量不合格的原因为氨甲环酸与重金属发生络合反应,由于金属离子存在,造成氨甲环酸顺式-对氨甲基环己烷甲酸及其他杂质增加,影响产品质量,增加用药安全隐患[13]。
本研究发现,氨甲环酸氯化钠注射液导致ADR的报告数量显著多于其他两种药品,可能原因为:氨甲环酸氯化钠注射液的销售量大于其他两种药品;另一方面,在生产过程中,Cl–可能增加杂质的产生。氨甲环酸氯化钠注射液较氨甲环酸注射液的主要成分多了氯化钠,该药说明书中指出,静脉滴注应以5% ~10%葡萄糖溶液稀释,而未提到用氯化钠溶液稀释,推测可能是溶媒的原因导致氨甲环酸氯化钠注射液ADR发生率高。有研究[14]指出304L不锈钢材质若处于含有Cl–的溶液中,其材质组成成分Cr3+很容易被腐蚀游离出来,从而与Cl–结合生成CrCl3。氨甲环酸氯化钠注射液相比氨甲环酸注射液成主要成分含有Cl–,易在溶液中生成CrCl3,而Cr3+属于重金属离子,可与氨甲环酸发生络合反应,造成注射液中杂质增加,影响产品质量。
综上所述,发生氨甲环酸注射剂所致ADR的患者年龄在65 ~ 75岁居多,但在性别方面无显著差异,ADR可致老年患者多个系统/器官损害,且根据ADR报告结果显示3种药品可能存在说明书中未提及的ADR,现有说明书对临床用药的警示作用不充分,需进一步研究补充。临床治疗中,老年患者用药剂量应进行个体化调整。研究显示氨甲环酸氯化钠注射液所致ADR报告数远多于氨甲环酸注射液和注射用氨甲环酸,这可能与其生产工艺过程易产生杂质有关,也提示相关生产企业可考虑优化生产工艺,提高药品质量,减少药品使用过程中因质量而产生ADR的概率,保证患者用药安全。
