吉非替尼对晚期非小细胞肺癌化疗失败后的临床观察
2022-09-19张秋丽
张秋丽
肺癌在全球范围内发病率、死亡率均位居第一,主要起源于支气管黏膜或气管,尽管无传染性,但呈现出明显的家族聚集特点及遗传易感性,根据病理特点如病灶位置、转移情况等的不同可划分为不同类型,非小细胞肺癌(non-small cell lung cancer,NSCLC)所占比重高,80%以上肺癌患者属于NSCLC[1]。NSCLC在早期不容易被发觉,主要表现为咳嗽、痰中带血,容易被忽视,多数患者体检时发现,往往已经进入中晚期,部分甚至转移,已经不适合手术切除治疗,治疗难度大、预后差[2]。NSCLC病因机制复杂,考虑与环境、遗传、免疫及营养等多种因素有关。通常对于晚期NSCLC患者化疗是可靠方案,近年来新型化疗药物的出现,NSCLC治疗有了更多可能性,但基于患者个体差异的影响及耐受性不同,5年生存率仍较低,化疗失败率高[3]。随着近年来医疗卫生技术的进步及分子靶向治疗的进展,吉非替尼在晚期NSCLC治疗中得以应用,其作为一种表皮细胞生长因子受体(epidermal growth factor receptor,EGFR),能够对肿瘤血管生成起到抑制作用,通过对酪氨酸激酶的选择性抑制,使得该信号传导系统被阻断,将恶性肿瘤形成中的重要环节切断,促进肿瘤凋亡。为探究其应用效果,选取2018年12月—2020年12月内蒙古自治区赤峰市医院肿瘤内科共收治120例晚期NSCLC化疗失败患者,对研究结果进行汇总,详细见如下报告。
1 资料与方法
1.1 一般资料
2018年12月—2020年12月内蒙古自治区赤峰市医院收治NSCLC患者,共计120例,均为晚期患者,且经过化疗治疗失败,所有患者入院后编号,按照随机数字表分为n=60的两个组别。观察组:男(34例)、女(26例),年龄42~77岁,平均(59.63±4.02)岁,病理类型:鳞癌4例,腺癌35例,腺鳞癌21例;TNM分期:ⅢB期24例,Ⅳ期36例。对照组:男35例、女25例,年龄41~78岁,平均(59.53±4.09)岁,病理类型:鳞癌3例,腺癌38例,腺鳞癌19例;TNM分期:ⅢB期25例,Ⅳ期35例。两组差异无统计学意义(P>0.05),有可比性。
1.2 纳入与排除标准
纳入标准:(1)胸部X线、MRI检查诊断确诊为NSCLC,且均处于晚期[4]。(2)患者表示知情,自愿配合,医学伦理委员会许可。(3)患者年龄41~78岁,可正常交流;(4)经过化疗评估显示治疗失败;(5)能够准确回答医师问询,沟通交流正常,配合度佳。排除标准:(1)脏器受到严重损害或衰竭;(2)精神意识混乱、不清;(3)同时合并其他类型恶性肿瘤;(4)不配合调查或用药,拒绝沟通;(5)免疫缺陷及凝血障碍;(6)经检查存在其他肺部相关疾病;(7)资料缺失、不全;(8)药敏试验显示患者过敏。
1.3 方法
对照组:给予多西他赛(江苏奥赛康,国家药准字H20080443,规格:1 mL:40 mg)治疗,治疗前1天给予患者地塞米松口服,16 mg/次,1次/d,连用3 d,给予多西他赛静脉滴注,药物用量以75 mg/m2为宜,静脉滴注1 h,21 d/次。观察组:给予吉非替尼(厂家正大天晴药业,国家药准字H20193135,规格:0.25 g/片)口服治疗,给药剂量为每次250 mg,每天进行1次治疗。治疗时间为3个月。治疗期间监测两组患者有无不良反应发生,并积极进行处理,针对不良反应严重且无法耐受者应对用药剂量做出相应的调整或暂停治疗。
1.4 观察指标
对患者进行免疫功能及生活质量评估,做好记录,统计分析其改善程度,采集患者肘部静脉血,测定肿瘤标志物水平,观察实验室指标改善情况,判断疗效,监测不良反应,记录并组间比较。(1)肿瘤标志物水平检测。需要清晨空腹采血,离心处理后(5 min)分离血清,尽早完成检测。血清癌胚抗原(carcinoembryonic antigen,CEA)指标检测方法为化学发光免疫法;采用电化学发光检测法对血清细胞角蛋白19片段(cytokeratin-19-fragment,CYFRA21-1)水平予以检测,糖类抗原125(carbohydrate antigen 125,CA125)采用ELISA法检测。免疫功能指标采用ReLIA II-多功能免疫检测仪(北京海富达科技有限公司)检测。(2)生活质量采用QOL-75量表,围绕躯体健康、心理健康、物质生活、社会功能4项指标进行评估,每项赋分总分100分,生活质量越好对应的分值越高。(3)疗效标准。完全缓解(complete remission,CR):各项症状未再出现,临床指标经检测发现均已正常,靶病灶消失,未出现新增病灶,1个月以上无进展。部分缓解(partial remission,PR):经治疗症状较入院时有改善,但尚未完全恢复,靶病灶减小,1个月以上无进展;疾病稳定(stable disease,SD):靶病灶缩小但未达到PR。疾病进展(progressive disease,PD):靶病灶增加,或可见新病灶的出现。总有效率=(完全缓解例数+部分缓解例数)/总例数×100%[5]。
1.5 统计学处理
肿瘤标志物水平、生活质量评分等以及临床疗效等数据均应用SPSS 22.0软件进行处理,计量资料表示为(±s),采用t检验;计数资料表示为n(%),采用χ2检验,P<0.05表示差异有统计学意义。
2 结果
2.1 两组患者肿瘤标志物水平比较
各项肿瘤标志物CEA、CYFRA21-1、CA125参数经统计学软件处理显示治疗后均较治疗前有所降低,差异有统计学意义(P<0.05),组间比较治疗前两组差异无统计学意义(P>0.05),治疗后观察组均低于对照组,差异有统计学意义(P<0.05)。见表1。
表1 两组患者肿瘤标志物水平比较(ng/mL,±s)

表1 两组患者肿瘤标志物水平比较(ng/mL,±s)
注:t1/P1值表示两组治疗前比较,t2/P2值表示两组治疗后比较。
2.2 两组免疫功能指标比较
检测患者免疫功能指标,可以发现治疗后两组CD4+、CD4+/CD8+提高,CD8+降低,统计学计算显示差异有统计学意义(P<0.05),统计学软件计算组间差异显示治疗前差异无统计学意义(P>0.05),治疗后差异比较有统计学意义(P<0.05),具体见表2。
表2 两组免疫功能指标比较(±s)

表2 两组免疫功能指标比较(±s)
注:t1/P1值表示两组治疗前比较,t2/P2值表示两组治疗后比较。
2.3 两组生活质量评分比较
患者各项生活质量评分在治疗前差异有统计学意义(P<0.05),组间比较治疗前差异无统计学意义(P>0.05),治疗后观察组较对照组提高显著,差异有统计学意义(P<0.05),见表3。
表3 两组生活质量评分比较(分,±s)
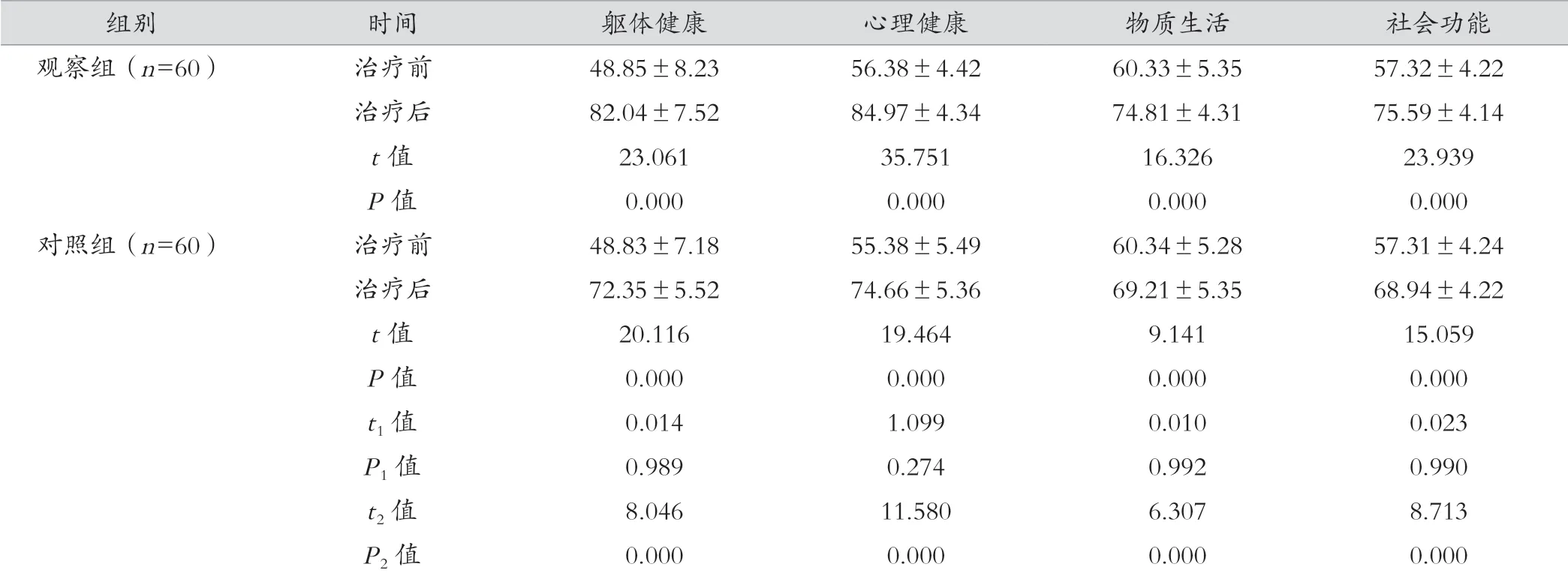
表3 两组生活质量评分比较(分,±s)
注:t1/P1值表示两组治疗前比较,t2/P2值表示两组治疗后比较。
2.4 两组患者治疗效果比较
患者总缓解例数比较,观察组(n=50)多于对照组(n=40),组间差异经统计学处理差异有统计学意义(P<0.05),见表4。
2.5 两组患者不良反应发生率比较
两组患者治疗期间均有不良反应发生,但观察组仅占11.7%,较对照组低,差异有统计学意义(P<0.05),不良反应详细类型及占比情况见表5。
3 讨论
NSCLC是老年多发病,病因机制复杂,发病率逐年攀升[6]。文献报道[7-8],肺部血供丰富,主要来源于支气管与肺循环,当出现NSCLC后会转移至血道,但在临床上缺乏典型的表现,不利于早期检出。当发展到一定程度会使得心、肾等系统受累,错失了手术最佳时机,为临床治疗增加了难度,5年生存率低。化疗是临床治疗晚期NSCLC的常见手段,主要以含铂类化疗方案为主,其对于患者部分症状有效,可使得癌细胞转移受到不同程度抑制,但药物毒副作用大,容易出现胃肠道反应、脱发以及皮疹等不良反应,部分患者由于无法耐受药物不良反应抗拒治疗,导致化疗失败[9]。
临床针对化疗失败晚期NSCLC患者多强调延长患者生存期、提高生活质量。通常,化疗失败后多选择多西他赛、长春瑞滨等二线化疗药物治疗,但药物不良反应大,患者经过一次失败治疗,接受度不高,效果不甚理想[10]。以往研究[11]报道,晚期NSCLC患者多存在EGFR表达量增加,EGFR酪氨酸激酶家族能够在细胞内传导细胞外信号,在阻断细胞凋亡方面具有一定的作用,能够促进肿瘤细胞活性及侵袭性的增强,基于这一机制给予EGFR及其信号传导的靶向治疗能够实现对肿瘤细胞增殖及血管生成的抑制。此次研究观察组患者接受的是吉非替尼治疗,从治疗结果看,观察组总有效率为83.3%,高于对照组,体现了该治疗方案的有效性。作为EGFR酪氨酸激酶抑制剂,吉非替尼能够与ATP产生竞争性结合,进而实现对EGFR细胞中酪氨酸激酶域自磷酸化的抑制,使得下游信号传递被阻断,在抑制肿瘤血管生成、细胞增殖方面有着显著的作用[12]。吉非替尼作用于机体,可使得人肿瘤细胞衍生系肿瘤生长受到显著的抑制,在实施放化疗治疗及激素药物治疗时,抗肿瘤活性能够得到显著提升,应用于晚期NSCLC患者,症状改善更明显。以往有学者[13]在研究中发现针对一线化疗失败的晚期NSCLC患者给予吉非替尼分子靶向治疗,患者2年生存率能够达到50%~60%。通过安全性分析,发现该药物细胞毒性相对较轻,不良反应多为腹泻、恶心等,且大多为Ⅰ级、Ⅱ级,患者可耐受。作为一种酸性糖蛋白,CEA主要来源于人类胚胎抗原决定簇,在3~6个月胎儿消化系统及泌尿系统腺体细胞中有着较高的表达。成人体内或良性疾病患者仅存在较少表达,多在10 ng/mL以下。NSCLC患者伴随CEA高表达,广泛分布于血液、淋巴系统等。作为细胞角蛋白家族成员,CYFRA21-1在肿瘤细胞与上皮细胞有着较高的表达,多为不溶性,在上皮细胞恶化过程中会受到蛋白酶的激活作用,大量被释放于血液,会呈现出高表达,与患者预后密切相关,且能够反映出疾病严重程度。CA125主要来源于胚胎期体腔上皮,但表达量较少。健康人中血CA125整体表达低,能够起到润滑、抗感染等作用,可有效抵御异物。当出现恶性肿瘤尤其是输卵管癌、卵巢癌或肺癌后会导致CA125大量分泌,呈现出高表达。本研究观察组患者治疗后肿瘤标志物CEA、CYFR19、CA125水平均降低,与对照组组间比较差异有统计学意义(P<0.05),表明经过该方案治疗,患者肿瘤标志物相关指标能够得到更为显著的改善。晚期NSCLC患者多伴随免疫功能受损,增加了患者的身心不适,降低生活质量[14-15]。为观察不同治疗方案效果,两组患者均接受免疫功能检测,可见两组均改善,治疗前后观察组差值更大,提示其获益更大,改善更为明显。在生活质量方面,两组治疗后尽管均有所提升,但观察组较对照组提升明显,提示应用吉非替尼治疗能够提高患者免疫功能,有利于生活质量的改善。学者张洪涛等[16]在研究中将92例铂类方案化疗失败的中晚期非小细胞肺癌患者随机分为试验组与对照组,分别给予吉非替尼与培美曲塞治疗,结果显示试验组患者治疗后肿瘤标志物MMP-7以及MMP-9指标均降低,低于对照组,两组总有效率比较,试验组为84.78%,高于对照组的78.26%,差异有统计学意义(P<0.05),与本研究结果一致。但在用药安全性方面,试验组与对照组差异无统计学意义(P>0.05),与本研究存在一定的差异,考虑与样本收集量有关。本研究尽管两组均有不良反应发生,但观察组明显较低,提示该药物治疗安全性。需要注意的是,吉非替尼尽管具有良好的靶向性,且细胞毒性少,但在接受治疗过程中部分患者会出现耐药,治疗后存在一定的复发几率。长时间应用吉非替尼可能存在一定的耐药性[17],因此,在用药方案方面应掌握好时间间隔,尽可能采用隔天服用的方式,以减少耐药,同时降低患者经济负担,减少疾病的复发,提高患者生活质量。但受现有条件限制,样本小,且未能长远跟踪随访,远期效果尚不明确,应进行大量试验观察,优化试验方法与流程,加强质量控制,获得可靠的结果,为临床提供数据支持。
综上所述,文章体现了中华医学会肺癌临床诊疗指南的相关标准,将吉非替尼应用于晚期NSCLC化疗失败患者,有利于肿瘤标志物水平及生活质量的改善,安全可靠,此研究结果能够为NSCLC化疗失败患者后期标准制定提供借鉴,可予以推广。
