4D-CT联合呼吸门控技术应用于肺癌立体定向体部放疗的临床研究
2022-09-03孙晨楠毛海燕魏本飞刘申香
孙晨楠, 毛海燕, 魏本飞, 韩 晓, 刘申香, 袁 昕
(1. 扬州大学附属医院 肿瘤科, 江苏 扬州, 225100; 2. 扬州大学医学院, 江苏 扬州, 225100)
近年来,肺癌发病率逐年上升,已成为当前最常见的恶性肿瘤之一。据国家癌症中心的流行病学调查[1]显示, 2020年全国新发肺癌病例约220万,死亡病例约180万。虽然放疗技术日益成熟,并逐步进入精确放疗时代,但是呼吸运动仍是一个影响疗效的主要因素。呼吸门控技术联合4D-CT是控制胸部肿瘤呼吸运动问题的常见方法[2], 能够减少放疗过程中呼吸运动对靶区的影响。本研究探讨4D-CT联合呼吸门控技术应用于肺癌立体定向体部放疗的效果,现报告如下。
1 资料与方法
1.1 一般资料
将2019年6月—2021年12月扬州大学附属医院肿瘤科32例经病理证实的转移性或原发性肺癌患者(共54个病灶)纳入本研究,其中男26例,女6例,平均年龄(68.78±8.33)岁,转移性肺癌15例,肺内转移病灶数量2~4个。采用Varian Eclipse15.5制订计划,利用立体定向放疗设备Varian IX实施放射治疗。所有患者均签署书面知情同意书。纳入标准: 具有病理学证据的原发性或转移性肺癌者; 无放疗禁忌证者; 预计生存期≥3个月者; 依从性好者。排除标准: 存在放疗禁忌证者; Kamofsky功能状态(KPS)评分<70分者; 预计生存期<3个月者; 依从性差者。
1.2 治疗设备
治疗设备包括实时体位监测系统(RPM)、美国Varian Eclipse15.5系统、美国Varian IX直线加速器和西门子64排大孔径放疗专用CT模拟机。
1.3 靶区定义
内靶区(ITV)是基于呼吸运动造成的影响提出的概念,以减少脱靶或漏靶的现象[3]。本研究中因4D-CT的作用,将ITV视为临床靶区与呼吸运动引起内边界变化范围之和。计划靶区(PTV)包括ITV及摆位误差产生的总范围。所有的ITV根据所在部位进行外扩形成PTV。肺上部肿瘤均匀外放0.3 mm; 肺中部肿瘤头脚方向均匀外放0.5 cm, 左、右、前、后方向均匀外放0.3 cm; 肺下部肿瘤头脚方向均匀外放0.8 cm, 左、右、前、后方向均匀外放0.5 cm。
1.4 定位与图像扫描
为保证放疗效果,患者定位前先进行严格的呼吸训练,从而保持节律一致的呼吸运动。采用立体定向体部放疗(SBRT)立体固定架固定体位,患者双手交叉,抱肘置于额部,取仰卧位,在红外线摄像头辅助下勾画激光定位线,确保其位于照射野内。每位患者均采用4D-CT进行图像采集,扫描范围上至环甲膜,下至肝下缘,平静呼吸状态下以层距3 mm进行增强扫描。图像采集的同时,在患者上腹部放置呼吸监控装置监控患者呼吸。启动呼吸门控系统,患者在技师的指导下完成呼吸门控图像采集,保证采集到的每层图像均带有时相标签,将所得CT数据组通过4D软件程序进行处理,共得到10组CT图像。
1.5 计划设计
所有患者10组图像上均需勾画GTV, 将10组图像融合成全时图像,得到常规放疗计划的ITV1, 通过一定范围的外扩形成PTV1, 用于模拟常规放疗下的CT图像。选取呼吸幅度较小的30%~70%的图像融合,得到ITV2, 按上述方式外扩形成PTV2, 从而形成呼吸门控图像。放疗技术采用容积旋转调强放射治疗(VMAT)技术进行SBRT, 对于双肺多发的病灶,包括肿瘤间距>5 cm的病灶,均采用多中心、多靶点照射。所有患者均采用SBRT、大分割,计划给予6兆伏高能X线(6MV-X)照射PTV,放疗总剂量为60 Gy, 1周5次。由放射物理师与临床医师共同确认治疗计划,将计划传输至放疗机房。所有患者均行呼吸门控计划。每次治疗前先行加速器自带的锥形束计算机断层扫描(CBCT)扫描,根据骨性标志纠正摆位误差,再行RPM实时监控呼吸运动,密切注意PTV轮廓与影像中肿瘤的位置关系,若三维方向的摆位误差>2 mm, 则调整至允许范围后实施放射治疗。见图1。
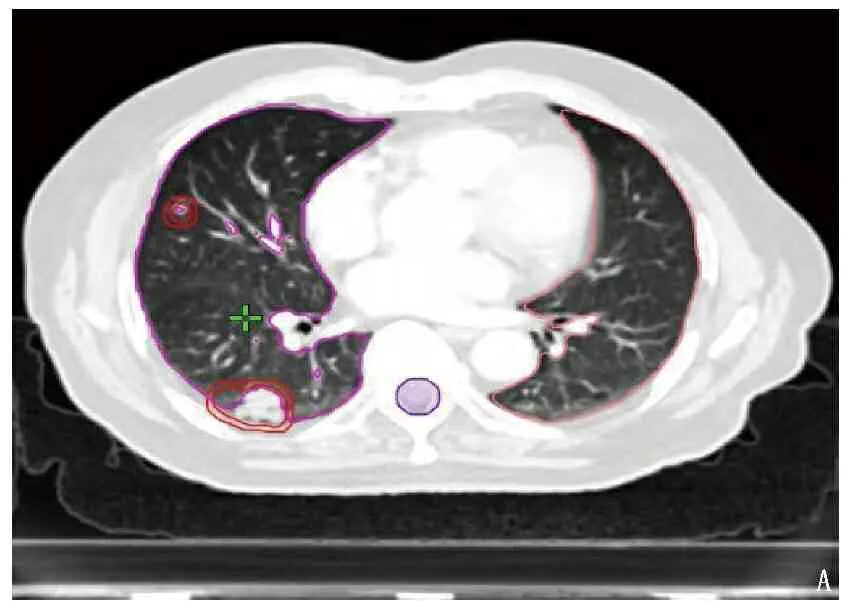
1.6 观察指标
比较2种计划的靶区体积,观察2种计划靶区剂量,包括靶区接受的平均剂量(Dmean)、靶区接受的最小剂量(Dmin)、靶区接受的最大剂量(Dmax)、95%PTV接受的剂量(D95)、50%PTV接受的剂量(D50)和5%PTV接受的剂量(D5)。比较2种计划的危及器官体积及剂量,包括危及的双肺体积和脊髓体积,正常肺组织接受放射剂量高于20 Gy照射的体积百分比(V20)、正常肺组织接受放射剂量高于5 Gy照射的体积百分比(V5)、双肺接受的平均剂量(MLD)、脊髓接受的Dmax和脊髓1 cm3体积接受的剂量(D1cc)。所有患者治疗结束3个月内随访观察放射性反应发生情况及疗效。
1.7 统计学方法
本研究采用SPSS 19.0软件对数据进行统计分析, 2种计划的ITV、PTV靶区体积及剂量差异均采用配对样本t检验。P<0.05为差异有统计学意义。
2 结 果
2.1 2种计划的靶区体积比较
门控计划的靶区体积小于常规计划,差异有统计学意义(P<0.001), 见表1。

表1 2种计划的靶区体积比较 cm3
2.2 2种计划的靶区剂量比较
呼吸门控计划D95高于常规计划,差异有统计学意义(P=0.007); 呼吸门控计划的适形指数(CI)更接近1,靶区适形性更好,差异有统计学意义(P=0.005), 见表2。

表2 2种计划的靶区剂量比较
2.3 2种计划的危及器官体积及剂量比较
呼吸门控计划的MLD小于常规计划,差异有统计学意义(P=0.001); 呼吸门控计划的V20、V5与常规计划比较,差异有统计学意义(P=0.009); 门控计划中的脊髓D1cc小于常规计划,差异有统计学意义(P=0.024), 但是2种计划的危及器官体积比较,差异无统计学意义(P>0.05), 见表3。

表3 2种计划的危及器官体积及剂量比较
2.4 随访结果
本研究采用实体瘤疗效评价标准(RECIST1.1)评估患者疗效,所有患者治疗结束3个月内随访观察放射性反应发生情况及疗效。采用门控计划的32例患者中, 1级放射性肺炎6例, 2级放射性肺炎2例,发生率为25.0%, 未出现需要临床干预的不良反应。所有患者治疗总有效率为65.6%。见图2。
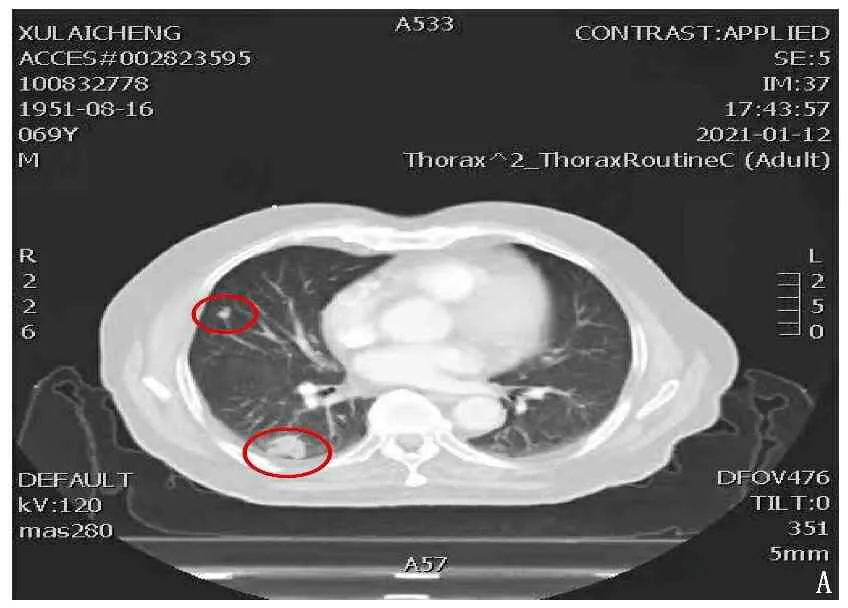
3 讨 论
肺癌患者的综合治疗极其重要,往往需要化疗、靶向治疗和免疫治疗等手段控制肿瘤生长,之后再进行局部治疗。肺多发转移瘤意味着患者失去了手术治疗的机会,因此放射治疗是该类患者尤为重要的治疗方法。本研究纳入32例肺癌患者, 15例患者存在多发肺转移瘤。研究[4-5]表明,直径小于5 cm的病灶最适合行立体定向放疗,因疗程短且局部控制率高,其在临床上被广泛应用。然而SBRT的前提是必须保证每次治疗位置相对固定,但呼吸运动、扫描方式和体位固定方法均会影响治疗位置。因此,很多学者采用4D-CT扫描方式、真空垫联合热塑膜等方法来减少摆位误差[6-7], 但这些方法仅能解决单病灶的难题,对于多发肺转移瘤的患者,尤其是双肺多发和肿瘤间距较大者采用常规放疗计划,往往需要多次放射治疗,多次摆位,延长治疗总时间,导致患者失去治疗信心[8]。使用单个中心治疗多个病灶,会出现靶区剂量分布不均,额外增加对正常组织的照射,影响SBRT的治疗效果[9], 因此需要一种多中心、多靶点的放疗技术对此类患者进行治疗。本研究采用4D-CT联合呼吸门控技术对多发肺转移瘤进行立体定向治疗,使用多中心、多靶点的动态技术照射,旨在精确追踪多个肿瘤位置,实现单次治疗对多个病灶进行大分割照射,从而缩短治疗疗程。
呼吸门控技术的最大局限性在于延长患者单次治疗时间。研究[10-11]提出采用呼吸门控技术结合非均整模式或增大剂量传递率等方法改善呼吸门控技术,而呼吸门控计划对多发肺转移瘤患者具有显著优势,能有效减小对呼吸运动幅度的影响和单次照射不同呼吸时相的误差。此类患者最主要的不良反应为放射性肺炎。Meta分析[12]结果表明,非小细胞肺癌经立体定向放疗后放射性肺炎发生率约为18.4%, 本研究随访结果显示,放射性肺炎发生率为25.0%, 均是1级或2级放射性肺炎,不需要临床干预。本研究接受放射治疗的肺癌患者数量有限,收集的临床数据较少,结果可能存在一定偏倚,但能初步说明呼吸门控计划较常规计划具有优越性。作者后续将纳入更多肺癌患者,进一步证实呼吸门控计划的可行性。
综上所述, 4D-CT联合呼吸门控技术可应用于肺癌的SBRT, 尤其对于多发的肺转移瘤患者而言,精确追踪多个肿瘤位置能够有效减少呼吸运动对治疗的影响和单次照射内的摆位误差,保证治疗效果。
