急性颅内前循环大血管闭塞血管内治疗再通后早期神经功能恶化的影响因素分析
2022-09-02陈松王驰王伟邱玉发吕楠杨鹏飞肖国栋舒张
陈松 王驰 王伟 邱玉发 吕楠 杨鹏飞 肖国栋 舒张
卒中是导致我国患者死亡和残疾的主要原因之一,其中大血管闭塞与卒中的不良预后密切相关[1-2]。近些年逐步发展的血管内治疗被证实对大血管闭塞有更好的开通效果,相比静脉溶栓也具有更长的时间窗[3-7]。早期神经功能恶化(early neurological deterioration,END)指患者血管内取栓开通治疗后在短期内神经功能突然恶化或者呈渐进性、阶梯型恶化,不仅使取栓的有益效果完全丧失,甚至还会加剧神经功能恶化,严重影响了急性颅内前循环大血管闭塞患者的长期预后。目前应用较为广泛的END定义是患者取栓术后72 h内观察到美国国立卫生研究院卒中量表(NIHSS)评分相比术前升高≥4分[8-9]。目前的研究中广泛讨论了静脉溶栓后发生END的相关危险因素,但少有对取栓术后血管再通患者发生END情况的探讨[10-11]。因此,本研究旨在探索经支架联合中间导管血管内治疗成功开通闭塞血管患者发生END的危险因素,为临床决策提供参考依据。
1 对象与方法
1.1 对象
回顾性连续纳入2018年3月1日至2020年12月31日江苏省太仓市第一人民医院神经外科(31例)、海军军医大学第一附属医院(61例)及苏州大学附属第二医院神经内科(35例)卒中中心住院的急性颅内前循环大血管闭塞患者的临床资料。
纳入标准:(1)年龄≥18岁;(2)发病时间至股动脉穿刺时间≤6 h或超时间窗患者符合应用扩散加权成像或CT灌注成像联合临床不匹配对醒后卒中和晚就诊卒中患者使用Trevo装置行神经介入治疗(diffusion-weighted imaging or CT perfusion assessment with clinical mismatch in the triage of wake up and late presenting strokes undergoing neurointervention with Trevo,DAWN)或缺血性卒中影像学评估后血管内治疗3(endovascular therapy following imaging evaluation for ischemic stroke,DEFUSE3)研究6~24 h内存在核心梗死或低灌注不匹配的患者[12-14];(3)符合《中国缺血性脑卒中诊治指南2019》中诊断标准的急性缺血性卒中且经头部血管成像[CT血管成像(CTA)、MR血管成像(MRA)或DSA,以DSA为“金标准”]证实为前循环大血管闭塞[15];(4)接受支架联合中间导管血管内治疗。
排除标准:(1)临床信息不全;(2)既往卒中史;(3)颅内出血性疾病;(4)入院时NIHSS评分>35分;(5)严重肝肾功能不全;(6)存在泌尿系统感染或其他部位感染等严重应激情况;(7)合并重要器官功能衰竭、恶性肿瘤;(8)采用局部麻醉手术方式。
伦理及知情同意:本研究方案符合赫尔辛基宣言(Helsinki guidelines)[16]。研究方案经江苏省太仓市第一人民医院和海军军医大学第一附属医院及苏州大学附属第二医院伦理委员会批准。患者或其家属均签署诊疗知情同意书。
1.2 临床资料收集及分组
收集患者临床病历信息,包括年龄、性别、糖尿病史[17]、高血压病史[18]、饮酒史(每天饮酒含乙醇量≥15 g,连续时间≥3个月)[19]、吸烟史(每天吸烟≥1支,连续时间≥6个月)[20]、心房颤动史、抗血小板聚集药物服用史、抗凝药物服用史、他汀类药物服用史、发病至入院时间、药物溶栓、发病至穿刺时间、术前NIHSS评分、闭塞部位(大脑中动脉、颈内动脉)及各中心手术量(根据国家卒中中心建设标准,低手术量中心定义为机械取栓<20例/年,高手术量中心定义为机械取栓≥20例/年)[21]。
取栓后72 h对患者进行NIHSS评分,END定义为与术前比较,术后NIHSS评分升高≥4分[8-9]。根据患者支架联合中间导管血管内治疗血管开通后患者是否发生END分为END组和非END组。NIHSS评分及介入取栓术均由拥有独立取栓经验3年以上的医师完成。
1.3 治疗方法
经诊断明确为急性颅内前循环大血管闭塞的患者,以Seldinger技术穿刺右侧股动脉后置入8 F动脉鞘。导引导管到位后将中间导管输送到梗死部血栓近端,尽量靠近梗死处。微导管在微导丝辅助下缓慢通过梗死血管段,微导管造影明确血栓远端位置。将Solitaire支架(Medtronic公司,美国)经微导管于梗死处释放,支架停留约5 min,关闭冲洗等渗盐水,50 ml注射器连接于中间导管末端“Y”型阀处进行负压抽吸,同时将支架与微导管一并拉入中间导管内,随后拉出体外。过程中50 ml注射器在导引导管末端进行持续负压抽吸。复查造影,评估颅内血管开通情况,若血管开通情况不满意,则重复上述操作过程。根据术者评估患者耐受及获益程度决定实施取栓次数,当取栓次数≥5次仍无法开通血管时结束操作,以尽量、尽快开通血管为目标,术后即刻、术后24 h复查头部CT判断有无颅内出血。
1.4 血管再通评价
采用改良脑梗死溶栓(modified thrombolysis in cerebral infarction,mTICI)分级评价术后即刻闭塞血管开通情况,其中mTICI 0~2a级为闭塞血管未开通,2b~3级为闭塞血管成功开通[22]。
1.5 统计学分析

2 结果
2.1 一般资料
本研究共纳入患者127例,其中男67例(52.8%),女60例(47.2%);年龄24~91岁,平均(68±12)岁;高血压病72例,糖尿病22例,心房颤动58例;吸烟18例,饮酒17例;低手术量中心31例,高手术量中心96例;基线NIHSS评分2~35分,中位数评分16.00(13.00,20.00)分;用药情况:抗血小板聚集药物16例,他汀类药物7例,抗凝药物17例;颈内动脉闭塞33例(26.0%),大脑中动脉闭塞94例(74.0%)。
2.2 单因素分析结果
127例中,发生END患者29例(22.8%)。END组患者男18例,女11例;年龄36~88岁,平均(67±13)岁。非END组患者98例中,男49例,女49例;年龄24~91岁,平均(68±12)岁。低手术量中心发生END 17例(54.8%),高手术量中心发生END 12例(12.5%)。低手术量中心END发生率明显高于高手术量中心(χ2=23.839,P<0.05)。
单因素分析结果显示,梗死部位位于颈内动脉、取栓次数≥3次及低手术量中心两组间差异有统计学意义(均P<0.05),其他因素两组间差异均无统计学意义(均P>0.05)。见表1。
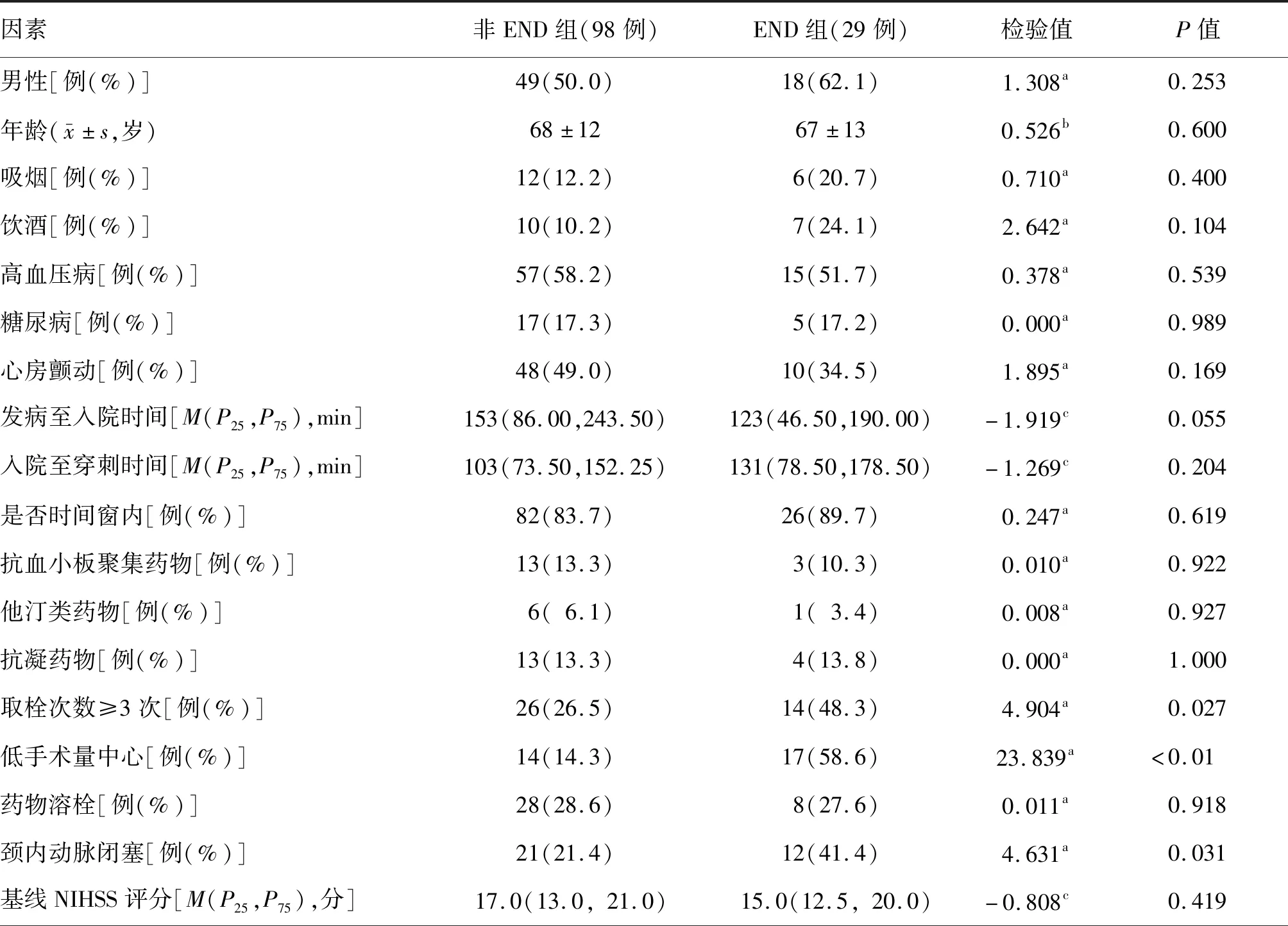
表1 非END组与END组急性颅内前循环大血管闭塞患者一般及临床资料比较结果
2.3 多因素分析结果
将发病至入院时间、取栓次数≥3次、低手术量中心及颈内动脉闭塞纳入多因素Logistic回归分析中,结果显示,取栓次数≥3次及低手术量中心均为患者发生END的独立危险因素(均P<0.05)。见表2。

表2 联合中间导管血管内治疗后颅内前循环大血管闭塞患者早期神经功能恶化影响因素的Logistic回归分析结果
3 讨论
目前END研究更多关注于静脉溶栓患者,关于END的定义尚无统一标准,Tei等[23]的一项多中心研究将 END 定义为7 d内加拿大神经量表(Canadian neurological scale,CNS) 评分较基线下降至少1分。更多研究以NIHSS评分作为神经功能评价量表,如Awadh等[9]的研究将END定义为72 h NIHSS评分较基线增加4分或以上。尽管由于END定义不同其发生率差异较大,但文献报道行静脉溶栓患者END发病率13%~38%,未行静脉溶栓患者发生率5%~40%[24-26],总体而言并不罕见。随着患者血管内治疗比例的增加,术后血管再通患者中仍有部分患者发生END,应该引起神经介入医师的重视。
本研究结果表明,取栓次数≥3次与发生END有关,目前关于取栓次数与患者获益间的关系仍然具有争议。取栓次数增加虽然能提高血管再通率,但取栓次数的增加也延长了取栓手术的时间,同时重复取栓将加重对血管内皮损伤的影响,相关研究结果显示,血管内治疗可对血管内膜造成线性薄层损伤,从而发生开通血管的再闭塞,或增加术后患者颅内出血转化的发生风险[27-28]。Shi等[29]的研究表明,与3次以内取栓患者相比,3次以上取栓患者良好预后发生率明显降低[9.8%(6/61)比39.7%(29/73),P=0.001];超过3次的取栓是良好预后的不利因素(OR=0.284,95%CI:0.091~0.882,P=0.030)。Bai等[30]的研究结果表明,取栓超过3次的患者获得良好结果的可能性随着取栓次数的增加逐渐下降(3次、4次、5次或5次以上取栓患者的可能性分别为44.4%、26.3%、14.8%)。多项研究同样显示,机械取栓1次血管成功再通相较于多次取栓后血管成功再通有更好的临床结果及更低的并发症发生率[5,31-33]。若取栓超过5次仍无法成功开通血管,再欲挽救缺血半暗带的可能性将下降,表明了过于多次的取栓操作可能是不必要的[32,34-36]。
不同中心之间的取栓效果差异应该在卒中中心建设过程中引起重视。2015年发表的5项随机对照研究[37-41]以及后续2项超时间窗取栓研究[13-14]结果使卒中的血管内治疗迅速普及。但是最初机械取栓均在经验丰富的卒中中心完成,这种模式可能因运转时间过长而延长患者血管再通时间。解决这一问题的办法是增加取栓中心的数量,但中心的增加可能导致每个中心取栓数量减少。美国疾病预防控制中心支持的一项Paul Coverdell国家急性卒中项目(Paul Coverdell National Acute Stroke Program,PCNASP)收集了2008年至2018年入院单独行血管内治疗或联合静脉溶栓患者,研究将取栓中心分为低手术量中心(取栓<15例/年)、中手术量中心(取栓15~30例/年)以及高手术量中心(取栓>30例/年)。结果表明,以中手术量中心为参考,低手术量中心良好预后可能性明显低于中手术量中心(校正OR=0.79,95%CI:0.60~0.82,P<0.01),而症状性颅内出血风险更高(校正OR=1.32,95%CI:1.02~1,70,P=0.034)。而高手术量中心在症状性颅内出血及院内病死率方面与中手术量中心差异不大,但高手术量中心良好预后率明显更高(校正OR=1.25,95%CI:1.13~1.39,P<0.01)。同时该研究分析了近11年美国在不同医院接受卒中血管内治疗患者数量的变化趋势。结果显示,随着取栓技术的普及,高取栓量(卒中血管内治疗数量>30例/年)的中心比例逐渐增加[42]。根据国家卒中中心建设标准,本研究将参与中心分为低手术量中心(取栓<20例/年)和高手术量中心(取栓≥20例/年),本研究低手术量中心END发生率为54.8%,高手术量中心END发生率为12.5%,差异有统计学意义,提示我们在取栓中心增加的过程中应该重视不同中心间手术量的差异,只有大多数中心普遍达到高手术量中心标准,患者能够就近快速得到治疗才能进一步广泛提高救治效果。
本研究的局限性在于,研究中纳入的中心较少,未将手术量中心分为低、中、高手术量中心,未进一步分析中手术量中心与低、高手术量中心之间是否存在差异。此外,关于取栓手术最佳麻醉策略目前仍存在许多争议,而基层医院采用局部麻醉手术患者较少,为保证一致性,本研究排除了采用局部麻醉手术方案的病例,局部麻醉患者术后即可进行NIHSS评分对比,因而本研究可能降低了对比意义。
综上所述,本研究的结果显示,在急性颅内前循环大血管闭塞血管内治疗后血管再通患者中,取栓次数≥3次及低手术量中心是发生END的危险因素。
