离子液体中电沉积锕系元素的研究现状
2022-09-01刘坤琳李叶凡
刘坤琳,李叶凡,曹 智
中核四0四科学技术研究院,甘肃 嘉峪关 735100
世界范围内有大约450个核反应堆,提供全球大约11%的电力,反应堆核裂变过程中不产生温室气体,被认为是一种缓解气候变暖的有力方案[1]。然而,这些核反应堆每年会产生成千上万吨乏燃料,为了实现核能的可持续发展,必须对这些乏燃料进行循环再利用。目前,乏燃料后处理主要分为湿法和干法两种。前者的经典成熟工艺为PUREX工艺,采用无机酸将乏燃料中的锕系氧化物进行溶解,然后采用含磷有机萃取剂将锕系金属离子萃取到有机相中,经洗涤、反萃、纯化、转化得到锕系氧化物。干法后处理主要分为:氟化物挥发法[2]和熔盐电解法[3-5]。熔盐电解法又可以分为三类:(1) 电解沉积,在氧化物电解提取过程中,锕系氧化物以氯酰配位阳离子(或氯氧化物)的形式溶解在碱金属或碱土金属卤化物中,然后以氧化物的形式电沉积锕系元素;(2) 电解精炼,该工艺最初是为金属燃料开发的,将乏燃料溶解在熔融的碱金属氯化物介质中(通常以金属为阳极,采用牺牲阳极的方式将金属转化为金属离子),然后选择性电沉积锕系元素;(3) 电解还原,在熔融LiCl或CaCl2介质中,通过Li或Ca在锕系氧化物上的初始沉积,将锕系氧化物直接电化学还原为相应金属。上述传统方法存在许多缺点,例如:湿法后处理工艺流程长,存在核临界安全风险,并产生大量高、中、低水相放射性废物;以碱金属或碱土金属卤化物为电解质的干法后处理需高温操作(工艺温度为773 K或更高)、能耗高、熔盐介质腐蚀性强。近些年来,为了解决上述方法存在的问题,研究人员以低温有机熔融盐(即离子液体)为电解质,采用电沉积的方式对乏燃料中的锕系元素进行回收[6-8]。
1 离子液体
1.1 离子液体的组成
离子液体是一种由有机阳离子与无机阴离子或有机阴离子组成、温度低于100 ℃下为液体的低温熔融盐[9]。有机阳离子主要包括吡啶类阳离子、咪唑类阳离子、吡咯类阳离子、季铵盐类阳离子、季膦盐类阳离子等,阳离子类型示于图1。阴离子主要包括硝酸根、卤素阴离子、含氟类阴离子以及含氰酸根阴离子等,阴离子类型示于图2。

图1 离子液体的阳离子类型Fig.1 Cation types of ionic liquids
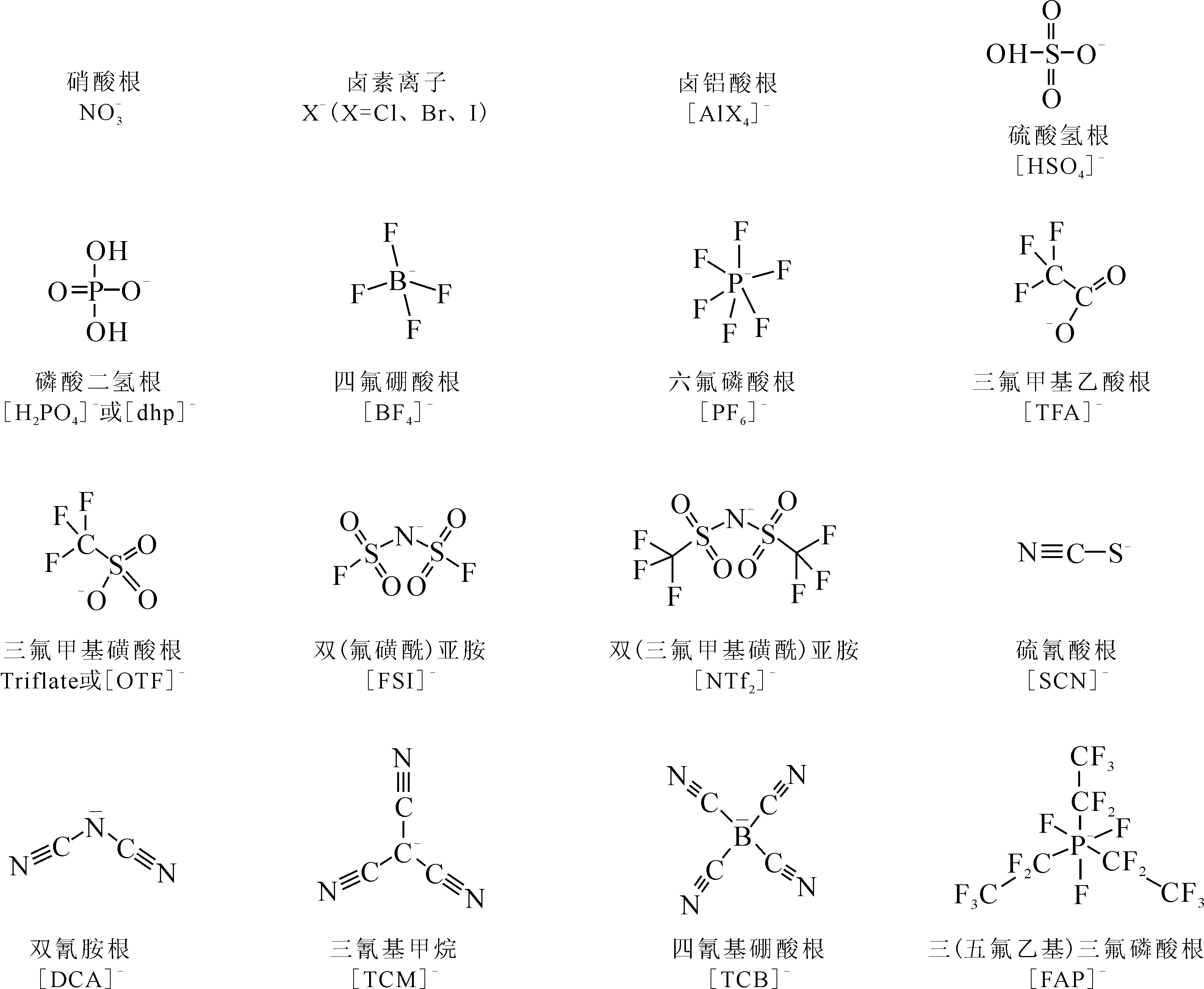
图2 离子液体的阴离子类型Fig.2 Anion types of ionic liquids
1.2 离子液体的分类

2 离子液体中电沉积锕系元素
2.1 锕系元素在第一代离子液体中的电沉积
1) 铀沉积
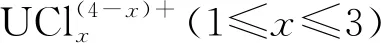
(1)
(2)
(3)
(4)
(5)
(6)
因此,在卤铝酸离子液体中,高价铀离子常与卤离子以配合物的形式存在,U(Ⅵ)的还原产物与离子液体的种类、离子液体的酸碱度相关,且高价铀不能直接被还原为金属单质,从U(Ⅵ)到U(Ⅴ)也可能经历多步转化反应。
2) 镎沉积
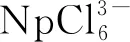
综上所述,卤铝酸基离子液体仅适用于An(Ⅵ)与An(Ⅲ)之间的转化,不能将An(Ⅲ)还原为An(0),其原因为卤铝酸离子液体的电化学窗口较窄且阴极稳定性较差。
2.2 锕系元素在第二代离子液体中的电沉积
1) 钍沉积
在293 K时,Bhatt等[20]研究了[Th(NTf2)4-(HNTf2)]·2H2O在三甲基一丁基季铵盐双(三氟甲基磺酰)亚胺([Me3NnBu][NTf2])离子液体中的电化学行为,当阴极电位相对于氧化还原参比电极二茂铁阳离子/二茂铁(Fc+/Fc)为-2.20 V(或相对于标准氢电极为-1.80 V)时,Th(Ⅳ)通过一步法转化为Th,而钍金属与空气接触后转化为ThO2。作者将此还原过程与钍在LiCl-KCl熔盐体系(400 ℃时)还原过程进行比较,得出在离子液体中该还原过程比在熔盐体系中更容易发生的结论。
2) 铀沉积
在铀的电沉积过程中,铀氧化物(UO2、UO3、U3O8)在活泼金属作用下可以直接进行电化学还原,也可以采用氧化剂(HNO3、Cl2、F2等)将其转化为可溶于离子液体的U(Ⅵ)化合物或者U(Ⅳ)化合物,然后进行电沉积,得到铀金属或者UO2。
(1) 铀氧化物直接电化学还原

(2) 铀酰化合物U(Ⅵ)的电沉积

2006年,Sornein等[27]研究了[UO2Cl4]2-在离子液体1-丁基-3-甲基咪唑双(三氟甲基磺酰)亚胺([BMIM][NTf2])和三正丁基-甲基铵双(三氟甲基磺酰)亚胺([MeBu3N][NTf2])中的电化学行为,研究表明[UO2Cl4]2-在[BMIM][NTf2]和[MeBu3N][NTf2]中经一步单电子还原生成[UO2Cl4]3-(还原电位分别为-1.44 V和-1.8 V(vs Ag/Ag+)),随后发生了化学反应。同时发现[UO2Cl4]3-在[BMIM][NTf2]中比[UO2Cl4]3-在[MeBu3N][NTf2]中稳定,作者将其原因归结为[UO2Cl4]3-中的Cl与[BMIM]+中C—H形成C—H…Cl氢键强于[UO2Cl4]3-与[MeBu3N]+之间形成的C—H…Cl氢键。为了进一步研究[UO2Cl4]2-的还原机理,2011年Sornein等[28]提出[UO2Cl4]2-经一步单电子还原为[UO2Cl4]3-、[UO2Cl4]3-发生化学反应生成[UO2Cl4-x]x-3和xCl-,[UO2Cl4-x]x-3失去一个电子转化为U(Ⅳ),故U(Ⅵ)经电子转移-化学反应-电子转移过程转化为U(Ⅳ)。
综上所述,将U(Ⅵ)化合物或离子转化为U(Ⅳ)的反应机理可以分为两步单电子路径、一步两电子路径或者电子转移-化学反应-电子转移路径。
(3) 铀卤化物U(Ⅳ)的电沉积

(4) 有机铀盐U(Ⅳ)的电沉积
Jagadeeswara等[30]先将UO2溶于HNTf2溶液中,在80 ℃下采用旋转蒸发器将其蒸干得到U(NTf2)4粉末,然后将其溶于离子液体[MPPi]-[NTf2]中,100 ℃下,U(Ⅳ)在铂电极上电化学还原,其循环伏安曲线上出现了四个还原峰,其电极电势分别为-0.64、-1.45、-2.10、-2.77 V(vs Fc/Fc+),前三个还原峰归结为U(Ⅳ)转化为U(Ⅲ),第四个还原峰为U(Ⅲ)转化为铀金属。该项研究给出的启发是将锕系氧化物与HNTf2反应生成An(NTf2)4,该有机铀盐能够溶解在离子液体中,解决了锕系氧化物在离子液体中溶解难的问题,实现了锕系氧化物到锕系金属的转化。
(5) 阴离子、阳离子和裂片离子对铀电沉积的影响



综上所述,对于铀的电沉积而言,无论是U(Ⅵ)还是U(Ⅳ)的电沉积,沉积产物主要是UO2,沉积产物为铀金属的相关报道较少,少数关于铀金属产物的报道,其沉积过程均是从U(Ⅳ)转化为U(0),而非从U(Ⅵ)转化为U(0)[28, 30]。
3) 镎和钚沉积

4) 镅沉积
2014年,Sankhe等[37]第一次采用离子液体对241Am进行恒电位沉积,共采用六种室温离子液体,分别为三种与水混溶的离子液体([C2mim]NO3、[C4mim]BF4、[C8mim]Br)和三种与水不混溶的离子液体([C8mim]PF6、[C8mim][NTf2]、1-辛基-1-甲基吡咯双(三氟甲基磺酰)亚胺([C8mpy]-[NTf2])。考察了离子液体黏度、pH值和温度对241Am沉积效果的影响,研究发现:三种与水混溶的离子液体随着其黏度的增大,241Am沉积效果越来越好,当采用[C8mim]Br时,对241Am的电沉积最好;在三种与水不混溶的离子液体中241Am会钝化,沉积效果不佳,当加入异丙醇,随着离子液体与异丙醇混合物黏度的减小,241Am沉积效果越来越好,当采用[C8mpy][NTf2]时,对241Am的电沉积最好,45 min内约99.6%的241Am发生沉积。
3 离子液体类型对比
通过对上述应用于锕系元素电沉积离子液体类型的分析,其阴离子主要为[NTf2]-、阳离子主要为咪唑类阳离子,结合前期文献[38]调研,根据离子液体的物理性质(熔点、黏度、电导率、电化学窗口、溶解能力)和化学稳定性对其类型进行比较,对阴阳离子类型进行筛选,结果列入表1。由表1可知:对于有机阳离子用于电沉积而言,哌啶类、吡咯类和咪唑类阳离子优于其他类阳离子;对于有机阴离子用于电沉积而言,[NTf2]-型阴离子优于其他类阴离子。因此,第二代离子液体用于锕系元素的电沉积优先顺序为:[哌啶类]-[NTf2]>[吡咯类][NTf2]>[咪唑类][NTf2]。
4 结论与展望
综述了锕系元素在第一代和第二代离子液体中的电化学行为,研究结果表明采用离子液体回收核燃料中锕系元素可行。卤铝酸离子液体仅适用于An(Ⅵ)与An(Ⅲ)之间的转化,不能将An(Ⅲ)还原为An(0)。在第二代离子液体中,铀的电沉积集中在U(Ⅵ)还原为U(Ⅳ),U(Ⅳ)还原为U(0)的报道不多。电沉积Th、Np、Pu、Am的相关研究较少。目前该领域处于理论研究阶段,需加强基础研究,重点研究方向包括但不限于以下几方面:

表1 离子液体物理性质与化学稳定性对照表Table 1 Comparison table of physical properties and chemical stability of ionic liquids
(1) 需合理设计离子液体阴阳离子结构,降低离子液体黏度、提高金属化合物的溶解度以及拓宽离子液体的电化学窗口;
(2) 需研究锕系金属离子与离子液体阴离子配位的方式及其对电沉积电位的影响;
(3) 需研究锕系金属离子在离子液体中存在的形式及锕系金属离子电沉积的机理;
(4) 需研究[NTf2]-阴离子型离子液体的辐射稳定性。
