钙镁二元水合盐复合热化学储热单元的储热特性研究
2022-08-25刘洪芝刘思琪叶振东程禧龙
刘洪芝,刘思琪,叶振东,程禧龙,张 弛
(上海理工大学 环境与建筑学院,上海 200093)
符号说明:
A ——断面面积,m2;
CP——比热容,kJ/(kg·K);
d ——单个通道材料厚度,m;
Ds——扩散系数,m2/s;
Ds0——表面扩散指数前常数,m2/s,Ds0=4.37×10-5m2/s;
Es——活化能,J/mol;
h ——对流换热系数,W/(m2·K);
hm——对流传质表面传质系数,m/s;
H ——吸附热,J/kg;
Ks——吸附速率常数,1/s;
m ——质量,g;
qv——体积储热密度,MJ/m3;
Q ——热量,kJ;
R ——气体常数,8.314 J/(mol·K);
RH ——相对湿度;
t ——时间,min;
T ——温度,℃;
u ——空气流速,m/s;
U ——空气的截面周长,m;
V ——体积,m3;
w ——质量分数;
x ——吸附量,g/g;
ω ——含湿量,g/kg;
ρ ——密度,kg/m3;
ε ——孔隙率;
τ ——弯曲因子;
η ——热回收率;
下标
0 ——初始状态;
storage ——储热过程;
release ——放热过程;
dry ——干燥;
f ——最终状态;
g ——空气;
s ——固体;
H2O ——水;
in ——入口;
out ——出口;
eq ——平衡状态。
0 引言
储热技术中的水合盐热化学储热主要通过水合盐与水蒸气之间的气-固脱水/水合反应进行储热/放热[1],因其反应温度与太阳能集热器温度一致,相比于显热和潜热储热技术,具有储热密度高、长期储热过程中热损失小等特点,非常适合太阳能、工业余废热等低品位能源的储存[2-3]。
虽然纯水合盐具有较高的理论储热密度[4],但是纯水合盐存在易潮解、高温下可能发生水解反应、水蒸气在水合盐反应床内的传质阻力较大等问题。因此,目前研究的大多将水合盐填充到多孔材料的孔内制备成水合盐复合热化学储热材料,其在传热传质性能、反应动力特性和循环稳定性等方面较纯水合盐有了较大改善[5]。复合水合盐热化学储热材料可以在开式热化学储热系统和闭式热化学储热系统中进行储热/放热[6],其中开式热化学储热系统相比闭式热化学储热系统结构简单,储热密度高,国内外学者对采用复合水合热化学储热材料的开式储热系统进行了试验和数值模拟研究。
WU等[7-8]试验测试了硅胶-CaCl2的开式热化学储热系统的储热性能,并采用数值模拟进一步优化了其储热性能。当热源温度为90 ℃时,其体积储热密度约为425 MJ/m3。CLARK等[9]测得水泥-35% SrCl2和水泥-50% SrCl2在堆积反应床内的体积储热密度分别为346,490 MJ/m3。李威等[10]制备了膨胀石墨 -15% K2CO3,并模拟了其在具有堆积反应床的开式储热系统中的储热性能,其热功率和热回收率分别为97 W和81.2%。LIU等[11]试验测得硅藻土-9.6% LiCl的开式储热系统在60 ℃下再生的体积储热密度为269 MJ/m3。
另一方面,研究表明由2种水合盐混合制成的二元水合盐的动力特性和循环稳定性都有了较大的改善[12]。但是,目前关于具有高储热密度的二元水合盐复合热化学储热系统的研究较少,更进一步,摩尔比为1:2的MgCl2和CaCl2组成的二元水合盐在保证循环稳定性和水合动力特性的前提下,储热密度高[12]。因此,本文采用天然介孔材料硅藻土(WSS)和MgCl2/2CaCl2制备钙镁二元水合盐复合热化学储热单元,并对该储热材料的特性如多孔特性、微观形貌、循环稳定性进行研究;最后,建立一维热质耦合模型模拟该储热单元在开式热化学储热系统中的储热性能,重点研究钙镁二元水合盐的质量分数和相对湿度的影响。
1 储热单元的制备和特性研究
1.1 制备方法
钙镁二元水合盐复合热化学储热单元的多孔基底材料是产自日本北海道北部地区的硅藻土(WSS),主要成分为 SiO2,孔径范围为 4~20 nm[13],比表面积为136.66 m2/g。首先,将WSS在800 ℃下高温烧结,并制成如图1所示的蜂窝状结构[13]。采用真空浸渍法将摩尔比为1:2的MgCl2(Adamas,纯度>96%)和CaCl2(Gregent,纯度>98%)的二元水合盐填充到WSS的孔内,制备成钙镁二元水合盐复合热化学储热单元,空气通道的壁厚和边长分别为0.28,1.31 mm,钙镁二元水合盐的质量分数w计算如下:


图1 WSS的蜂窝状结构Fig.1 The WSS honeycomb elements
表1列出了钙镁二元水合盐复合热化学储热单元样品,根据钙镁二元水合盐充填质量分数不同命名为 WSS7,WSS13,WSS20。
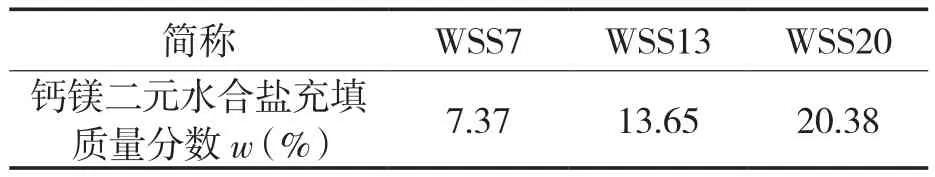
表1 钙镁二元水合盐复合热化学储热单元样品Tab.1 Thermochemical heat storage unit sample based on composite calcium-magnesium binary salt hydrates
1.2 多孔特性
采用标准氮气吸附/解吸法(康塔IQ)测定该钙镁二元水合盐复合热化学储热材料的比表面积和孔体积,结果见表2。随着钙镁二元水合盐充填质量分数的增加,复合热化学储热材料的比表面积、孔体积、孔隙率随之减少,可以初步判定钙镁水合盐充填于WSS的孔内。

表2 钙镁二元水合盐复合热化学储热材料的多孔特性Tab.2 Porous properties of thermochemical heat storage material based on composite calciummagnesium binary salt hydrates
1.3 微观形貌
采用扫描电镜(日本电子公司,SM-6700F)测得钙镁二元水水合盐复合热化学储热材料的微观形貌,如图2所示。从图中可以看到,WSS是由直径为3~5 μm的硅质微晶球体构成,这些微粒子间形成细孔。MgCl2/2CaCl2的加入,使得WSS20的表面较为光滑,二元水合盐的分布较为均匀。

图2 钙镁二元水合盐复合热化学储热材料的SEMFig.2 SEM images of thermochemical heat storage material based on composite calcium-magnesium binary salt hydrates
1.4 循环稳定性
循环稳定性试验测试原理如图3所示,储热过程的温度为100 ℃,持续时间120 min,放热过程的温度为30 ℃,相对湿度为65%,持续时间为240 min。图4示出了WSS20的稳定性测试结果,经过连续12次储热-放热循环后,放热过程结束时吸附量波动性较小,根据本试验室前述研究可知,WSS-22.4% CaCl2[13]和 WSS-9.6% LiCl[11]分别经过25,250次储热-放热循环后的稳定性很好,可以基本证实本文基于WSS载体材料所制备的钙镁二元水合盐复合热化学储热材料在热化学储热系统中的具有良好的稳定性。
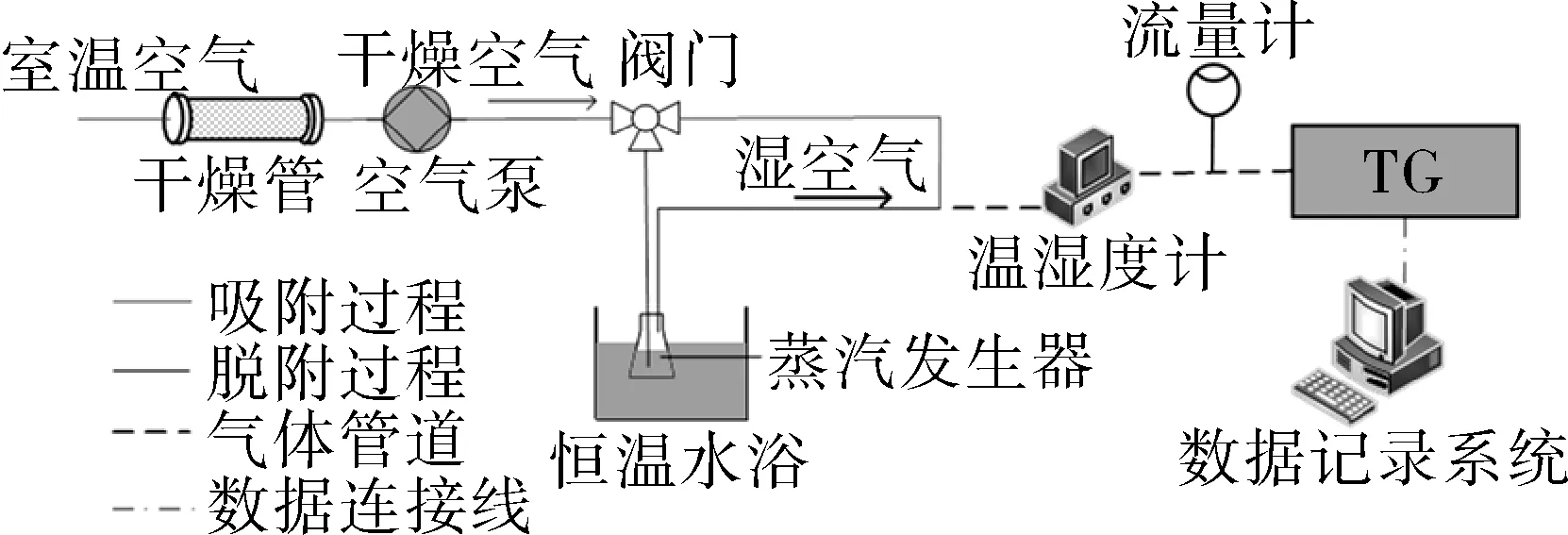
图3 循环稳定性测试试验原理Fig.3 Experimental setup of circulation stability

图4 WSS20的循环稳定性测试结果Fig.4 Circulation stability test result of WSS20
2 储热单元的数值模拟
钙镁二元水合盐复合热化学储热单元在开式储热系统中的储热/放热过程如图5所示[6]。储热过程中,高温、低湿的空气流经热化学储热单元,储热单元温度升高,水合盐复合热化学储热材料在高温下脱附,脱附产生的水蒸气随流经的空气流出。在此过程中,热能以化学能的形式储存在经过脱附的钙镁二元水合盐复合热化学储热材料中。放热过程中,低温且高相对湿度的空气流经脱附后的热化学储热单元,钙镁二元水合盐复合热化学储热材料吸附湿空气中的水蒸气放出热量,通过对流换热,钙镁二元水合盐复合热化学储热材料将产生的热量传递给流经的空气。

图5 开式热化学储热系统Fig.5 The schematic diagram of the open thermochemical heat storage system
2.1 物理模型
钙镁二元水合盐复合热化学储热单元的物理模型如图6所示。由于该储热单元的空气通道的结构和成分均匀,可认为所有空气通道都是相同的,故可将单个通道作为模拟的研究对象。

图6 钙镁二元水合盐复合热化学储热单元的物理模型Fig.6 The physical model of the thermochemical heat storage unit
2.2 数学模型
2.2.1 模型假设
为建立并求解控制方程,需要对模型进行如下的假设:空气为理想气体且不可压缩;空气的压力、温度、含湿量在垂直于流动方向不发生变化;空气的流速沿程不变;钙镁二元水合盐复合热化学储热材料的比热、密度、温度等沿厚度方向不变;钙镁二元水合盐复合热化学储热材料沿长度方向的导热忽略不计。
2.2.2 控制方程
空气侧水蒸气的质量守恒方程:

钙镁二元水合盐复合热化学储热材料内水蒸气的质量守恒方程:

空气的能量平衡方程:

钙镁二元水合盐复合热化学储热材料的能量守恒方程:

其中,基于WSS的水合盐复合热化学储热材料的比热容经测定与吸附量成正比[14],故有:

对流换热系数h和对流传质表面传质系数hm可通过刘伊斯关系式描述。

采用线性推动力(LDF)模型描述吸附速率为[15]:
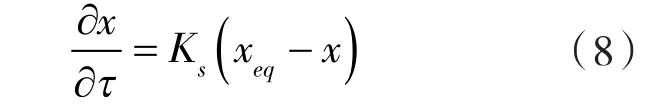
其中,xeq为相对湿度有关的函数,xeq=f(RH),可通过水蒸气吸附分析仪(hydrosorb-1000)测得,如图7所示。

图7 钙镁二元水合盐复合热化学储热材料的平衡吸附量Fig.7 The equilibrium water uptake of thermochemical heat storage material based on composite calcium-magnesium binary salt hydrates
基于前述研究[16],传质系数Ks可表示为:

其中,扩散系数Ds可由下式表示:
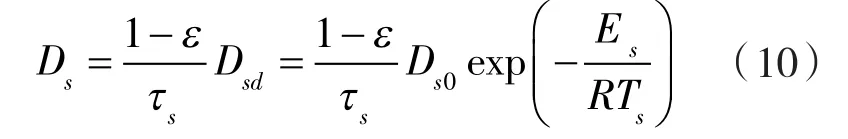
当吸附条件为25 ℃,RH=95%时,将传质系数Ks带入LDF模型中可以得到钙镁二元水合盐复合热化学储热材料的吸附量的变化曲线,如图8所示。随着二元水合盐含量的增加,该材料达到吸附平衡的时间延长,同时吸附量也随之增加。

图8 钙镁二元水合盐复合热化学储热材料在25 ℃,95%时吸附量随时间的变化Fig.8 Sorption kinetics of thermochemical heat storage material based on composite calcium-magnesium binary salt hydrates at 25 ℃,95%
2.2.3 初始条件和边界条件
(1)初始条件。
放热过程:

储热过程:

(2)边界条件。
入口边界条件:当 z=0 时,ωg= ωg,in,Tg=Tg,in。
2.2.4 网格无关性验证
通过COMSOL Multiphysics软件对控制方程求解[18]。选取的网格数分别为 85,341,868,1 133储热单元内各个位置(50,100,195 mm)的网格无关性结果如图9所示。当网格数≥868时,偏差很小,故在本模拟中选取网格数为868。

图9 网格无关性验证Fig.9 Grid independence verification
2.2.5 模型可靠性验证
模拟计算文献[11]中的WSS-9.6% LiCl储热单元,储热过程的高温空气温度为80 ℃,流量为4 m3/h;放热过程的湿空气温湿度为25 ℃,93%,流量为3 m3/h。将模拟结果与试验结果进行对比,结果如图10所示,相对误差见表3。本文所建立的一维数学模型得到的储热单元在储/放热过程中,内部各点的温度变化与试验值变化趋势一致。由表3可知,在储/放热初期,误差较大,此后不同位置温度的误差均在10%左右,结果吻合较好。

图10 模型可靠性验证Fig.10 Model reliability verification
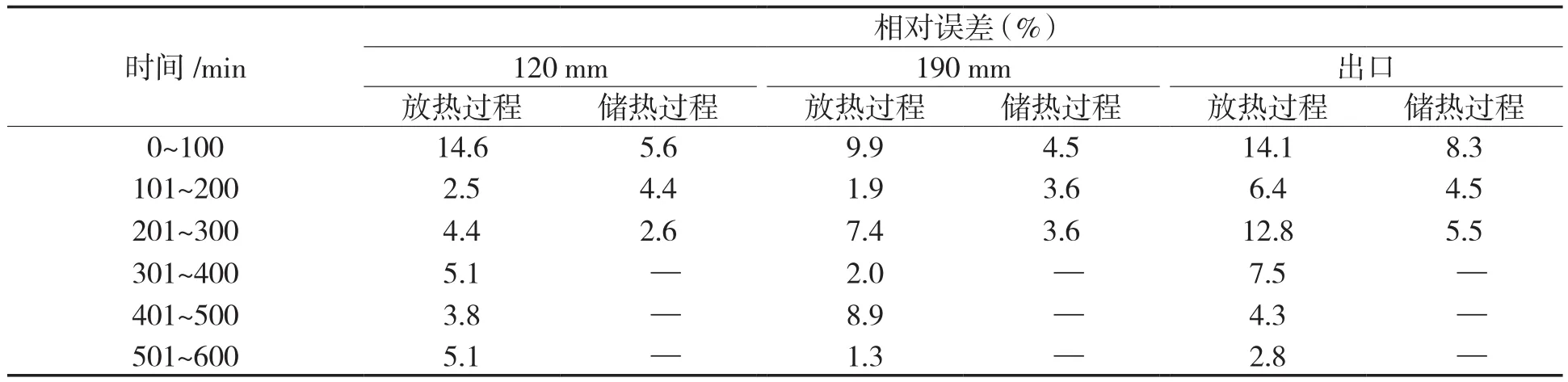
表3 模拟结果与试验结果的相对误差Tab.3 Relative errors of calculated results and experimental results
3 结果分析与讨论
储热密度、放热功率和热回收效率是衡量热化学储热系统非常重要的参数。体积储热密度为放热过程中释放的热量与储热单元体积的比值[11],如下式所示:

开式热化学储热系统的放热功率的计算式如下式所示:

3.1 钙镁二元水合盐的质量分数的影响
当入口空气温度为25 ℃,相对湿度为95%,入口空气流量为4 m3/h时,通过计算得到钙镁二元水合盐复合热化学储热单元出口空气温度如图11所示。钙镁二元水合盐的质量分数对储热单元的出口空气最大温度的影响较小,其出口空气的最大温度分别为63.5,60.3,62.4 ℃。由水合盐复合热化学储热材料的机理可知,首先多孔材料内水合盐和空气中的水蒸气发生水合反应,反应放热量大,故储热单元的出口空气温度急剧增加,但出口空气的最大温度受限于水合反应放热量。随着反应的进行,下游的多孔材料内水合盐继续吸附水蒸气,盐含量大的储热单元可以长时间输出较高温度的空气。因此,钙镁二元水合盐的质量分数对储热单元的出口空气的高温持续时间影响较大。当进出口空气温差大于15 ℃时,WSS7,WSS13和WSS20的出口空气温度高于40 ℃的持续时间分别为171,237,438 min。图12示出了储热单元的放热功率随着钙镁二元水合盐的质量分数的变化。由于WSS20的出口空气维持高温的时间较长,WSS20的放热功率超过20 W的持续时间是WSS13的2倍,故WSS20更适合作为储热单元使用。

图11 钙镁二元水合盐的质量分数对出口空气温度的影响Fig.11 The effect of mass fraction of the salt hydrates on outlet air temperature

图12 钙镁二元水合盐的质量分数对放热功率的影响Fig.12 The effect of mass fraction of the salt hydrates on thermal release power
3.2 入口空气相对湿度的影响
钙镁二元水合盐复合热化学储热单元入口空气的温度为25 ℃,相对湿度分别设定为40%,60%,80%和95%,入口空气流量为3 m3/h。计算得到钙镁二元水合盐复合热化学储热单元WSS20的出口空气温度随相对湿度的变化情况如图13所示。
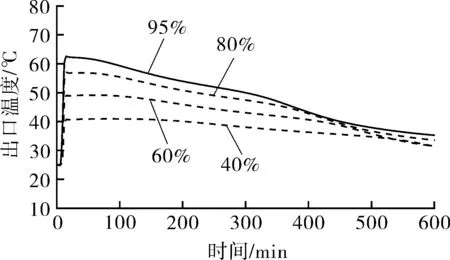
图13 入口空气相对湿度对储热单元出口空气温度的影响Fig.13 The effect of inlet relative humidity on outlet air temperature
出口空气最大温度随入口空气相对湿度增加而显著升高。当储热单元的入口空气相对湿度为40%,60%,80%,95%时,其出口空气最大温度分别为 41,49,57,62 ℃。由图 7可知,钙镁二元水合盐复合热化学储热材料的平衡吸附量随相对湿度增加而显著增加。流经储热单元的空气的温度与钙镁二元水合盐复合热化学储热材料的吸附放热量有关,在高相对湿度的条件下,平衡吸附量大,吸附放热量相应增加,因此,出口空气的温度也随着相对湿度的增大相应增加。
从图13还可以看出,出口空气温度高于40 ℃的放热时间也随着入口空气相对湿度的增加而延长。入口空气相对湿度为40%时,储热单元的放热时间为201 min,当相对湿度为60%,80%,95%时,储热单元的放热时间分别为417,438,450 min。高入口空气相对湿度下,下游的钙镁二元水合盐复合热化学储热材料对应的空气相对湿度大于其在低入口空气相对湿度下的值,因此高出口温度的持续时间也相应延长。
图14示出了入口空气相对湿度对钙镁二元水合盐复合热化学储热单元的放热功率的影响,随着入口空气相对湿度的增加,储热单元的放热功率也随之增大。放热功率与钙镁二元水合盐复合热化学储热材料在吸附过程中的动力学性能密切相关[19],高入口空气相对湿度条件下具有较高的水蒸气分压,可以增强钙镁二元水合盐复合热化学储热材料的传质推动力,进而使放热功率增大。在相对湿度为95%时,储热单元的出口空气最大放热功率可达37.7 W,实际使用中可根据所需功率调整储热单元的数目。

图14 入口空气相对湿度对放热功率的影响Fig.14 The effect of inlet air relative humidity on thermal release power
图15示出了不同入口空气相对湿度时钙储热单元WSS20的储热密度。如前所述,由于出口温度的提升和放热时间的延长,其储热密度随着入口空气相对湿度的增加而不断上升,最大体积储热密度可达416.05 MJ/m3。
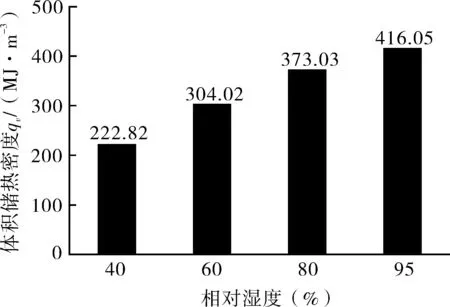
图15 入口空气相对湿度对储热单元的储热密度的影响Fig.15 The effect of inlet air relative humidity on volumetric heat storage density
4 结论
(1)钙镁二元水合盐复合热化学储热材料的比表面积、孔体积、孔隙率随着钙镁二元水合盐填充质量分数的增加而减小,初步判定钙镁二元水合盐位于WSS的介孔内,且WSS20的稳定性较好。
(2)入口空气相对湿度的增加可有效提高钙镁二元水合盐复合热化学储热单元出口的最大温度、延长出口空气高温持续时间、提高其放热功率和储热密度。钙镁二元水合盐的质量分数的增加可以有效延长出口空气高温(>40 ℃)的持续时间,其中钙镁二元水合盐的填充质量分数为20.38%的WSS20具有较好的储热性能,其储热密度是WSS13的1.5倍,为416 MJ/m3。
(3)由于该储热单元体积较小,实际应用中可根据热用户的需求,通过叠加储热单元的方法提高其放热功率。因此,该钙镁二元水合盐复合热化学储热单元对提高储存太阳能或工业余热、废热等低品位热源的利用率有重要意义。
