非洲猪瘟病毒P72蛋白合成肽疫苗的构建及其免疫效力评估
2022-08-23徐娅玲张霁辉黄世会冉雪琴王嘉福
徐娅玲,张霁辉,牛 熙,李 升,黄世会,冉雪琴,王嘉福
(1.贵州大学生命科学学院,贵阳 550025;2.贵州大学农业生物工程研究院,贵阳 550025;3.贵州大学动物科学学院,贵阳 550025)
非洲猪瘟(African swine fever,ASF)是由非洲猪瘟病毒(African swine fever virus,ASFV)引起家猪、疣猪、欧洲野猪和美洲野猪等不同品种猪发病的急性、烈性传染病[1],主要症状为肺水肿、严重抑郁、高热、发绀、无食欲、多器官广泛出血等[2],对环境有极强的抵抗能力,在-20 ℃ 112 d后仍具有感染能力[3],中国动物病原微生物名录中将其列为一类动物疫病,该病首次发现于肯尼亚[4],后传播到西班牙、意大利、法国、格鲁吉亚、俄罗斯等国家[5-6],2018年初在中国辽宁省沈阳市首次暴发,由于其高致死性,对中国生猪养殖业造成巨大经济损失[7],但目前仍无有效疫苗预防,一旦发现,只能采取捕杀方式,因此对于ASF疫苗的研究尤为重要。
目前,ASF的疫苗研发中病毒载体疫苗与减毒活疫苗免疫原性较强[8-9]。但病毒载体疫苗安全性尚不能完全确定,易突变为强毒株[10],减毒活疫苗可能会导致猪产生高热、食欲不振、轻微神经衰弱症状,部分猪甚至因感染而急性死亡[11]。因此,安全性更高的疫苗对于ASF至关重要。以抗原表位为基础设计的合成肽疫苗能诱导机体产生对特定表位的免疫反应,并避免其他可能导致过敏性反应的无关表位的潜在影响,具有极高的安全性[12]。P72蛋白作为ASFV主要的衣壳蛋白,有较多的抗原表位[13],2014年 Phillips[14]通过基因定位发现该蛋白存在多个抗原反应区域。郭晶等[15]也通过P72多表位融合蛋白诱导机体产生了特异性抗体及其良好的免疫原性。有效的B细胞和T细胞表位可通过免疫信息学分析确定,但表位的免疫原性必须通过试验验证。因此,本研究通过生物信息学的方法评估和选择P72蛋白中能诱导B细胞和T细胞应答的抗原表位,制备合成肽疫苗,免疫小鼠,评估合成肽的免疫效力,以期为ASF合成肽疫苗研究提供理论依据。
1 材料与方法
1.1 氨基酸序列、试验动物
ASFV CAS19-01/2019株(GenBank登录号:MN172368.1)P72蛋白氨基酸序列(GenBank登录号:QGJ83444.1);3~5周龄SPF级雌性健康BALB/c小鼠(许可编号:EAE-GZU-2021-P014)购自重庆腾鑫生物技术有限公司。
1.2 主要试剂
弗氏完全与不完全佐剂(Sigma公司);牛血清白蛋白(BSA)、ELISA包被液、ELISA终止液、TMB显色液、红细胞裂解液、小鼠脾脏细胞分离试剂盒(Solarbio公司);RPMI-1640细胞培养基、100目与200目细胞筛、PBS、小鼠白细胞介素2(IL-2)ELISA试剂盒、IL-4 ELISA试剂盒、小鼠免疫球蛋白G(IgG)ELISA试剂盒、小鼠γ干扰素(IFN-γ)ELISA试剂盒(湖南艾方生物科技有限公司);抗体CD3+、CD8+、CD4+(杭州联科生物技术股份有限公司);辣根过氧化物酶(HRP)标记的山羊抗小鼠IgG (Goat Anti-Mouse IgG-HRP)(上海艾比玛特医药科技有限公司)。
1.3 方法
1.3.1 抗原表位分析 利用ExPASy在线分析工具ProtParam (https:∥web.expasy.org/protparam/)预测P72蛋白分子质量、等电点、不稳定系数和半衰期;利用Netphos在线软件(https:∥services.healthtech.dtu.dk/service.php NetPhos-3.1)预测其磷酸化位点;SOPMA (https:∥npsa-prabi.ibcp.fr/cgi-bin/npsa_automat.pl?page=npsa_sopma.html)预测其蛋白二级结构;利用IEDB在线软件(http:∥tools.immuneepitope.org/main/)预测其T细胞抗原表位、表面可及性、可塑性、抗原及亲水性;利用ABCpred (https:∥webs.iiitd.edu.in/raghava/abcpred/)、SVMtrip (http:∥sysbio.unl.edu/SVMTriP/)在线软件预测其B细胞抗原表位。
1.3.2 合成肽疫苗的构建 根据预测的结果,将筛选的T细胞抗原表位与B细胞抗原表位以随机组合的方式进行整合,整合的肽段由南京金斯瑞生物科技有限公司偶联KLH蛋白合成多肽P72-1与P72-2。
1.3.3 小鼠免疫 3~5周龄SPF级BALB/c雌性小鼠30只,随机分为3组:P72-1、P72-2和PBS组每组10只。P72-1和P72-2组分别腹腔注射免疫合成肽疫苗P72-1和P72-2,PBS组腹腔注射免疫PBS作为阴性对照,共免疫3次,每隔14 d免疫一次,剂量50 μg/只,首免佐剂为弗氏完全佐剂,二、三免佐剂为弗氏不完全佐剂。
1.4 免疫效果评估
1.4.1 特异性抗体检测 采用ELISA方法检测免疫后P72-1与P72-2特异性抗体,分别用10 μg/mL的P72-1与P72-2蛋白包被ELISA板,经封闭液封闭后,加入以1∶10稀释于PBS中的免疫动物血清,37 ℃孵育1 h,PBST洗3次,加入100 μL HRP标记的山羊抗小鼠IgG(1∶10 000)37 ℃孵育1 h,PBST洗3次,加入TMB显色液常温避光反应15 min,加入100 μL ELISA终止液,酶标仪测定D450 nm值,根据P/N(阳性D450 nm值/阴性D450 nm值)计算是否产生特异性抗体及其抗体效价,免疫组(P)/PBS组(N)>2.1即视为检测到特异性抗体。
1.4.2 脾脏淋巴细胞增殖试验 每组随机取3只小鼠,断颈处死后浸泡于75%乙醇中10 min,于超净工作台分离淋巴细胞,100 μL/孔加到96孔细胞板中,用终浓度为10 μg/mL的P72-1、P72-2刺激淋巴细胞,无抗原组为对照,37 ℃、5% CO2条件下培养68 h后每孔添加10 μL CCK-8,37 ℃放置1 h,测定D490 nm值,根据测量的吸光度,按照下式计算刺激指数(SI):SI=(特异性抗原刺激孔平均D490 nm值-本底D490 nm值)/(无抗原刺激孔平均D490 nm值-本底D490 nm值)。
1.4.3 流式细胞术检测T淋巴细胞亚群 抽取首免56 d后小鼠外周血于抗凝管内,加入20 μL荧光标记流式抗体CD3+、CD4+、CD8+,混匀,室温避光放置20 min后加入450 μL溶血素,混匀,室温避光放置20 min,流式细胞术检测外周血淋巴细胞亚群精准计数。
1.4.4 细胞因子检测 采集P72-1、P72-2及PBS组小鼠首免后14、28和42 d的血清100 μL,根据试剂盒说明书检测细胞因子IL-2、IL-4和IFN-γ含量。
1.4.5 统计分析 试验数据均用 GraphPad Prism 8.0软件进行分析,所有试验设置 3 个重复样品,用t检验进行差异显著性分析。试验结果以平均值±标准差表示。P<0.05表示差异显著;P<0.01表示差异极显著。
2 结 果
2.1 抗原表位分析结果
P72蛋白的分子式为C3303H5036N904O948S18,分子质量为73 154.89 u,由646个氨基酸组成,平均亲水系数为-0.392,不稳定系数为38.30,是稳定性亲水蛋白,在哺乳动物中的半衰期为30 h;其蛋白结构中含有88个磷酸化位点:31个丝氨酸(Ser)位点、7个苏氨酸(Thr)位点、50个酪氨酸(Tyr)位点;二级结构中α-螺旋、β-转角、延伸链和无规则卷曲分别占19.35%、5.42%、25.08%和50.15%。通过IEDB、ABCpred、SVMtrip在线软件预测B细胞与T细胞抗原表位,结果见表1、2,综合各项分析结果,最终确定P72-1由4条多肽组成,多肽序列位置587-606、520-528、203-211、39-58位氨基酸处;P72-2由4条多肽组成,多肽序列位置为626-634、298-306、232-251、110-129位氨基酸处。

表1 P72蛋白B细胞表位分析
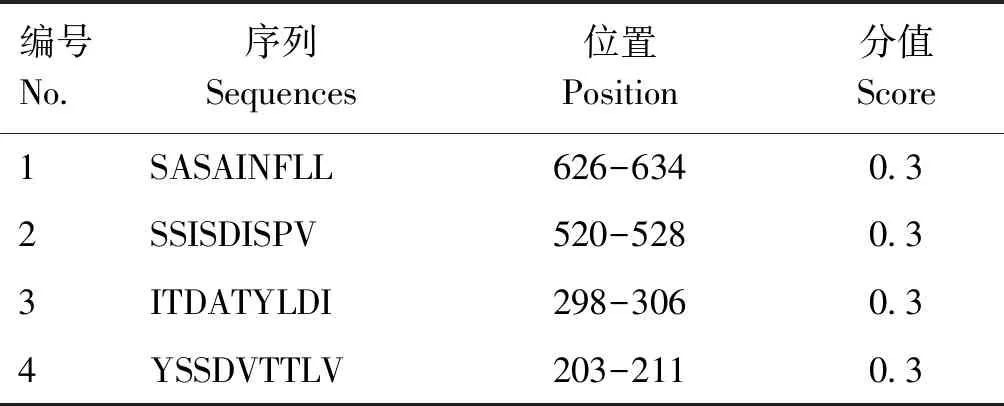
表2 P72蛋白T细胞表位分析
2.2 特异性抗体水平检测
采用ELISA方法分析每次免疫后小鼠血清中特异性抗体效价,合成肽疫苗免疫组小鼠接种后分别能检测到针对P72-1与P72-2的特异性抗体反应,且抗体水平明显高于PBS组,最高抗体水平出现在一免后28 d,P72-1最高效价为1∶25 600,P72-2最高效价为1∶12 800,PBS组小鼠血清中未检测到特异性抗体(图1)。
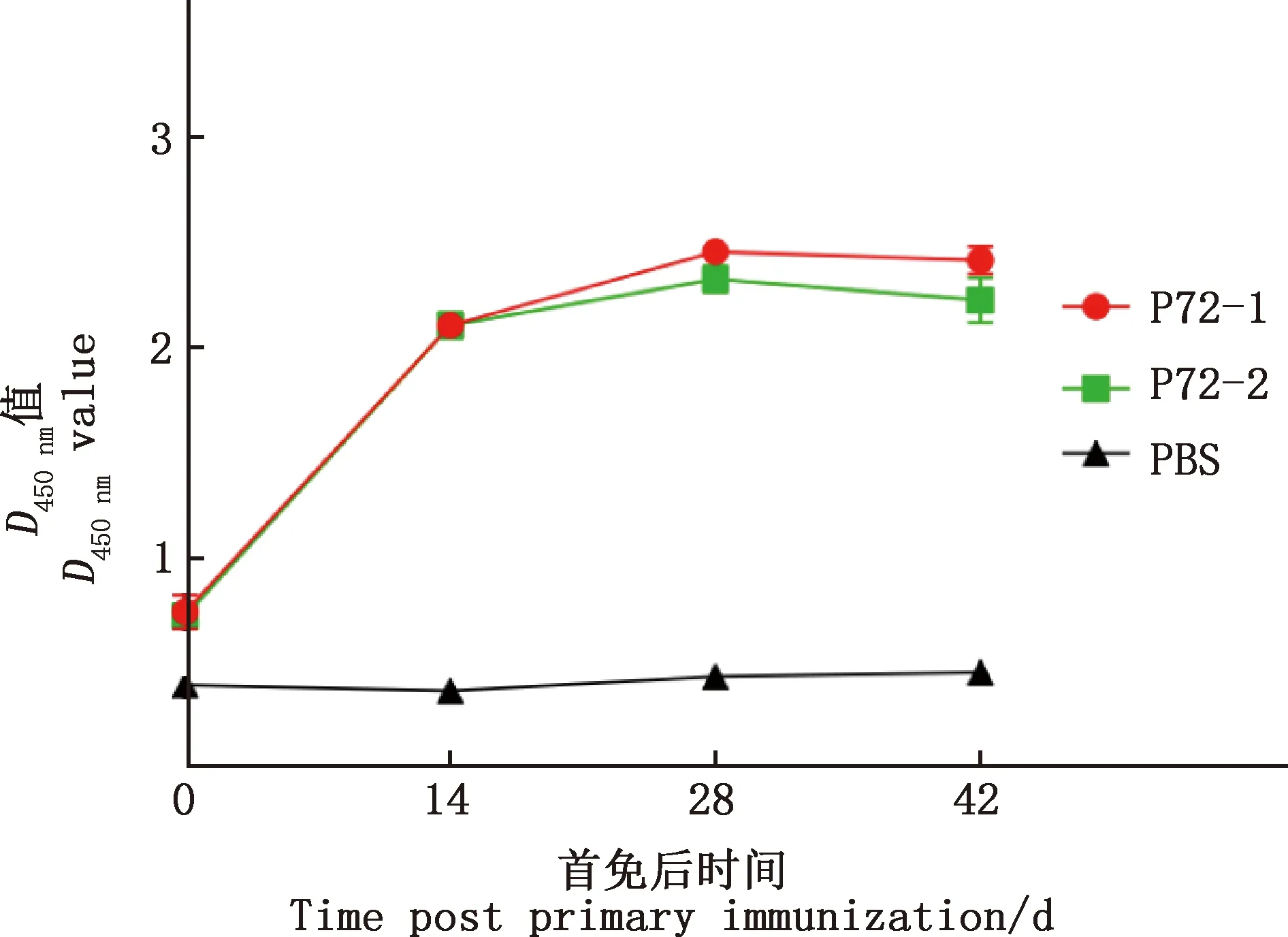
图1 免疫小鼠特异性抗体检测Fig.1 Detection of specific antibodies in immunized mice
2.3 脾脏淋巴细胞增殖试验
由图2可知,合成肽疫苗免疫组的刺激指数均极显著高于PBS组(P<0.01);P72-1组高于P72-2组,但无显著性差异(P>0.05),表明P72-1、P72-2合成肽疫苗能诱导机体的特异性脾脏淋巴细胞增殖。

*,差异显著(P<0.05);**,差异极显著(P<0.01);无*,差异不显著(P>0.05)。下同*,Significant difference (P<0.05);**,Extremely significant difference (P<0.01);No *,No significant difference (P>0.05).The same as blow图2 合成肽引起的脾脏淋巴细胞增殖Fig.2 Spleen lymphocyte proliferation induced by synthetic peptides
2.4 T细胞亚群检测
小鼠分别免疫P72-1、P72-2、PBS制备的合成肽疫苗56 d后,取外周血对T淋巴细胞亚群表达水平情况进行比较,结果见图3。由图3可知,P72-2组的CD4+T淋巴细胞的比例最高,达到77.0%,其次是P72-1组占比75.9%,PBS组为70.6%。CD8+T淋巴细胞的比例最高的是PBS组,为27.8%,P72-1与P72-2占比分别为22.6%和21.6%。将合成肽疫苗组与PBS组的CD4+/CD8+比值进行分析,结果见图4。由图4可知,合成肽疫苗组的CD4+/CD8+比值显著高于PBS组(P<0.05),且P72-2显著高于P72-1(P<0.05),表明P72-1、P72-2能显著诱导体液免疫与细胞免疫,P72-2诱导能力更强。

图3 T细胞亚群检测结果Fig.3 Detection results of T cell subsets

图4 T细胞亚群CD4+/CD8+比值Fig.4 CD4+/CD8+ ratio of T cell subsets
2.5 细胞因子检测
取免疫后42 d小鼠血清,通过ELISA方法检测小鼠外周血中细胞因子IFN-γ、IL-2、IL-4的含量。由图5可知,与PBS组相比,P72-1和P72-2组的IFN-γ、IL-2、IL-4含量均升高,其中P72-1和P72-2组的IL-4、IL-2含量在免疫后42 d时极显著升高(P<0.01),在免疫后28 d时,除P72-1组IL-2含量显著升高外(P<0.05),其合成肽疫苗组检测值均极显著升高(P<0.01);在免疫后14 d时,P72-2组IFN-γ与IL-4含量均显著升高(P<0.05),P72-1组IL-4含量极显著升高(P<0.01);P72-1与P72-2组细胞因子IL-4、IL-2、IFN-γ各个检测值之间均存在差异,但只在IL-2上存在显著性差异,表现为P72-2组显著或极显著高于P72-1组(P<0.05;P<0.01)。

A,IL-2;B,IFN-γ;C,IL-4图5 合成肽引起的细胞因子变化Fig.5 Cytokine changes induced by synthetic peptides
3 讨 论
非洲猪瘟是一种高度传染的出血性疾病,病死率接近100%[16],近年来在非洲、欧洲、亚洲等地频繁暴发,严重影响了区域间的生猪及猪肉副产品的贸易流通,对全球养猪业造成灾难性的打击[17],但其病原体ASFV结构复杂且缺乏负责诱导保护性免疫抗原的知识,尚未研发出有效的非洲猪瘟疫苗。
P72是ASFV的主要结构蛋白,基因序列高度保守,在病毒感染后期表达,对病毒衣壳的形成具有重要意义[18],已有许多研究利用P72蛋白作为候选抗原研制疫苗。谢灵志[19]利用P72蛋白制备重组腺病毒载体疫苗注射小鼠后,引起了小鼠淋巴细胞的增殖及细胞因子分泌,显著增强了机体的细胞免疫应答水平;Chen等[20]通过反向遗传学方法表达P72蛋白构建的新城疫病毒rNDV/P72,不仅在小鼠模型中产生了高水平的特异性IgG抗体,还促进了T淋巴细胞的增殖,提升了机体的免疫应答水平;但目前对于P72蛋白优势抗原表位的免疫效力研究还鲜有报道,因此,本研究利用P72蛋白的优势抗原表位制备了合成肽疫苗P72-1与P72-2,并对其免疫效力进行评估。
利用生物信息学方法预测、筛选蛋白抗原表位已成为表位疫苗研究的首选方法,不仅能提升疫苗的安全性,同时能保留较强的抗原性[21]。本试验利用生物信息学方法对P72蛋白抗原表位进行分析预测,经筛选得到8个优势抗原表位,与传统表位筛选过程比,此方法有工作量小、准确性高等优点,并已成功应用在猪O型口蹄疫病毒合成肽疫苗的研究中[22]。本研究制备的合成肽疫苗P72-1与P72-2包含的优势B细胞与T细胞抗原表位在机体内引起了良好的免疫反应,间接ELISA结果表明,免疫小鼠在首免14 d后就产生了高效价特异性抗体,这与EV-D68病毒的合成肽疫苗引起的特异性抗体效果一致[23],证明筛选的抗原表位具有良好的免疫原性。本研究通过对免疫组小鼠外周血及血清检测发现免疫组小鼠的T细胞亚群指数与细胞因子增殖情况显著高于对照组,表明疫苗显著提高了机体的免疫应答水平。此外,淋巴细胞的增殖试验作为反映机体淋巴细胞增殖的一种方法,能有效评价机体的免疫功能[24],本试验结果显示免疫后脾脏淋巴细胞显著增殖情况,表明疫苗显著提高了机体的细胞免疫应答水平。唐华[22]构建的A型口蹄疫病毒合成肽疫苗在小鼠体内导致T细胞亚群显著变化;孟媛等[25]制备的塞尼卡病毒VP1蛋白的亚单位疫苗在小鼠模型中引发了显著的细胞因子变化;魏冰[26]在研究Th表位合成肽对O型口蹄疫病毒合成肽疫苗的增效作用中发现小鼠T淋巴细胞的转化率显著上升。这些研究都表明了具有良好免疫效力的疫苗能显著激活机体的免疫应答,本研究基于优势抗原表位设计的合成肽疫苗P72-1与P72-2具有良好的免疫效力。
尽管本试验制备的合成肽疫苗免疫小鼠后在小鼠体内有较好的免疫反应,但ASFV的感染机制尚未完全明确,且未进行猪的免疫效力评价及攻毒保护试验,后续研究中还需继续筛选更多抗原的优势表位来优化疫苗的设计,以期能获得更好的免疫保护效果。
4 结 论
本研究初步探索了ASFV P72蛋白合成肽疫苗的免疫效力,通过分析P72蛋白的结构和预测其抗原表位,成功构建了多肽疫苗P72-1与P72-2,通过免疫小鼠,表明该疫苗具有良好的免疫原性,为ASFV多肽疫苗的研制奠定技术基础。
