静注人免疫球蛋白辅助常规疗法治疗小儿重症肺炎的有效性及安全性分析
2022-08-17孔雪
孔 雪
(蚌埠市第一人民医院,安徽 蚌埠 233000)
小儿肺炎是儿科多发的呼吸道性疾病,该疾病的主要发病原因是细菌、病毒、支原体以及衣原体感染,发病后,若治疗不及时,患儿会出现气促、咳嗽、气喘、肺部鸣音等一系列表现与症状,既会进展成为重症肺炎,重症肺炎的临床症状主要以咳嗽、发热、气憋以及紫绀等为主,若病情较重,还会出现惊厥、呼吸困难等,提升了发生多个器官功能衰竭的机率,这类患儿如果得不到及时且有效的抢救,将会对患儿的肾脏、大脑等造成十分严重的损害,甚至是会危及到患儿的生命安全[1]。目前,临床上针对小儿重症肺炎患儿的治疗,主要以常规抗感染、强心、镇静、氧疗、利尿以及抗病毒方案为主,但是疗效不够理想,而在近年来的多项研究中显示,小儿重症肺炎的发病与发展和患儿的自身免疫功能间有着密切的相关性,特别是以Ig(免疫球蛋白)分泌量不足最为典型,故认为增强患儿的免疫功能对其疾病预后的改善具有积极作用[2-3]。基于此,本文选取92例入我院治疗的小儿重症肺炎患儿,研究了小儿重症肺炎患儿以常规方案治疗,及以常规方案联合人免疫球蛋白静注治疗的有效性与安全性,现将内容报告如下:
1 对象和方法
1.1 对象
选取92例2019年8月-2020年8月期间入我院治疗的小儿重症肺炎患儿,以随机抽取方式进行对等分组,A组(n=46):单以常规疗法开展治疗,本组患儿男性26例,女性20例;患儿年龄7个月~6岁,均值(3.11±0.79)岁;发病到入院时间分布在2~16d之间,均值(7.52±0.73)d;合并症:17例伴随有心力衰竭者,20例伴随有呼吸衰竭者,合并中毒性脑病9例;B组(n=46):除了开展常规治疗之外,再以人免疫球蛋白静注作为辅助,本组患儿男性24例,女性22例;患儿年龄6个月~7岁,均值(3.24±0.81)岁;发病到入院时间1~15d,均值(7.43±0.68)d;合并症:心力衰竭伴随者19例,呼吸衰竭伴随者21例,同时出现中毒性脑病者6例;此次研究已经获得我院伦理委员会授权,且比较2组相关数据显示无显著差异(P>0.05),证实对比可行。
入组标准:(1)所有患儿均经临床确诊与小儿重症肺炎疾病相关诊断标准一致,并经多项检查确诊疾病;(2)所有患儿家属均已同意参与研究,还签了知情同意书。
排除标准:(1)机体营养不良者;(2)并发先天性疾病者;(2)并发其他重要脏器功能障碍者;(3)2周使用过抗生素者;(4)合并免疫缺陷疾病者;(5)合并支气管畸形者;(6)具有药物过敏史者;(7)合并恶性肿瘤者;(8)患有中毒性脑病或呼吸衰竭者;(9)合并心力衰竭者。
1.2 方法
A组患儿以常规疗法开展治疗,主要包括吸氧、消炎、解痉、增强微循环、纠正水电解质失衡、补液、补充营养、呼吸道通畅维持等基础治疗,对于并发心力衰竭者,再对其使用洋地黄型药物进行强心治疗;对于出现呼吸衰竭的患者而言,再对其施予正压通气进行干预,抗感染药物选择阿奇霉素[生产厂商:江苏吴中医药集团有限公司苏州制药厂,批准文号:国药准字H20010606,规格:2.5mL∶0.25g(按C38H72N2012计)],进行静注,用量:1mg/(kg·d),对患儿持续治疗7d的时间。
B组患儿在A组患儿治疗的基础上,再给予其人免疫球蛋白[生产厂商:上海生物制品研究所有限责任公司,批准文号:国药准字S10970081,规格:300mg(10%,30mL)],进行静滴辅助治疗,用量:200~400mg·kg·d-1,患儿需要持续用药治疗7d。
1.3 指标观察
(1)评价2组临床疗效:治疗后,经实验室、影像学检查各项体征恢复正常,咳嗽、发热消失,经过检查,发现其肺部湿啰音均已消失,判定为显效;治疗后,相关指标已经基本上恢复正常,咳嗽、发热等表现都明显减轻,经查体后,发现肺部仅有轻微湿啰音,判定为有效;治疗后,患儿相关的体征与症状均不见任何改善,相关症状无任何缓解甚至加重,判定为无效。(显效例数+有效例数)/总病例数*100%=总有效率。
(2)治疗前、后,检测分析两组患儿的免疫功能指标,取患儿的外周静脉血5mL,以3000 r/min的速度对其进行离心处理,持续10min,提取上清液,以免疫比浊法对其免疫球蛋白G(IgG)、免疫球蛋白A(IgA)以及免疫球蛋白M(IgM)水平进行检测。
(3)对2组患儿发生不良反应的相关情况进行分析、研究,其中,不良反应主要即皮疹、嗜睡、恶心呕吐。
(4)记录2组患儿的临床症状消失时间,其中,临床症状消失时间主要即咳嗽消失时间、喘息消失时间、肺部湿啰音消失时间以及住院总时间。
1.4 数据分析处理
2 结果
2.1 对比2组的治疗效果
治疗后,进行治疗疗效对比,发现B组的治疗总有效率相对比A组显著较高,P<0.05,见表1。

表1 对比2组的治疗效果[n(%)]
2.2 对比2组治疗前后的免疫功能指标
2组治疗前的各项免疫功能指标,统计学分析结果显示无显著意义(P>0.05);但治疗后,B组的IgG、IgA及IgM水平均较A组明显更高,P<0.05,见表2。
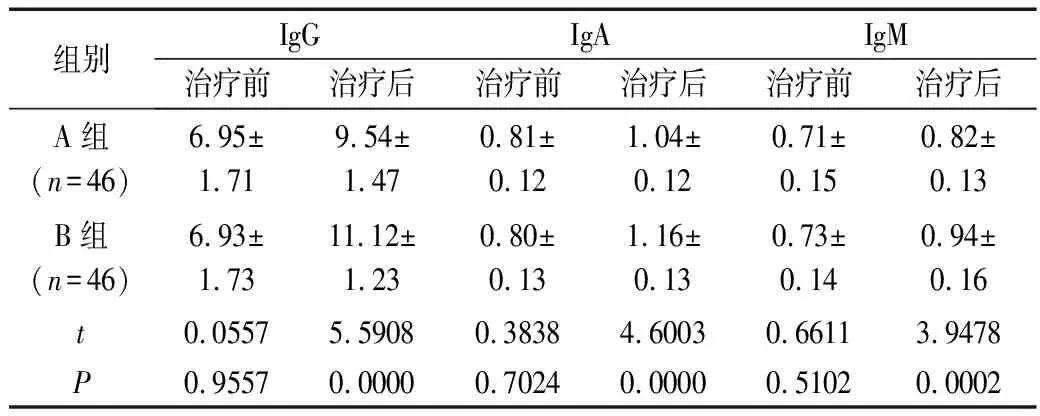
表2 各项免疫功能指标(mg/mL)
2.3 对比2组的不良反应发生率
A组患者治疗后有1例(2.17%)患者发生嗜睡、0例(0.00%)患者发生皮疹、1例(2.17%)患者发生恶心呕吐,不良反应的总发生率为2例(4.34%);B组患者治疗后有1例(2.17%)患者发生嗜睡、1例(2.17%)患者发生皮疹、1例(2.17%)患者发生恶心呕吐,不良反应的总发生率为3例(6.52%);两组评分数据对比(χ2=0.2115,P=0.6455>0.05),不具有统计学意义。
2.4 对比2组的症状缓解与住院情况
治疗后,对比2组的症状缓解与住院情况,显示B组的咳嗽消失时间、喘息消失时间、肺部湿啰音消失时间、住院总时间相对比A组显著较低,P<0.05,见表3。
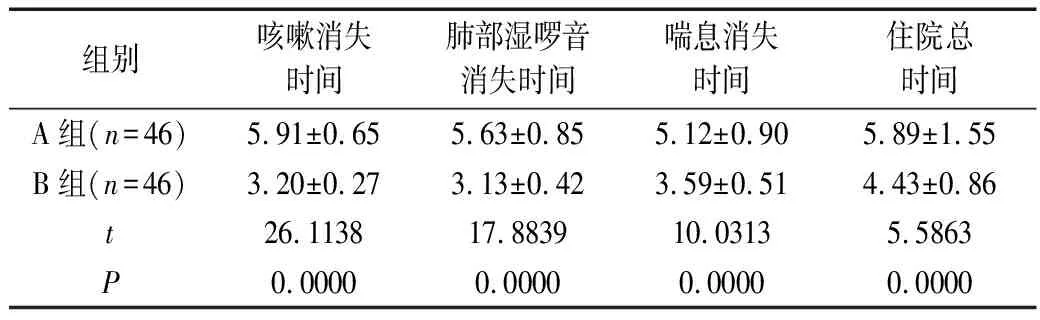
表3 临床症状消失时间与住院总时间(d)
3 讨论
对于小儿重症肺炎而言,其是儿童呼吸系统较为普遍的感染性高危疾病,以冬、春季气候发生变化时为疾病的高发期,夏季偶有发生,对于患儿的生命健康危害极大,该疾病的诱发病菌比较多,例如临床中极为常见的小儿肺部感染病毒、肺炎链球菌以及金黄色葡萄球菌等,此类病原菌会在在患儿的肺部黏附,并于局部发生增殖,对肺部的正常循环造成影响,导致气道发生阻塞,病情恶化后会对患儿毛细血管当中的内皮细胞、肺泡上皮细胞等造成损伤,致使肺泡的表面无法产生活性物质,降低肺部的顺应性,形成肺实变,增加低氧血症发生的风险。近年来,伴随着环境污染问题的逐步加重,加上儿童本身的免疫功能较弱,使儿童发生重症肺炎的风险不断升高,呈现为逐年上升的趋势,发病后,患儿如果未能得到及时且有效的治疗,病情进展甚至是极有可能引发呼吸衰竭,对患儿的生命安全造成十分严重的危害。因此,临床上需要及时采取科学且合理的治疗方案,对该类患儿的病情加以控制,以确保患儿的生命健康,促进预后[4-5]。当前,临床上对于小儿重症肺炎患儿的治疗主要以吸氧、促进分泌物排出、抗感染、抗炎以及抗菌等常规治疗为主,再配合以补液、营养支持以及止咳、解痉、平喘等方面的治疗,但是其整体的疗效不佳[6]。近年来,有学者提出,小儿重症肺炎的临床预后与患儿的免疫力功能间有着密切的相关性,故认为以人免疫球蛋白静注辅助常规疗法可以提升小儿重症肺炎的临床疗效。
对于免疫球蛋白,其能够维持好人类的各项免疫功能,当中的IgG一般来说都是以单体存在,在免疫球蛋白含量当中可以占70%~75%,是初级性免疫应答当中持久性最高的一类抗体,可以对外毒素进行有效中和,对吞噬细胞具备的吞噬活性进行合理调控[7]。IgA则是存在量仅低于IgG的一种蛋白,在人类机体被刺激之后,最早产生的一种抗体,并于黏膜的免疫过程中发挥出一定的作用,具有一定的呼吸道类感染病症防御效果[8]。IgM则是一种有着极强溶菌、杀菌以及促吞噬功能的抗体,是人类机体防御系统当中至关重要的一种因子[9]。而在本次的研究结果当中显示,治疗后,B组患儿的IgA、IgM以及IgG相较于A组患儿明显更低,P<0.05,而B组患儿的治疗有总有效率相对比A组患儿显著较高,P<0.05,治疗后,对比2组的症状缓解与住院情况,显示B组的咳嗽消失时间、喘息消失时间、肺部湿啰音消失时间以及住院总时间显著低于A组,P<0.05,这一结果表明,采用人免疫球蛋白为患儿静注治疗之后,小儿重症肺炎患儿血液当中的IgG水平有了明显的提升,对患者儿机体的免疫调节功能进行了有效改善,使患儿的症状缓解时间、住院时间均有缩短,究其原因可能是:对于人免疫球蛋白而言,其成份大多都是蛋白质,且其成份当中还含有大量的抗病毒以及多种IgG抗体,因此,药物经过静脉滴注的方式进入到患儿的血液当中之后,使得患儿的IgG水平有了明显的升高,进而能够增强患儿的免疫功能,并使其具备更强的对抗感染能力,对于患儿具有十分关键的作用,患儿的疾病治疗疗效得到了有效提升[10]。此外,本次研究的结果还显示,治疗后,B组患儿出现不良反应的概率相较于A组患儿差异并不明显,P>0.05,这表明以人免疫球蛋白进行辅助治疗后,可以提升小儿重症肺炎患儿的疗效,但是不会增加其药物相关不良反应发生率,具有更高的安全性。
小儿重症肺炎患儿以人免疫球蛋白进行治疗,可以增加患儿的免疫功能,并缩短患儿的咳嗽消失时间、喘息消失时间、住院总时间等,提升患儿的疾病治疗效果。
