国家基本药物目录药品备选库形成机制设计与路径模拟*
2022-08-12杜雯雯徐伟经天宇
杜雯雯,徐伟,经天宇
(中国药科大学国际医药商学院,南京 211198)
我国基本药物制度自2009年实施以来,在保障医疗机构临床用药需求、促进药品公平可及、提升临床合理用药水平等方面发挥了至关重要的作用[1-3]。作为基本药物制度的重要载体之一,国家基本药物目录(简称国家基药目录)的制定和调整向来是关系人民健康福利、影响我国医药行业发展的重大事件。从程序上看,国家基药目录的制定与调整主要包含两大步骤,一是形成药品备选目录,二是对备选目录进行遴选[4]。作为目录调整的先行步骤,药品目录备选库形成机制对于最终药品的准入具有重要影响。相比于其他国家或地区鼓励社会各界参与申报的做法,我国基药目录药品备选库形成仍以部门遴选为主,社会参与度、机制透明度均有待进一步提高。基于此,笔者在本文首先对典型国家/地区药品目录备选库形成机制进行梳理和对比,总结其中可供我国参考的经验;在此基础上结合我国实际及相关政策指导和要求,设计国家基药目录药品备选库遴选方案,并利用现有资料及2020年江苏省医疗机构药品采购数据进行路径模拟,验证设计方案的可行性,以期为国家基药目录备选库形成机制的优化与完善提供建议和参考。
1 典型国家和地区药品目录备选库形成机制及对我国的启示
1.1典型国家和地区药品目录备选库形成机制 从典型国家和地区经验来看,当前除我国基药目录、加拿大CLEAN药品目录(the Carefully selected and Easily Accessible at No Charge Medicines,CLEAN Meds)[5]采取部门遴选制外,其他国家/地区药品保障目录主要采取申报制,包括中国台湾、日本等地实行的企业申报制[6-8],中国香港、南非等地选择的医院申报制[9-12],以及世界卫生组织(WHO)、英国和泰国采取的开放式申报制[13-18]。通过比较梳理可知,无论是部门遴选制、企业申报制、医院申报制还是开放式申报制,均存在优点和不足。具体总结见表1。
1.2对我国基药目录药品备选库形成机制的启示 由表1可知,尽管以部门组织专家遴选的形式可以快速实现对目录的调整,但与典型国家/地区药品保障目录多元化的药品备选库形成机制相比,此举透明程度较低、依赖专家的主观经验较多,导致药品备选名单的科学性和客观性得不到保证。

表1 典型国家/地区药品目录备选库形成机制对比
当前,大多数国家或地区采用企业申报制形成其药品保障目录备选库,但实行企业申报制要求药品目录本身已经相对完整,目录调整的流程体系也相对成熟和稳定。而自2009年以来,我国基药目录仅进行了3次国家层面大范围调整,目录本身仍有较大扩容调整空间,且我国医药企业尤其是仿制药企业众多,若此时采用企业申报制必然造成大规模重复申请,降低目录申报效率。
WHO基本药物标准清单、中国香港医管局药物名册以及南非基药目录备选库均选择或囊括了医院申报制,其中WHO不限制申报主体,中国香港和南非均规定仅医疗机构或卫生工作者有申请资格,并强调不接受企业递交申请[12,19]。WHO虽不限制申请主体,但由于企业提交的资料常存在偏向性且未必能反映临床实际需求,故相较于其他主体其申请通过率偏低(表2);中国香港和南非要求医院在申请中详细注明目标用药患者群组详情,包括患者专科组别、疾病种类、严重程度等,反映的临床需求真实性较高[12,20]。作为指导临床用药的核心目录,基药目录所收载的药品须与临床主要用药需求相吻合,故我国在形成基药目录药品备选库时,应当征询医疗机构意见。
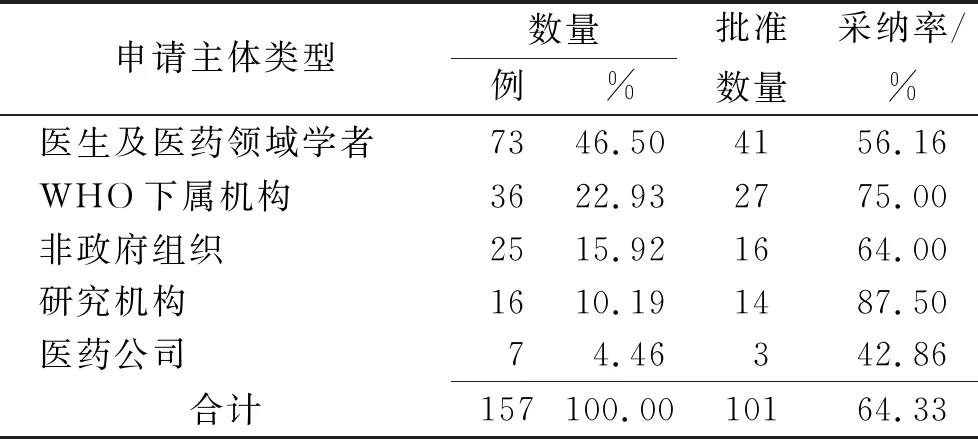
表2 2019版WHO基本药物标准清单申请采纳情况
2 我国基药目录药品备选库形成机制设计
《国务院办公厅关于完善国家基本药物制度的意见》(国办发〔2018〕88号)提出,基本药物的遴选要“以诊疗规范、临床诊疗指南和专家共识为依据”,“强化循证决策,突出药品临床价值”。可见,尊重临床意见、以临床真实需求为导向是我国基药目录制定的核心和关键。考虑到我国现阶段推进基药目录调整工作的可操作性,同时鉴于基药目录指导临床合理用药的定位,以及需与医保政策有效衔接[21-22],笔者建议我国基药目录药品备选库可由原来的部门遴选制调整成以临床诊疗指南推荐品种为主导、医保和医疗机构为重要补充的药品目录备选库形成机制(图1)。
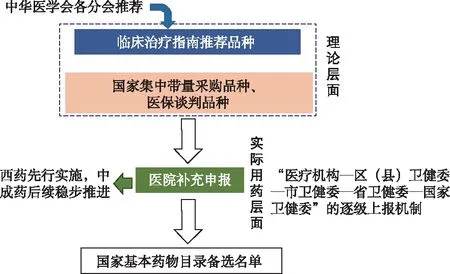
图1 我国基药目录药品备选库形成机制(建议)
2.1基于临床诊疗指南形成初步备选名单 由国家卫健委组织专家检索临床诊疗指南,整理出指南推荐的药品品种,形成初步名单。临床诊疗指南是基于系统评价证据、平衡不同干预措施利弊、能为患者提供最佳医疗保健推荐意见的有效工具[23],对于促进卫生保健事业发展和医疗质量提升具有重要作用。当前我国临床诊疗指南大部分由中华医学会各分会及其学组制定并更新,以抗肿瘤用药为例,2016年1月—2021年5月,在我国上市的抗肿瘤用药共60个品种,其中50个已进入中国临床肿瘤学会(Chinese Society of Clinical Oncology,CSCO)临床诊疗指南,且>90%药品在上市1年后即可进入指南(图2)。因此笔者建议,指南的选取可直接采用中华医学会各分会制定的临床诊疗指南,或者由其负责推荐各疾病治疗领域常用权威指南,并对外公开相关信息,以保证指南选取的公正性和可靠性。

图2 2016—2021年在我国上市的抗肿瘤药进入指南情况
2.2增补不在遴选范围内的国家集中带量采购和医保谈判品种 在上述基础上,参照医保部门所发文件,增补不在上述名单范围内的国家集中带量采购和医保谈判品种,从而实现与医保药品目录及其相关政策衔接。随着国家集中带量采购的不断推进,我国基本形成了至少一年一次采购周期的模式,具体开展和要求各地落地时间见表3。由表3可知,国家在组织药品集中带量采购时,其中标品种、品规数量正逐渐增加,政策落地越来越迅速;同时,随着集中采购规则的不断完善,药品采购周期随中选企业数量增多而增长。截至2021年10月,国家集中带量采购中选药品按品种共计187个,其中92个为非基药品种。作为医院未来可能大量、连续采购的产品之一,与国家集中带量采购药品形成稳定衔接机制是国家基药目录在动态调整中必须完成的一环。

表3 国家药品集中带量采购政策内容汇总
同样,我国医保谈判药品的数量也呈现逐年增加势态(图3)。截至2021年11月,医保协议期内谈判药品部分药品品种共221个,其中非基药品种204个。由于医保谈判药品多为近年来新上市、疗效确切且具有较高临床价值的药品,涵盖了癌症、糖尿病、心脑血管、风湿免疫、消化等众多疾病治疗领域,实现基药目录与其衔接将有助于提高该部分药品在临床的可及性。
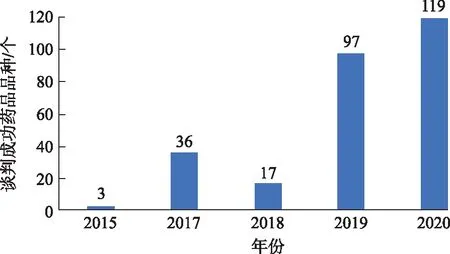
图3 历年药品谈判成功数量(2019年包含新增和续约)
2.3医疗机构补充意见,形成国家基本药物备选库 在理论层面的基础上,进一步组织医院就临床用药实际进行品种增补,形成国家基药目录备选名单。考虑到由医疗机构直接向国家卫健委提交药品备选库补充意见可行性不高,因此建议参考南非做法,积极发挥地方卫健委作用,由其首先负责统计地方医院补充意见,再统一上报至国家卫健委,形成“医疗机构-区(县)卫健委-市卫健委-省卫健委-国家卫健委”的逐级上报机制。
与西药相比,当前中成药临床使用不规范现象较严重,故笔者建议国家基药目录在设计和调整中成药备选方案时,可以采取“小步走”“主循证”战略,即重视中成药临床证据质量,小范围、多阶段进行增补和调整,在中成药药品备选库路径设计中,暂时不安排“医院补充申报”这一路径,而是选择委托中医学专家从中医临床诊疗指南中筛选部分药品进行补充,如古方、经方、验方等。
此外,为提高医疗机构补充申报效率,规避过度申报,同时使补充申报品种能够真正基于临床用药实际,笔者建议增设以下4项条件对医疗机构补充申报品种作出限制:①发布国家基药目录调整通知之日起5年之内,经国家药监部门批准上市的新通用名药品;②发布国家基药目录调整通知之日起5年之内,根据临床试验结果向国家药监部门补充申请并获得批准,适应证、功能主治等发生重大变化的药品;③条件①、②的药品外,其余申报品种必须在医疗机构近1年内有使用记录;④如果是化学药品种,则必须是通过仿制药一致性评价的品种、参比制剂或原研药。
3 我国基药目录药品备选库方案路径模拟
3.1西药备选库:以抗肿瘤药为例 笔者根据我国癌症发病率,选取排名前10的病种,即以肺癌、胃癌、肝癌、结直肠癌、食管癌、前列腺癌、胰腺癌、淋巴瘤、乳腺癌、甲状腺癌为代表,模拟抗肿瘤用药基本药物西药备选库形成路径。
首先,假设以CSCO发布的上述10大病种的最新临床诊疗指南(表4)作为最终推荐治疗指南,梳理后可得纳入临床诊疗指南并且已经在国内上市(截止时间:2021年5月30日)的西药,按品种共计143个,其中独家品种57个,非独家品种86个。而我国目前可用于治疗上述10大癌症的药品按品种计共233个,其中独家品种98个,非独家品种135个。可见,采取从临床诊疗指南中筛选药品的方式,可一定程度缩小遴选范围,确保初步遴选出来的药品为临床推荐用药。

表4 10个代表性癌症病种临床诊疗指南名称
其次,进一步比对国家前4批次集中采购和医保谈判品种,对药品备选库名单进行增补;同时,依托江苏省2020年全省医疗机构药品采购数据库,结合上述拟定医疗机构补充申报条件限制,最大范围地模拟医院补充申报药品品种。
在上述基础上,剔除已经纳入基药目录品种,最终形成抗肿瘤用药基本药物西药备选库,各部分药品增补数量情况见表5。由表5可知,若按照本文设定方案执行,则最终10个癌症病种西药备选库将纳入药品品种150个,其中独家品种70个,非独家品种80个。

表5 不同条件下抗肿瘤治疗西药品种数
3.2中成药备选库 2021年初,国家中医药管理局发布首批中成药治疗优势病种临床应用指南,分别为中成药治疗血管性痴呆、冠心病、小儿急性上呼吸道感染、新生儿黄疸等优势病种14部临床应用指南。该部分指南遵循国际循证指南研制规范,充分尊重中医药辨证施治特色,故笔者以上述指南为例梳理推荐品种。由于国家中医药管理局目前仅对外发布了12个指南(表6),因此本文最终从指南中整理出中成药按品种93个,其中独家品种31个,非独家品种62个。

表6 中成药治疗优势病种临床应用指南
在上述基础上,进一步就医保谈判药品对中成药药品备选库名单进行增补(由于国家集中带量采购品种均为西药,因此在中成药药品备选库设计路径中,只需要考虑国家医保谈判品种),同时剔除已经在基药目录内的品种,最终可得:若仅从理论层面出发,则中成药药品备选库将纳入药品106种,其中独家药品71种,非独家药品35种。表7为不同条件下中成药药品备选库纳入品种情况。

表7 不同条件下中成药药品备选库纳入情况
4 总结
迄今为止,我国共发布了2009版、2012版、2018版3版国家基药目录,在推进基本药物制度实施、指导临床合理用药方面发挥了重要作用。随着药品市场不断发展,如何构建科学合理的药品遴选机制成为目录调整的关键工作之一。鉴于药品备选目录形成机制决定了药品遴选范围,因此当前除了对基药目录的评审标准和程序进行完善外,目录备选库形成机制同样需要优化与改进。通过借鉴典型国家和地区的经验做法,同时结合基药目录指导临床合理用药的定位,与医保政策的有效衔接以及我国政策指导方针,笔者建议未来国家基药目录可以形成以临床诊疗指南推荐品种为主导、医保和医疗机构为重要补充的药品目录备选库形成机制。在此种机制下,既可以体现目录在遴选药品过程中对循证决策理念的贯彻,又可充分尊重临床意见,并且能够与医保相关政策进行有效衔接,这对于进一步提高国家基药目录的适用性、权威性、科学性具有重要意义。
