人参总皂苷对伊立替康及其代谢产物在大鼠体内药动学的影响*
2022-08-12朱延焱冯炎林梅紫薇胡国新平丽田伟强
朱延焱,冯炎林,梅紫薇,胡国新,平丽,田伟强
(1.浙江省丽水市中心医院药学部,丽水 323000;2.温州医科大学药学院,温州 325035;3.浙江大学药物安全评价研究中心,杭州 310058)
人参为五加科植物人参PanaxginsengC.A.Mey的根。现代药理研究表明,人参具有广泛药理活性,包括抗肿瘤、抗高血压、抗疲劳、增强免疫等作用[1]。含人参的中药制剂临床广泛用于恶性肿瘤的辅助治疗。有研究指出,含人参制剂可以减少化学治疗(化疗)所致不良反应[2],亦有观点认为人参可以提高化疗疗效。伊立替康(irinotecan,CPT-11)是半合成喜树碱衍生物,属选择性DNA 拓扑异构酶Ⅰ抑制剂。2020年美国国立综合癌症网络(National Comprehensive Cancer Network,NCCN)结肠癌[3]、直肠癌[4]指南推荐:CPT-11与氟尿嘧啶、亚叶酸钙联合(FOLFIRI方案)是复发或转移性结直肠癌的一线化疗方案,疗效确切。笔者在本实验观察人参总皂苷与CPT-11合用后,CPT-11及其活性代谢产物7-乙基-10-羟基喜树碱(7-ethyl-10-hydroxycamptothecin,SN-38)在大鼠体内药动学的变化,以期为临床中西药联用提供参考。
1 材料与方法
1.1仪器 超高液相色谱-XEVO TQD 三级四重杆串联质谱联用仪(美国Waters),含有电喷雾离子源(electro-spray ionization,ESI),色谱工作站:Masslynx 4.1;Beckman 22R台式TGL-16G离心机(上海安亭科学仪器厂);XW-80A涡旋混合器(海门市其林贝尔仪器制造有限公司);XS105分析天平(上海梅特勒-托利多仪器有限公司,感量:0.01 mg);Milli-Q A10 超纯水系统(美国Millipore公司)。
1.2试药 注射用盐酸伊立替康(江苏恒瑞医药股份有限公司,规格:每支40 mg,批号:180712AF);SN-38(江苏恒瑞医药股份有限公司,纯度>98%,批号:A0816AS);人参总皂苷(西安维奥生物科技有限公司,批号:171110,总皂苷含量≥80%);卡马西平片(江苏鹏鹞药业有限公司,批号:1606161,规格:每片0.1 g);甲酸(色谱级,Aladdin chemistry Co.,Ltd,批号:E2022005);乙腈(色谱级,Tedia Company,批号:19085037)和甲醇(色谱级,Tedia Company,批号:19055136);其余常规化学试剂均为分析纯或优级纯(上海化学试剂公司)。
1.3实验动物 SD大鼠12只,无特定病原体(SPF)级,雌雄各半,体质量220~250 g,均购自温州医科大学动物实验中心,实验动物生产许可证号:SYXK(浙)2015-0009。所有SD大鼠饲养在温度相对恒定和自然通风的实验环境下[温度(25±1)℃,相对湿度(55±10)%,12 h光照和12 h黑暗交替,给予标准饲料喂养,自由饮水],适应7 d后进行实验。
2 方法与结果
2.1色谱条件 Waters Acquity UPLC BEH C18柱(2.1 mm×50 mm,1.7 μm),流动相:A 0.1%甲酸-B乙腈 (77:23),流速:0.4 mL·min-1,柱温:35 ℃,进样量2 μL。总运行时间为2.5 min。Masslynx 4.1版软件(Waters Corp.)用于数据采集和仪器控制。
2.2质谱条件 采用多反应监测(multiple reaction monitoring,MRM)模式,正离子MRM方式检测,驻留时间200 ms。扫描范围m/z:100→1000。MRM模式下CPT-11、SN-38、卡马西平离子跃迁分别为m/z587.3→167.2、m/z393.2→349.2、m/z237.1→194.2。ESI,电离电压;3.5 kV,锥孔电压:30 V,离子源温度150 ℃;雾化温度 498 ℃;雾化气流速 800 L·h-1,锥孔气流速50 L·h-1,碰撞气流速0.15 mL·min-1。
2.3血浆样品的处理 血浆样品采用乙腈沉淀蛋白方法,取大鼠血浆100 μL,加入乙腈200 μL,100 ng·mL-1卡马西平100 μL,涡旋2 min,13 000 r·min-1离心10 min (r=17 cm),取上清液100 μL,加入超纯水100 μL,混合后进样2 μL,超高效液相色谱-串联质谱(UPLC-MS/MS)法分析,测定大鼠血浆CPT-11及SN-38含量。
2.4给药方案与样品采集 SD大鼠12只,体质量220~250 g,雌雄各半,采用随机数字表法分成实验组与对照组,每组6只,禁食12 h后于实验当天上午给药,实验组灌胃人参总皂苷400 mg·kg-1,0.5 h后尾静脉注射CPT-11 20 mg·kg-1;对照组灌胃同体积0.9%氯化钠溶液,0.5 h后尾静脉注射CPT-11 20 mg·kg-1,分别于给药后 0.083,0.5,0.75,1,1.5,2,3,4,6,8,10,12,24 h经尾静脉取血约 0.2 mL,置含肝素的抗凝试管,13 000 r·min-1离心10 min(r=17 cm),上清液即血浆,-20 ℃ 保存待处理。
2.5方法学考察
2.5.1方法专属性考察 取 SD大鼠空白血浆100 μL,置 1.5 mL EP管,其余按“2.3”项下血浆样品处理方法操作,在本实验UPLC-MS/MS条件下进样2 μL分析,获得空白血浆色谱图;将一定浓度CPT-11标准系列溶液加入空白血浆,同法操作,获得相应色谱图,取静脉注射CPT-11后 SD大鼠 30 min时间段血浆样品,同法操作,得色谱图。血浆内源性杂质不干扰样品测定。同法测定大鼠血浆SN-38方法专属性。CPT-11保留时间0.43 min,SN-38保留时间0.75 min,内标卡马西平保留时间1.57 min,三者分离良好并在相应离子通道中相不干扰,见图1。
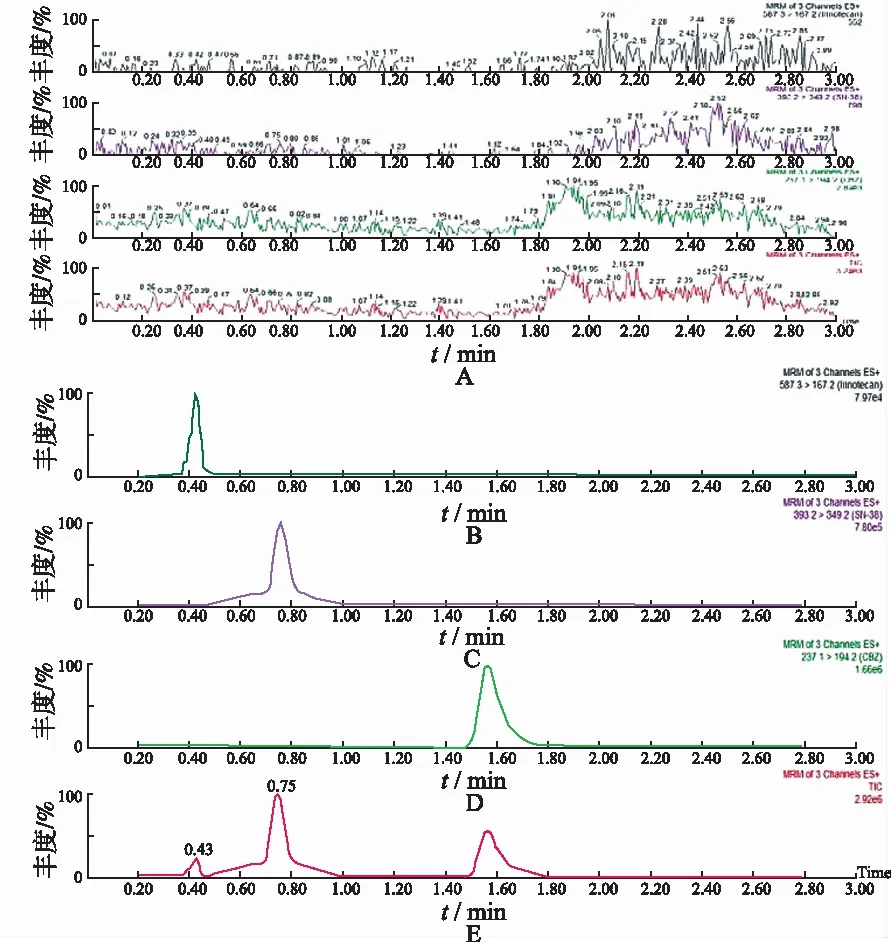
A.空白血浆;B.CPT-11;C.SN-38;D.卡马西平;E.CPT-11+SN-38+卡马西平。
2.5.2线性范围与定量限考察 精密量取4 mg·mL-1内标卡马西平溶液70 μL,加入CPT-11系列浓度溶液20 μL,置1.5 mLEP管,离心浓缩系统挥干,加入大鼠空白血浆100 μL,配制成CPT-11血浆浓度分别为0.005,0.05,0.5,1,2,5,20 μg·L-1标准模拟血浆工作曲线,按“2.3”项方法处理。所得结果以CPT-11血浆浓度为横坐标,所得CPT-11及内标峰面积比值为纵坐标,以最小二乘法进行回归运算,求得直线回归方程:Y=9998X(r=0.999)在0.005~20 μg·L-1内线性关系良好,考察定量下限为0.001 μg·L-1。同法测得大鼠血浆SN-38回归方程为:Y=9918X(r=0.999)在0.005~20 μg·L-1内线性关系良好,考察定量下限为0.001 μg·L-1。
2.5.3精密度实验 配制低、中、高浓度CPT-11血浆质控样本,按“2.3”项进行处理,进样2 μL,UPLC-MS/MS法分析。每浓度样品5个,连续测定 3 d,考察日内及日间精密度。CPT-11日内精密度与日间精密度RSD分别为5.71%~7.30%、5.71%~9.33%。同法测得大鼠血浆SN-38日内及日间精密度,RSD分别为5.73%~7.68%、3.20%~9.35%。
2.5.4回收率实验 配制低、中、高浓度CPT-11血浆质控样本各6份,按“2.3”项操作,进样2 μL测定,记录CPT-11峰面积(As);另取空白血浆,按“2.3”项操作,得空白基质,再加入用流动相配制的CPT-11对照品溶液,制备含空白基质的复合溶液,进样2 μL测定,记录峰面积(Am),按公式R=As/Am×100%,计算提取回收率。本实验条件下,血浆CPT-11提取回收率88.81%~97.81%;RSD 3.35%~13.34%。同法测得大鼠血浆SN-38提取回收率95.60%~106.29%;RSD 3.18%~12.55%。
2.5.5稳定性实验 本实验条件下,测得低、中、高浓度血浆CPT-11样品,室温放置24 h稳定性,RSD 5.13%~7.18%;样品置-20 ℃冰箱保存0,1,3 d稳定性,RSD 8.09%~10.61%;样品两次解冻冻融稳定性,RSD 7.43%~12.11%。同法测定大鼠血浆SN-38室温放置24 h稳定性,RSD 3.40%~9.35%;样品置-20 ℃冰箱保存0,1,3 d稳定性,RSD 5.47%~8.85%;样品2次解冻冻融稳定性,RSD7.63%~10.63%
2.6CPT-11及其代谢产物SN-38药动学特征 UPLC-MS/MS法测定实验组与对照组各时间点大鼠血浆CPT-11及SN-38浓度,DAS 3.1 版药动学软件处理血药浓度-时间数据,采用统计矩方法求算相应药动学参数,其中Cmax为实测值。采用SPSS21.0版软件对主要药动学参数进行统计分析。药时曲线见图2,药动学参数结果见表1。
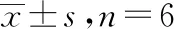
表1 两组大鼠血浆CPT-11与SN-38药动学参数

图2 两组大鼠血浆CPT-11与SN-38药-时曲线(n=6)
3 讨论
CPT-11是晚期或转移性结直肠癌一线化疗药物,化疗会导致严重不良反应,如骨髓抑制、迟发性腹泻、恶心呕吐、肝肾功能损害等,因此化疗期间临床上常使用辅助药物减轻化疗不良反应。人参具有大补元气、复脉固脱、补脾益肺、生津养血、安神益智等功效。有研究显示,人参可以减轻化疗所致不良反应[2]。亦有观点认为,人参可以提高化疗疗效,增强化疗药物细胞毒作用。人参以及含人参的中药制剂是临床常用辅助药物,如参麦注射液、生脉胶囊等。常见用法是化疗当天联合应用,于化疗药物使用前给药。因此,本实验中大鼠给药时,实验组单次灌胃人参总皂苷,0.5 h后尾静脉注射给予CPT-11,以模拟临床常见给药方式。
临床FOLFIRI方案中CPT-11剂量是180 mg·(m2)-1,按照体表面积1.7 m2、体质量60 kg、根据人体与实验大鼠剂量换算,大鼠给药剂量约33.15 mg·kg-1,但预实验时大鼠死亡率较高,且状态很差,活动度严重下降,奄奄一息,提示给药剂量偏大。给药10 mg·kg-1,血药浓度太低,检测受限。笔者参考文献[5],给药剂量定为20 mg·kg-1。CPT-11给药20 mg·kg-1,浓度测定与大鼠状态均较理想,因此本实验大鼠CPT-11给药剂量定为20 mg·kg-1。
CPT-11疗效与不良反应与SN-38紧密相关,SN-38活性是CPT-11原药1000倍,也是CPT-11剂量限制性毒性迟发型腹泻的主要原因。本实验条件下,大鼠给予人参总皂苷以及尾静脉注射CPT-11后,实验组与对照组药动学参数进行双尾配对t-检验,发现CPT-11大鼠体内药动学参数,实验组与对照组比较,人参总皂苷对CPT-11的药动学参数无明显影响,但明显延长SN-38大鼠体内半衰期(t1/2),差异有统计学意义。
CPT-11在体内经羧酸酯酶(存在组织、血清以及肝细胞内)作用下,转化成具有活性的代谢产物SN-38,在体内另一个代谢途径经细胞色素P450,其中主要为CYP3A4代谢生成7-乙基-10-[4-N-(5-氨基戊酸)-1-哌啶基]-羰基氧喜树碱(7-ethyl-10-[4-N-(5-aminovaleric acid)-1-piperidyl]-carbonyloxycamp-tothecin,APC)和7-乙基-10-(4-氨基-1-哌啶基)-羰基氧喜树碱[7-ethyl-10-(4-amino-1-piperidinyl)-carbonyloxycamptothecin,NPC][6]。而人参的主要活性成分人参皂苷化合物K(compound K)、原人参二醇(protopanaxadiol,PPD)、原人参三醇(Protopanaxatriol,PPT)对 CYP3A4均有强抑制性[7]。本实验条件下,与人参总皂苷合用,SN-38在大鼠体内半衰期延长,但对CPT-11药动学参数影响不大,这可能与人参皂苷给药方式有关。人参皂苷对CYP3A4酶的抑制作用单次给药作用不明显,需长期给药方可显现。另外影响CPT-11体内血药浓度还有一个重要因素,即肝细胞微粒体内将SN-38代谢成无活性的SN-38葡萄糖醛酸苷(7-ethyl-10-hydroxycamptothecin glycuronide,SN-38G)酶,尿苷二磷酸葡萄糖醛酸转移酶1A1(UDP-glucuronosylt transferase 1A1,UGT)[8],UGT1A1基因多态性对CPT-11体内血药浓度有影响。因此研究人参总皂苷对CPT-11血药浓度的影响,可能需要进一步消除UGT1A1酶对CPT-11及SN-38的干扰。
笔者在本实验研究条件下发现人参总皂苷可以延长大鼠体内CPT-11及其活性代谢产物SN-38半衰期,但人参总皂苷对CPT-11及SN-38影响的作用机制,以及如何进一步消除其他因素影响,仍值得进一步研究。
