纳米Fe3O4的制备及其催化的非均相Fenton高效降解亚甲基蓝
2022-08-05杨鹏辉敬思怡张静蕾春炜龙高雨如杨菲
杨鹏辉,敬思怡,张静蕾,春炜龙,高雨如,杨菲
(西安石油大学 化学化工学院,陕西 西安 710065)
Fenton氧化法是处理高浓度难降解染料废水的常用手段之一[1-3]。均相Fenton反应在实际应用中存在体系pH低、催化剂无法循环使用、易造成二次污染等问题[3-4]。在非均相Fenton反应中,纳米Fe3O4由于催化活性高、易于回收而备受关注[5-6]。纳米Fe3O4的制备方法及平均粒径等均会对Fe3O4-H2O2体系处理染料废水的效果产生影响。本实验利用易于工业化的共沉淀法制备了平均粒径为20 nm 的Fe3O4,研究了纳米Fe3O4-H2O2体系降解亚甲基蓝废水的影响因素,考察了催化剂的稳定性,讨论了反应机理。
1 实验部分
1.1 试剂与仪器
FeCl3·6H2O、FeSO4·7H2O、30%过氧化氢、盐酸、亚甲基蓝、邻菲啰啉均为分析纯。
Aeris X射线衍射仪;FTIR-850傅里叶变换红外光谱仪;T-2600型紫外可见分光光度计。
1.2 催化剂的制备[7]
称取一定量FeCl3·6H2O和FeSO4·7H2O,用蒸馏水溶解后加入少量盐酸。将反应液置于30 ℃的恒温水浴中,在快速搅拌下滴加0.4 mol/L氨水溶液,直至pH为10,此时溶液中有大量黑色Fe3O4生成。将反应液在60 ℃晶化1 h后抽滤,用无水乙醇洗涤数次,50 ℃真空干燥得到Fe3O4纳米颗粒。
1.3 亚甲基蓝的催化降解
移取30 mg/L亚甲基蓝溶液100 mL于250 mL三口瓶中,用4 mol/L盐酸调节溶液pH,加入一定量纳米Fe3O4催化剂和H2O2,开启机械搅拌,在一定时间取适量反应液,过滤后用紫外分光光度计在664 nm处测定其吸光度,用式(1)计算去除率。
(1)
式中E——去除率,%;
c0,c1——亚甲基蓝的初始浓度与t时刻亚甲基蓝的浓度,mg/L。
2 结果与讨论
2.1 纳米Fe3O4的表征
由图1纳米Fe3O4的XRD谱可知,2θ= 30.2,35.5,43.4,53.7,57.2,62.8°处的特征峰分别对应于Fe3O4标准谱中的(220)、(311)、(400)、(422)、(511)、(440)晶面,表明合成的是具有立方反尖晶石结构的Fe3O4,信噪比高,结晶度良好;图2所示Fe3O4的红外光谱中,571 cm-1处可见FeO的特征吸收,3 384 cm-1处可见羟基吸收,表明纳米Fe3O4表面存在大量羟基。由Debye-Scherrer公式计算可得所制备纳米Fe3O4平均粒径为20.17 nm。

图1 纳米Fe3O4的XRD谱Fig.1 XRD pattern of nano-Fe3O4
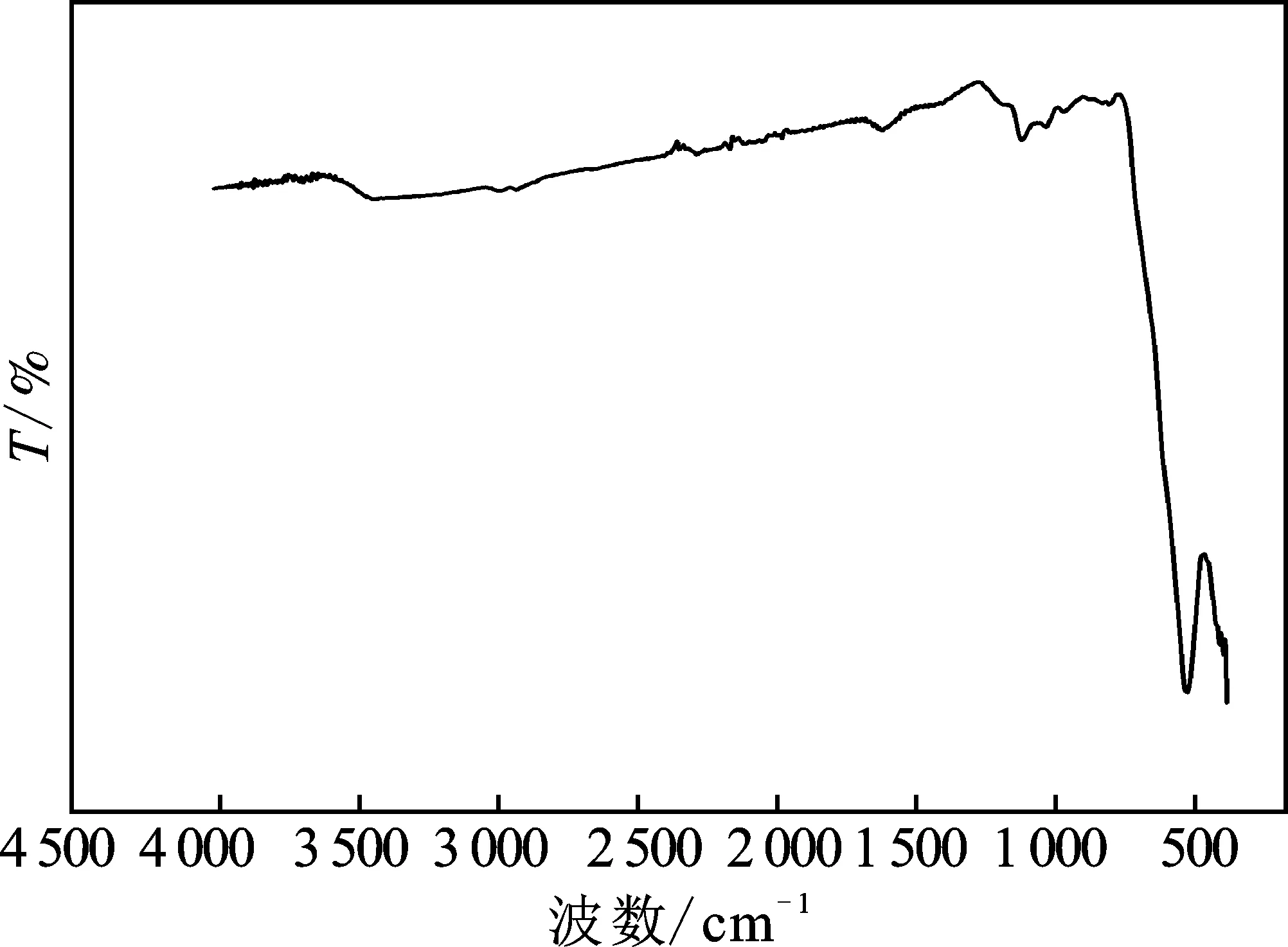
图2 纳米Fe3O4的IR谱Fig.2 IR spectrum of nano-Fe3O4
2.2 H2O2加量对亚甲基蓝去除率的影响
在30 ℃,pH为4,纳米Fe3O4加量为1 g/L,反应时间100 min时,考察H2O2加量对30 mg/L亚甲基蓝去除率的影响,结果见图3。
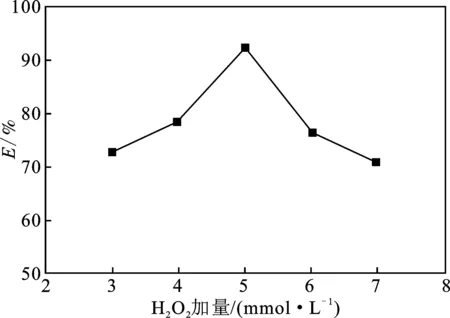
图3 H2O2加量对亚甲基蓝去除率的影响Fig.3 Effect of H2O2 dosage on the removal efficiency of methylene blue
由图3可知,H2O2加量对亚甲基蓝的去除率影响显著。当H2O2加量为3 mmol/L时,去除率仅为73.0%;当加量增加至5 mmol/L时,去除率达到93.3%,之后去除率逐渐降低。当加量增加至7 mmol/L 时,去除率仅为70.2%。
羟基自由基是反应体系中降解亚甲基蓝的主要活性物。当H2O2加量较小时,反应不足以产生足量的·OH降解亚甲基蓝,使亚甲基蓝去除率较低。当加量超过5 mmol/L时,过量的H2O2会消耗反应体系中的·OH,见式(2)~式(4),使亚甲基蓝去除率降低[4]。因此,H2O2的最佳加量为5 mmol/L。

(2)
(3)

(4)
2.3 pH值对亚甲基蓝去除率的影响
pH值适用范围是评价非均相Fenton催化剂性能的重要指标。在30 ℃,H2O2加量为5 mmol/L,纳米Fe3O4加量为1.0 g/L,反应时间100 min时,考察对pH值对30 mg/L亚甲基蓝去除率的影响,结果见图4。

图4 pH值对亚甲基蓝去除率的影响Fig.4 Effect of pH on the removal efficiency of methylene blue
由图4可知,对于所制备的纳米Fe3O4,亚甲基蓝去除率随pH值变化较平缓。
与文献[6,8-10]中非均相催化剂最佳pH = 3.0不同,所制备的纳米Fe3O4在pH=4.0时去除率最高,达到93.5%。随着pH值增大,去除率逐渐降低。当pH=6.0,接近中性的条件下,100 min时去除率仍然可达70%左右,表明所制备的纳米Fe3O4是pH值适应范围广的非均相Fenton催化剂。
2.4 催化剂循环使用特征
为了考察催化剂的循环使用特征,将降解反应完成后的纳米Fe3O4磁分离,用蒸馏水洗涤、干燥后在相同实验条件下重复用于相同质量浓度的亚甲基蓝废水的处理,实验结果见图5。

图5 纳米Fe3O4循环使用特征Fig.5 Recycling character of nano-Fe3O4
由图5可知,经过5次循环使用,亚甲基蓝的去除率略有降低,但均在90%以上。
反应完成后,溶液中总铁的含量经邻菲啰啉分光光度法测定为18.21 mg/L,占总投加量的2.50%,表明在实验条件下,催化剂中铁离子的溶出量非常少。以上实验结果表明纳米Fe3O4催化剂稳定性良好,可循环多次使用。
2.5 非均相Fenton高效降解亚甲基蓝
在实验条件下,催化剂铁离子的溶出量非常少,表明亚甲基蓝的降解主要可归因于纳米Fe3O4表面上的非均相Fenton氧化反应。由表1可知,与文献中纳米Fe3O4相关的研究对比,本研究制备的纳米Fe3O4可在较少H2O2加量下实现亚甲基蓝的降解,H2O2用量少,效果好。

表1 相关Fe3O4催化剂性质对比 Table 1 Characteristics comparison of nano-Fe3O4
为了证实所制备纳米Fe3O4的高效性,考察了在30 ℃,pH为3,H2O2加量为5 mmol/L,纳米Fe3O4加量为1 g/L时Fe3O4催化H2O2氧化降解30 mg/L 甲基橙的效果,结果见图6。

图6 纳米Fe3O4催化H2O2降解甲基橙 Fig.6 Degradation of methyl orange catalyzed by nano-Fe3O4
由图6可知,200 min时,甲基橙的去除率达到90%以上,表明所制备纳米Fe3O4是高效的非均相Fenton催化剂。
2.6 反应机理
随着降解反应的进行,反应液在664 nm处的特征峰不断降低,100 min时已消失殆尽,表明此时亚甲基蓝的共轭结构已经被破坏。纳米Fe3O4表面上的Fe2+催化吸附在其表面上的H2O2产生吸附态的·OH,吸附态的·OH将亚甲基蓝降解为有机小分子化合物,并最终矿化为二氧化碳和水。纳米Fe3O4表面上的Fe2+可通过H2O2还原表面上的Fe3+而再生,开始新的催化氧化循环。
由以上分析,亚甲基蓝的降解主要是纳米Fe3O4表面上的非均相Fenton氧化反应引起的。纳米Fe3O4催化H2O2氧化降解亚甲基蓝的机理可表示为[15]:

≡Fe3++ ·OHads+ H2O
(5)

(6)

(7)

(8)

(9)
3 结论
通过共沉淀法制备了纳米Fe3O4非均相Fenton催化剂,该催化剂可高效催化H2O2降解染料废水,H2O2用量少,pH适应范围广,效果好。催化剂稳定性良好,循环使用5次,去除率仍可达到90%以上。降解反应以纳米Fe3O4表面上的非均相Fenton氧化反应为主。
