载塞克硝唑Poloxamer188®复合聚L-乳酸薄膜的药物释放行为
2022-08-05陈玉佳王瑛颖董欣孙丽敏王浩
陈玉佳,王瑛颖,董欣,孙丽敏,王浩
(1.锦州医科大学药学院,辽宁 锦州 121000;2.西安杨森制药有限公司,陕西 西安 710309;3.锦州医科大学附属第一医院,辽宁 锦州 121000)
药物的控制释放一直是药剂学的热点问题,这其中,对药物的缓释是控制释放的关键。在口服-肠道吸收、腔道/病灶部位局部给药、微粒分散体系在靶部位释放药物等诸多情景下,药物的缓慢释放都有其意义,例如:在治疗窗内持续不断的供给药物、减少给药次数、降低单剂量大量给药时的毒性等等,这些都会改善药物的治疗指数、提高患者的适应性[1-3]。
影响制剂中药物释放行为的因素很多,从制剂中所使用材料的角度看,主要有制剂的基本材料,添加材料和药物本身。对于一些剂型,如片剂、颗粒剂、乳膏、栓剂等,基本材料和添加材料的比例有时可以十分接近,制剂中药物本身的量亦较大,甚至可以接近和大于辅料的量。而对于微球、脂质体、凝胶、电纺纤维等给药体系,一般来说基本材料所占要大于添加材料,且药物在制剂中的量则比辅料的量小很多[4-7]。在任何制剂中,基本材料-添加材料-药物三者的性质和含量比都会对制剂的性能产生明显的影响。例如,基本材料为水不溶材料时,添加材料和复合材料在水中的分散和溶解行为将直接影响药物从制剂中的溶出和释放行为,水溶性的添加材料和水不溶基本材料质量比的增减会导致体系亲水性、浸润性、崩解性、溶蚀性的变化[8-9]。
通过以往相关研究的启发,本文采用水不溶高分子材料聚L-乳酸为基本材料制备膜剂,在其中复合水溶性的表面活性剂Poloxamer188®,通过其添加量的不同调节膜剂中药物的释放行为[10]。实验中采用水溶性药物塞克硝唑为模型药物,发现其本身在膜剂中添加量的增减亦能够影响其释放行为。在预实验的基础上,本文考察了3种Poloxamer188®添加量和3种塞克硝唑添加量共9种膜剂,这9种样品能够体现药物较完全释放和释放量较小等情形。
1 仪器与试药
扫描电子显微镜(TM3000,日本Hitachi);离子溅射仪(日本Hitachi,E-1010);广角X-射线衍射仪(D/MAX-2500,日本Rigaku);差示热分析仪(Pyris,美国Perkin Elmer);高效液相色谱仪(日本Hitachi);色谱柱:SinoChrom ODS-BP C18 (大连Elite,4.6 mm×200 mm,5 μm),恒温空气浴摇床(THZ-82A型,浙江金坛天竟实验仪器厂)。
塞克硝唑(纯度99.4%,大连美仑生物技术有限公司,批号:A0125A);Poloxamer188®(大连美仑生物技术有限公司,Basf进口分装);聚L-乳酸(PLLA,Mw=153 300,PDI=1.31,以n-十二醇为引发剂丙交酯合成,首端基n-十二烷,末端基羟基,山东药物研究院有限公司,批号:21042501);二氯甲烷(分析纯,天津天力化学试剂有限公司);乙腈(色谱纯,天津科密欧化学试剂有限公司);磷酸二氢钾(分析纯,辽宁瑞泉试剂有限公司);纯净水(杭州娃哈哈集团)。
2 方 法
2.1 载药薄膜的制备
将处方量的塞克硝唑、Poloxamer188®、聚L-乳酸置于4 mL的二氯甲烷中磁力搅拌12 h至材料全部溶解,然后用二氯甲烷定容至5 mL,继续磁力搅拌12 h使混合均匀,得到透明均一的溶液。见表1,根据塞克硝唑和Poloxamer188®添加量的不同,得到分别命名的共3个系列、9种待铺膜溶液,以考察Poloxamer188®和塞克硝唑复合量对药物释放行为的影响。所有待铺膜溶液中聚L-乳酸的添加量均为0.5 g。
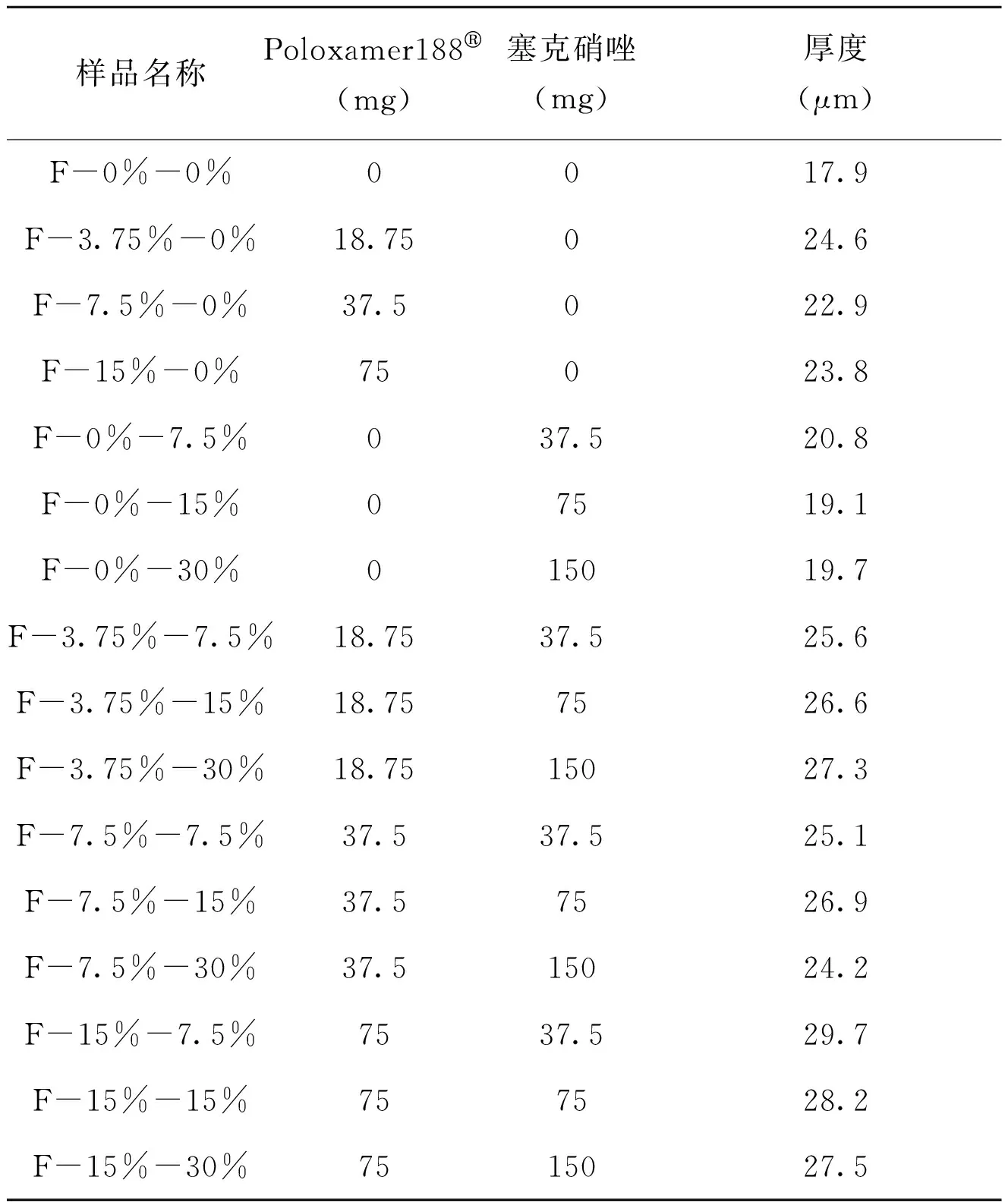
表1 待铺膜溶液中Poloxamer188®和塞克硝唑的添加量/百分占比及相应产品命名
载药薄膜制备在空气氛中进行,空气温度为(20±5)℃,相对湿度为(60±5)%。过程为:在玻璃板上倒上配制好的溶液,用玻璃棒推赶液流直至在玻璃板上形成均匀的溶液层,保持溶液层在平板上连续即没有液膜上有玻璃板露出的现象,也避免气泡存在的现象。用手术刀片揭开干薄膜的一角并顺势将其剥离玻璃板,并在(20±5)℃下真空干燥24 h。将干燥后的薄膜层叠100层后形成厚多层膜,用游标卡尺卡住厚多层膜听见轻微的“噔”声后读数,除以100即得膜的厚度,测量3次结果取平均值。
2.2 仪器表征
将系列薄膜剪切成2 mm×5 mm小片后用导电胶固定在金属台上并用金真空蒸镀后置于扫描电子显微镜下观察。差示热分析测试条件:称量10 mg薄膜置于差示热分析仪,氮气流保护下温度量程从25~450 ℃,升温速率:5 ℃/min。广角X-射线衍射测试条件:剪下5 cm×5 cm薄膜固定在镂空的金属片上并置于广角X-射线衍射仪。扫描范围:5°~80°,扫描速率:8°/min,室温下测试。
2.3 塞克硝唑释放曲线的绘制
采用HPLC-UV方法测定释放介质中塞克硝唑的含量,按参考文献的方法,色谱条件如下[11-12]。色谱柱:Dikma Diamonsil C18(4.6 mm×250 mm,5 μm),流动相:磷酸二氢钾0.05 mol/L溶液(pH=5.4)-乙腈(v/v=85/15),检测波长:311 nm,流速1.0 mL/min,柱温:30 ℃,进样量:20 μL[10]。
将样品剪切成约5 cm×5 cm正方形条,使得每片的质量约为100 mg,浸入25 mL纯水释放介质中。置于恒温空气浴摇床)中在37 ℃,100 r/min条件下振摇释放。在设定的时间点取出全部释放介质进行塞克硝唑的含量测定。并在释放介质中重新添加25 mL新的释放介质。绘制塞克硝唑的经时累计质量释放量和百分释放率曲线,由于药物的释放在溶液中进行,故质量释放量采用浓度表示。
塞克硝唑的百分释放率计算公式为:
释放百分率(R%) =释放介质中塞克硝唑浓度×释放介质体积/纤维中的塞克硝唑质量×100%。
对所得百分释放率曲线采用适当的方程式进行拟合。
3 结 果
3.1 薄膜形态
所制得的产品在外观上的肉眼观察结果均为连续的有一定机械强度的薄膜。纯聚L-乳酸薄膜(F-0%-0%)透明;当其中复合有Poloxamer188®而无塞克硝唑时(F-3.75%-0%、F-7.5%-0%、F-15%-0%)透明度稍有下降;当其中载有塞克硝唑而无Poloxamer188®时(F-0%-7.5%、F-0%-15%、F-0%-30%),随着载药量的升高薄膜逐渐泛白,由透明变为半透明。当薄膜中即有Poloxamer188®又有塞克硝唑时,均为随着塞克硝唑载量的升高,薄膜逐渐泛白,由透明变为半透明。同时,也可发现当塞克硝唑载量相同时,随着Poloxamer188®量的增高,薄膜的透明度逐渐降低,见图1。
系列薄膜在扫描电子显微镜下经50和500倍放大后的微观形态,可知薄膜表面光滑,没有结晶、团块、分相结构等存在。这提示薄膜中各种材料复合良好,见图1。

注:#为50倍,标尺2 mm;##为500倍,标尺200 μm图1 Poloxamer188®复合聚L-乳酸载药薄膜扫描电子显微镜下形态
3.2 材料复合与载药
塞克硝唑的熔点峰和分解峰的峰值分别在78.58 ℃和215.54 ℃处,Poloxamer188®的熔点峰和分解峰的峰值分别在56.27 ℃和385.53 ℃处,聚L-乳酸的熔点峰和分解峰的峰值分别在180.67 ℃和337.63 ℃处。成膜后,塞克硝唑和Poloxamer188®的熔点峰和分解峰均体现不明显,但是聚L-乳酸的熔点峰和分解峰均有所体现,且根据塞克硝唑和Poloxamer188®的载量不同而有变化,可以作为薄膜中3种材料复合状态的指征峰。
聚L-乳酸成膜后的差示热分析曲线相比于聚L-乳酸原料,其熔点峰位置变化不明显,分解峰的位置稍向高温移动,还有一个明显的放热峰,这可能是由于成膜时高分子链发生规则排列后所蓄积的能量。3个有Poloxamer188®复合但是未载塞克硝唑的薄膜(F-3.75%-0%、F-7.5%-0%、F-15%-0%)的热分析曲线上聚L-乳酸的熔点峰和分解峰位置相对于聚L-乳酸原料和聚L-乳酸薄膜均几乎无变化,这提示Poloxamer188®的复合对聚L-乳酸影响甚微。当聚L-乳酸薄膜中复合有Poloxamer188®且后者载量较高时(如F-7.5%-0%、F-15%-0%),Poloxamer188®的吸热峰有所显现,且向高温移动约5 ℃,这也是成膜后Poloxamer188®有序取向所导致的。
当薄膜中载有塞克硝唑而无Poloxamer188®,且塞克硝唑载量较低时(F-0%-7.5%、F-0%-15%),聚L-乳酸的熔点峰位置几乎无变化,这说明此时小分子药物在聚L-乳酸中的复合虽然对其结构有序-无序转化影响较小。但当塞克硝唑载量较高(F-0%-30%)时,聚L-乳酸的熔点峰几乎消失,说明此时聚L-乳酸的有序结构几乎被破坏。而且,此时聚L-乳酸分解峰的位置向低温移动约5 ℃,同时随着塞克硝唑载量的升高,聚L-乳酸的熔点峰和分解峰发生了联合,在曲线上形成一个“高原”形态,范围在(170~360)℃,塞克硝唑的分解峰也在此范围内,这些都说明塞克硝唑在薄膜中的包裹促进了聚L-乳酸的热分解。
当薄膜中既载有塞克硝唑又复合有Poloxamer188®,且Poloxamer188®复合量较少时(F-3.75%-7.5%、F-3.75%-15%、F-3.75%-30%、F-7.5%-7.5%、F-7.5%-15%、F-7.5%-30%),热分析曲线的形状与有Poloxamer188®复合但是未有塞克硝唑载药时的情况类似。表现在曲线上能见到聚L-乳酸的熔点峰和热分解峰,且两者的位置与聚L-乳酸原料差别不大,提示此时薄膜中聚L-乳酸的有序性受到影响的程度不明显。当薄膜中塞克硝唑和Poloxamer188®载量均较高时(F-7.5%-7.5%、F-7.5%-15%、F-7.5%-30%),热分析曲线上聚L-乳酸的熔点峰和分解峰均较为明显,且两者均向低温移动约5 ℃,说明此时薄膜中聚L-乳酸的有序性受到明显影响。根据理论和以往的同类型研究的结果,均相分散型体系中,基质高分子的有序性会因为小分子的复合而受到影响,并且同时会有利于小分子在体系中的移动,进而有利于小分子的释放[8],见图2。
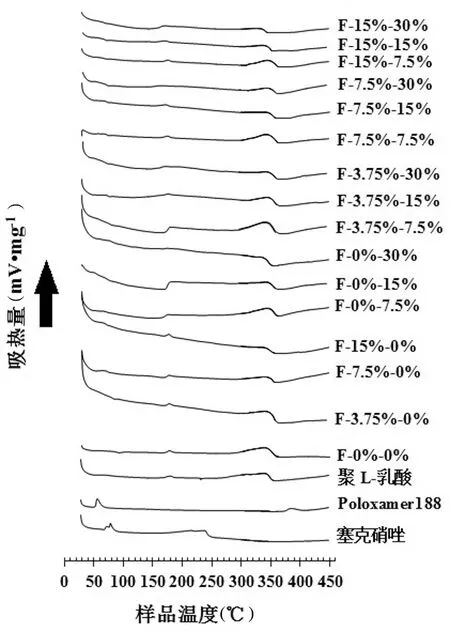
图2 样品差示热分析曲线
由热重分析曲线可见塞克硝唑质量减少开始于约140 ℃,在240 ℃几乎分解完毕;聚L-乳酸质量减少开始于约250 ℃,在350 ℃几乎分解完毕;Poloxamer188®质量减少时开始于约170 ℃,在约400 ℃几乎分解完毕。对于载药膜剂,药物载量变化时热重曲线变化明显且呈现规律性,以F-15%-7.5%、F-15%-15%、F-15%-30%为例,质量减少均开始于约140 ℃。且随着样品温度的升高,当载药量从7.5%升高至15%、30%时,热重曲线下降量随之增大。提示在复合薄膜中,塞克硝唑的热稳定性并未受到高分子基质的保护。热重曲线佐证了差示热分析曲线[8],见图3。

图3 样品热重分析曲线
塞克硝唑、Poloxamer188®和聚L-乳酸均有明显的特征峰,其他样品的X-射线衍射图谱均相似。均相溶液-铺膜后,纯聚L-乳酸薄膜即F-0%-0%在21.38°、23.74°、26.62°这3个2θ有明显但衍射强度较低的峰。其他复合膜的X-射线衍射图谱均在此位置有衍射峰,且衍射强度相近,这说明聚L-乳酸基质是薄膜表面复合状态的决定性因素。Poloxamer188®载量的变化对衍射图谱无影响,但是塞克硝唑载量对图谱影响明显,体现在当其载量为30%时即F-3.75%-30%、F-7.5%-30%、F-15%-30%的图谱上在2θ为7.16°和14.4°有明显但衍射强度较低的峰,但前者的衍射强度要大于后者;当塞克硝唑载量为15%时,即F-3.75%-15%、F-7.5%-15%、F-15%-15%的图谱上在2θ为7.16°处的衍射峰依然存在,但14.4°处的不存在;当塞克硝唑载量为7.5%时,这两个峰均不存在。塞克硝唑的图谱上衍射强度最大的峰在2θ为7.08°处,其在2θ为14.3°处亦有强度较大的衍射峰,所以载药薄膜上随着塞克硝唑有无和增减而出现和消失的两个衍射峰与塞克硝唑相关。这说明药物的增加虽未影响薄膜表面的基本复合状态,但药物特征峰的出现提示此时药物在薄膜表面存在状态的变化,即可能一部分药物以结晶状态存在[8],见图4。

图4 原料及薄膜样品X-射线衍射图谱
3.3 塞克硝唑释放行为
图5A和图5B分别为无Poloxamer188®复合载塞克硝唑膜剂中塞克硝唑的质量释放量曲线和换算后的百分释放率曲线,可见,聚L-乳酸薄膜中无Poloxamer188®复合时,其百分释放率均较少,三者分别为8.23%、8.79%和10.28%,但是已经呈现出随着塞克硝唑载量升高其本身的百分释放率逐渐升高的趋势。塞克硝唑水溶性较好,所以其在基质中载量的升高不但可以提高体系的亲水性,而且其在释放时能够提供更多的孔道以利于其本身的释放。若使塞克硝唑从水不溶聚L-乳酸薄膜中更多的释放显然需要在其中复合水溶性分子。

A:无Poloxamer188®复合系列载药薄膜质量释放量;B:无Poloxamer188®复合系列载药薄膜百分释放率;C:有Poloxamer188®复合系列载药薄膜质量释放量;D:有Poloxamer188®复合系列载药薄膜百分释放率图5 膜剂中塞克硝唑的经时释放曲线
图5C为系列复合有Poloxamer188®的膜剂中塞克硝唑的质量释放量曲线,可知F-15%-30%释放了最多的药物,突释量和最终释放量分别为397.09 μg/mL和544.72 μg/mL,而F-3.75%-7.5%释放了最少的药物,突释量和最终释放量分别为5.15 μg/mL和21.06 μg/mL。
为了具体考察Poloxamer188®载量和塞克硝唑载量对药物释放行为的影响,将绝对释放量换算成百分释放量,见图5D,可知Poloxamer188®载量3.75%组释放的药物量占膜剂中总药物的量最少,随着Poloxamer188®的载量升高至7.5%和15%,两组膜剂中药物的百分释放量逐渐增高。例如,当塞克硝唑的载量为7.5%时,Poloxamer188®的载量从3.75%升高至7.5%和15%后,相应的突释量和平台期释放量的增加值分别为2.75%、8.60%、44.26%和11.25%、57.15%、74.76%。以往一些研究提示,以聚L-乳酸为基质材料的药物释放系统中,表面活性剂的存在会影响药物的释放行为一般,当表面活性剂的复合量增高时,药物的释放速率和百分释放率会明显增高。表面活性剂增加药物释放速率的机理有很多。主要原因有:表面活性剂较好的水溶性为整个体系提供了较好的亲水性,且表面活性剂载量越多,体系的亲水性会越好;表面活性剂亦会从体系中释放,其释放后会在基质内留下空隙有利于药物的释放;表面活性剂也会增溶药物,其与药物的质量比逐渐增加时会促进药物溶出、释放会逐渐加快。
本实验还发现当Poloxamer188®载量相同时,随着塞克硝唑载量从7.5%升高至15%和30%,其百分释放量也会逐渐增加。以Poloxamer188®的载量为15%为例,当塞克硝唑的突释量和平台期释放量的增加值分别为44.26%,54.04%,69.09%和74.76%,88.28%,94.78%,塞克硝唑的载量也会影响其本身的释放行为,这是因为塞克硝唑在水中溶解度较高,其在体系中的存在与表面活性剂在体系中存在时提高体系的亲水性和致空隙特性进而增加药物释放的机理相似。显然,Poloxamer188®和塞克硝唑均可以增加药物的释放。
但是,Poloxamer188®对增加药物释放的作用较塞克硝唑更强。当塞克硝唑载量从7.5%升高至15%和30%时,Poloxamer188®的载量为3.75%时,药物的百分释放率增量分别为6.16%和3.23%;Poloxamer188®的载量为7.5%时,药物的百分释放率增量分别为11.68%和4.90%;Poloxamer188®的载量为15%时,药物的百分释放率增量分别为13.52%和6.50%。另一方面,当Poloxamer188®的载量从3.75%升高至7.5%和15%时,塞克硝唑的载量为7.5%时,其百分释放率增量分别为45.90%和17.62%;塞克硝唑的载量为15%时,其百分释放率增量分别为51.42%和19.46%;塞克硝唑的载量为30%时,其百分释放率增量分别为53.09%和21.05%。当增量相同时,相比于塞克硝唑,Poloxamer188®使得药物释放百分率增加的量更大。例如,载量从7.5%升高至15%时,另一者载量相同时,Poloxamer188®对药物的百分释放率增量影响更大,这可以从F-7.5%-7.5%、F-7.5%-15%、F-15%-7.5%三者的释放曲线比较得出。
复合量高和载药量大时,均有利于药物的快速释放,并且会导致较大的突释。降低后,药物释放变慢,逐渐呈现较长的缓释相。因此,本实验提出了一种调节聚L-乳酸电纺纤维中药物释放的方法。当Poloxamer188®和塞克硝唑载量在恰当值时,药物的释放曲线呈现明显的缓释相,这可以作为Poloxamer188®复合聚L-乳酸薄膜对药物释放行为调节的一种手段继续研究。
为了进一步研究药物的释放机理,对系列薄膜的百分释放率曲线对多种常见药物释放拟合方程式进行了拟合,发现按照Peppas方程式lgQt/Q∞=lgk+nlgt拟合后的回归系数较高,见图6。
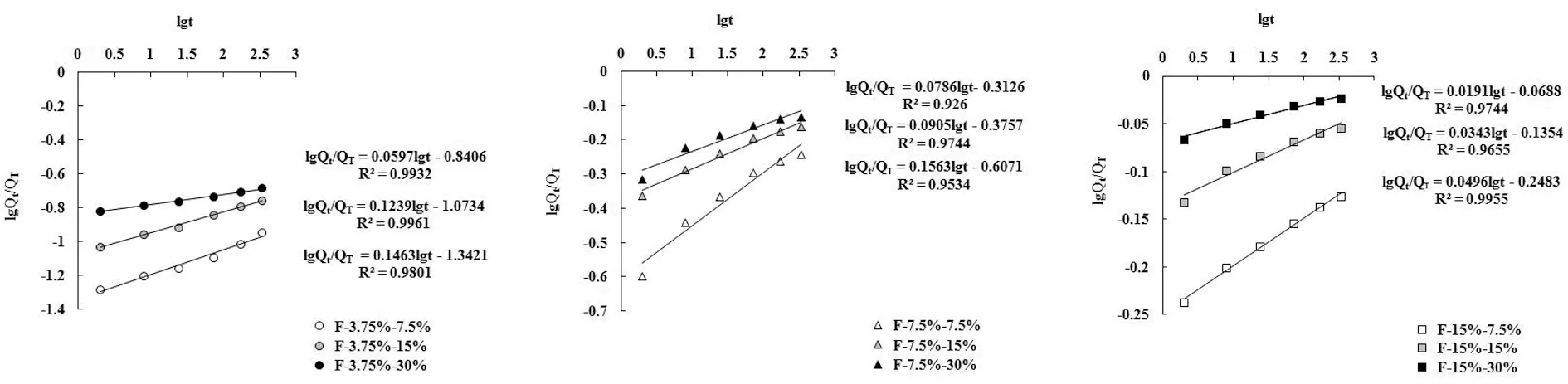
图6 塞克硝唑的百分释放率曲线Peppas方程式lgQt/QT=lgk+nlgt拟合结果
随着膜剂中塞克硝唑载量的增加,n值逐渐减小;随着Poloxamer188®载量的增加,n值变化无规律。n可能反映释放的机理,但具体的意义尚待明确。由图4可知,当Poloxamer188®载量相同时,最终释放百分率减去突释点的释放百分率的差值有逐渐减小的趋势。突释点释放的药物一般聚集于薄膜的表面且与基质材料结合的不紧密,最终释放量为从薄膜深处至外部能够释放的药物总量,又知较多的塞克硝唑会使得基质中亲水性和孔道密度增多,那么n值可能反映的是该因素,其能指示非突释部分药物的释放能力。
差示热分析曲线提示了当薄膜中塞克硝唑载量较高时,其降低聚L-乳酸的有序性,可能有助于药物的释放。X-射线衍射图谱提示了较高载药量时薄膜表面结晶态药物的存在,药物释放曲线提示了此时突释量和最终释放量的增加。这都在药物释放结果中得到了证明。
4 结 论
本文通过共溶剂-铺膜法制备了载有塞克硝唑的Poloxamer188®复合聚L-乳酸薄膜,发现Poloxamer188®载量和塞克硝唑的载量的增加均可以使得药物的百分释放率增加,后者比前者的影响更大。当Poloxamer188®和塞克硝唑载量在恰当值时,药物的释放曲线呈现明显的缓释特征,这可以作为Poloxamer188®复合聚L-乳酸薄膜对药物释放行为调节的一种手段继续研究。
基于高分子的膜剂是一种较为“古老”的剂型,国内外研究的均较少,且一般用于药物的速释。部分原因在于非速释型膜剂采用的成膜材料为水不溶高分子,用其载药后缺少调节药物释放的手段,且药物的释放往往不完全。本文为水不溶药物高分子膜剂的药物释放调控提供了一个参考。实际上,膜剂是一种快速制备手段,其工业化和自动化程度高,产品重现性好、且单位时间产量大。膜剂本身作为皮肤和粘膜给药系统也十分合适。本文最终得到了释放行为理想的塞克硝唑膜剂,可以作为口腔和阴道微生物感染时的药剂进一步进行研究开发[11-12]。
扫描电子显微镜对药物的包裹和材料复合评价能力有限,辅助X-射线衍射和差示热分析等手段可以进一步地考察药物的包裹情况。且仪器表征可以通过药物的释放行为相互佐证。
