一株红树植物内生真菌Pseudallescheria boydii L32的代谢产物*
2022-08-05陈若兰黎子洋巫惠珍罗艺盟佘志刚熊亚红李春远
陈若兰,黎子洋,巫惠珍,罗艺盟,佘志刚,熊亚红,李春远
1. 生物基材料与能源教育部重点实验室/华南农业大学材料与能源学院,广东 广州 510642
2. 中山大学化学学院,广东 广州 510275
红树林真菌因特殊的沿海生存环境,能产生结构多样的具有各种活性的新代谢产物,是农药和医药开发的重要资源之一[1-3]。半红树植物苦槛蓝Myoporum bontioides在我国沿海分布广泛,其不同组织部位蕴含着丰富的内生真菌资源[4],在对其部分内生菌株代谢产物的研究中,我们获得了10 多个具有强抗菌活性的新代谢物,包括细胞松弛素生物碱、环六脂肽、色原酮、异香豆素及六、七元单环内酯等结构类型[5-7]。本文研究纯化自该植物叶片的另1 株真菌Pseudallescheria boydiiL32 的代谢产物,共分离鉴定了10 个单体代谢物(图1),包括2,2′-oxybis(1,4)-di-tert-butylbenzene(1),livistone B(2),simplicildone A(3),simplicildone B(4),botryorhodine B(5),(-)-regiolone(6),citreoanthrasteroid B(7),豆甾-4-烯-3-酮(8),丁二酸(9)和草酸(10)。其中代谢物1,3,4,5,7,8为首次从Pseudallescheria属分离得到。活性测试显示,代谢物1,4,5,6 对O6 血清型大肠杆菌(人致病性),代谢物1,5 对O78 血清型大肠杆菌(禽致病性)显示出抑菌活性。
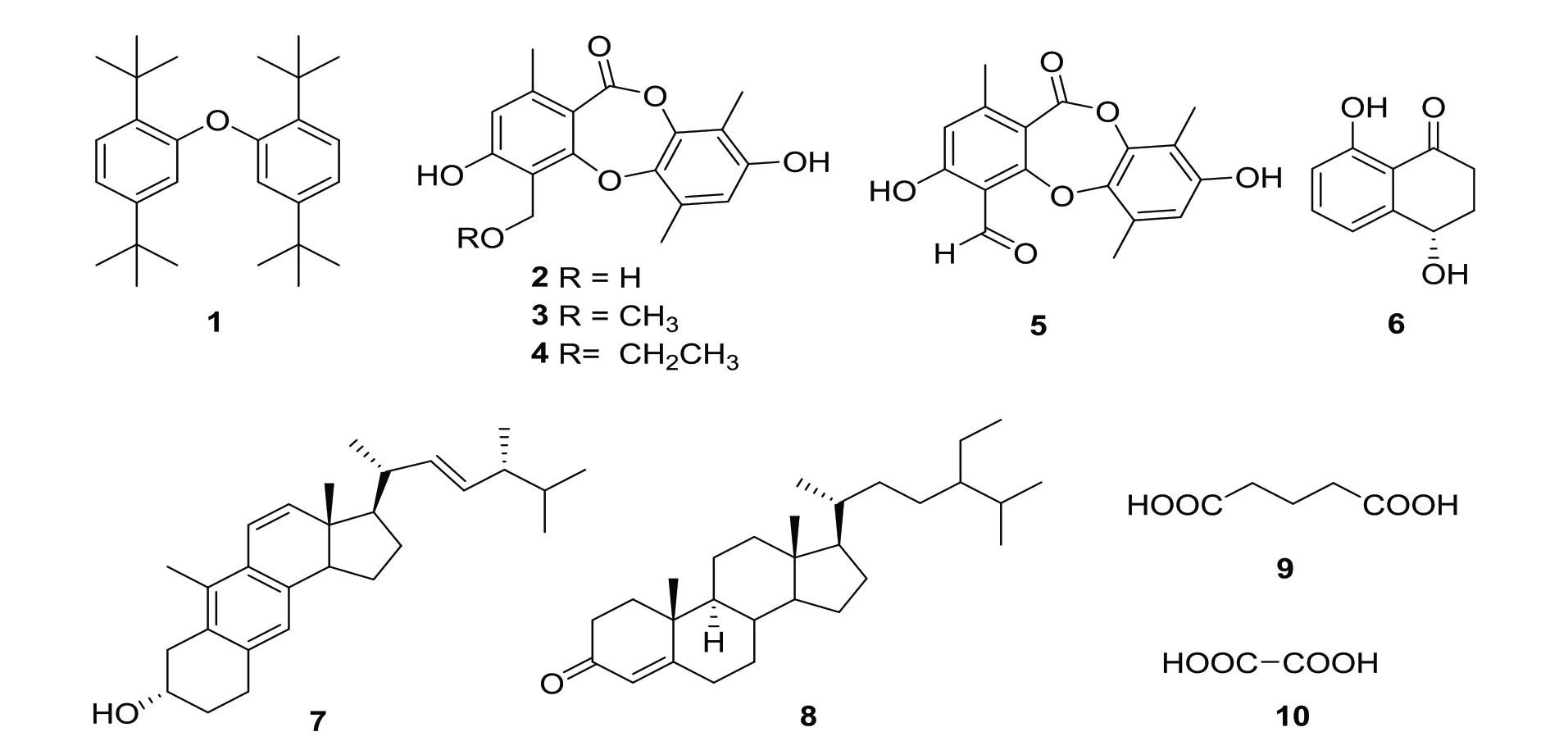
图1 代谢物1~10的结构Fig.1 The structures of compounds 1-10
1 实验部分
1.1 仪器、试剂及材料
Bruker Biospin AV 600 核磁共振波谱仪,MDS SCIEX APCI 2000 液质联用仪,Horiba SEPA-300旋光仪。GF254 薄层及200-300 目柱层析硅胶(青岛海洋化工公司),Sephadex LH-20 凝胶(GE Healthcare),其他试剂为分析纯。Pseudallescheria boydiiL32 分离自苦槛蓝叶片,通过PCR 扩增真菌核糖体ITS 基因区段,并登陆NCBI数据库Blast搜索与MK646016.1 菌株对比(相似度99.82%)得到鉴定,大肠杆菌(O6,O78 血清型)引自华南农业大学天然资源再生与利用研究室,保藏于华南农业大学材料与能源学院。
1.2 菌种发酵培养及分离
采用与文献相同的大米培养基[8]、培养体积及培养时间,将发酵物用乙醇萃取3次,减压浓缩得提取物31.2 g,通过常规微生物代谢产物分离流程[8],分别得到代谢物1(5.1 mg),2(3.5 mg),3(2.2 mg),4(2.3 mg),5(6.1 mg),6(1.8 mg),7(3.2 mg),8(2.6 mg),9(60.4 mg),10(35.1 mg)。
1.3 抗菌活性测试
用二倍稀释法[9]测试代谢物1~8 体外对O6,O78 血 清 型 大 肠 杆 菌(Escherichia coliO78 和Escherichia coliO6,购自上海烜雅生物科技有限公司)抗菌活性,以最小抑菌浓度(MIC)表示抗菌效果,用头孢拉定作阳性对照,平行测定3次。
1.4 代谢物波谱数据
代谢物1:C28H42O,黄色油状物,ESI -MSm/z394.36[M+H]+,1H NMR(400 MHz,acetoned6)δ7.57(d,J= 8.6 Hz,2H),7.47(d,J= 2.5 Hz,2H),7.26(d,J= 8.6,2.5 Hz,2H),1.37(s,18H),1.30(s,18H)。13C NMR(100 MHz,acetone-d6)δ148.6,148.2,139.3,125.4,124.9,119.9,35.5,35.1,31.7,30.6。
代谢物2:C17H16O6,白色粉末,ESIMSm/z317.14[M+H]+,1H NMR(400 MHz,acetone-d6)δ6.65(s,1H),6.53(s,1H),5.06(s,2H),2.39(s,3H),2.38(s,3H),2.14(s,3H)。13C NMR(100 MHz,acetone-d6)δ166.0,163.9,161.4,153.4,144.8,144.5,143.8,128.2,116.4,116.3,115.4,114.9,113.7,56.1,21.2,16.8,9.3。
代谢物3:C18H18O6,无色固体,ESIMSm/z353.1[M+Na]+,1H NMR(400 MHz,CDCl3)δ8.40(s,1H),6.62(s,1H),6.43(s,1H),5.04(s,2H),4.87(s,1H),3.52(s,3H),2.46(s,3H),2.33(s,3H),2.23(s,3H)。13C NMR(100 MHz,CDCl3)δ163.8,161.0,160.3,151.2,145.5,143.8,143.7,127.0,116.7,114.6,113.5,113.5,110.7,68.2,58.9,21.4,17.2,9.3。
代谢物4:C19H20O6,无色固体,ESIMSm/z345.1[M+H]+,1H NMR(400 MHz,acetone-d6)δ6.67(s,1H),6.53(s,1H),4.85(s,2H),3.64(q,J= 7.0 Hz,2H),2.38(s,3H),2.38(s,3H),2.14(s,3H),1.19(t,J= 7.0 Hz,3H)。13C NMR(100 MHz,acetone-d6)δ163.3,160.7,160.3,153.4,146.9,145.4,144.5,128.3,116.3,115.6,114.8,114.1,113.6,66.7,62.9,21.3,16.5,15.5,9.3。
代谢物5:C17H14O6,无色固体,ESIMSm/z313.1[M-H]-,1H NMR(400 MHz,acetone-d6)δ10.72(s,1H),6.76(s,1H),6.58(s,1H),2.50(s,3H),2.34(s,3H),2.17(s,3H)。13C NMR(100 MHz,acetone-d6)δ194.6,166.3,165.9,162.5,154.7,154.1,144.1,143.3,128.1,117.8,115.7,114.1,113.9,111.7,22.2,17.0,9.4。
代谢物6:C10H10O3,无色晶体,ESIMSm/z179.1[M+H]+,= -4.2(c0.10,MeOH),1H NMR(400 MHz,acetone-d6)δ12.46(s,1H),7.53(dd,J= 8.4,7.2 Hz,1H),7.12(d,J= 7.2 Hz,1H),6.83(d,J= 8.4 Hz,1H),4.89(dd,J= 8.5,3.8 Hz,1H),4.71(s,1H),2.74(m,1H),2.67(m,1H),2.33(m,1H),2.13(m,1H)。13C NMR(100 MHz,acetone-d6)δ204.6,162.4, 147.1, 136.6, 117.4, 116.2, 115.3,66.8,35.0,32.7。
代谢物7:C28H40O,无色油状物,ESIMSm/z393.3[M+H]+,= +23.5(c0.10,CHCl3),1H NMR(400 MHz,acetone-d6)δ6.64(s,1H),6.63(d,J= 9.6 Hz,1H),6.47(d,J= 10.0 Hz,1H),5.31(dd,J= 6.4,4.8 Hz,1H),5.27(dd,J=7.1 Hz,1H),4.04(m,1H),2.97(dd,J= 16.5,5.2 Hz,1H),2.81(m,2H),2.80(m,1H),2.45(dd,J= 16.3,7.6 Hz,1H),2.17(s,3H),2.02~ 1.86(m,5H),1.75 ~ 1.46(m,5H),1.30(d,J=11.8 Hz,3H),1.16(d,J=6.6 Hz,3H),0.96(d,J= 6.8,3.0 Hz,3H),0.86(d,J= 6.5 Hz,3H),0.58(s,3H)。13C NMR(100 MHz,acetoned6)δ140.1,137.3,136.3,135.6,133.1,132.3,132.0,131.2,124.6,123.8,67.7,52.6,51.1,44.3,43.7,41.8,37.2,33.8,32.2,30.3,28.7,22.6,21.2,20.3,20.0,18.1,14.4,11.7。
代谢物8:C29H48O,无色油状物,ESIMSm/z413.4[M+H]+,= +39.2(c0.10,CHCl3),1H NMR(400 MHz,CDCl3)δ5.72(s,1H),1.18(s,3H),0.92(d,6.6 Hz,3H),0.86(d,7.2 Hz,6H),0.82(d,7.2 Hz,3H),0.71(s,3H),2.45~1.03(m,29H,不含1.18 的甲基及1.6 附近水峰信号)。13C NMR(100 MHz,CDCl3)δ199.5,171.6,123.0,56.2,55.6,53.6,45.5,42.6,39.1,38.4,36.7,35.6,35.2,34.5,33.7,33.5,32.6,29.7,28.3,26.2,24.3,23.6,21.0,19.7,19.1,18.9,17.5,12.1,12.0。
代谢物9:C4H6O4,无色晶体,ESIMSm/z119.1[M+H]+,1H NMR(400 MHz,DMSO-d6)δ12.15(br s,2H),2.40(s,4H)。13C NMR(100 MHz,DMSO-d6)δ173.4,28.9。
代谢物10:C2H2O4,无色晶体,ESIMSm/z91.0[M+H]+,1H NMR(400 MHz,DMSO-d6)δ13.75(br s,2H)。13C NMR(100 MHz,DMSO-d6)δ161.1。
2 结果与讨论
ESIMS 谱m/z394.36[M+H]+,1H NMR 谱δ7.57(d,J= 8.6 Hz,2H),7.47(d,J= 2.5 Hz,2H),7.26(d,J=8.6,2.5 Hz,2H)3 组氢化学位移及偶合常数表明代谢物1 有2 个对称的1,2,4-三取代苯环,δ1.37(s,18H),1.30(s,18H)的峰形及积分表明存在4 个叔丁基,13C NMR 谱观察到δ148.6,148.2,139.3,125.4,124.9,119.9 共6 组芳香碳信号,结合分子式C28H42O 进一步证明有2个对称的苯环存在且二者通过氧原子连接。与文献[10]对照,数据基本一致,鉴定代谢物为2,2′-oxybis(1,4)-di-tert-butylbenzene。
代谢物2 的1H NMR 谱δ6.65,6.53 的单峰及13C NMR 谱δ113.7~163.9 的12 个芳香碳,推测存在2 个五取代苯,166.0 是酯羰基碳。1H NMR谱2.39(s,3H),2.38(s,3H),2.14(s,3H)是3个取代在苯环上的甲基,5.06(s,2H)是与氧或羟基相连的亚甲基。结合ESIMS 数据剩余的相对分子质量,将剩余的结构单元归属为羟基和氧。与文献[11]对照,数据基本一致,鉴定为livistone B。
代谢物3 的1H NMR 谱比代谢物2 多出1 个甲氧基信号δ3.52(s,3H)。对比剩余数据表明它们其他的结构单元一致,因此代谢物3 是2 中的1 个羟基变为了甲氧基的衍生物,与文献[12]对照,数据基本一致,鉴定为simplicildone A。
代谢物4 的1H NMR 谱比代谢物2 多出δ3.64(q,J= 7.0 Hz,2H),1.19(t,J= 7.0 Hz,3H)的乙氧基信号,ESIMS 谱也显示前者比后者多出28的相对分子质量,根据化学位移值可初步判断该乙氧基连接在脂肪碳上,与文献[12]对照,数据基本一致,鉴定为simplicildone B。
代谢物5 的1H NMR 谱δ10.72(s,1H)及13C NMR 谱δ194.6 比代谢物2 多出1 个醛基,同时后者连羟基的亚甲基(δH4.85,δc56.1)在前者1H NMR 谱中未被观察到,据此推测代谢物5 是代谢物2羟甲基转化为醛基的衍生物,与文献[13]对照,数据基本一致,鉴定为botryorhodine B。
代谢物6 的1H NMR 谱δ7.53(dd,J= 8.4,7.2 Hz,1H),7.12(d,J=7.2 Hz,1H),6.83(d,J=8.4 Hz,1H)是苯环上互为邻位的3 组氢。滴加重水后根据1H NMR 谱信号消失情况,发现有2 个羟基,δ12.46(s,1H)是与羰基形成分子内氢键的羟基,4.71(s,1H)是另1 个羟基。13C NMR 谱δ162.4,147.1,136.6,117.4,116.2,115.3 再次确认了苯环的存在,此外还显示有1 个羰基(δ204.6),1 个连羟基的亚甲基(δ66.8)及另2 个亚甲基(δ35.0 和32.7)信号。该代谢物核磁及比旋光度与文献[14]报道基本一致,鉴定为(-)-regiolone。
代谢物7的1H NMR 谱δ6.64~5.27 有5个双键氢 的 信 号,13C NMRδ140.1~123.8 有10 个 双 键碳,推测可能含有苯环。1H NMR 谱δ4.04(m,1H)是连羟基的次甲基信号,δ2.17(s,3H)及δ1.30~0.58 之间积分分别为3 的5 组氢是6 个甲基信号,据此与文献[15]报道代谢物的核磁及比旋光度数值对比基本一致,鉴定为citreoanthrasteroid B。
代 谢 物8 的1H NMR 谱 在δ0.71~2.45 高 场 区的化学位移(通常为脂肪甲基、亚甲基、次甲基信号)和积分情况以及对应的13C NMR 谱δ12.0~56.2 的碳均与典型的甾醇特征吻合[16],其中δH1.18(s,3H),0.92(d,6.6 Hz,3H),0.86(d,7.2 Hz,6H),0.82(d,7.2 Hz,3H),0.71(s,3H)是6 个甲基信号。此外,δH5.72(s,1H)是双键H信号;13C NMR 谱δ199.5,171.6,123.0 说明存在1 个羰基且与上述双键共轭,据此与文献[17]对照,数据基本一致,鉴定为豆甾-4-烯-3-酮。
代谢物9 的1H NMR 谱δ12.15(br s,2H)和2.40(s,4H)是羧基H 和连接羧基的亚甲基信号,分别对应于13C NMR 谱δ173.4 的羧基碳和28.9 的亚甲基信号,结合ESIMSm/z119.1[M+H]+的分子离子峰并与文献[18]对照,数据基本一致,鉴定为丁二酸。
代谢物10 的1H NMR 谱δ13.85(br s,2H)是羧基H 信号,对应于13C NMR 谱δ161.1 的羰基碳信号,结合ESIMSm/z91.0[M+H]+的分子离子峰并与文献[19]对照,数据基本一致,鉴定为草酸。
上述代谢物1,3,4,5,7,8首次从Pseudallescheria属分离得到,丰富了该菌属的代谢产物库。文献报道代谢物2 和3 具有磷酸二酯酶5 抑制活性[20],代谢物5具有抗枯草芽孢杆菌Bacillus subtilis、土曲霉菌Aspergillus terreus、尖孢镰刀菌Fusarium oxysporum活性及抑制人子宫颈癌细胞(Hela)、脐静脉内皮细胞(HUVEC)、慢性骨髓性白血病细胞(K562)增殖活性[13],代谢物7 具有抗表皮葡萄球菌Staphylococcus epidermidis, 蜡样芽孢杆菌Bacillus cereus、副溶血弧菌Vibrio parahaemolyticus活性及乙酰胆碱酯酶抑制活性[21],但尚未见所分离代谢物抗大肠杆菌活性的研究报道。本文活性测试结果显示,代谢物1,4,5,6对人致病性O6 血清型大肠杆菌MIC 分别为50,12.5,25,100 μg/mL,代谢物1,5 对禽致病性O78 血清型大肠杆菌MIC 均为100 μg/mL,其余所测MIC 值均高于200 μg/mL(阳性对照头孢拉定对O6 和O78血清型大肠杆菌MIC 分别为3.13 和6.25 μg/mL)。代谢物4,5 对O6 型大肠杆菌活性相对较强,且结构中含有的容易修饰的活泼位点较多,如羟基、芳甲基、醛基等,因此可优先考虑作为抗O6 血清型大肠杆菌的先导代谢物开展结构改造研究。禽大肠杆菌是由致病性大肠杆菌所引起的禽病,是危害家禽养殖业的重要传染病之一[22],其中O78型大肠杆菌引起的禽大肠杆菌病在国内较为常见[23],但专用的防治兽药极少,后续有必要开展代谢物1,5 防治O78 型禽大肠杆菌病的体内疗效研究。
