顶空—气相色谱法快速测定米粉中的二氧化硫残留量
2022-08-02黄丽孙琦蒙舒婷范云燕庞洁
黄丽 孙琦 蒙舒婷 范云燕 庞洁
(南宁市疾病预防控制中心 广西 南宁 530023)
1 前言
米粉是广西的特色食品,是当地的主食之一,部分不法生产商为延长米粉的保质期或维持其外观,会在制作时违规使用添加剂,二氧化硫作为一种漂白剂、防腐剂、抗氧化剂,常被添加其中。2011年,全国食品安全整顿办公室印发《食品中可能违法添加的非食用物质和易滥用的食品添加剂品种名单(第五批)》[1],其中将焦亚硫酸钠列入易滥用的食品添加剂名单,故对米粉中二氧化硫含量的检测十分重要。
GB5009.34—2016《食品安全国家标准 食品中二氧化硫的测定》[2]使用的是蒸馏滴定法,检测效率不高,难以实现大批量检测。目前,有较多研究采用离子色谱法测定各类食品中的二氧化硫残留量[3-6],但前处理需蒸馏提取样品,检测效率不高。顶空—气相色谱法是《中国药典》[3]推荐方法,在检测中药材中二氧化硫含量方面应用广泛,具有准确性高、重复性好,检出限低、检测效率高的优点。本文以药典方法为基础,对该方法进行改进,采用顶空—气相色谱法快速测定米粉中的二氧化硫,以满足大批量食品安全检测的需求。
2 实验部分
2.1 试验材料
样品:市售鲜米粉、干米粉;腐竹中二氧化硫含量测定内部质控样品(大连中食国实检测技术有限公司);米粉中二氧化硫含量测定能力验证盲样(广西CDC专项)。
试剂:85%磷酸(AR,国药集团化学试剂有限公司);无水亚硫酸钠(GR,天津市科密欧化学试剂有限公司);乙二胺四乙酸二钠(AR,广州新建精细化工厂);甘露醇(AR,天津市大茂化学试剂厂)。
辅材:玻璃小导管(12×55 mm);钳口顶空瓶(20 mL)。
2.2 试验仪器
气相色谱仪(7890A,配备6790A顶空进样器,安捷伦);移液器(5~10 μL,10~100 μL,20~200 μL,100~1 000 μL,0.5~5.0 mL,1~10 mL,艾本德);万分之一精密电子天平(CPA224S,赛多利斯),千分之一精密电子天平(XP5003SDR,梅特勒);超声波清洗器(SK5200LH,上海科导超声仪器有限公司)。
2.3 实验方法
2.3.1 试剂
甘露醇—乙二胺四乙酸二钠溶液:称取甘露醇5.00 g、乙二酸四乙酸二钠1 g,加水至1 000 mL(配制后存储于4℃条件下可稳定半年)。
2.3.2 标准溶液配制
称取无水亚硫酸钠0.1 g(精确到0.000 1 g),置于100 mL容量瓶中,用甘露醇—乙二胺四乙酸二钠溶液定容至刻度,得标准液浓度为1.00 mg/mL(配制后存储于4℃条件下可稳定1周)。
低浓度标准曲线:分别量取标准溶液5、10、30、60、80、100、150 μL,置于20 mL顶空瓶中,加水至10 mL,得到标准系列含量为5、10、30、60、80、100、150 μg。
高浓度标准曲线:分别量取标准溶液120、250、500、700、1 000、1 500 μL,置于20 mL顶空瓶中,加水至10 mL,得到标准系列含量为120、250、500、700、1 000、1 500 μg。分别向各顶空瓶中置入盛有1.00 mL 85%磷酸的玻璃小导管,钳好顶空瓶盖,颠倒顶空瓶摇匀,与样品同处理后待测。
2.3.3 样品处理
称取粉碎样品0.5~2 g(精确到0.001 g),置于20 mL顶空瓶中,加入甘露醇-乙二胺四乙酸二钠溶液10.00 mL,向顶空瓶中置入盛有1 mL 85%磷酸的玻璃小导管,钳好顶空瓶盖,颠倒顶空瓶摇匀,超声提取5 min,待测。
2.3.4 仪器条件
气相色谱仪:进样口:温度200℃;分流比∶10∶1;色谱柱:GS-GasPro(30 m×320 m,0 μm);流速:3 mL/min;柱温:初始温度100℃,升温速率50℃/min,升至200℃,保持3 min;检测器:ECD,300℃。
顶空进样器:加热箱90℃;样品平衡时间10 min;定量环90℃;传输线100℃;进样持续时间0.5 min。
2.4 结果计算
试样中的二氧化硫含量按以下公式计算:
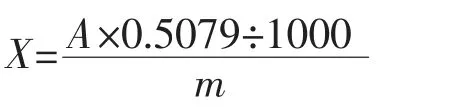
式中:X——样品中二氧化硫的含量(g/kg);A——试样中亚硫酸钠的含量 (μg);m——取样量(g);0.5079——亚硫酸钠与二氧化硫质量的转换因子。
3 结果与讨论
3.1 提取效果影响因素
3.1.1 顶空进样器仪条件选择
选取加热箱温度为70℃、80℃、90℃,在相同气相色谱条件下,分别考察平衡10 min、20 min、30 min相同浓度标准溶液的峰面积,并进行比较,结果见图1。

图1 不同顶空条件相同气相条件下相同浓度标液的峰面积比较图
由图1可以看出,加热箱90℃、样品平衡时间10 min和加热箱80℃、样品平衡时间30 min进行测定,可以获得较大的峰面积。但考虑到节省检测时间,故采用加热箱90℃、样品平衡时间10 min为最佳方案。
3.1.2 前处理方式的优化
实验过程中,本文尝试采用水、氢氧化钠与氯化钠溶液分别作为浸泡液配制标准溶液,结果显示,标准溶液稳定性较差,只能临用配制,一次性使用。浸泡液参考《中国药典》[4]二氧化硫残留量检测第二法气相色谱法中使用的0.5%的甘露醇与0.1%EDTA-2Na混合溶液浸泡液,可以使二氧化硫标准溶液及样品提取液中的二氧化硫稳定。
二氧化硫的检测方法大多使用盐酸进行酸化提取,但盐酸的挥发性易对仪器造成损害,也会与二氧化硫发生反应,产生一氯甲烷干扰峰[4]。部分方法使用硫酸[5]溶液,但硫酸易引入本底值,也不宜采用。采用磷酸可避免不利因素,且不影响检测结果。由于样品酸化后二氧化硫会立即溢出,即使迅速压好顶空瓶盖也难以避免,故事先将酸置于玻璃小试管内,再将小试管放入盛有样品的顶空瓶中,用玻璃小试管将酸与样品相隔绝,压盖密封后再倾倒顶空瓶让其相互反应,可以获得较好的重现性。
通过实验考察,各前处理方式对加标回收率的影响见表1。可以看出,加入磷酸1.00 mL,超声提取5 min可以获得较高的回收率。

表1 各种前处理方式测定结果的回收率
3.2 线性范围考察
使用该方法测定标准溶液,得到二氧化硫色标准品谱图见图2,二氧化硫的保留时间为1.8min。以标准溶液含量为横坐标,峰面积为纵坐标,绘制标准曲线,得到低浓度、高浓度范围曲线见图3和图4。相关系数均>0.9990,表明在5~150μg及120~1 500 μg含量范围内,线性关系均良好。检测过程中可以根据样品含量选择相应的浓度曲线以准确定量。

图2 二氧化硫标准品气相色谱图

图3 5~150 μg标准曲线
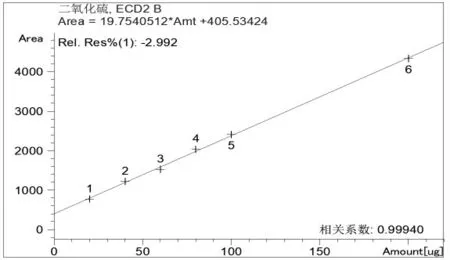
图4 120~1 500 μg标准曲线
3.3 方法检出限(LOD)与定量限(LOQ)
根据仪器3倍信噪比与10倍信噪比,分别计算仪器的检出限与定量限,得到仪器检出限为2 μg,定量限为8 μg。以取样量5 g计,该方法的检出限为0.000 2 g/kg,定量限为0.000 8 g/kg。
3.4 方法准确性
3.4.1 加标回收
分别取鲜米粉和干米粉空白基质样品各3组,每组1对平行样,分别添加低、中、高浓度,按该方法前处理操作,得到测定结果均值计算回收率见表2。实验表明,回收率良好,范围84%~97%,鲜米粉与干米粉的平均回收率分别为91%与90%,满足样品检测要求。

表2 加标回收试验
3.4.2 盲样考核
本实验室参加广西省疾病控制与预防中心专项米粉中二氧化硫的测定盲样考核,采用国标方法GB5009.34—2016蒸馏滴定法进行测定。同时,测定了腐竹中二氧化硫含量质控样品作为实验室内部质控。使用该方法测定盲样与国标滴定法测定结果的数据对比见表3。实验表明,滴定法与气相色谱法测定盲样与质控样结果的z值均<2,结果满意。2种方法测定腐竹质控样6次所得到的2组数据,经过T检验,得到P值为0.6,P>0.05,说明2种检测方法得出的检测结果一致。

表3 滴定法与气相色谱法检测结果比较
检测过程中发现,滴定法取样量为2~5 g才能保证其灵敏度与准确性,而气相色谱法仅需取样0.5~1.0 g,即可准确测定。在样品量有限的情况下,使用气相色谱法有利于重复测定。对两者测定的RSD值进行比较,气相色谱法略优于滴定法。腐竹质控样测定的标准偏差均较大,不排除质控样品本身的均匀性导致偏差。
3.5 样品检测情况
用该方法抽样检测南宁市市售鲜米粉和干米粉共70份,结果显示,2份样品检出二氧化硫残留,其余均未检出,检出率为3%,且2份检出样品的二氧化硫含量较低,分别为0.000 6 mg/kg与0.001 5 mg/kg。
4 结论
采用顶空—气相色谱法测定米粉中的二氧化硫残留量,具有前处理简单、重现性好、自动化程度高的特点。ECD检测器具有较高的灵敏度,检出限可达2 μg,检测时取用少量均匀试样就可进行检测。测定1个样品所需的上机时间仅10 min,使用111位全自动顶空进样装置,可以实现一天检测上百份样品,具有蒸馏滴定法不可比拟的优势。
此次对市售鲜米粉与干米粉抽样检测,虽有二氧化硫检出,但含量极低。在米粉的加工过程中,为改善口感会添加食用淀粉,不排除添加物中的二氧化硫带入,故对于非法添加的界定,还需对米粉加工过程加以调查才能确定。目前,GB2760《食品安全国家标准 食品添加剂使用标准》[1]中并未对鲜湿米粉及干米粉的二氧化硫残留量进行明确限定。部分市售米粉的成分并无详细标识,需对米粉的加工生产进行更加细致地监管,才能有效保护消费者的身体健康。
