亲油性Fe3O4微粒的制备及磁化强度的研究*
2022-08-02迟佳龙
迟佳龙
(黑龙江省化工研究院,黑龙江 哈尔滨 150078)
Fe3O4微粒由于其本身具有的反尖晶石结构和超顺磁性,使其体现出很多与其他纳米材料不同的特性。在其表面包覆上不同的官能团使其体现出不同的性能,目前,Fe3O4微粒已经应用于密封、水处理、机械减震、扬声器、生物提取等众多领域[1-4]。制备Fe3O4微粒的方法有化学共沉淀法、机械研磨法、溶胶-凝胶法、水热法等[5],其中化学共沉淀法具有制备条件简单、粒径容易控制等优点,是目前主流的制备方法。磁化强度是指磁性材料在外加磁场中被磁化时所能达到的最大磁化强度,磁化强度越大,在磁场中受力就越大,反之受力就小,是Fe3O4微粒主要性能指标。
本文采用化学共沉淀法制备亲油性Fe3O4微粒,并对不同条件下制备的亲油性Fe3O4微粒磁化强度进行了分析。
1 实验部分
1.1 试剂及仪器
Fe2SO4·7H2O(AR国药集团化学试剂有限公司);FeCl3·6H2O(AR国药集团化学试剂有限公司);NH3·H2O(AR汕头西陇化学试剂有限公司);油酸(AR上海阿拉丁试剂有限公司)。
DJ1C-60型增力搅拌器(江苏大地自动仪器厂);B-260型恒温水浴锅(上海亚荣生化仪器厂);SHZ-D型不锈钢循环水真空泵(邦西仪器科技有限公司);DHG-9030A型鼓风干燥箱(上海精宏实验设备有限公司);Y500型X射线衍射(丹东奥龙射线仪器有限公司);FTIR-650型傅里叶红外光谱仪(天津港东);JM-1型振动样品磁强计(中科院物理研究所)。
1.2 实验过程
化学共沉淀法制备Fe3O4微粒。按照一定的Fe2+和Fe3+摩尔比,称取FeSO4·7H2O和FeCl3·6H2O,分别用蒸馏水溶解,然后将上述两种溶液放入一个烧杯中混合。在另一烧杯中加入一定量的NH3·H2O搅拌状态下迅速倒入混合溶液。快速搅拌一定时间后升温至特定温度,用油酸调节pH值至9。持续搅拌一定时间后,放在磁铁上沉淀10min,倒出上层清液,再往沉淀层倒入100℃蒸馏水,搅拌均匀,抽滤,反复用100℃蒸馏水清洗5次,烘干即得黑色样品备用。
2 结果与讨论
2.1 影响Fe3O4微粒磁化强度的制备条件
共沉淀法是指在溶液中含有两种或多种阳离子,它们以均相存在于溶液中,加入沉淀剂,经一定温度和时间沉淀反应后,可得到各种成分均一的沉淀。所以阳离子的摩尔比、反应温度和反应时间在化学共沉反应中是重要的影响因素。
采用化学共沉淀法制备Fe3O4微粒化学反应式为:
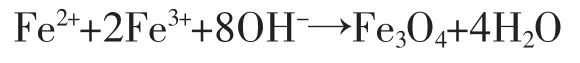
根据化学共沉淀法及上述化学反应式,确定影响制备Fe3O4微粒磁化强度的几个主要反应条件为:(1)Fe2+和Fe3+摩尔比;(2)反应温度;(3)反应时间。通过这3个反应条件的优化,确定出Fe3O4微粒最大磁化强度的制备条件。
2.2 影响Fe3O4微粒的磁化强度制备条件的确定
根据课题组以前的实验数据和参考文献[7-9],确定本文影响Fe3O4微粒磁化强度的制备条件见表1,得到的样品通过振动样品磁强计测试并绘制磁滞回线,从而分析出不同制备条件对磁化强度的影响。

表1 Fe3O4微粒的制备条件Tab.1 Preparation conditions of Fe3O4 particles
2.3 不同制备条件对Fe3O4磁化强度的影响
2.3.1 铁离子摩尔比的影响 按照1.2实验过程,确定反应温度是95℃,反应时间是25min,改变Fe2+和Fe3+的摩尔比。考察Fe2+和Fe3+的摩尔比对于磁化强度的影响,结果见图1、2。

图2 铁离子摩尔比对Fe3O4微粒磁化强度的影响Fig.2 Effect of molar ratio of iron ions on magnetization of Fe3O4 particles
按照共沉淀生成Fe3O4的化学方程式,Fe2+和Fe3+的摩尔比应该为1∶2,在NH3·H2O过量的条件下就会生成Fe3O4。但在实际的实验过程中,Fe2+极易被氧化生成Fe3+,这就造成了Fe2+和Fe3+的摩尔比失衡。由图1、2可知,这是由于当Fe2+和Fe3+的摩尔比小于5.5∶10(mol∶mol)时,体系中的Fe3+比较多,碱性条件下就会产生Fe2O3,Fe2O3属于α型晶胞结构,从而降低了磁性,所以磁化强度就低。当Fe2+和Fe3+的摩尔比大于5.5∶10(mol∶mol)时,体系中Fe2+比较多,在碱性条件下就会产生FeO·H2O,而FeO的晶体结构是立方晶体结构,部分晶体呈菱形,并具有反磁性。从而降低了磁化强度。因此,当Fe2+和Fe3+的摩尔比为5.5∶10(mol∶mol)时,其他条件相同,Fe3O4的磁化强度最大。
2.3.2 反应温度的影响 按照1.2实验过程,确定Fe2+∶Fe3+为5.5∶10(mol∶mol),反应时间25min,改变反应温度,分析反应温度对于磁化强度的影响,结果见图3、4。

图3 Fe3O4微粒不同温度的磁回滞线Fig.3 Magnetic hysteresis lines of Fe3O4 particles at different temperatures

图4 温度对Fe3O4微粒磁化强度的影响Fig.4 Effect of temperature on magnetization of Fe3O4 particles
由图3、4可知,当反应温度较低时,形成反式尖晶石结构的熟化速率很慢,Fe3O4不能完美形成反式尖晶石结构,所以磁化强度就低。当反应温度升高至85℃时,熟化温度高加快形成反式尖晶石结构的速率,完美反式尖晶石结构的Fe3O4增多,所以磁化强度也逐渐升高。但当温度继续升高超过85℃时,Fe3O4结构中的Fe2+会加快和空气中的氧结合发生氧化,从而形成Fe2O3,所以磁化强度开始下降。因此,当反应温度为85℃的条件下,制备的Fe3O4的磁化强度最大。
2.3.3 反应时间的影响 按照1.2实验过程,确定Fe2+∶Fe3+为5.5∶10(mol∶mol),反应温度85℃,改变反应时间,考察反应时间对于磁化强度的影响,结果见图5、6。

图5 Fe3O4微粒不同反应时间的磁回滞线Fig.5 Magnetic hysteresis lines of Fe3O4 particles at different reaction times
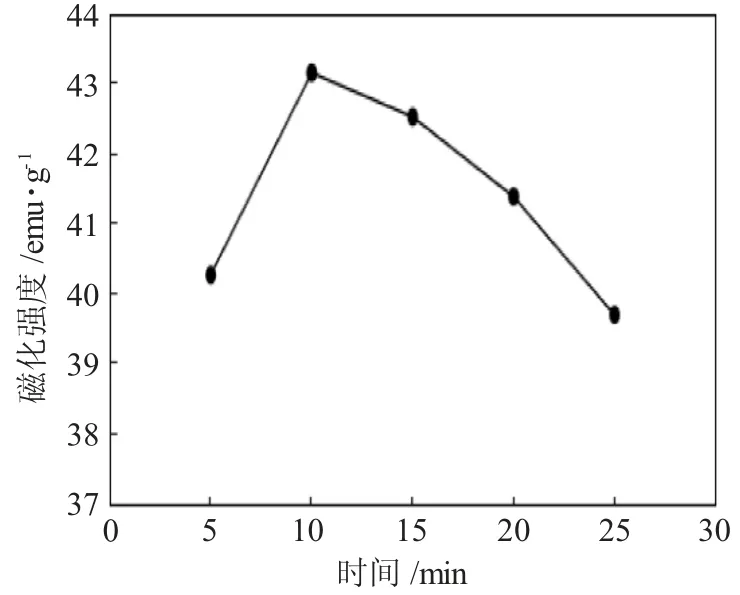
图6 反应时间对Fe3O4微粒磁化强度的影响Fig.6 Effect of reaction time on magnetization of Fe3O4 particles
由图5、6可知,Fe3O4的磁化强度随着反应时间的加长呈现先增大后减小的趋势。这是因为Fe2+∶Fe3+在碱性条件下共沉淀形成反尖晶石结构需要一定的时间,时间短,反尖晶石结构低;随着反应时间的增加,形成尖晶石结构的程度逐渐增多。所以,磁化强度呈现增长的趋势,当反应时间继续增加,Fe3O4基本上形成尖晶石结构后,部分Fe3O4长时间和氧分子接触发生氧化,形成Fe2O3。因此,当反应时间为10min条件下,制备的Fe3O4的磁化强度最大。
综上,最大磁化强度的Fe3O4微粒的制备条件为:Fe2+∶Fe3+为5.5∶10(mol∶mol)、反应温度85℃、反应时间10min。
2.4 最大磁化强度的Fe3O4微粒的XRD与FT-IR分析
通过对最大磁化强度的条件下制备的Fe3O4微粒样品进行XRD与FT-IR测试,并分析其结构与亲油性。
2.4.1 Fe3O4微粒的XRD分析
图7为Fe3O4微粒的XRD图。
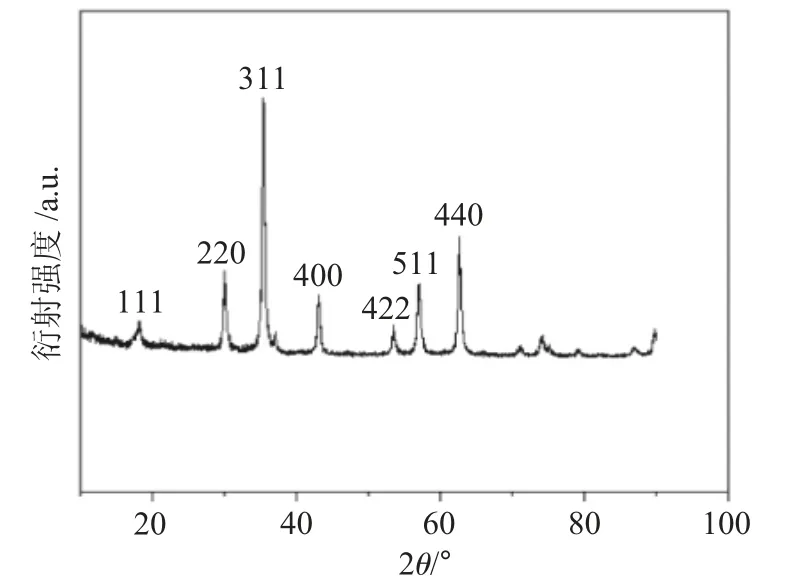
图7 Fe3O4微粒的XRD图Fig.7 XRD diagram of Fe3O4 particles
由图7可知,XRD谱图上2θ在18.36°,30.13°,35.02°,42.74°,53.62°,57.18°,62.37°处的衍射分别为(111),(220),(311),(400),(422),(511),(440)晶面衍射峰。通过对比Fe3O4标准图谱(JCPDS19-0629卡)仍为反尖晶石结构的晶体,晶型结构完整且纯度较高。
2.4.2 Fe3O4微粒的FT-IR分析
图8为Fe3O4微粒的FT-IR图。

图8 Fe3O4微粒的FT-IR图Fig.8 FT-IR diagram of Fe3O4 particles
由图8可知,590cm-1处为Fe-O键的红外特征吸收峰,它的峰高最高,红外特征最明显。在2925和2840cm-1处为-CH2-的伸缩振动峰,2260cm-1处为积累双键吸收峰,在1633cm-1处为C=C的伸缩振动峰。1420cm-1处为-COO-的漂移吸收峰。通过FTIR谱图可见,油酸和Fe3O4微粒之间确实有化学键存在[6],Fe3O4微粒已经被油酸包覆,实现了亲油性能。
3 结论
采用化学共沉淀法通过加入油酸可以制备出亲油Fe3O4微粒,并且不影响Fe3O4微粒的反尖晶石结构。化学共沉淀法制备最大磁化强度的Fe3O4微粒的条件为:Fe2+∶Fe3+为5.5∶10(mol∶mol),反应温度85℃,反应时间10min,在此条件下制备出的Fe3O4微粒的磁化强度为43.15emu·g-1。
