中国光学相干断层成像技术在缺血性脑血管病介入诊疗中的应用专家建议
2022-08-02中国研究型医院学会介入神经病学专业委员会
中国研究型医院学会介入神经病学专业委员会
光学相干断层成像(optical coherence tomography,OCT)作为一种血管内成像技术,在冠状动脉诊疗领域已得到广泛认可。在欧洲心胸外科协会(European Association for Cardio-Thoracic Surgery,EACTS)2014年的心肌血运重建指南中,OCT对于评估冠状动脉病变特征及优化支架置入术的应用价值均为Ⅱa类证据推荐[1]。在脑血管领域,国内外一些医疗中心已尝试通过OCT来评估脑血管病变、斑块性质并指导介入治疗,但尚缺乏共识和规范。为此,中国研究型医院学会介入神经病学专业委员会组织国内有丰富介入诊疗临床经验的脑血管病专家,结合OCT的临床应用实践及文献资料,共同制定OCT在脑血管诊疗领域的成像方法、图像分析及临床应用的中国专家建议,旨在指导OCT在脑血管病介入诊疗中的合理、安全应用,为OCT在脑血管领域开展深入研究奠定基础。
1 OCT技术概述
OCT技术的成像原理类似于超声成像,只是用光波代替了声波,其图像分辨率高于血管超声。相对于MR血管成像、CT血管成像、血管超声、经颅多普勒等无创检查方法,OCT属于有创的血管腔内影像检查,其需要在DSA的辅助下进行术中实时检查,可作为DSA二维图像的补充。当患者血管病变性质无法判断、血管斑块易损性需要量化评估、介入治疗术中及随访观察时,可以考虑进一步行OCT检查。
1.1 OCT技术成像原理
OCT以近红外光作为光源,发出信号臂和参考臂两束光线。信号臂发射到被测物质,如血管壁;参考臂发射到反光镜上,起到参照作用。信号臂与参考臂反射回来的两束光信号,会叠加或抵消从而形成新的波形。通过改变反光镜的位置来改变参考臂的长度,继而得到不同深度的组织信号。由于组织性状不同,从组织中反射回来的光信号强弱不等,之后可经计算机处理重建光信号,产生组织微结构的横断面图像[2]。
根据成像原理,OCT技术可分为时域OCT(time domain OCT,TD-OCT)和频域OCT(frequency domain OCT,FD-OCT)两种类型。红细胞吸收光线会干扰OCT成像效果,因此在成像时需要尽可能清除血液。TD-OCT在检测时为营造血管内无血环境,需要使用球囊阻断靶血管近端血流,可能引起缺血症状或发生病变血管远端缺血情况,且操作相对复杂;而FD-OCT具有更快的成像速度,仅需快速注射对比剂即可清除血液干扰而无需球囊阻断近端血流,操作简单且安全性更高。因此,FD-OCT是目前最常用的技术。最新一代的ILUMIEN OPTIS系统成像速度更快,能够使OCT和血管造影进行自动校准并实现三维重建,有助于精确的支架定位[3],该系统整合了血流储备分数功能,具备血管结构和功能学评估功能,扩展了OCT的应用领域。
1.2 OCT系统介绍
OCT成像系统的组件构成包括成像引擎、显示器、一体化的驱动马达和光学控制器(drive-motor optical controller,DOC)、隔离变压器、CD/DVD光驱、文件架、USB接口、主电源开关、键盘和鼠标。成像导管工作长度135 cm,头端外径2.7 F,外包亲水涂层。导管头端及距头端20 mm处各有1个专用标识,目前常用的OCT成像导管的光学透镜位于近端标识。由于OCT采用的近红外光无法穿透血流(红细胞)成像,因此需通过导引导管快速注射晶体溶液或对比剂清除血液,才能使血管壁及血管腔清晰成像。
1.3 OCT应用于缺血性脑血管病的价值和局限性
在缺血性脑血管病的介入诊疗中,OCT虽然尚未常规使用,但相对于其他传统的影像学评估手段,其能够提供更多血管管壁和腔内信息,有利于缺血性脑血管病的精准介入治疗。
应用价值:(1)评估脑血管病变性质,如动脉粥样硬化、夹层形成等;(2)评估动脉粥样硬化斑块的易损性、斑块进展及药物治疗后的效果;(3)指导脑血管支架的选择;(4)术后即刻评价支架的置入情况,如支架贴壁不良、膨胀不良、病变覆盖不全、边缘夹层、组织脱垂及支架内血栓形成等;(5)支架置入术后长期随访评估新生内膜增生和支架内再狭窄等[4-5]。
应用的局限性:(1)不能用于存在脑血管造影禁忌证的患者;(2)不适合应用于迂曲的脑血管。
推荐意见:(1)了解血管内OCT技术成像原理,选择FD-OCT,利于快速成像;(2)掌握OCT在脑血管介入中的应用价值及局限性。
2 OCT图像采集
2.1 图像采集过程
在完成脑血管造影,确定病变部位后,将导引导管及微导丝置于目标血管的适当位置。微导丝头端或保护伞近端至病变远端距离应不少于7.0 cm。在颈动脉支架置入前,先置入保护伞。启动OCT机器,创建新病例并输入患者信息。给驱动马达和光学控制器套上无菌塑料保护罩。取出OCT成像导管并用肝素等渗盐水浸湿纱布擦拭,激活亲水层。以3 ml的100%碘对比剂从侧孔推注冲洗成像导管管腔,直至从导管头端流出3滴对比剂,并保留注射器。连接成像导管和DOC,将导管衬套插入DOC端口中并顺时针旋转直至固定。
校准导管:对照屏幕上的校准标记手动校准或自动校准。启动实时扫描成像,成像导管沿0.014英寸(0.356 mm)导丝或保护伞自带的导丝送至病变处或支架远端,OCT导管近端标识需超过病变5 mm,以便识别出病变远端的正常血管。通过实时造影和成像导管上的标记确保导引导管与靶血管同轴,以利于管腔内的血液冲洗完全。根据病变血管部位设置高压注射泵参数,包括冲洗速率、总冲洗量及最高限压,或者准备含足量对比剂的注射器进行手动注射。注入对比剂,管腔充分冲洗,光镜自行回撤,从而获得血管OCT横断面图像。
一般来说,为充分显像,颈动脉颅外段成像推注的参数为:速度10 ml/s,剂量20 ml,限压2 068.43 kPa(300磅力/平方英寸);椎动脉颅外段成像推注的参数为:速度10 ml/s,剂量20 ml,限压2 068.43 kPa;颅内动脉成像推注的参数为:速度4 ml/s,剂量8 ml,限压2 068.43 kPa。术者和OCT操作者应做好密切配合,在快速推注对比剂之前,推注少量对比剂以再次确认导管的同轴性,尽量保证单次冲刷完成成像,避免多次对比剂冲洗,减少对比剂用量。
2.2 图像采集范围
既往研究中,OCT在脑血管系统中的应用部位包括颅外段和颅内段。目前颅外段血管如颈内动脉窦部、颈段、岩段、椎动脉起始部应用较多,颅内段血管如颈动脉颅内段及基底动脉也有应用报道[4,6-17]。对于大脑中动脉M1段及以远,基于目前的OCT导管,仅有动物及尸体研究报道,尚未成功应用于临床[7]。由于OCT成像导管的设计是基于冠状动脉,在迂曲的脑血管中应用时,存在一定的局限性。对于严重迂曲的血管,反复尝试可导致光学透镜损坏、血管损伤等[16,18]。此外,迂曲的脑血管可导致血管冲洗不良或产生不均匀旋转伪像,必要时需重复成像或加大冲洗速率[18]。在颅内血管成像时,必要时可配合中间导管使用[5]。目前,OCT技术可观察的血管直径范围为7 mm左右,穿透深度为0.1~2.0 mm[2],对于巨大的动脉瘤、管径偏大的血管、脂质或者血栓覆盖下的血管壁等无法完全成像。
2.3 图像采集的局限性及影响成像质量的原因
OCT作为目前分辨率最高的血管内成像技术,具有可观察血管内细微结构的优势,但在应用中也存在一定的局限性:由于组织穿透性较低,OCT评估弥漫性病变的斑块负荷及血管直径的能力有限[19];由于光衰减,大量血栓及脂质的存在会影响OCT对血管壁外膜层的评估;颅内血管相对迂曲,对于大脑中动脉,指引导管难以到达,血管远端预留空间不足,目前的OCT成像较难实现[4]。
影响OCT成像质量的主要原因[18]:(1)指引导管与靶血管未同轴,不能实现血管内血液有效冲洗;(2)推注对比剂速度缓慢或推注量不足,血液冲洗不充分;(3)术者推注对比剂与图像采集不同步;(4)OCT成像导管边支冲洗不充分,有血液或气泡残留;(5)推注的对比剂中掺有血液,或对比剂浓度过低;(6)脑血管严重弯曲、钙化病变易造成成像导管损坏,并出现伪像;(7)动脉直径过大(>7 mm)及开口或分叉处病变。
推荐意见:(1)熟悉血管内OCT的操作方法,术中冲洗管腔血液,利于清晰成像。(2)确保导引导管与靶血管同轴,根据病变血管部位设置高压注射泵参数,以利于管腔内的血液冲洗完全,从而获得血管OCT横断面图像。(3)颈动脉颅外段成像推注的参数为:速度10 ml/s,剂量20 ml,限压2 068.43 kPa;椎动脉颅外段成像推注的参数为:速度10 ml/s,剂量20 ml,限压2 068.43 kPa;颅内动脉成像推注的参数为:速度4 ml/s,剂量8 ml,限压2 068.43 kPa。(4)若成像质量不理想,立即分析影响成像质量的可能原因,予以纠正。
3 OCT图像的解读
3.1 正常血管结构及常见的病变特征
如果一个区域里有一些高折射率的颗粒,如脂肪泡或者红细胞,那么这个区域可能拥有比较强的背散射和非常强的衰减。如果一个区域有大量的小颗粒(如纤维蛋白),那么这个区域就有较强的背散射和比较弱的衰减。由于血管壁的组织成分有所变化,OCT图像可呈现出不同的光信号特征,从而清晰地呈现血管壁结构。脑血管的管壁内膜为弹力纤维层,反射信号高,在OCT图像上表现为高信号亮带状;中膜为平滑肌层,反射信号微弱,表现为信号较低暗带;外膜为细胞外基质和外弹力膜,表现为高信号,亮度不均一(图1a)。
经组织病理验证,OCT对识别不同类型的斑块成分具有较高的敏感度与特异度,图像分辨率可达到10 μm,是血管内超声的10倍[20]。动脉粥样硬化斑块在OCT图像上表现为血管壁增厚,血管壁的三层结构(内膜、中膜及外膜)缺失。
纤维斑块、钙化斑块和脂质斑块在OCT图像上表现特征各有不同。在OCT图像上,纤维斑块表现为同质、高信号和弱衰减区域,可见内弹力膜或外弹力膜;若纤维帽组织表现出信号不连续,和(或)伴有斑块内空腔形成,则为斑块破裂(图1b);脂质斑块表现为强衰减区域、低信号,边缘模糊,表面有高信号带的纤维帽(图1c);钙化斑块表现为低信号或不均匀区域,但边缘锐利(图1d)。在心血管领域,基于病理结果与OCT图像特征比较予以证实,易损斑块的最主要表现形式为具有大脂质核心的薄纤维帽(<65 μm)斑块(thin-capfibroatheroma,TCFA)[21]。在颈动脉斑块中,基于OCT如何界定TCFA的纤维帽厚度尚无定论。

在血栓识别方面,OCT不仅可以识别造影无法发现的微小附壁血栓,还可以利用红细胞的光散射现象分析血栓的性质[22]。红色血栓主要由红细胞和纤维蛋白组成,白色血栓主要由血小板及纤维蛋白组成。OCT的信号减弱模式主要受血栓内红细胞密度影响,红色血栓信号不强,呈现为高背反射伴有阴影的图像;白色血栓信号强,呈现为阴影较少的低背反射图像(图1e,1f)。
此外,OCT还能识别更加细微的病变特征[21]。胆固醇结晶表现为信号强度较高、衰减较低的薄线性区域,通常位于纤维帽或脂质斑块坏死核心中与脂质伴行;新生滋养血管为无信号空隙、轮廓清晰[23];巨噬细胞表现为高亮伴有强衰减的点状信号。尽管目前OCT的分辨率无法观察到单个巨噬细胞,但可通过量化分析巨噬细胞密度的方法以探究炎性反应在动脉粥样硬化斑块中的作用[24-25]。OCT对夹层诊断的敏感度较高,可以发现血管内的微小夹层,表现为较强的信号,可见血管壁间有间隙[26]。新生滋养血管在OCT图像上表现为多个(至少3个)连续截面中观察到的直径为50~300 μm的低信号和边缘锐利的空洞样结构,也被称为微通道[27]。
3.2 脑血管OCT图像存在的不足
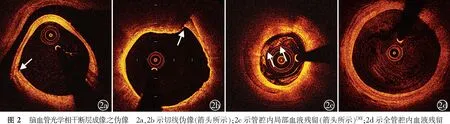
OCT伪像是指由成像系统或其他原因造成的图像畸变或与血管解剖结构存在的差异,包括血液残留、错层伪像、气泡伪像、切线伪像、饱和伪像和导丝损坏等(图2)。由于OCT的组织穿透力有限(0.5~1.5 mm)[4],无法完成血管壁长段纵断面的成像,对于巨大斑块或者混合斑块,难以完全区分钙化与脂质。管腔内或管壁上若附着红血栓,由于信号的衰减可导致血管壁外膜层结构无法成像,出现类似脂质斑块的伪影。评估炎性斑块时,难以准确定量识别巨噬细胞,且由于巨噬细胞的强衰减信号特性,形成类似脂质坏死核心成像,影响对深层的脂质评估[24]。当巨噬细胞与微小钙化、胆固醇结晶或内外膜同时出现时,明显增加识别血管壁内病变图像的难度。
推荐意见:(1)建议应用血管内OCT图像识别正常血管壁的结构,并对易损斑块、动脉夹层形成及附壁血栓等进行鉴别;(2)建议应用血管内OCT图像识别斑块类型,并对脂质池、钙化结节、巨噬细胞浸润等成分特征进行鉴别;(3)建议识别OCT图像的伪像,包括血液残留、错层伪像、气泡伪像、切线伪像、饱和伪像和导丝损坏等。
4 OCT在缺血性脑血管病介入诊疗中的应用
OCT技术在评估颅外病变及颅内病变中均有所应用。基于目前的OCT成像导管材料,OCT技术可以用于椎-基底动脉[14]相关病变。对于前循环病变,OCT技术检查的可视范围可达颈动脉岩骨段。
4.1 术前评估
术前可以通过OCT评估颈动脉粥样硬化斑块的形态特征,从而识别易损斑块,指导介入治疗。在冠状动脉的介入诊疗领域,已有研究报道术前通过OCT对冠状动脉斑块形态进行评估,有助于指导选择介入治疗措施并预测患者术后的疗效[31-32]。有研究表明,通过OCT所观察到的斑块图像特征,并基于斑块的“薄纤维帽”特征,可预测动脉粥样硬化斑块的破裂和血栓发生风险,对症状性颈动脉斑块进行识别[33]。同样,基于OCT斑块特征的研究结果,说明OCT斑块特征与颈动脉狭窄程度以及缺血症状存在一定相关性[34-35]。因此,在脑血管介入治疗前利用OCT评估斑块特征,识别易造成缺血事件的高危斑块,指导颈动脉介入治疗,特别是对血管狭窄程度未达到干预程度,但存在易损斑块的病变具有重要意义。同时OCT能够准确测量病变的血管直径、提供参考血管直径和病变长度[36-37],为术者选择适宜的支架与球囊类型提供客观依据。
4.2 评价介入治疗后的即刻效果
目前,OCT已被用于评价支架置入术后相关支架即刻的膨胀率、支架贴壁性、病变组织向血管腔内的突出及支架内血栓形成等。在OCT图像中,采用支架即刻膨胀率(支架的膨胀率:支架最小面积/平均参考管腔面积×100%)来评价上述支架置入后的功能结构特征变化[38],通常将<90%作为评价支架膨胀不良的界值。当支架支撑杆表面至管腔表面之间的轴向距离大于支架支撑杆的厚度时,定义为支架贴壁不良。支架支撑杆厚度的突出距离为10~200 μm,因此可将支架支撑杆表面至管腔表面之间的轴向距离>200 μm定义为支架贴壁不良[21,39-40](图3a)。组织突向管腔内的定义是支架置入后,血管壁表面的组织经支架网状结构向管腔内突出[41-42]。当支架放置在薄纤维帽斑块或坏死核心表面时,斑块组织被支架“挤压”突入管腔更常见。根据突入管腔内组织成分不同,可分为斑块或血栓。突入管腔内斑块表面通常光滑且无明显的信号衰减(图3a),而血栓突出表面通常不规则且伴有强光学衰减[21,38](图3b)。通过使用闭环支架有助于解决颈动脉易损斑块支架置入后组织向血管腔内突出的问题,尤其是突出>500 μm的斑块组织[40]。在OCT图像上,即刻发生的支架内血栓的定义是支架置入即刻出现局限性突入管腔内的不规则团块(图3c)[43]。在颅内血管急性闭塞再通术中,应用OCT可以对治疗过程中的病变性质,如夹层、动脉粥样硬化性狭窄等病变进行识别,指导手术策略的制定[15]。

4.3 介入治疗后随访
OCT可用于介入治疗后随访以了解支架术后内膜的修复、支架内再狭窄、新生动脉粥样硬化和血栓形成等[44-46]。如果OCT能够识别支架支撑杆上覆盖组织,则称为支架支撑杆覆盖(图4a)[47-48];如果OCT未观察到支架支撑杆上覆盖组织,则称为支架支撑杆未覆盖(图4a)[47]。Gonzalo等[49]根据OCT图像特征,将动脉壁新生内膜分为以下三类:(1)均质型,均匀高密度反向散射,不伴信号衰减(图4b);(2)非均质型,低密度反向散射且信号不均匀,伴局部信号衰减(图4c);(3)分层型,若出现双层的光学信号,通常血管腔近场侧壁成像为高反射信号(外膜层),远场侧壁成像为低反射信号,即内膜层(图4d)。基于OCT的北美症状性颈动脉内膜切除试验法计算血管腔的狭窄率[33],即为(病变远端血管参考直径-狭窄病变最小管腔直径)/病变远端血管参考直径×100%。当支架狭窄率≥50%时,定义为支架内再狭窄[50]。当新生内膜出现钙化、脂质成分或胆固醇结晶时定义为新生动脉粥样硬化[38](图4e)。随访时支架内血栓形成定义为出现在内膜表面或漂浮于管腔内支架小梁上的不规则团块(图4f)[51]。研究结果表明,支架支撑杆未覆盖(OR=8.26,95%CI:6.82~10.04;P<0.01)和支架贴壁不良(OR=13.03,95%CI:10.13~16.93;P<0.01)与晚期支架内血栓形成密切相关[38,52-53]。
推荐意见:(1)通过术前OCT,评估动脉粥样硬化斑块的形态特征、识别易损斑块,从而指导介入治疗;(2)支架置入后即刻行OCT,对支架贴壁等情况进行评估,及时发现支架内血栓形成;(3)支架置入术后采用OCT随访时,可以了解支架置入术后内膜修复、支架内再狭窄、新生动脉粥样硬化斑块和血栓形成等情况。
5 结论
综上所述,OCT可准确评估脑血管病变、斑块性质,并指导临床介入诊疗。对于有条件的医疗中心,建议规范化应用OCT指导缺血性脑血管病的介入精准治疗。未来应建立中国缺血性脑血管病患者OCT临床研究数据库,提供OCT在脑血管病诊疗中的循证医学证据。
执笔刘锐(东部战区总医院);胡伟(中国科学技术大学附属第一医院);孙文(中国科学技术大学附属第一医院);韩云飞(东部战区总医院)
参与讨论专家名单(按姓氏汉语拼音排序) 曹辉(南京脑科医院);曹文锋(江西省人民医院);陈长青(中南大学湘雅医院);陈光辉(东部战区总医院);陈国华(武汉市第一医院);陈红兵(中山大学附属第一医院);陈星宇(厦门大学附属中山医院);杜鹃(东部战区总医院);范进(西部战区总医院);樊小兵(东部战区总医院);高连波(中国医科大学附属第四医院);高小平(湖南省人民医院);郭富强(四川省人民医院);韩巨(山东省千佛山医院);韩云飞(东部战区总医院);杭春华(南京大学医学院附属鼓楼医院);胡伟(中国科学技术大学附属第一医院);黄晓松(湖南省脑科医院);贾颐(西安高新医院);蒋智林(北部战区总医院);焦力群(首都医科大学宣武医院);柯开富(南通大学附属医院);李冰(山东省烟台毓璜顶医院);李长茂(湖南省娄底市中心医院);李敏(江苏省中医院);李永坤(厦门大学第一附属医院);林航(解放军联勤保障部队第九○○医院);林敏(福建省第二人民医院);刘德志(上海中医药大学附属曙光医院);刘建林(西安交通大学第一附属医院);刘锐(东部战区总医院);刘圣(南京医科大学第一附属医院);刘文华(武汉市第一医院);刘新峰(东部战区总医院);刘新通(广东省第二人民医院);刘煜敏(武汉大学中南医院);刘运海(中南大学湘雅医院);骆翔(华中科技大学同济医学院附属同济医院);吕秋石(东部战区总医院);马敏敏(东部战区总医院);马宁(首都医科大学附属北京天坛医院);缪中荣(首都医科大学附属北京天坛医院);南光贤(吉林大学中日联谊医院);牛国忠(杭州市第一人民医院);彭斌(北京协和医院);濮捷(湖北省中医院);秦超(广西医科大学第一附属医院);石进(空军特色医学中心);石忠松(中山大学孙逸仙纪念医院);孙钦建(山东省立医院);孙文(中国科学技术大学附属第一医院);汤永红(南华大学附属南华医院);田喜光(武警广东省总队医院);王国平(中国科学技术大学附属第一医院);王君(解放军总医院第一医学中心);王启章(深圳市中西医结合医院);王守春(吉林大学白求恩第一医院);王水平(安徽医科大学第一附属医院);王苇(扬州大学附属医院);汪银洲(福建省立医院);王振(长沙市中心医院);吴明华(江苏省中医院);吴伟(山东大学齐鲁医院);吴志强(广东省东莞市人民医院);肖国栋(苏州大学附属第二医院);徐格林(东部战区总医院);薛建中(江苏省常熟市第二人民医院);杨清武(陆军军医大学第二附属医院);杨世泉(解放军联勤保障部队第九○二医院);杨新健(首都医科大学附属北京天坛医院);叶瑞东(东部战区总医院);殷聪国(杭州市第一人民医院);尹琳(大连医科大学附属第二医院);殷勤(东部战区总医院);岳炫烨(天津医科大学总医院);张光运(空军特色医学中心);张桂莲(西安交通大学第二附属医院);张锦华(浙江大学医学院附属邵逸夫医院);张猛(陆军特色医学中心);张勇(青岛大学附属医院);赵振强(海南医学院第一附属医院);周志明(皖南医学院弋矶山医院);朱良付(河南省人民医院);朱其义(山东省临沂市人民医院);朱双根(深圳市龙华区中心医院);朱武生(东部战区总医院)
