眶上外侧入路夹闭后循环动脉瘤七例并文献复习
2022-08-02仇尤佳王紫兰陈周青顾枫谈心王世鑫王伟朱昀王中
仇尤佳 王紫兰 陈周青 顾枫 谈心 王世鑫 王伟 朱昀 王中
在颅内动脉瘤中,后循环动脉瘤较前循环动脉瘤少见,其占所有动脉瘤的8%~15%[1]。基底动脉顶端动脉瘤是最常见的后循环动脉瘤,占后循环动脉瘤的50%以上[2]。基底动脉位于颅底深部的脚间池内,邻近后组脑神经、穿支动脉、脑干等颅内重要结构,基底动脉瘤一旦破裂预后较差,术后病死率和病残率均高于前循环动脉瘤[3]。虽然随着神经影像学、显微手术技术及术中辅助技术的进步,后循环动脉瘤显微手术效果有所改善,但手术夹闭对术者的操作仍然是个考验。目前治疗后循环动脉瘤的手术入路包括颞下入路、翼点入路、乙状窦后入路等[4]。眶上外侧入路由Hernesniemi等[5]于2005年首次提出,是经典翼点入路的改良版本,该入路位置靠前、骨瓣小、创伤小。但该入路在后循环动脉瘤的夹闭中应用较少。2015年12月至2021年1月苏州大学附属第一医院神经外科采用眶上外侧入路治疗7例后循环动脉瘤,现报道如下。
1 对象与方法
1.1 对象
回顾性分析2015年12月至2021年1月连续收治于苏州大学附属第一医院神经外科的后循环动脉瘤患者7例的病历资料。本研究方案经苏州大学附属第一医院医学伦理委员会批准(伦理号:2021伦研批第290号),患者或其家属均签署了知情同意书。
纳入标准:(1)术前行CT血管成像(CTA)或DSA检查明确诊断为后循环动脉瘤;(2)选择使用眶上外侧入路夹闭。排除标准:(1)临床资料及随访资料不完整;(2)不适合手术夹闭或患者选择介入治疗;(3)有严重基础疾病者。
1.2 方法
1.2.1资料收集:收集患者的一般资料(年龄、性别和病史,如高血压病、糖尿病等)、临床资料包括临床症状、入院Hunt-Hess分级、治疗方式、疗效、围手术期并发症及随访(随访时间、随访方式及随访结果)等。高血压病的诊断标准参照《中国高血压防治指南(2018年修订版)》[6],糖尿病诊断标准参照《中国2型糖尿病防治指南(2020年版)》[7]。Hunt-Hess分级标准参照《中国蛛网膜下腔出血诊治指南2019》[8]。
1.2.2影像学检查:所有患者完善头部CT或CTA,明确动脉瘤的部位、大小及瘤顶指向和瘤颈宽径。结合患者症状及CT影像判断动脉瘤是否破裂。使用Mimics 21.0医学影像控制系统(Materialise公司,比利时)三维重建动脉瘤及载瘤动脉,模拟眶上外侧入路骨窗范围,测量分叉角度、动脉瘤颈宽径、动脉瘤直径以及动脉瘤颈与后床突的距离(即瘤颈至后床突的垂直距离[9])以判断是否可通过此入路夹闭动脉瘤。将基底动脉顶端动脉瘤两侧大脑后动脉所呈夹角分为“T”型、“Y”型、“箭头”型[9]以观察分叉角的形状是否影响手术夹闭。
1.2.3手术夹闭:手术采用眶上外侧入路夹闭,患者取仰卧位,头部稍高于心脏水平,头向对侧偏15°~30°。取眶上外侧弧形切口,逐层切开皮肤、皮下及帽状腱膜,取3 cm×4 cm骨瓣,悬吊硬脑膜。轻抬额底,可见视神经,剪开视神经及颈内动脉周围蛛网膜,以释放脑脊液。打开Liliequist膜,越过鞍背后床突,显露载瘤动脉及瘤体,充分游离瘤颈。将动脉瘤夹置于瘤颈,缓慢释放动脉瘤夹,直至完整夹闭瘤颈。夹闭后严密缝合硬脑膜,无需放置硬膜外引流。夹闭动脉瘤后术中多普勒超声证实瘤内无血流通过,周围动脉血流通畅,术后常规行CT或CTA检查证实动脉瘤夹闭完全,无新发出血则手术成功。
1.2.4围手术期并发症和随访:观察围手术期并发症发生情况,如肌力下降、术后脑神经损伤、脑出血、脑梗死、感染等。术后6个月通过门诊和电话进行临床随访,采用格拉斯哥预后量表(GOS)评分[10]评估患者预后, GOS评分1~3分为预后较差,4~5分为预后较好;术后6个月门诊复查CTA,明确动脉瘤是否夹闭完全或复发。
2 结果
2.1 一般资料
7例患者为女性,年龄46~77岁,平均(59±11)岁;术前有突发头痛症状6例,伴恶心呕吐5例,突发意识障碍3例,无症状因健康体检发现1例;Hunt-Hess分级Ⅰ级3例,Ⅱ级1例,Ⅲ级3例;基底动脉顶端动脉瘤5例,大脑后动脉瘤1例,小脑上动脉瘤1例;破裂动脉瘤6例,未破裂动脉瘤1例;动脉瘤直径2.05~8.39 mm,平均(4.3±2.1) mm;动脉瘤颈与后床突的距离为0.34~15.30 mm,平均(7.7±5.1) mm;基底动脉顶端动脉瘤两侧大脑后动脉分叉角度为140.17°~180.00°,平均(156±6)°。见表1。
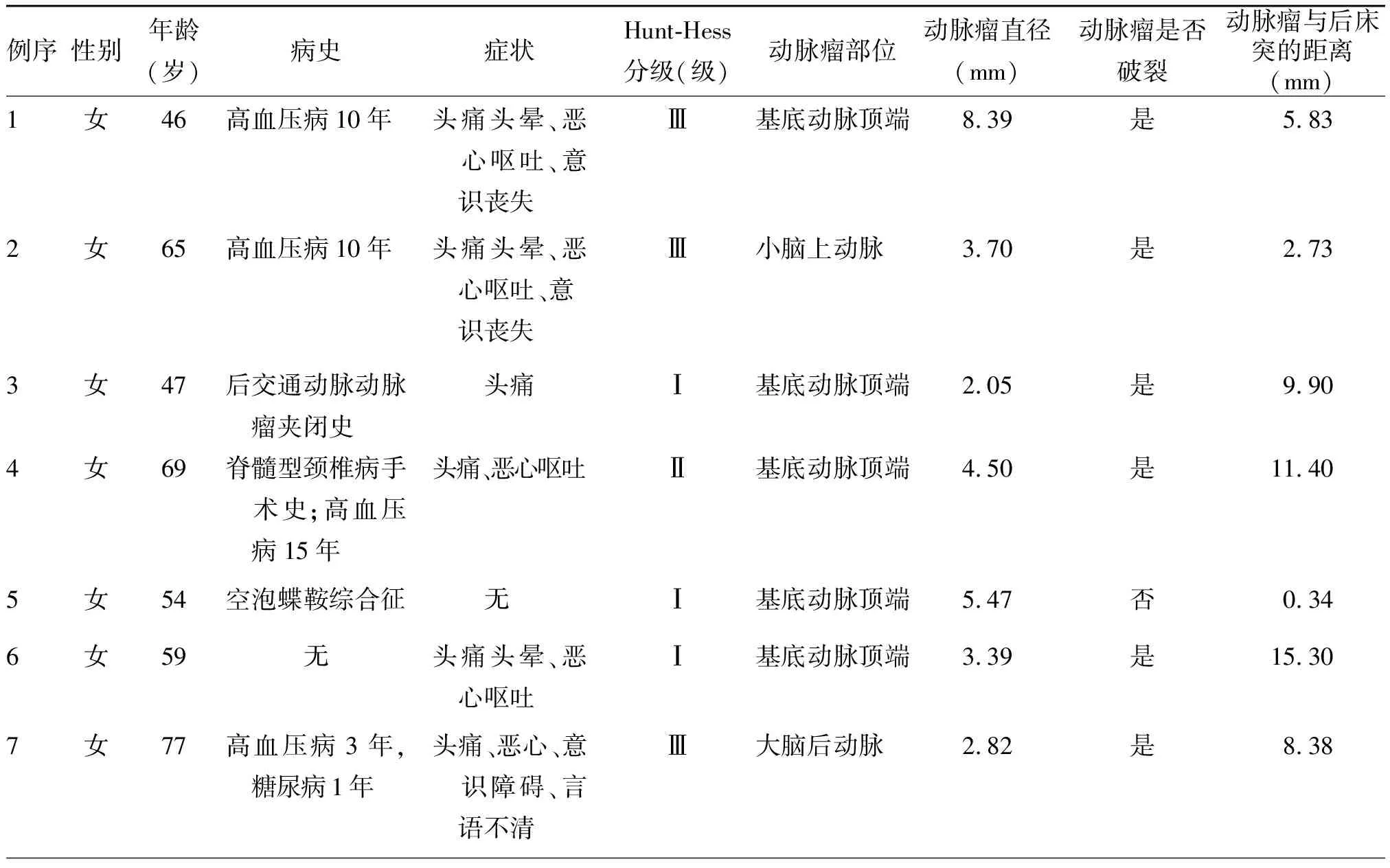
表1 7例经眶上外侧入路夹闭的后循环动脉瘤患者的临床资料
2.2 手术效果及围手术期并发症
患者手术均采用眶上外侧入路,手术时长90~240 min,平均(144±50) min;切口长度6~8 cm,中位长度为8(7,8) cm。夹闭动脉瘤后术中多普勒超声证实瘤内无血流通过,周围动脉血流通畅,术后常规进行CT或CTA复查证实动脉瘤夹闭完全,未见新发出血。围手术期出现肌力下降4例,出院后恢复正常肌力1例;后组脑神经麻痹导致的饮水呛咳1例,出院时已恢复;动眼神经麻痹3例,出院后缓解1例,另2例仍有上睑下垂的症状;脑梗死1例,出现言语功能及肢体活动障碍,予扩张脑血管、改善微循环、扩容补液等处理;肺部感染1例,予抗感染治疗。
2.3 随访结果
所有患者术后6个月进行临床或影像学随访,GOS评分5分4例,4分1例,3分2例;门诊CTA复查均示动脉瘤夹闭完全,无复发。
典型病例1女,54岁,因外院健康体检头部CT发现基底动脉顶端动脉瘤,于2019年11月1日就诊于苏州大学附属第一医院神经外科。患者既往患有空泡蝶鞍综合征。入院时体格检查:意识清楚,言语正常,对答切题;双侧瞳孔等大等圆,瞳孔直径3.0 mm,对光反射灵敏,眼球活动可,双眼颞侧视野缺损;伸舌居中,颈软无抵抗;四肢肌力、肌张力正常,双侧生理反射存在,病理征未引出;Hunt-Hess分级Ⅰ级。入院后于2019年11月3日行头颈部CTA及三维重建示基底动脉顶端动脉瘤(图1a,1b),动脉瘤两侧大脑后动脉分叉呈“Y”型,夹角为140.17°(图1c),动脉瘤瘤颈宽径5.47 mm,瘤颈高于后床突0.34 mm,瘤顶指向上方(图1d)。
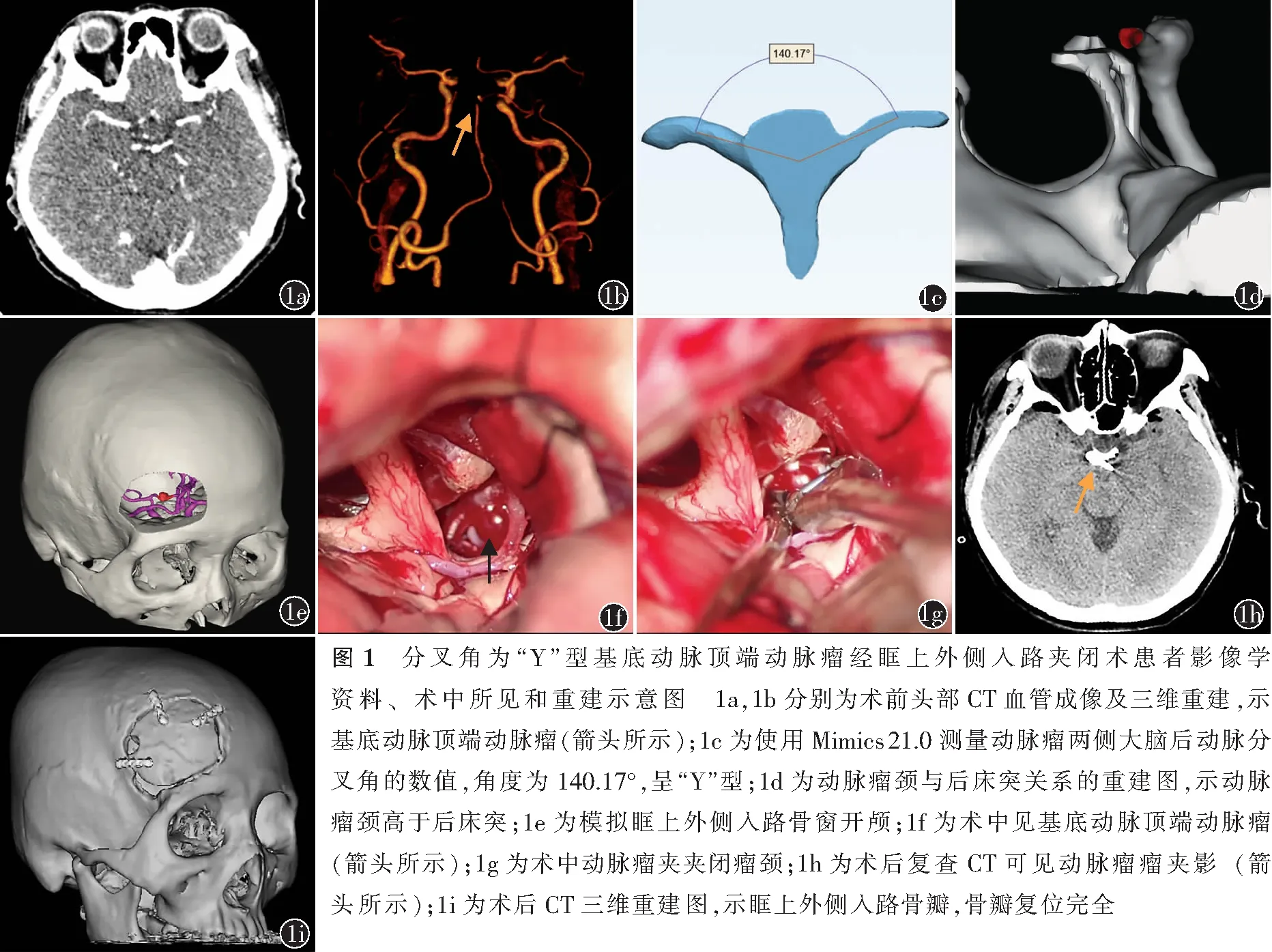
于2019年11月4日行脑血管造影术,示基底动脉顶端囊状动脉瘤,次日拟行动脉瘤夹闭术,模拟眶上外侧入路骨窗开颅(图1e)。取右侧眶上外侧弧形切口,打开颈动脉池,释放脑脊液,脑压下降,进一步打开第二间隙,可见基底动脉顶端动脉瘤(图1f),予以动脉瘤夹(德国贝朗公司,蛇牌,型号750)夹闭瘤颈(图1g),夹闭后经颅多普勒超声监测示载瘤动脉通畅,复查CT可见动脉瘤瘤夹影(图1h),未见明显新鲜出血,CT三维重建示骨瓣完全复位(图1i)。术后给予止血、脱水、抗癫痫等对症支持治疗。患者出院时意识清楚,自动睁眼,对答切题,双侧瞳孔等大等圆,瞳孔直径2.5 mm,双侧瞳孔对光反射灵敏;双眼颞侧视野缺损,四肢肌力Ⅴ级,肌张力不高。术后6个月电话随访,患者仍有双眼颞侧视野缺损,GOS评分5分。
典型病例2女,65岁,主因“意识不清12 h,呕吐1次”于2016年1月10日入诊苏州大学附属第一医院神经外科。患者既往有高血压病史10年余,未规律服药控制。患者于入院前12 h在家中被家属发现意识不清,昏迷倒地,无头部外伤,无肢体抽搐,无大小便失禁。急送至当地医院查头部CT,见鞍上池、环池、外侧裂池及三、四脑室高密度影,示蛛网膜下腔出血(图2a)。为求进一步诊治入诊本院。患者入院时体格检查:意识模糊,对答不切题;双侧瞳孔对光反射灵敏;颈抵抗(+);双侧肌力正常,肌张力不高,双侧Babinski征(-);Hunt-Hess分级Ⅲ级,格拉斯哥昏迷量表评分12分。急诊查CTA三维重建示左侧小脑上动脉瘤(图2b)。动脉瘤瘤颈宽径3.12 mm,动脉瘤直径3.70 mm,瘤颈高于后床突约2.73 mm,瘤顶指向颞侧(图2c)。
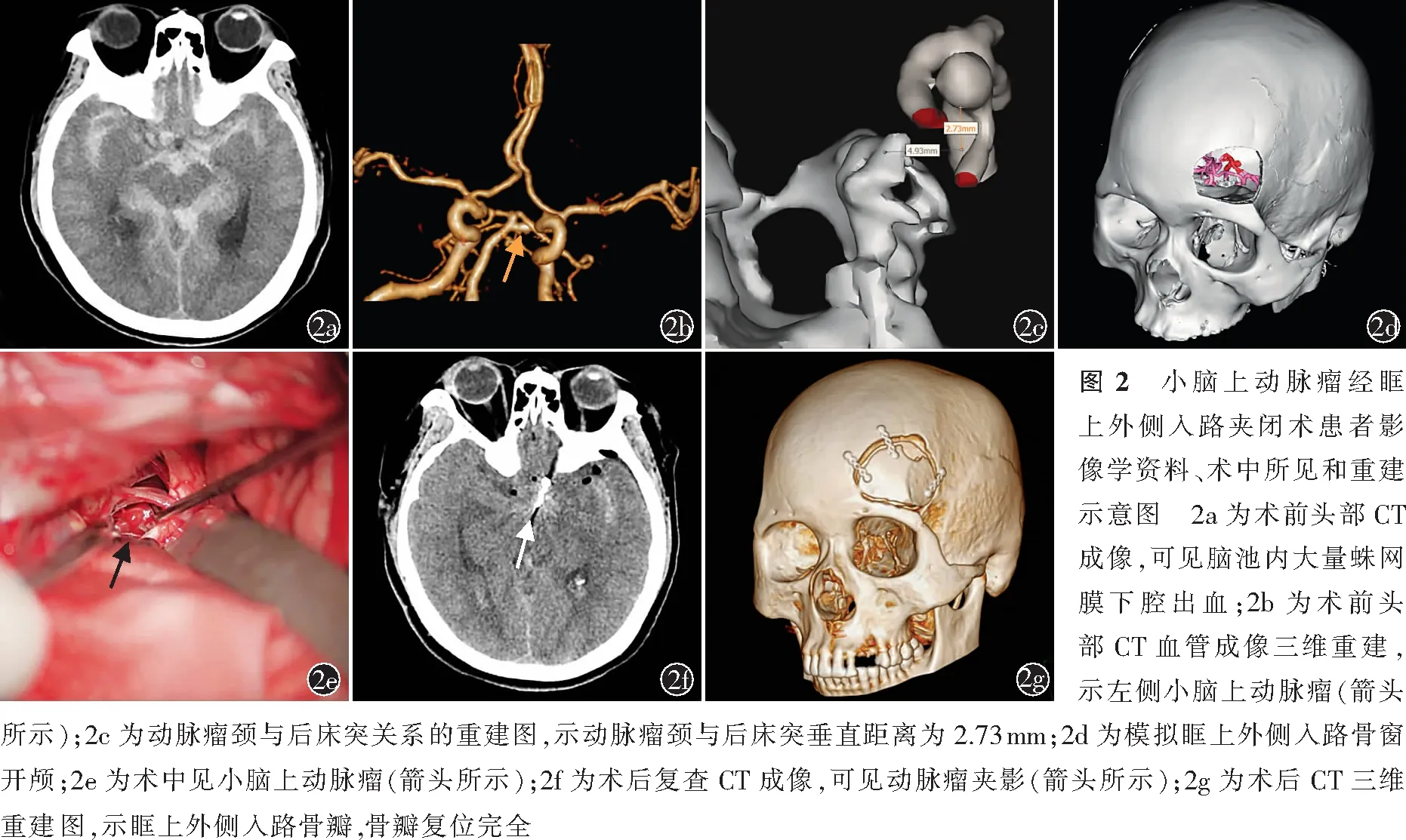
入院后予止血、脱水、抗血管痉挛对症治疗,于2016年1月12日行眶上外侧入路动脉瘤夹闭术,模拟眶上外侧入路骨窗开颅(图2d)。取左侧眶上外侧入路,暴露出第二间隙后分离出动脉瘤体,载瘤动脉为小脑上动脉(图2e),在第二间隙使用跨血管动脉瘤夹夹闭动脉瘤,可见瘤体完全夹闭,大脑后动脉及小脑上动脉保留完好。术后复查CT示鞍上偏左见金属动脉瘤夹影,动脉瘤夹闭完全(图2f),CT三维重建示骨瓣复位完全(图2g)。术后予止血、抗感染、脱水、营养神经等治疗,行蛛网膜下腔持续引流清除蛛网膜下腔出血。术后第2天患者偶有饮水呛咳,出院后缓解。出院时患者意识清醒,双侧瞳孔等大等圆,对光反射灵敏;右下肢肌力为Ⅳ级,其余肢体肌力Ⅴ级,肌张力不高;双侧生理反射存在,病理征阴性。术后6个月门诊随访,患者右下肢肌力肌张力恢复正常,GOS评分5分;CTA随访未见动脉瘤复发。
典型病例3女,46岁,主因“头晕头痛4 d”于2015年12月8日就诊于苏州大学附属第一医院神经外科。患者既往高血压病10余年,口服复方利血平氨苯蝶啶控制。入院时体格检查:意识清楚,言语正常,对答切题;双侧瞳孔等大等圆,瞳孔直径2.5 mm,对光反射灵敏,眼球活动可;伸舌居中;颈软无抵抗;四肢肌力正常,肌张力不高;双侧生理反射存在,病理征未引出;Hunt-Hess分级 Ⅲ 级。患者于入院前4 d突发头痛伴头晕,逐渐加重,有恶心呕吐,无抽搐,无大小便失禁。急查头部CT见鞍上池高密度影,示蛛网膜下腔出血(图3a);CTA三维重建示基底动脉顶端动脉瘤(图3b)。动脉瘤直径8.39 mm,瘤颈宽径4.87 mm,瘤顶指向前方,瘤颈高于后床突5.83 mm(图3c),动脉瘤两侧大脑后动脉分叉呈“Y”型,分叉角为160.60°(图3d)。
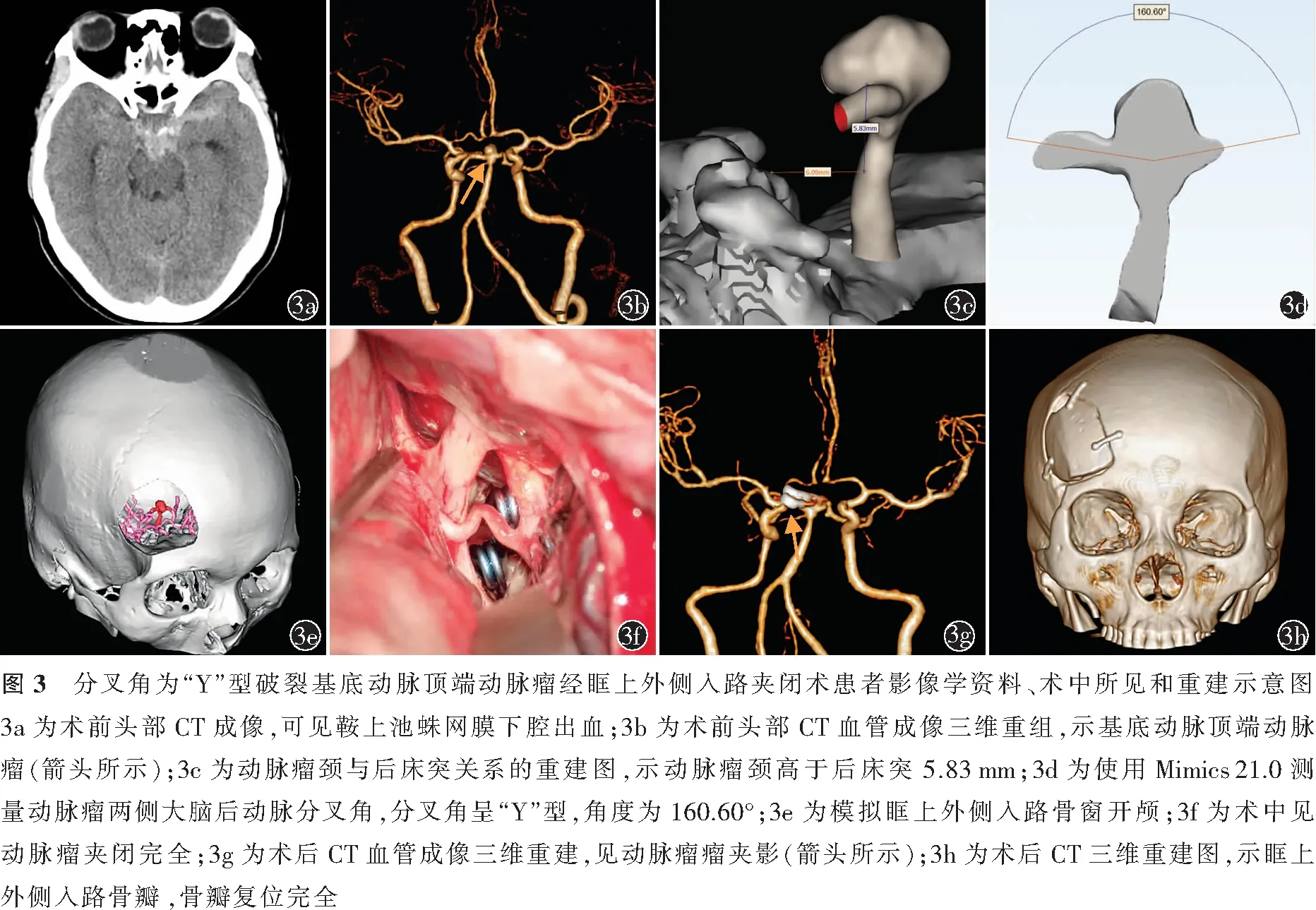
入院后予止血、抗血管痉挛、抗凝、降血压等对症治疗,于2015年12月10日行右侧眶上外侧入路动脉瘤夹闭术,模拟眶上外侧入路骨窗开颅(图3e)。显微镜下打开额底池、视交叉池、颈内动脉周围池、终板池,释放出血性脑脊液,颅内压下降。打开侧裂,抬起额叶,充分暴露出第二间隙,清除鞍上池血肿,沿第二间隙分离出动脉瘤体,载瘤动脉为基底动脉,在第二间隙使用动脉瘤夹(德国贝朗公司,蛇牌,型号750)夹闭动脉瘤,可见瘤体大部分夹闭,动脉瘤颈远端稍有残留,再用动脉瘤夹(德国贝朗公司,蛇牌,型号742)夹闭残留动脉瘤(图3f)。术后复查CTA三维重建见动脉瘤瘤夹影(图3g),CT三维重建示骨瓣完整复位(图3h)。术后给予止血、脱水、抗感染、抗脑血管痉挛的治疗,住院期间未见明显术后并发症。出院时患者双侧瞳孔等大等圆,对光反射灵敏;伸舌居中;四肢肌力Ⅴ级,肌张力正常;双侧生理反射存在,病理征未引出。术后6个月电话随访,患者恢复良好,GOS评分5分。
3 讨论
后循环动脉瘤破裂出血的风险为 50%,每年动脉瘤破裂出血发生率约为10%,2年内病死率高达60%[11]。后循环动脉瘤中以基底动脉顶端最多见,占50%,其次为小脑后下动脉、大脑后动脉及小脑上动脉[12]。目前后循环动脉瘤的治疗手段主要是血管内治疗和开颅动脉瘤夹闭术。随着神经介入技术的发展,介入治疗已经成为治疗后循环动脉瘤的主要治疗方式[13]。介入治疗较手术治疗更为简单,医师学习曲线短及成功率高,患者神经功能损伤小,恢复周期短[14-15],但其不适用于巨大、宽颈动脉瘤及有穿通支血管从瘤颈发出或从大脑后动脉发出的动脉瘤[16-17]。基底动脉顶端动脉瘤由于瘤壁直接受到血流冲击,复发倾向高[18]。支架的使用在降低动脉瘤复发率的同时,也增强了血流重塑,促进动脉瘤血栓形成,诱导动脉瘤颈内皮化,降低血管再通率[19]。此外,支架的使用也会带来如穿支血管梗死、术后需长期服用抗血小板聚集药物等问题[20]。在闭塞程度上,手术夹闭明显优于血管内治疗。有研究结果表明,动脉瘤的闭塞程度可以预测后期动脉瘤破裂风险,因此早期完全夹闭动脉瘤,可改善患者预后,减少患者随访频率和治疗费用[21]。
后循环动脉瘤腹侧为枕骨斜坡和蝶骨鞍背,背侧为脑干腹侧部,手术视野狭小,主要利用动脉瘤外侧的间隙,轻度牵拉脑组织以产生相对较大的操作空间,从而完成动脉瘤夹闭术[11]。术中对丘脑穿支动脉的显露十分重要,这些关键的穿支血管起自大脑后动脉P1段及后交通动脉,动眼神经与这一区域解剖关系密切。在眶上外侧入路得到推广前,常用于治疗基底动脉顶端动脉瘤的手术入路包括颞下入路和翼点入路。颞下入路最早由Drake[22]提出,其优点是手术路径短,术中操作空间更大,更易显露瘤顶指向后方或后下方的动脉瘤,适用于瘤颈平行或低于后床突的动脉瘤。但该入路难以观察对侧大脑后动脉P1段,并且对颞叶的牵拉较大,易出现颞叶挫伤和Labbe静脉的损伤,在优势半球可造成术后暂时性语言功能障碍[23-25]。Yasargil等[26]推广翼点入路治疗基底动脉顶端动脉瘤。这种方法能更好地显露对侧大脑后动脉P1段及其穿支血管,并减少对颞叶的牵拉损伤,合并前循环动脉瘤时还可以同时夹闭前循环动脉瘤;但前、后床突的存在影响对瘤体的直视,也增加了显露动脉瘤体背侧丘脑穿支的难度,因此只适用于后床突以上且瘤顶朝上的动脉瘤;第二、三间隙虽然可作为自然间隙进行手术操作,但空间狭小,对颈内动脉、视神经及动眼神经牵拉较大[27-28]。
眶上外侧入路最早由Hernesniemi等[5]提出,是对翼点入路的改良方案,其较传统翼点入路更靠前,对鞍区、鞍上、前交通动脉区域的暴露较好,对脚间池暴露较差,通过第二间隙为鞍区提供了较为良好的手术视野。因此,眶上外侧入路不仅适用于鞍区和鞍上区的颅内病变,也适用于鞍后区如基底动脉上部和椎间窝的颅内病变。在动脉瘤的手术方案中,眶上外侧入路主要用于前循环动脉瘤的夹闭,而经眶上外侧入路治疗后循环动脉瘤却开展甚少,我们也认为,并非所有的后循环动脉瘤均适合眶上外侧入路,一些瘤颈低于后床突的动脉瘤难以通过该入路开展。本组7例患者动脉瘤均位于鞍后,瘤颈高于后床突0.34~15.30 mm,且基底动脉顶端动脉瘤的瘤顶朝向前或前上方,采用眶上外侧入路可以从前方直视瘤颈予以夹闭。Tjahjadi等[9]认为,基底动脉顶端动脉瘤两侧大脑后动脉分叉角较大的动脉瘤患者更适用于眶上外侧入路,但并未给出具体的分叉角数值或范围。本组病例中,分叉角度为140°~180°,所有基底动脉顶端动脉瘤完全夹闭。我们认为,分叉角在140°以上对夹闭动脉瘤无影响,但由于样本量的局限,我们不能统计出动脉瘤能够夹闭的分叉角最小值。夹闭高于后床突的后循环动脉瘤时需要适度地抬起额叶,目前能够完全夹闭的动脉瘤瘤颈高出后床突的最大值为15.30 mm,若高度过高则需要过度抬举额叶,可能会加大额叶挫伤的风险。术后并发症中,3例出现动眼神经麻痹导致的上睑下垂和复视症状,可能的原因包括:(1)术中牵拉或刺激到动眼神经;(2)蛛网膜下腔出血后血性脑脊液刺激。基底动脉顶端与动眼神经解剖学关系密切,动眼神经走行于大脑后动脉和小脑上动脉之间,因而分离动脉瘤时要注意保护动眼神经。王红光等[2]认为,动眼神经损伤的主要原因可能为神经表面滋养的微血管撕裂造成缺血性损伤。因此动脉瘤夹闭术中应避免钝性分离,自脑组织侧锐性剪开动眼神经周围的柱状蛛网膜及组织。本组1例患者术后复查CT示双侧基底节区梗死灶,该患者术后有言语功能及肢体活动障碍,四肢肌力下降,考虑可能术中牵拉或误夹细小的穿支动脉导致术后出现脑血管痉挛,继而出现穿支动脉供血区域梗死。
眶上外侧入路作为对翼点入路的改进,在治疗后循环动脉瘤方面有其独特优势:(1)开颅时间短,对出血较严重的患者可很快开颅到达血肿部位;减少开颅相关并发症如脑脊液漏、硬膜外血肿和感染等的发生风险[29]。(2)手术切口相较翼点入路更短,一般在发际后,仅需切开较少的颞肌,对患者的外观影响小。(3)骨瓣小,一般无需放置硬膜外引流管,术后恢复较快,减少患者的住院费用。但眶上外侧入路也有其局限性:(1)由于后床突的限制,动脉瘤瘤颈若低于后床突则无法从前方直视,使用该入路有夹闭不完全或误夹的风险;(2)对基底动脉背侧区域的显露有限,若瘤顶朝向后方则会给夹闭带来困难;(3)眶上外侧入路的操作和可视范围相较翼点入路窄,一旦发生术中动脉瘤破裂等意外情况,局限的视野可能会影响操作。因此,开展眶上外侧入路夹闭后循环动脉瘤对术者的经验和操作要求较高。术前需影像学检查明确动脉瘤位置,结合患者情况综合判断是否适合该入路,我们的经验是:对于Hunt-Hess分级为Ⅰ~Ⅲ级,及有动脉瘤破裂蛛网膜下腔出血的患者,尽早行手术治疗。颅内动脉瘤破裂出血后14 d内为再出血的危险期,早期手术清理血肿不仅可降低脑血管痉挛发生的风险,还可以尽可能规避再出血的发生。Hunt-Hess分级Ⅳ、Ⅴ级患者可能伴有脑水肿或较重的脑血管痉挛,自身对手术的耐受程度差。此外,眶上外侧入路的骨瓣小不足以去骨瓣减压[30],因此Hunt-Hess分级Ⅳ、Ⅴ级患者不宜使用眶上外侧入路。对于动脉瘤瘤颈高于后床突且瘤顶朝前或前上的患者可优先考虑此入路。在手术过程中抬起额叶时要注意对额叶的牵拉,必要时可打开侧裂扩大视野以充分暴露瘤颈及动脉瘤与两侧大脑后动脉的关系,术中注意保护载瘤动脉和穿支动脉,避免损伤到周围的神经。若术中需使用临时阻断夹,需要控制好临时阻断的时间,避免夹闭时间过长而引起深部穿支动脉区梗死。夹闭后应用经颅多普勒超声或FLOW 800监测两侧大脑后动脉的血流是否通畅,避免误夹或夹闭不全。夹闭过程尽可能一次到位,避免反复夹闭血管,夹闭动作轻柔缓慢,避免剪切力过大导致瘤颈撕裂。
在对后循环动脉瘤的治疗上,眶上外侧入路开颅速度快、创伤小、术后恢复快,但其适用范围也较为局限,因此,入路的选择并无绝对优劣,神经外科医师仍然需要根据患者情况、动脉瘤位置以及术者自身手术操作水平选择最佳的入路方式。
