时间限制性饮食改善模拟失重下大鼠心脏谷氨酰胺代谢和心脏功能
2022-08-02王馨佩周嘉恒胡旭晖李沛凌刘美杰张佳欣王盼盼
许 可,王馨佩,安 冏,周嘉恒,胡旭晖,李沛凌,刘美杰,张佳欣,王盼盼,张 星,李 嘉
(空军军医大学: 1航空航天医学系康复与疗养教研室, 2基础医学院学员三大队,陕西 西安 710032)
我国空间站建造规划显示,我国将在未来两年内建成以核心舱为控制中心,问天、梦天实验舱为主要实验平台的常年有人照料的空间站。届时,我国航天员在轨飞行时间将会大幅增长,研究长期失重环境对航天员的影响及防护显得愈加紧迫和重要。已有研究表明,失重或模拟失重会导致机体心功能下降、心肌萎缩和立位耐力下降等一系列心血管系统的变化,严重危害航天员健康[1-2]。但是,目前失重所致心血管结构和功能改变的具体机制仍未完全阐明,针对失重所致心血管功能紊乱的防护措施的效果也十分有限。
心脏是高耗能器官,其能量代谢对心脏的结构和功能至关重要[3-5]。已有研究表明,在航天飞行和地面模拟失重(卧床试验)期间,航天员/受试者的血糖、血脂和胰岛素浓度水平均发生了显著变化[6]。我们课题组前期研究发现,模拟失重可显著降低大鼠心肌葡萄糖的摄取和氧化磷酸化,影响心脏的能量代谢[7]。谷氨酰胺(glutamine,Gln)是人体含量最丰富的非必需氨基酸和重要的氮运载体,在机体内参与能量代谢、抗氧化和细胞内信号转导等重要过程,但是Gln在心脏中的代谢特点及模拟失重对其的影响尚不清楚。已有研究表明,时间限制性进食(time-restricted feeding,TRF)是一种不减少或几乎不减少热量摄入,但将每日进食时间限制在4~12 h的饮食限制方法,可显著改善机体的能量代谢[8-10]。本实验旨在研究探讨模拟失重对心脏Gln代谢的影响及TRF对其的改善作用。
1 材料与方法
1.1 材料
健康雄性成年Sprague-Dawley 大鼠由空军军医大学实验动物中心提供。TRIzol试剂盒购自Thermal Fisher公司;PrimeScript RT Master Mix和SYBR Green PCR试剂购自Takara公司;BCA蛋白测定试剂盒购自碧云天公司;anti-GAPDH和anti-GLUD1购自Cell Signaling Technology公司, anti-GLS1购自Abcam公司;M199购自Sigma公司;fluo-4购自Invitrogen公司;Ⅰ型胶原酶购自Gibco公司。
1.2 方法
1.2.1 大鼠模拟失重模型的建立 18只大鼠,体质量(200±20)g,随机分为对照组、尾部悬吊(hindlimb uploading,HU)组和HU+TRF组,每组6只。HU和HU+TRF组按本实验室已建立的方法进行动物饲养与尾部悬吊[11],尾吊4周。在整个实验期间,将大鼠置于12 h光照/12 h黑暗循环(开灯时间在6∶00 am,ZT0;关灯时间在6∶00 pm,ZT12)。对照组和HU组每日不限进食时间,HU+TRF组每日进食时间限制在ZT13至ZT21这8 h之间。3组大鼠在整个实验期间自由获取饮水。为排除进食量的影响,每组大鼠按照数量给予相同食量。
1.2.2 心脏功能评估 HU 4周后,在超声(VisualSonics VeVo770)下检测大鼠左室射血分数(ejection fraction,EF)和缩短分数(fractional shortening,FS)。
1.2.3 Gln代谢物质检测 心肌组织中Gln、谷氨酸及α-KG物质浓度由中国药科大学药物质量控制与药物警戒重点实验室采用液相色谱串联质谱测定[12]。
1.2.4 Western blotting检测 将组织剪碎后加入裂解液匀浆,12 000 r/min 4 ℃离心20 min。用BCA蛋白测定总蛋白浓度。将样品进行SDS-PAGE电泳并转膜至PVDF膜后进行一抗孵育4 ℃过夜,洗涤后用辣根过氧化物酶标记的二抗孵育1 h,加入ECL混合物后用荧光显影技术发光成像。
1.2.5 定量PCR 往组织中加入TRIzol试剂,再按照5∶1体积比加入氯仿离心,得到上清液后加入异丙醇得到RNA。750 mL/L乙醇处理后加DEPC获得RNA样本。反转录获得cDNA,以此为模板使用SYBR Green PCR试剂盒在Bio-Rad PCR仪器上进行扩增。使用引物序列如下。
β-actin, forward:TCGTGCGTGACATTAAAGAG,
reverse:ATTGCCGATAGTGATGACCT;
Slc1a5, forward:ATATGTTCCCCTCCAATCTGGTGTC,
reverse:GCATCATTGAAGGAGTTG;
Slc7a5, forward:CCTACGGAGGATGGAACTATCTGA,
reverse:TGGGCAAGGAGATGATGATG。
1.2.6 成年大鼠心肌细胞的分离与心肌细胞收缩功能的测量 大鼠腹腔注射肝素(1 000 IU/kg),10 min后腹腔注射戊巴比妥钠(200 mg/kg),开胸迅速摘取心脏,依照本实验室已建立的方法,行主动脉逆行插管,将心脏悬挂于Langendorff灌流装置中,37 ℃恒温灌流心脏,用含1 g/L胶原酶消化分离出单个心室肌细胞[7]。将新鲜分离出的心肌细胞在预孵育过层粘连蛋白的培养皿上贴壁1 h,然后将附着的细胞在M199培养基中培养。将分离的成年大鼠心肌细胞按照是否添加α-酮戊二酸(α-ketoglutaric acid, α-KG)(4 mmol/L,2 h)的处理分为空白组和α-KG组。通过一对铂电极使用场刺激引发心肌细胞收缩,方波刺激,波宽5 ms,刺激电压10 V,刺激频率1.0 Hz,灌流速度为3 mL/min。通过fluo-4 (5 μmol/L)对细胞内Ca2+染色,在共聚焦显微镜下,通过不断扫描预先选定的细胞长轴检测细胞缩短幅值(收缩幅度/静息长度)和胞质Ca2+瞬变幅度(ΔF/F0),激发波长488 nm,接收波长500 nm。
2 结果
2.1 TRF改善模拟失重下大鼠心脏功能
与对照组相比,HU组大鼠心脏收缩功能降低,表现为EF和FS均显著降低;TRF可显著增加模拟失重大鼠心脏的EF和FS,改善心脏收缩功能(图1)。
2.2 TRF改善模拟失重下大鼠心肌Gln代谢
与对照组相比,HU大鼠心肌中Gln和谷氨酸含量显著增加,而α-KG含量显著降低;TRF则减少了HU大鼠心肌中Gln和谷氨酸的堆积,增加了α-KG的含量(图2)。

HU:尾部悬吊;HU+TRF:尾部悬吊+时间限制性饮食干预。 aP<0.05, bP<0.01。图1 小动物超声测量大鼠心脏功能指标
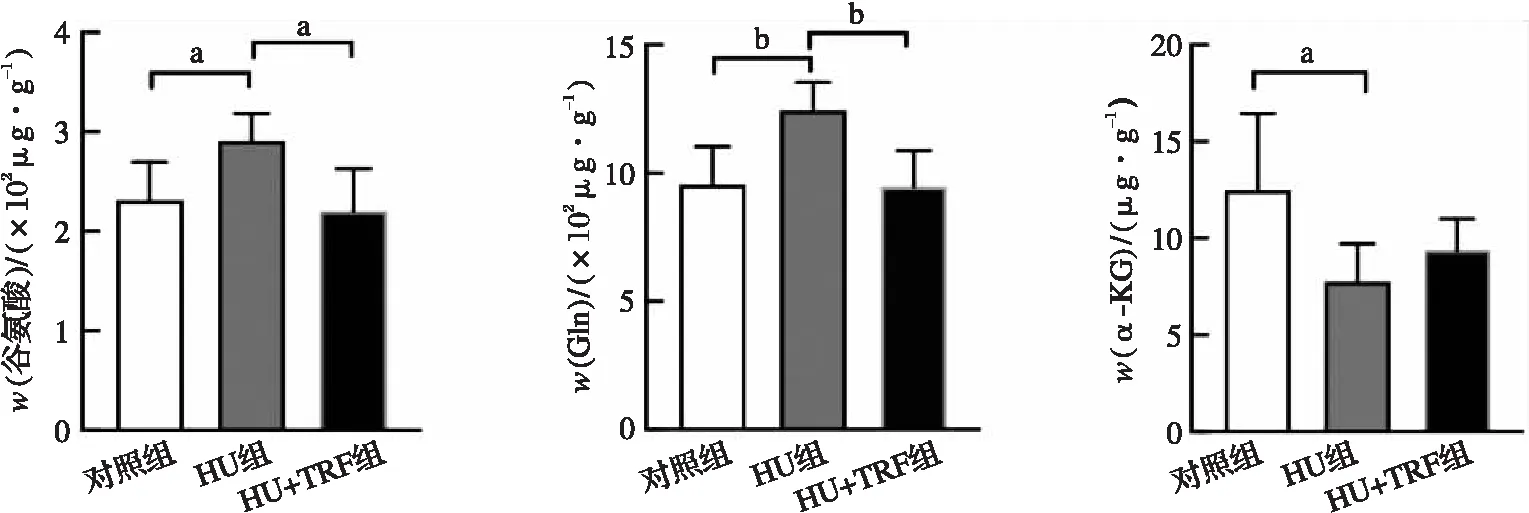
HU:尾部悬吊;HU+TRF:尾部悬吊+时间限制性饮食干预;α-KG: α-酮戊二酸;Gln:谷氨酰胺。 aP<0.05, bP<0.01。图2 各组大鼠心肌和血浆中Gln代谢物质的含量
2.3 TRF增加模拟失重下大鼠心肌谷氨酸脱氢酶(glutamate dehydrogenase, GLUD1)的表达
与对照组相比,HU大鼠心肌中Gln转运体Slc1a5和Slc7a5的mRNA表达水平并未发生显著改变。我们进一步检测了Gln代谢关键酶谷氨酰胺酶(glutaminase, GLS1)和GLUD1的表达,发现与对照组相比,HU大鼠心肌中GLS1蛋白表达未发生明显变化,但GLUD1的表达显著降低;TRF则可显著增加HU大鼠心肌中GLUD1的表达。这些结果表明,模拟失重可降低心肌组织中GLUD1表达,导致心肌组织中Gln和谷氨酸的累积而α-KG含量降低;TRF通过上调GLUD1的表达改善心肌组织中Gln的代谢(图3)。

HU:尾部悬吊;HU+TRF:尾部悬吊+时间限制性饮食干预;GLUD1:谷氨酸脱氢酶;GLS1:谷氨酰胺酶。aP<0.05; bP<0.01。图3 各组大鼠心肌中Gln代谢关键酶的表达
2.4 补充α-KG改善模拟失重下大鼠心肌细胞的收缩功能
为进一步探究Gln代谢与模拟失重大鼠心脏功能下降的关系,我们分离了HU 组大鼠心肌细胞,在1 Hz电场刺激下,通过fluo-3 染色在共聚焦线扫描模式下检测心肌细胞Ca2+浓度和心肌细胞收缩功能。结果显示,与空白组相比,补充α-KG可显著增加HU大鼠心肌细胞缩短幅值和Ca2+瞬变幅度,提示模拟失重可抑制心肌Gln代谢导致α-KG减少(图4),这可能是HU大鼠心脏功能降低的原因之一。

α-KG:α-酮戊二酸。 aP<0.05。图4 补充α-KG对模拟失重大鼠心肌细胞收缩功能的影响
3 讨论
对抗失重所致心血管系统改变的措施主要包括运动锻炼、着“企鹅服”、下体负压、补充液体、药物以及飞行前的适应性训练等[13]。然而,在上述防护措施的情况下,航天员在轨飞行时的峰值运动能力仍然降低[14-15]。此外,航天飞行过程中有时运动锻炼并不可行,例如在NASA双胞胎实验过程中,航天员斯科特·凯利由于受伤在任务的后半段运动量显著减少[16]。因此,寻找其他航天飞行防护对策十分重要。
TRF作为间歇性禁食的一种形式,不仅可以预防心血管疾病[17],治疗代谢性疾病,还可以提高健康水平。CHAIX等[18]研究表明TRF可以对抗高脂高糖饮食对机体的不良影响,包括改善小鼠胰岛素敏感性、防治肥胖和2型糖尿病的发生发展。TRF对于2型糖尿病患者和糖尿病前期受试者同样具有有益影响[19]。此外,TRF还被认为可以促进心血管健康,一项发表在Science杂志的研究表明,TRF可以有效改善衰老和高脂饮食诱导的果蝇心功能降低[20]。本研究表明,模拟失重可使大鼠心脏功能降低,而TRF可有效改善模拟失重大鼠的心脏功能,主要因为模拟失重会引起全身多器官组织代谢发生改变,如全身胰岛素样改变、白细胞糖酵解增加等。我们课题组前期的研究表明,TRF作为一种代谢性疾病的有效治疗方法,能有效改善HU大鼠糖代谢[7]。本研究还发现了HU大鼠Gln代谢异常,而TRF改善Gln的代谢也可能是TRF改善心脏功能的原因之一。
本研究表明模拟失重可显著降低GLUD1的表达,从而引起Gln代谢中Gln、谷氨酸的堆积以及α-KG的减少。我们在离体实验中发现,补充α-KG可增加模拟失重大鼠单个心肌细胞的收缩能力;在体实验表明,TRF可增加GLUD1的表达促进心肌Gln代谢,从而增加心肌组织中α-KG水平,有助于改善模拟失重大鼠的心脏功能,同时发现与对照组相比,TRF不能使HU大鼠心肌中GLS1蛋白表达发生明显变化,主要可能为GLS1在增殖的细胞中产生较为明显变化[21],如肿瘤细胞和内皮细胞等,而心肌细胞并非增殖细胞,因此在本研究中,HU并未对GLS1有明显的改变。
综上所述,本研究结果首次表明,模拟失重可抑制大鼠心脏Gln分解代谢,导致心脏功能下降;而TRF可促进心脏Gln分解代谢,改善模拟失重下大鼠心脏功能,为航天飞行心脏保护提供了新思路。
