栀子饮片及栀子配方颗粒的指纹图谱建立、含量测定及化学模式识别Δ
2022-07-29梁朝锋韩晓珂秦亚东周娟娟芜湖市中医医院药检室安徽芜湖4000安徽中医药高等专科学校药学系安徽芜湖400
梁朝锋,韩晓珂,秦亚东,徐 斌,祁 俊,周娟娟(.芜湖市中医医院药检室,安徽 芜湖 4000;.安徽中医药高等专科学校药学系,安徽芜湖 400)
栀子为茜草科植物栀子Gardenia jasminoidesEllis的干燥成熟果实,主要分布于我国长江以南地区,具有泻火除烦、凉血解毒、清热利湿等功效[1]。该药最早见于《神农本草经》,是我国卫生部首批颁布的药食两用资源,应用广泛[2-3]。现代研究表明,栀子主要含有环烯醚萜类[如去乙酰车叶草酸甲酯(deacetyl asperulosidic acid methylester,DAAME)、栀子苷等]、萜类(如西红花苷Ⅰ、西红花苷Ⅱ、苦番红花素等)、黄酮类(如芦丁等)、三萜类等成分[4],具有抗炎、调节免疫、抗氧化、治疗心血管系统疾病等药理作用[5-6]。目前,2020年版《中国药典》(一部)栀子“含量测定”项仅以栀子苷为指标性成分[1],但由于栀子成分复杂,因此对单一指标进行定量分析无法全面控制栀子的质量。
栀子配方颗粒是将栀子饮片经提取、浓缩制成的供临床用的颗粒剂,是栀子饮片的新形式。与原饮片相比,栀子配方颗粒具有免煎煮、方便携带、便于调剂和存储等优点,且成分同样复杂[7]。国家药典委员会于2021年颁布了栀子配方颗粒的质量标准,亦仅以栀子苷含量作为评价指标[8],难以全面控制其质量。笔者通过查阅文献可知,现有相关研究主要集中在栀子及其炮制品的质量评价方面[9-10],对栀子配方颗粒的评价甚少。指纹图谱是一种可量化的综合性鉴定手段,能全面反映中药中化学成分的内在特征[11-12]。化学模式识别可对多种现代仪器检测所得数据进行识别与处理,能更加客观地反映中药的质量信息,现已在中药质量研究领域得到广泛应用[13]。基于此,本研究采用高效液相色谱(high performance liquid chromatography,HPLC)法建立了栀子饮片及栀子配方颗粒的指纹图谱,并同法测定了其中DAAME、栀子苷、苦番红花素、芦丁、西红花苷Ⅰ、西红花苷Ⅱ的含量;采用化学模式识别分析了影响栀子饮片与栀子配方颗粒质量的差异性成分,旨在为其质量控制提供参考。
1 材料
1.1 主要仪器
本研究所用主要仪器有1200 型HPLC 仪(美国Agilent 公司),AL204 型电子天平、XP205 型电子天平(瑞士Mettler Toledo公司),KQ-500DE型数控超声波清洗器(昆山市超声仪器有限公司),HHW-4型数显恒温水浴锅(常州金坛双捷实验仪器厂),QE-100型多功能粉碎机(浙江屹立工贸有限公司)等。
1.2 主要药品与试剂
DAAME对照品(批号111786-201602,纯度94.3%)、栀子苷对照品(批号110749-201919,纯度97.1%)、苦番红花素对照品(批号112056-202001,纯度97.6%)、西红花苷Ⅰ对照品(批号111588-201704,纯度88.4%)、西红花苷Ⅱ对照品(批号111589-201705,纯度92.2%)均购自中国食品药品检定研究院;芦丁对照品(批号Yz112820,纯度≥98%)购自南京源植生物科技有限公司;乙腈、甲醇、甲酸、磷酸均为色谱纯,甲醇、乙醇均为分析纯,水为超纯水。
20批栀子饮片(编号S1~S20)于2020年6月-2021年7月分别购自安徽省芜湖市、河南省郑州市各药店和芜湖市中医医院药剂科,经芜湖市中医医院药检室徐斌副主任中药师鉴定为茜草科植物栀子G.jasminoidesEllis的干燥成熟果实。10 批栀子配方颗粒(编号PF1~PF10,每1.0 g相当于饮片10 g)于2020年6月-2021年3 月购自广东一方制药有限公司。20 批栀子饮片及10批栀子配方颗粒的来源信息见表1。
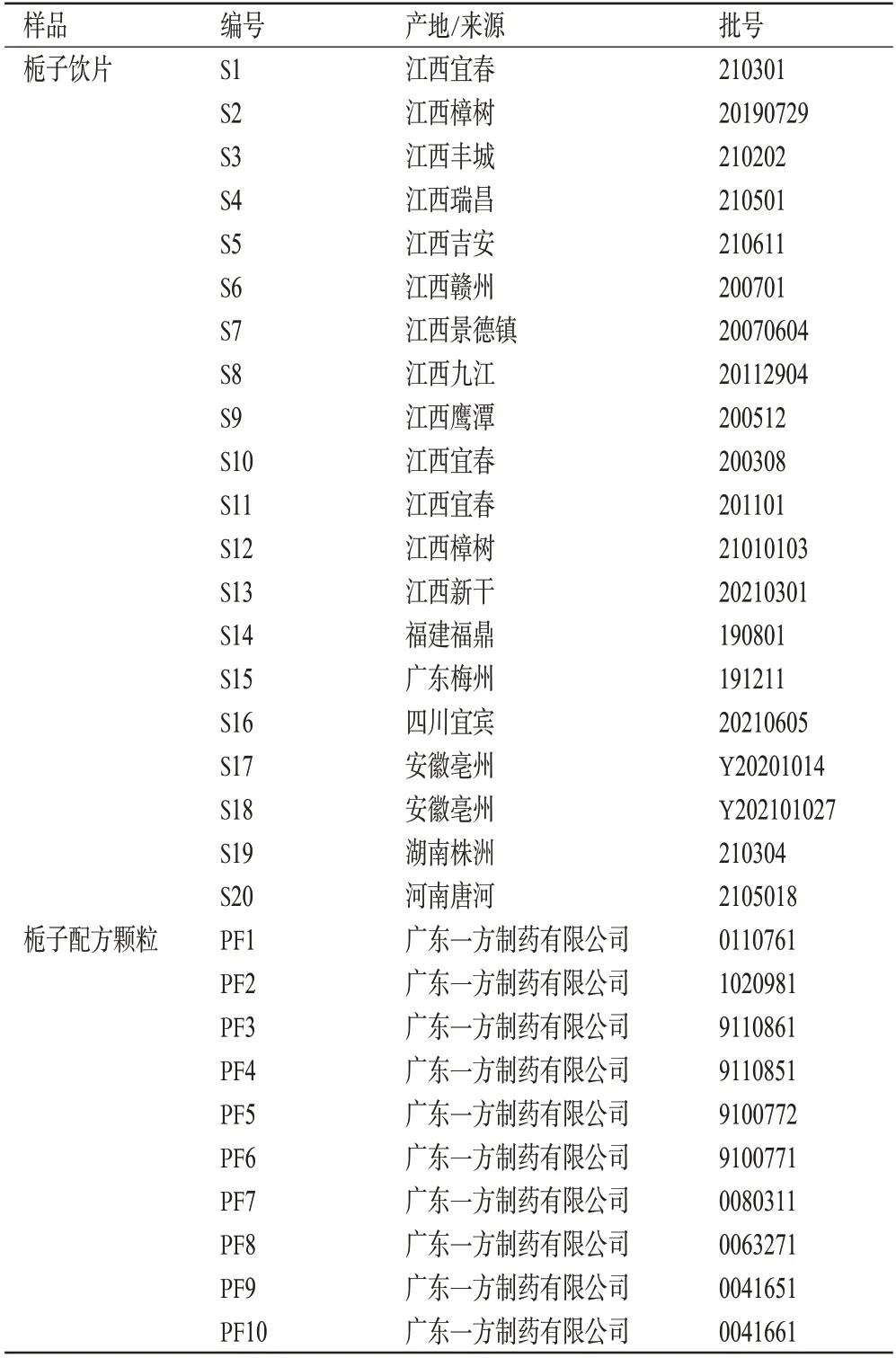
表1 20批栀子饮片及10批栀子配方颗粒的来源信息
2 方法与结果
2.1 色谱条件
以Agilent ZORBAX-SB C18(250 mm×4.6 mm,5µm)为色谱柱,以乙腈(A)-0.1%甲酸溶液(B)为流动相进行梯度洗脱(0~9 min,7%A→12%A;9~16 min,12%A→19%A;16~25 min,19%A→23%A;25~30 min,23%A;30~35 min,23%A→30%A;35~50 min,30%A→37%A;50~60 min,37%A→58%A);检测波长为238 nm(DAAME、栀子苷、苦番红花素、芦丁)、440 nm(西红花苷Ⅰ、西红花苷Ⅱ);柱温为30 ℃;流速为1.0 mL/min;进样量为10 μL。
2.2 混合对照品溶液的制备
分别取DAAME、栀子苷、苦番红花素、芦丁、西红花苷Ⅰ、西红花苷Ⅱ对照品适量,精密称定,加甲醇溶解,制成DAAME、栀子苷、苦番红花素、芦丁质量浓度分别为73.30、610.80、44.60、41.70 μg/mL和西红花苷Ⅰ、西红花苷Ⅱ质量浓度分别为148.90、20.03 μg/mL的2种混合对照品溶液。
2.3 供试品溶液的制备
取样品[栀子饮片粉末(过40 目筛)约0.2 g 或栀子配方颗粒(研细)约0.05 g],精密称定,置于具塞锥形瓶中,加70%甲醇25 mL,称定质量,超声(功率350 W、频率40 kHz)提取30 min,冷却至室温,再次称定质量,用70%甲醇补足减失的质量,摇匀,经0.22 μm微孔滤膜滤过,即得。
2.4 HPLC指纹图谱的建立
2.4.1 精密度试验 取“2.3”项下供试品溶液(编号S1),按“2.1”项下色谱条件进样测定6次,以栀子苷(6号峰)为参照峰,计算各共有峰的相对保留时间和相对峰面积。结果显示,各共有峰相对保留时间和相对峰面积的RSD均小于2.8%(n=6),表明方法精密度良好。
2.4.2 稳定性试验 取“2.3”项下供试品溶液(编号S1),分别于室温下放置0、2、4、6、8、10 h时按“2.1”项下色谱条件进样测定,以栀子苷(6号峰)为参照峰,计算各共有峰的相对保留时间和相对峰面积。结果显示,各共有峰相对保留时间和相对峰面积的RSD 均小于3.5%(n=6),表明供试品溶液于室温下放置10 h 内稳定性良好。
2.4.3 重复性试验 取样品(编号S1),共6 份,按“2.3”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,以栀子苷(6号峰)为参照峰,计算各共有峰的相对保留时间和相对峰面积。结果显示,各共有峰相对保留时间和相对峰面积的RSD 均小于3.0%(n=6),表明方法重复性良好。
2.4.4 指纹图谱的生成 取20批栀子饮片及10批栀子配方颗粒,按“2.3”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,将所得色谱数据导入《中药色谱指纹图谱相似度评价系统(2012版)》,分别以S1、PF1(色谱信息丰富且各色谱峰峰面积适中)为参照,采用中位数法生成对照图谱(S1为R1、PF1为R2),设置时间窗宽度为0.1,经多点校正后自动匹配,得到栀子饮片及栀子配方颗粒的HPLC叠加指纹图谱。结果显示,20批栀子饮片及10批栀子配方颗粒的叠加指纹图谱中均有24个共有峰,详见图1、图2。以S1 为参照,采用中位数法生成对照图谱(R3),得到栀子饮片及栀子配方颗粒的叠加指纹图谱。结果显示,30批样品的叠加指纹图谱中共有22个共有峰,详见图3。

图1 20批栀子饮片的HPLC叠加指纹图谱及对照图谱
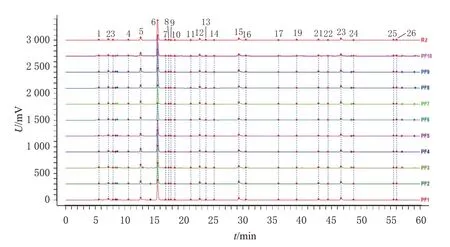
图2 10 批栀子配方颗粒的HPLC 叠加指纹图谱及对照图谱

图3 30批样品的HPLC叠加指纹图谱及对照图谱
2.4.5 共有峰指认 取“2.2”项下DAAME、栀子苷、苦番红花素、芦丁混合对照品溶液4 mL,西红花苷Ⅰ、西红花苷Ⅱ混合对照品溶液1 mL,置于10 mL 量瓶中,加70%甲醇定容,另取“2.3”项下供试品溶液,按“2.1”项下色谱条件进样测定,记录色谱图(图4)。通过与混合对照品对比,指认出2 号峰为DAAME、6 号峰为栀子苷、9号峰为苦番红花素、11号峰为芦丁、15号峰为西红花苷Ⅰ、17号峰为西红花苷Ⅱ。因6号峰响应最强,且该峰对应的成分栀子苷为2020年版《中国药典》(一部)中栀子的指标性成分,故以其为参照峰。
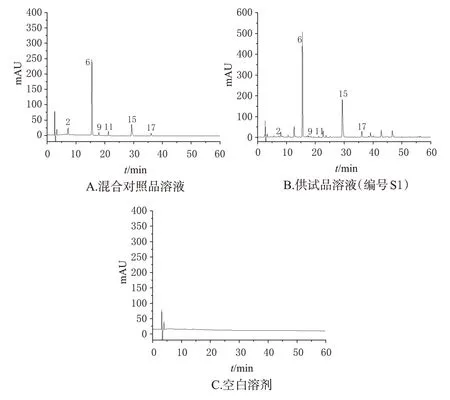
图4 DAAME等成分的混合对照品溶液、供试品溶液、空白溶剂的HPLC图
2.4.6 相似度评价 采用《中药色谱指纹图谱相似度评价系统(2012 版)》对20 批栀子饮片及10 批栀子配方颗粒进行相似度评价。结果显示,30 批样品与对照图谱(R3)的相似度均不低于0.96,表明不同产地栀子饮片与栀子配方颗粒间成分种类基本相同。结果见表2。

表2 30批样品的相似度评价结果
2.5 含量测定
2.5.1 系统适用性试验“取2.2”项下混合对照溶液及“2.3”项供试品溶液(按“2.4.5”项下方法处理)、空白溶剂(70%甲醇),按“2.1”项下色谱条件进样测定,记录色谱图,详见图4。由图4 可知,各色谱峰的分离度良好,空白溶剂对测定无干扰。
2.5.2 线性关系考察 精密吸取“2.2”项下DAAME、栀子苷、苦番红花素、芦丁混合对照品溶液0.5、2、4、6、8、10 mL,置于10 mL 量瓶中,加70%甲醇定容,得系列样品溶液Ⅰ;精密吸取西红花苷Ⅰ、西红花苷Ⅱ混合对照品溶液0.1、0.5、1、4、8、10 mL,置于10 mL 量瓶中,加70%甲醇定容,得系列样品溶液Ⅱ。取上述各溶液适量,按“2.1”项下色谱条件进样测定,记录峰面积。以各待测成分的质量浓度为横坐标(X)、峰面积为纵坐标(Y)进行线性回归。结果见表3。

表3 DAAME等成分的回归方程与线性范围
2.5.3 精密度试验 取“2.3”项下供试品溶液(编号S1),按“2.1”项下色谱条件进样测定6 次,记录峰面积。结果显示,DAAME、栀子苷、苦番红花素、芦丁、西红花苷Ⅰ、西红花苷Ⅱ峰面积的RSD 分别为2.85%、0.56%、0.98%、2.29%、0.20%、0.82%(n=6),表明方法精密度良好。
2.5.4 稳定性试验 取“2.3”项下供试品溶液(编号S1),分别于室温下放置0、2、4、6、8、10 h时按“2.1”项下色谱条件进样测定,记录峰面积。结果显示,DAAME、栀子苷、苦番红花素、芦丁、西红花苷Ⅰ、西红花苷Ⅱ峰面积的RSD 分别为0.95%、0.46%、2.29%、2.30%、0.27%、1.03%(n=6),表明供试品溶液于室温下放置10 h内稳定性良好。
2.5.5 重复性试验 取样品(编号S1),共6 份,按“2.3”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,记录峰面积并按外标法计算样品含量。结果显示,DAAME、栀子苷、苦番红花素、芦丁、西红花苷Ⅰ、西红花苷Ⅱ含量的RSD 分别为2.01%、0.90%、1.43%、1.28%、0.75%、0.85%(n=6),表明方法重复性良好。
2.5.6 加样回收率试验 精密称取DAAME、栀子苷、苦番红花素、芦丁、西红花苷Ⅰ、西红花苷Ⅱ对照品适量,加甲醇制成质量浓度分别为146.60、2 036.00、892.00、834.00、297.80、40.05 μg/mL 的单一对照品溶液。精密称取已知含量的样品(编号S1)粉末约0.1 g,共9 份,分别按已知含量的80%、100%、120%加入上述各单一对照品溶液,按“2.3”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,记录峰面积并计算加样回收率。结果显示,DAAME、栀子苷、苦番红花素、芦丁、西红花苷Ⅰ、西红花苷Ⅱ的平均加样回收率分别为100.83%(RSD=1.43%,n=9)、101.37%(RSD=1.62%,n=9)、99.50%(RSD=1.95%,n=9)、98.21%(RSD=1.35%,n=9)、99.96%(RSD=1.29%,n=9)、100.27%(RSD=1.47%,n=9),表明方法准确度良好。
2.5.7 样品含量测定 取20批栀子饮片及10批栀子配方颗粒各适量,按“2.3”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,记录峰面积并按外标法计算样品含量。每样品平行测定3次,结果见表4(栀子配方颗粒中6个成分含量已换算为饮片中含量)。
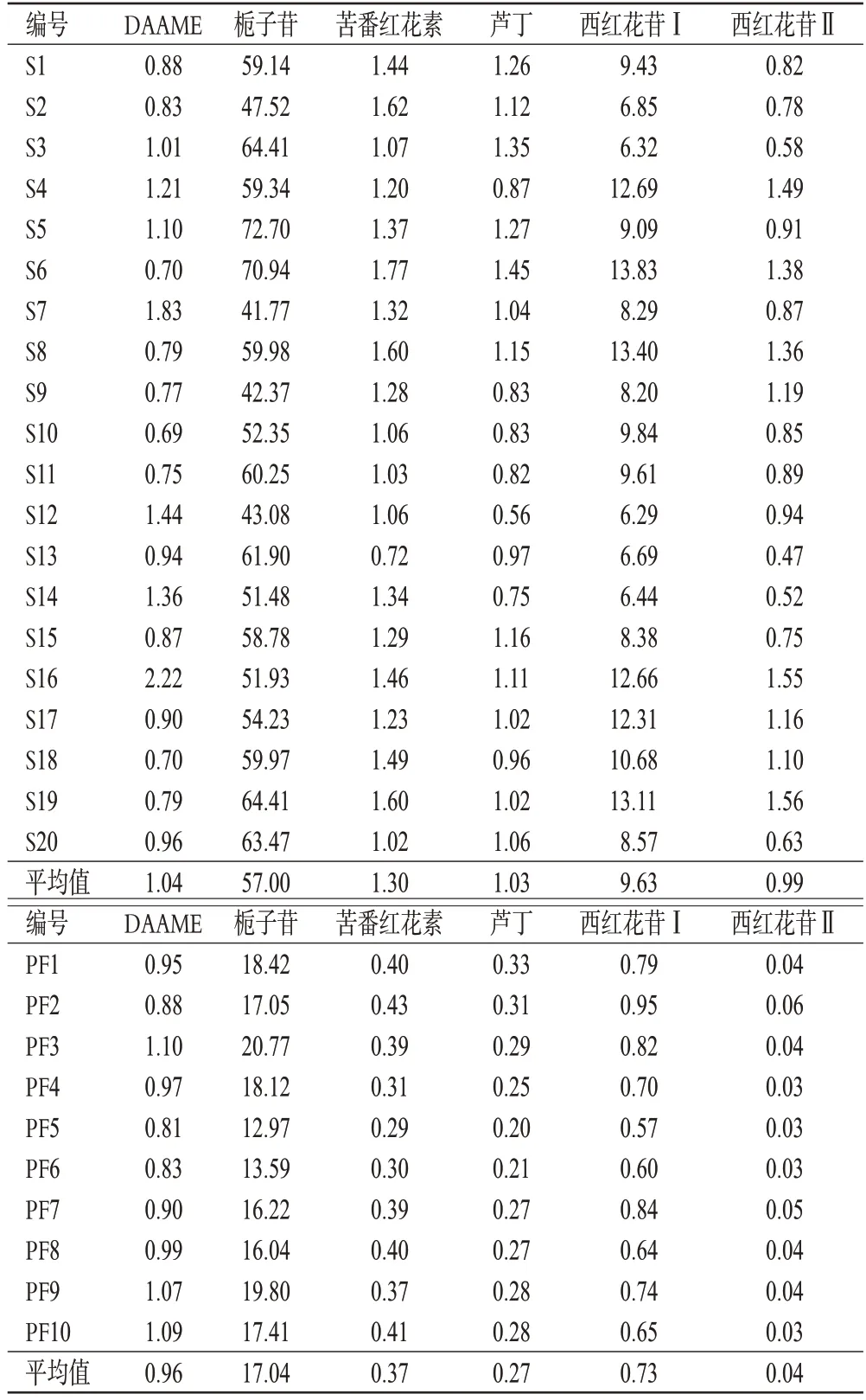
表4 DAAME等成分的含量测定结果(n=3,mg/g)
2.6 主成分分析
以30 批样品的22 个共有峰峰面积为变量构建30×22 数据矩阵,采用SIMCA 16.0 软件进行主成分分析。结果显示,20 批栀子饮片均分布于得分图的[t]1 正值象限,10批栀子配方颗粒均分布于得分图的[t]1负值象限;栀子配方颗粒聚集程度较高,栀子饮片聚集程度欠佳,如S4、S7、S12、S16 散在分布于得分图的[t]2 负值象限,表明不同样品中各成分的含量存在差异,这可能与栀子配方颗粒来自同一制药企业,而栀子饮片产地来源较广有关。结果见图5。
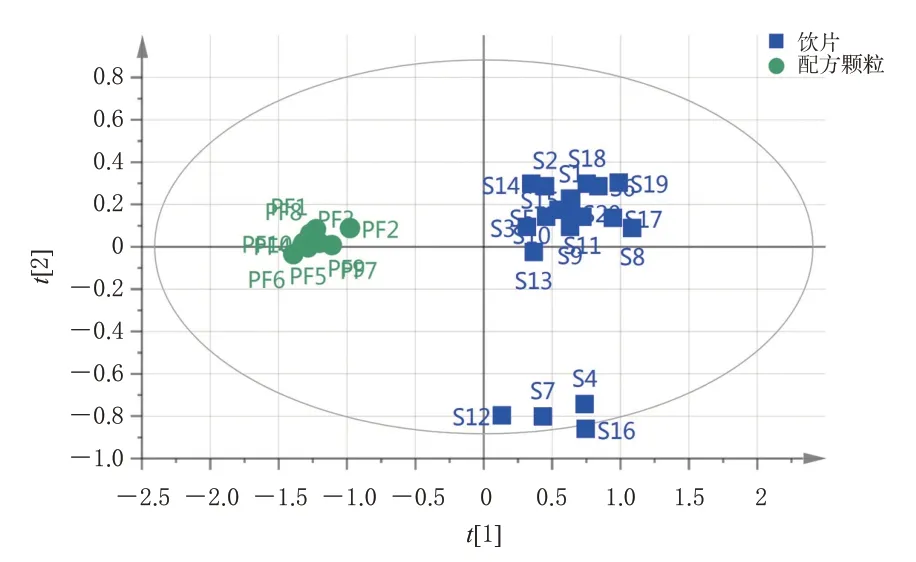
图5 30批样品的主成分分析得分图
2.7 聚类分析
以30 批样品的22 个共有峰峰面积为变量构建30×22 数据矩阵,以平方欧氏距离为测度,采用ORIGIN 9.1软件进行聚类分析。结果显示,当距离为1.25 时,30 批样品可聚为2类,其中S1~S20为一类,PF1~PF10为一类;当距离为0.75 时,30 批样品可聚为3 类,其中PF1~PF10 为一类,S4、S7、S12、S16 为一类,S1~S3、S5、S6、S8~S11、S13~S15、S17~S20 为一类,该结果与主成分分析结果基本一致。结果见图6。

图6 30批样品的聚类分析树状图
2.8 偏最小二乘法-判别分析
为进一步寻找影响栀子饮片和栀子配方颗粒质量的差异性成分,本研究以22个共有峰峰面积为变量,采用SIMCA 16.0软件进行偏最小二乘法-判别分析。结果显示,栀子饮片和栀子配方颗粒可被区分,分别聚集在[t]1负值象限和[t]1正值象限,与主成分分析结果基本一致。结果见图7。

图7 30批样品的偏最小二乘法-判别分析得分图
以栀子饮片与栀子配方颗粒的22 个共有峰峰面积为变量,采用SIMCA 16.0 软件对各共有峰的变量重要性投影(variable importance in projection,VIP)值进行分析,并以VIP 值>1 为标准[14]筛选贡献较大的差异性成分。结果显示,VIP值>1的共有峰依次为16号峰、14号峰、3 号峰、17 号峰(西红花苷Ⅱ)、15 号峰(西红花苷Ⅰ)、18号峰、22号峰、2号峰(DAAME)、21号峰,表明这9个共有峰对应的成分可能是影响栀子饮片与栀子配方颗粒质量的差异性成分。结果见图8。
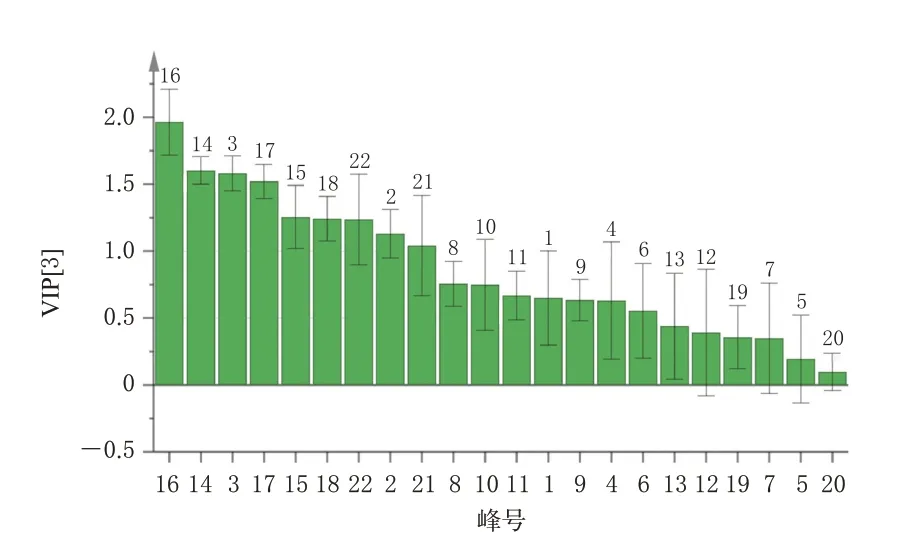
图8 22个共有峰的VIP 值
3 讨论
本课题组前期考察了不同流动相系统(乙腈-0.1%甲酸溶液、乙腈-0.2%甲酸溶液、乙腈-0.2%磷酸溶液)对色谱峰的分离效果及特征峰信息的影响,结果显示,以乙腈-0.1%甲酸溶液为流动相时,所得色谱峰信息较为丰富,各色谱峰峰形及分离度均较好;同时,本课题组在参考文献[15]的基础上,考察了不同检测波长(238、265、330、440 nm)下各色谱峰的吸收情况,结果显示,DAAME、栀子苷、苦番红花素、芦丁在238 nm 波长下,西红花苷Ⅰ、西红花苷Ⅱ在440 nm 波长下均有较大吸收。此外,本课题组还考察了不同提取溶剂(30%甲醇、50%甲醇、70%甲醇、甲醇及30%乙醇、50%乙醇、70%乙醇、乙醇)的提取效果,结果显示,以70%甲醇为提取溶剂时的提取效果最好;本课题组对不同提取方法(超声、回流)的考察结果显示,2种方法无差别,为了操作简便,故选择超声提取。
本研究结果显示,20 批栀子饮片和10 批栀子配方颗粒均有24个共有峰,30批样品则有22个共有峰,与对照图谱(R3)的相似度均不低于0.96,表明不同产地栀子饮片与栀子配方颗粒间成分种类基本相同。主成分分析结果显示,栀子饮片与栀子配方颗粒各分为一类,与聚类分析结果一致。有9个共有峰的VIP值>1,提示这9个共有峰对应的成分可能是影响栀子饮片与栀子配方颗粒质量的差异性成分。
含量测定结果显示,栀子饮片中DAAME、栀子苷、苦番红花素、芦丁、西红花苷Ⅰ、西红花苷Ⅱ的平均含量分别为1.04、57.00、1.30、1.03、9.63、0.99 mg/g;栀子配方颗粒中分别为0.96、17.04、0.37、0.27、0.73、0.04 mg/g。栀子配方颗粒中DAAME、栀子苷、苦番红花素、芦丁、西红花苷Ⅰ、西红花苷Ⅱ的含量分别为饮片含量的92.31%、29.89%、28.46%、26.21%、7.58%、4.04%,表明栀子饮片和栀子配方颗粒中,除DAAME 外,栀子苷等其余5个成分的含量相差较大。有研究表明,在水提过程中,由于结构类似成分发生了转化,DAAME的转移率可超过100%[16];而栀子苷及西红花苷类成分在加热过程中会发生降解[16];苦番红花素为单萜类成分,可溶于水、乙醇,且对热、光、酸及碱较敏感[17];芦丁在水中的溶解性较差[18]。这可能是导致栀子苷等5个成分转移率较低的原因,也提示饮片在加工制成颗粒的过程中,需要注意煎煮时间和温度。
综上所述,本研究所建指纹图谱和含量测定方法简便、重复性较好,结合化学模式识别可用于评价栀子饮片及栀子配方颗粒的质量;16号峰等色谱峰对应的9个成分可能是影响两者质量的差异性成分。
