卡格列净通过RAS 和TGF⁃β1/Smad 途径减轻高血压诱导的心肌肥厚和纤维化
2022-07-26李爱花王青青秦迎春谢亦璘严志强
李爱花,王青青,秦迎春,谢亦璘,严志强
(1.安徽理工大学医学院,安徽淮南 232001;2.中山市中医院,广东中山 528401;3.上海交通大学闵行校区生命科学与生物技术学院上海市生殖医学重点实验室,上海 200240;4.安徽理工大学附属奉贤区中心医院,上海 201499)
心血管疾病在全球范围内有较高的发病率和死亡率[1]。高血压是心血管疾病的独立危险因素,在心血管疾病的发病机制和病理性心室重构中起重要作用[2]。作为受高血压影响的多个器官之一,血压长期升高可引起以心肌肥厚和心肌纤维化为特征的病理性心室重塑。高血压促进心肌细胞肥厚性生长,心肌细胞大小增加[3]。心肌细胞肥大被认为是一种对超负荷刺激引起的适应性反应。然而,持续的刺激会导致心脏失代偿和心力衰竭[4]。高血压可促进成纤维细胞增殖,并诱导Ⅰ型胶原(Col1a)和Ⅲ型胶原(Col3a)过度表达,这两种胶原积聚在间质内[4]。这些会导致心肌纤维化,并最终导致左心室功能障碍[3,4]。心室肥厚是高血压患者发生心血管事件的独立危险因素,逆转心肌肥厚有助于降低患者发生心血管并发症的风险。
越来越多的证据表明肾素血管紧张素系统(RAS)与病理性心室重构有关[5]。血管紧张素原在肝脏中合成,经肾素裂解为效应分子血管紧张素Ⅱ(AngⅡ)[6]。作为RAS 的重要成员,Ang Ⅱ通过与血管紧张素Ⅱ型受体1(AGTR1)相互作用发挥作用[7]。RAS 成分也可以由细胞内和局部组织产生,在组织重塑中发挥重要作用[8]。研究发现心肌细胞和成纤维细胞同时表达AGTR1 和血管紧张素Ⅱ型受体2(AGTR2)[9]。Ang Ⅱ与AGTR1 的结合激活多个细胞内信号通路,包括促纤维化转化生长因子⁃β(TGF⁃β)通路[5]。TGF⁃β1 通路在刺激成纤维细胞的增殖和迁移以及促进细胞外基质的沉积中起着关键作用[10]。血管紧张素转换酶(ACE)抑制剂和Ang Ⅱ受体阻滞剂广泛用于治疗心血管疾病[11]。然而,心力衰竭的发病率和死亡率仍然很高。因此,需要一种治疗病理性心室重塑和心力衰竭的新策略。
卡格列净是钠⁃葡萄糖协同转运蛋白⁃2 抑制剂(SGLT2i)的成员之一,通过阻断肾小球对葡萄糖的再吸收而降低血糖[12]。卡格列净已被用于治疗2型糖尿病患者。除了降低血糖外,越来越多的证据表明卡格列净具有心血管保护作用。Meta 分析显示卡格列净治疗显著降低心衰事件[13]。有报道指出卡格列净可改善心脏代谢和舒张功能,降低血管硬度,降低血压[13,14]。体内和体外的研究表明卡格列净具有抗氧化和抗炎作用。卡格列净通过抑制mTOR/HIF⁃1α 信号通路显著改善糖尿病小鼠心脏的心功能和炎症反应[15]。卡格列净通过刺激多种抗氧化和抗炎信号通路来减轻异丙肾上腺素诱导的心脏氧化应激[16]。卡格列净通过刺激抗氧化和抗炎信号传导,减轻心脏的氧化应激,改善心脏缺血再灌注损伤,改善心脏功能[17]。同样,据报道,SGLT2i 的其他成员,如依格列净,可以减轻糖尿病小鼠的心肌纤维化,并在压力过度诱导的心力衰竭小鼠模型中保持心肌功能[18,19]。虽然卡格列净对心血管疾病的有益作用已有研究,但是,卡格列净对高血压引起的心脏重构的影响仍未报道。
本研究发现卡格列净可调节RAS 和TGF⁃β1/Smad 通路,可以预防高血压引起的心肌纤维化和病理性心肌肥厚。
1 材料与方法
1.1 实验动物和药物治疗
雄性自发性高血压大鼠(SHR)和正常血压大鼠(WKY)购自北京维通利华实验动物公司[批号:SCXK(京)2016⁃0006]。用普通饲料和自来水喂养大鼠,并维持在标准温度和光照条件下。20 周龄雄性大鼠随机分为WKY 组、SHR 组、卡格列净低剂量[SHR⁃CANA(30 mg/kg)]组和卡格列净高剂量[SHR⁃CANA(60 mg/kg)]组,每组8 例。卡格列净溶于0.8% 羧甲基纤维素钠中,每日灌胃1 次。WKY 组和SHR 组只接受羧甲基纤维素钠处理。采用尾袖法测量收缩压(SBP)和舒张压(DBP),使用BP⁃2010 系列血压计(Softron Biotechnology,北京,中国)。给药前及给药第1~8 周连续监测大鼠的血压、血糖及体重,每周测量1 次,每次监测时间为同一时间段。每周用血糖仪(鱼跃,中国)测定空腹8 h血糖。所有动物实验按照中国卫生部动物管理规定(2001 年第55 号文件)进行。
1.2 超声心动图
治疗8 周后,使用超声系统(Vevo 2100,visual⁃sonic,Inc,Toronto,Canada)和15 MHz 高频探头对实验动物进行超声心动图检查。大鼠以异氟醚麻醉(1.5%)。评估以下指标:舒张末期左室后壁厚度、收缩末期左室容积、舒张末期左室容积、收缩末期室间隔厚度、射血分数。
1.3 组织切片
给药治疗8 周后处死。分别称量全心重量和左心室重量。部分左心室在4 ℃下用4%多聚甲醛固定过夜。然后将组织脱水并包埋在石蜡中。切片厚度为4 μm,苏木精和伊红(HE)染色检测形态学。马松(Masson)三色法染色评估心肌纤维化(Solar⁃bio,北京,中国)。切片图像采用显微镜(BX53;奥林巴斯公司,日本东京)。使用ImageJ 软件对结果进行分析。
1.4 实时聚合酶链反应(RT⁃PCR)
心肌组织样品用TRIzol 试剂(Invitrogen 公司,美国)提取总RNA。使用RT Master Mix 进行PCR(MedChemExpress,New Jersey,USA)将总RNA逆转录成cDNA。使用2×SYBR 预混Ex Taq 试剂盒与ROX(康为,中国)进行RT⁃PCR。反应在95℃下2 min,95℃5 s,60℃30 s,然后循环40 次。信号在ABI Q6 机器上检测(应用生物系统公司,美国)。以GAPDH 作为内参。采用2⁃ΔΔCt的方法计算。本研究使用的PCR 引物序列见表1。
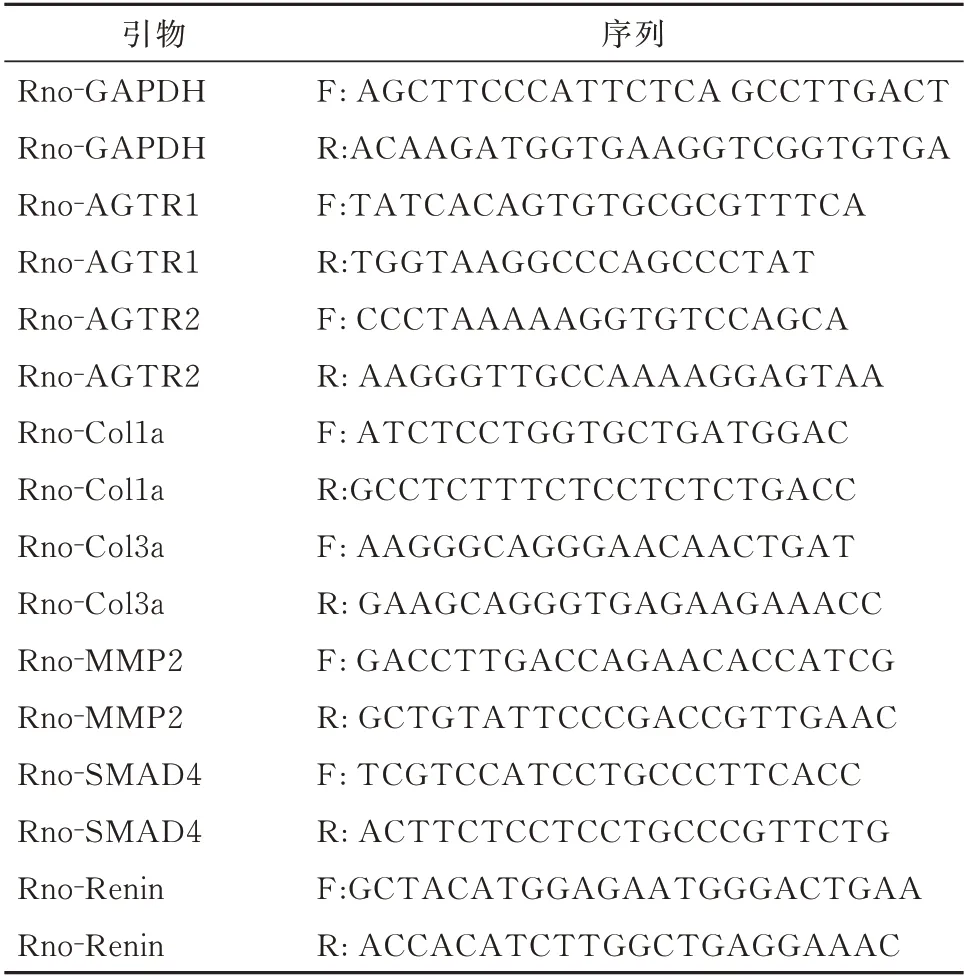
表1 引物序列Tab 1 Sequence primers
1.5 蛋白印迹法
左心室组织用含蛋白酶抑制剂的RIPA 缓冲液裂解(MedChemExpress,New Jersey,USA)并超声。蛋白浓度用BCA 法(碧云天,中国)测定。100 ℃煮沸10 min 后,蛋白经10% SDS ⁃聚丙烯酰胺凝胶分离,并转移到硝化纤维素膜(Thermofish,美国)。膜在室温下用含5%的脱脂奶粉Tris 缓冲液封闭1 h 后,然后用Ⅰ型胶原(Col1a)(1∶1 000,Proteintech,美国)、Ⅲ型胶原(Col3a)(1∶1 000,Pro⁃teintech,美国)、MMP2(1∶1 000,Proteintech,美国)、TGF⁃β1(1∶1 000,CST,美国)、Smad4(1∶1 000,CST,美国)、GAPDH(1∶1 000,Proteintech,美国)和β⁃Tubulin(1∶1 000,Proteintech,美国)的抗体在4℃下孵育过夜。与二抗孵育后,利用增强化学发光试剂(圣尔,中国)曝光蛋白条带。用Tanon 图像分析仪(Tanon Science,上海,中国)获取图像并进行分析。
1.6 统计学处理
2 结果
2.1 卡格列净对各组血压的影响
与WKY 组比较,SHR 组的收缩压、舒张压明显升高,差异具有统计学意义(P<0.01)。给药2~8周,与SHR 组比较,SHR⁃CANA(30 mg/kg)组及SHR⁃CANA(60 mg/kg)组收缩压均降低,差异具有统计学意义(P<0.01)。给药2 周,与SHR 组比较,SHR⁃CANA(60 mg/kg)组舒张压降低;给药3~8周,SHR⁃CANA(30 mg/kg)组及SHR⁃CANA(60 mg/kg)组舒张压较SHR 组均降低,差异具有统计学意义(P<0.01)。见表2。
表2 卡格列净对各组血压的影响(n=8,mmHg,±s)Tab 2 Effects of canagliflozin on blood pressure of rats in each groups(n=8,mmHg,±s)

表2 卡格列净对各组血压的影响(n=8,mmHg,±s)Tab 2 Effects of canagliflozin on blood pressure of rats in each groups(n=8,mmHg,±s)
注:与SHR 组比较,#P<0.01。
时间(周数)收缩压WKY 组140.70±4.40#139.50±5.43#150.70±9.44#144.00±8.17#147.60±12.09#149.30±10.07#138.00±5.60#156.80±9.70#147.20±1.97#2.661 0.001 012345678FP SHR 组201.80±21.91 209.40±8.70 230.30±14.49 212.30±7.88 217.50±16.20 226.50±13.71 208.00±7.024 235.70±5.30 234.60±15.78 SHR⁃CANA(30 mg/kg)组196.40±10.62 199.00±4.58 206.80±5.80#186.70±12.78#183.70±6.13#178.40±15.29#185.70±12.23#205.30±16.38#183.90±10.78#SHR⁃CANA(60 mg/kg)组207.80±9.43 196.30±6.21 191.80±10.59#187.20±12.81#183.70±10.85#185.80±17.57#173.30±5.73#202.60±14.73#175.80±11.5#舒张压WKY 组113.60±2.20#111.90±4.90#112.80±3.20#114.80±3.50#112.80±5.69#119.10±3.18#114.50±3.82#108.30±1.87#104.30±4.63#7.832<0.001 SHR 组165.50±11.89 164.10±8.46 192.10±9.96 188.60±5.06 174.10±9.36 174.00±10.42 164.80±2.43 195.70±13.80 191.90±12.34 SHR⁃CANA(30 mg/kg)组169.30±8.30 172.80±15.03 187.00±11.26 151.40±6.73#146.70±8.84#144.30±12.90#133.80±9.95#158.80±7.41#140.00±10.65#SHR⁃CANA(60 mg/kg)组166.00±18.43 166.20±6.80 172.30±4.57#142.30±12.06#141.20±16.40#134.70±11.28#115.20±5.61#133.00±2.94#132.80±5.13#
2.2 卡格列净对各组血糖和体重的影响
与SHR 组比较,SHR⁃CANA(30 mg/kg)组、SHR⁃CANA(60 mg/kg)组在给药后1~8 周血糖降低,差异具有统计学意义(P<0.01)。由于卡格列净在糖尿病患者和动物模型中有降低体重的作用[13,20],笔者研究了卡格列净对SHR 体重的影响。与SHR 组比较,SHR⁃CANA(30 mg/kg)组、SHR⁃CANA(60 mg/kg)组较SHR 组体重均有下降,差异具有统计学意义(P<0.01)。见表3。
表3 卡格列净对各组不同时期血糖和体重的影响(n=8,±s)Tab 3 Effects of canagliflozin on blood glucose and body weight of rats in each groups in different periods(n=8,±s)

表3 卡格列净对各组不同时期血糖和体重的影响(n=8,±s)Tab 3 Effects of canagliflozin on blood glucose and body weight of rats in each groups in different periods(n=8,±s)
注:与SHR 组比较,#P<0.01。
时间(周数)血糖(mmol/L)体重(g)WKY 组SHR 组SHR⁃CANA(30 mg/kg)组6.90±0.22 6.60±0.34#5.68±0.76#4.95±0.26#4.40±0.32#5.08±0.26#4.93±0.28#4.38±0.70#4.68±0.33#SHR⁃CANA(60 mg/kg)组6.80±0.37 6.55±0.58#5.60±0.36#4.98±0.81#4.00±0.24#4.15±0.17#4.78±0.28#4.48±0.36#4.18±0.30#WKY 组SHR 组012345678FP 6.73±0.22 7.00±0.56 7.00±0.56 6.48±0.66 6.30±0.32 6.33±0.67 6.40±0.50 6.53±0.92 6.50±0.59 7.23±0.81 7.83±0.55 7.03±0.76 6.70±0.55 6.20±0.53 6.80±0.50 6.50±0.41 7.08±1.10 6.63±0.46 313.00±8.29 327.80±19.33 334.80±15.44 343.00±8.76 335.30±6.70 339.80±6.70 332.50±6.25 341.00±3.74 342.50±10.41 319.30±17.67 330.80±7.27 337.80±3.10 336.00±7.87 338.00±4.69 350.80±7.32 347.00±4.76 348.80±7.54 339.00±6.83 SHR⁃CANA(30 mg/kg)组304.50±8.89 292.00±9.42#267.80±4.19#280.50±5.75#258.50±10.34#257.00±14.67#262.80±10.50#258.00±7.70#250.00±13.76#SHR⁃CANA(60 mg/kg)组312.50±16.92 296.00±9.90#291.30±6.24#271.30±3.86#259.80±2.87#255.00±8.60#246.30±7.46#244.00±8.60#252.00±5.29#2.553 0.001 51.027<0.001
2.3 卡格列净对各组左心室肥厚及功能的影响
卡格列净治疗8 周后,SHR 组的室间隔厚度、左室后壁厚度、收缩期末容积均较WKY 组增加,差异具有统计学意义(P<0.05)。与SHR 组比较,SHR⁃CANA(30 mg/kg)组、SHR⁃CANA(60 mg/kg)组室间隔厚度、左室后壁厚度、收缩期末容积均有所降低,差异具有统计学意义(P<0.05),见表4。检测心脏重量/体重(HW/BW)和左心重量/心脏重量(LHW/HW)的比值,与WKY组相比,SHR组的HW/BW和LHW/HW增加,差异有统计学意义(P<0.05),与SHR 组相比,SHR⁃CANA(30 mg/kg)组、SHR⁃CANA(60 mg/kg)组的HW/BW 和LHW/HW 降低,差异有统计学意义(P<0.05)。HE 染色结果显示,与WYK 相比,SHR 组心肌细胞横截面积较WKY 组显著增加,差异具有统计学意义(P<0.01)。与SHR 组比较,SHR⁃CANA(30 mg/kg)组、SHR⁃CANA(60 mg/kg)组心肌细胞横截面积显著减少,差异具有统计学意义(P<0.01),见图1和表5。
表5 卡格列净对各组心肌肥厚的影响(n=8,±s)Tab 5 Effects of canagliflozin on myocardial hypertrophy in each group(n=8,±s)

表5 卡格列净对各组心肌肥厚的影响(n=8,±s)Tab 5 Effects of canagliflozin on myocardial hypertrophy in each group(n=8,±s)
注:与SHR 组比较,#P<0.01。
HE 染色(心肌细胞横截面积,μm2)组别全心/体重(g/g)左心/全心(g/g)0.003 3±0.000 15#0.69±0.005 6#6 565.00±375.50#0.004 0±6.923e−0050.80±0.02314 030.00±885.40 0.003 7±1.431e−005#0.72±0.032#7 067.00±371.60#0.003 5±0.000 13#0.73±0.047#5 770.00±557.60#32.958.45169.80 0.000 10.002 70.000 1 WKY 组SHR 组SHR⁃CANA(30 mg/kg)组SHR⁃CANA(60 mg/kg)组FP
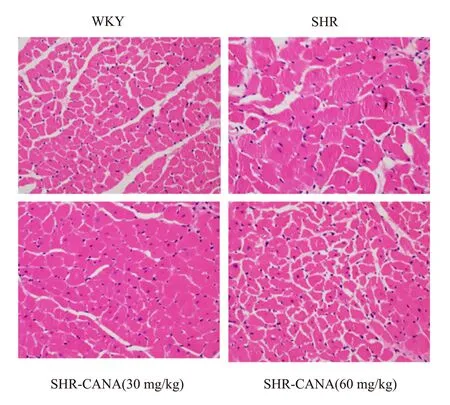
图1 各组心肌组织HE 染色(×40)Fig 1 HE staining of myocardial tissue in each group(×40)
表4 卡格列净对各组左心室肥厚及功能的影响(n=8,±s)Tab 4 Effects of canagliflozin on left ventricle cardiac hyper⁃trophy and function in SHRs(n=8,±s)
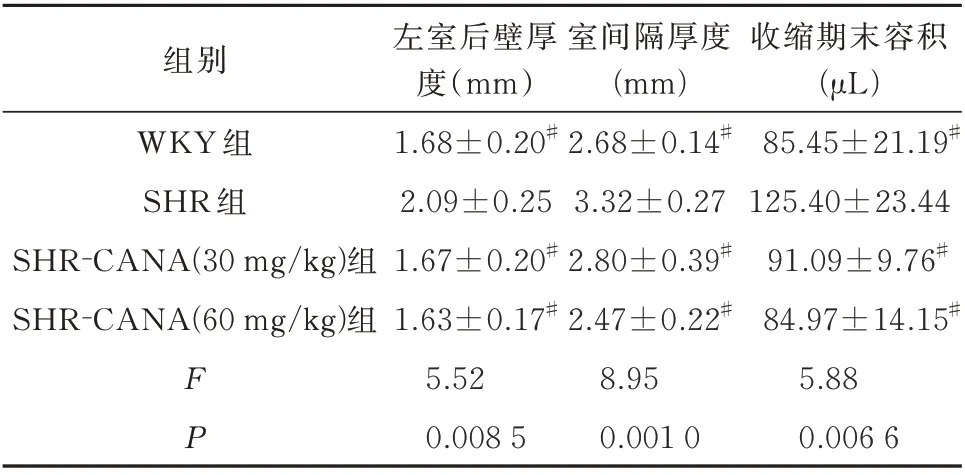
表4 卡格列净对各组左心室肥厚及功能的影响(n=8,±s)Tab 4 Effects of canagliflozin on left ventricle cardiac hyper⁃trophy and function in SHRs(n=8,±s)
注:与SHR 组比较,#P<0.01。
组别收缩期末容积(μL)左室后壁厚度(mm)室间隔厚度(mm)WKY 组SHR 组SHR⁃CANA(30 mg/kg)组SHR⁃CANA(60 mg/kg)组85.45±21.19#125.40±23.44 91.09±9.76#84.97±14.15#5.88 0.008 50.001 00.006 6 FP 1.68±0.20#2.09±0.25 1.67±0.20#1.63±0.17#5.52 2.68±0.14#3.32±0.27 2.80±0.39#2.47±0.22#8.95
2.4 卡格列净对各组心肌纤维化的影响
组织学检查显示,SHR 组心肌间质胶原体积较WKY 组增加,SHR⁃CANA(30 mg/kg)组、SHR⁃CANA(60 mg/kg)组减少。见图2。与WKY组相比,SHR 组Col1a 和Col3a 的表达显著升高。与SHR 组相比,SHR⁃CANA(30 mg/kg)组、SHR⁃CANA(60 mg/kg)组Col1a 和Col3a 的表达被抑制,差异有统计学差异(P<0.05)。与WKY 组相比,SHR 组MMP2 的相对mRNA 和蛋白水平升高,差异有统计学意义(P<0.01)。然而,与SHR 组相比,SHR⁃CANA(30 mg/kg)组、SHR⁃CANA(60 mg/kg)组MMP2 表达减少,差异有统计学意义(P<0.01),见图2~4 和表6。
表6 卡格列净对各组心肌纤维化的影响(n=8,±s)Tab 6 Effects of canagliflozin on myocardial fibrosis in each group(n=8,±s)

表6 卡格列净对各组心肌纤维化的影响(n=8,±s)Tab 6 Effects of canagliflozin on myocardial fibrosis in each group(n=8,±s)
注:与SHR 组比较,#P<0.05。
组别WKY 组Col1a/GAPDH(RT⁃PCR)1.00±0.00#Col1a/β⁃tubulin(western⁃blotting)0.067±0.003 2#Col3a/GAPDH(RT⁃PCR)1.00±0.00#MMP2/β⁃tubulin(western⁃blotting)0.34±0.22#MMP2/GAPDH(RT⁃PCR)1.00±0.00#SHR 组SHR⁃CANA(30 mg/kg)组SHR⁃CANA(60 mg/kg)组2.17±0.89 0.72±0.31#0.48±0.19#0.310±0.031 0.110±0.067#0.043±0.019#2.32±0.83 0.83±0.34#0.17±0.070#1.25±0.33 1.15±0.062#0.24±0.17#3.43±0.78 1.31±0.24#0.39±0.072#FP 7.292 27.68 12.16 16.61 31.35 0.0001 0.0112 0.0001 0.0024 0.0009
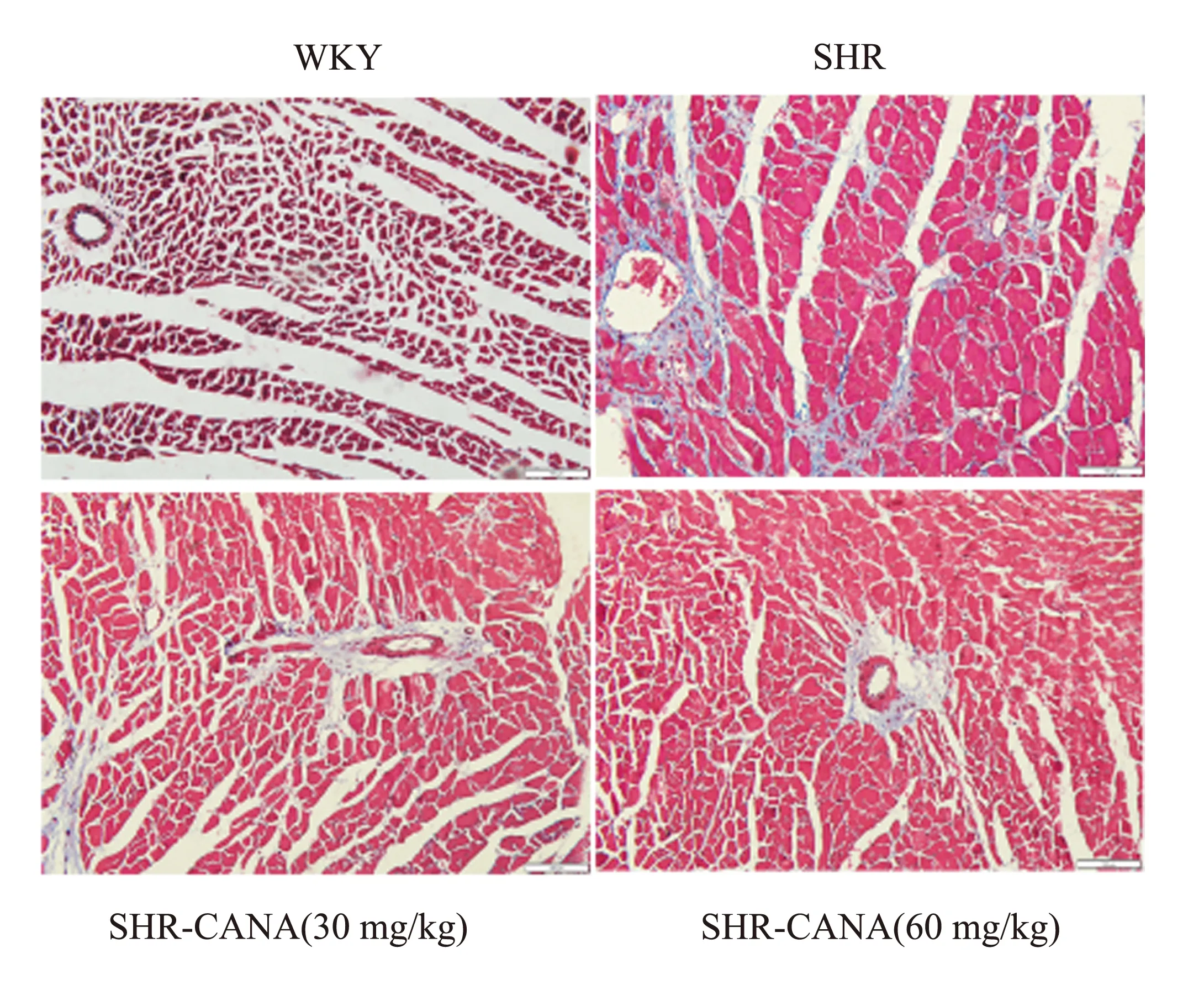
图2 各组心肌Masson 三色法染色(×40)Fig 2 Myocardial Masson Trichrome Stain in each group(×40)
2.5 卡格列净对各组心肌组织AGTR1、AGTR2、Renin、TGF⁃β1 和Smad4 表达的影响
与WKY 组相比,SHR 组的TGF⁃β1 及Smad4的mRNA 和蛋白水平显著升高,差异有统计学意义(P<0.01)。与SHR 组比较,SHR⁃CANA(30 mg/kg)组、SHR⁃CANA(60 mg/kg)组的TGF⁃β1 及Smad4 的mRNA 和蛋白水平降低,差异有统计学意义(P<0.01)。与WKY 组相比,SHR 组AGTR1 和肾素中mRNA 水平升高,而与WKY 组相比,SHR组AGTR2 mRNA 水平降低,差异均具有统计学意义(P<0.01)。与SHR 组相比,SHR⁃CANA(30 mg/kg)组、SHR⁃CANA(60 mg/kg)组AGTR1 及Renin 的mRNA 的表达降低,而SHR⁃CANA(30 mg/kg)组、SHR⁃CANA(60 mg/kg)组中AGTR2 mRNA 的表达显著升高,差异有统计学意义(P<0.01),见图5、6 及表7、8。
表7 卡格列净对各组心肌组织TGF⁃β1 和Smad4 表达的影响(n=8,±s)Tab 7 Effects of canagliflozin on the expression of TGF⁃β1 and Smad4 in myocardial tissue in each group(n=8,±s)
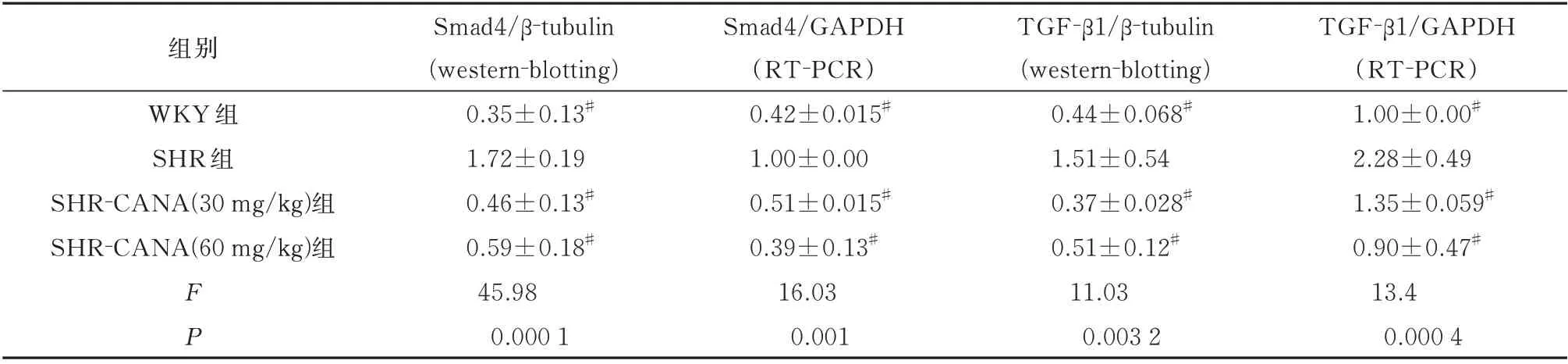
表7 卡格列净对各组心肌组织TGF⁃β1 和Smad4 表达的影响(n=8,±s)Tab 7 Effects of canagliflozin on the expression of TGF⁃β1 and Smad4 in myocardial tissue in each group(n=8,±s)
注:与SHR 组比较,#P<0.01。
组别TGF⁃β1/GAPDH(RT⁃PCR)Smad4/β⁃tubulin(western⁃blotting)Smad4/GAPDH(RT⁃PCR)TGF⁃β1/β⁃tubulin(western⁃blotting)WKY 组SHR 组SHR⁃CANA(30 mg/kg)组SHR⁃CANA(60 mg/kg)组1.00±0.00#2.28±0.49 1.35±0.059#0.90±0.47#45.9816.0311.0313.4 0.000 10.0010.003 20.000 4 FP 0.35±0.13#1.72±0.19 0.46±0.13#0.59±0.18#0.42±0.015#1.00±0.00 0.51±0.015#0.39±0.13#0.44±0.068#1.51±0.54 0.37±0.028#0.51±0.12#
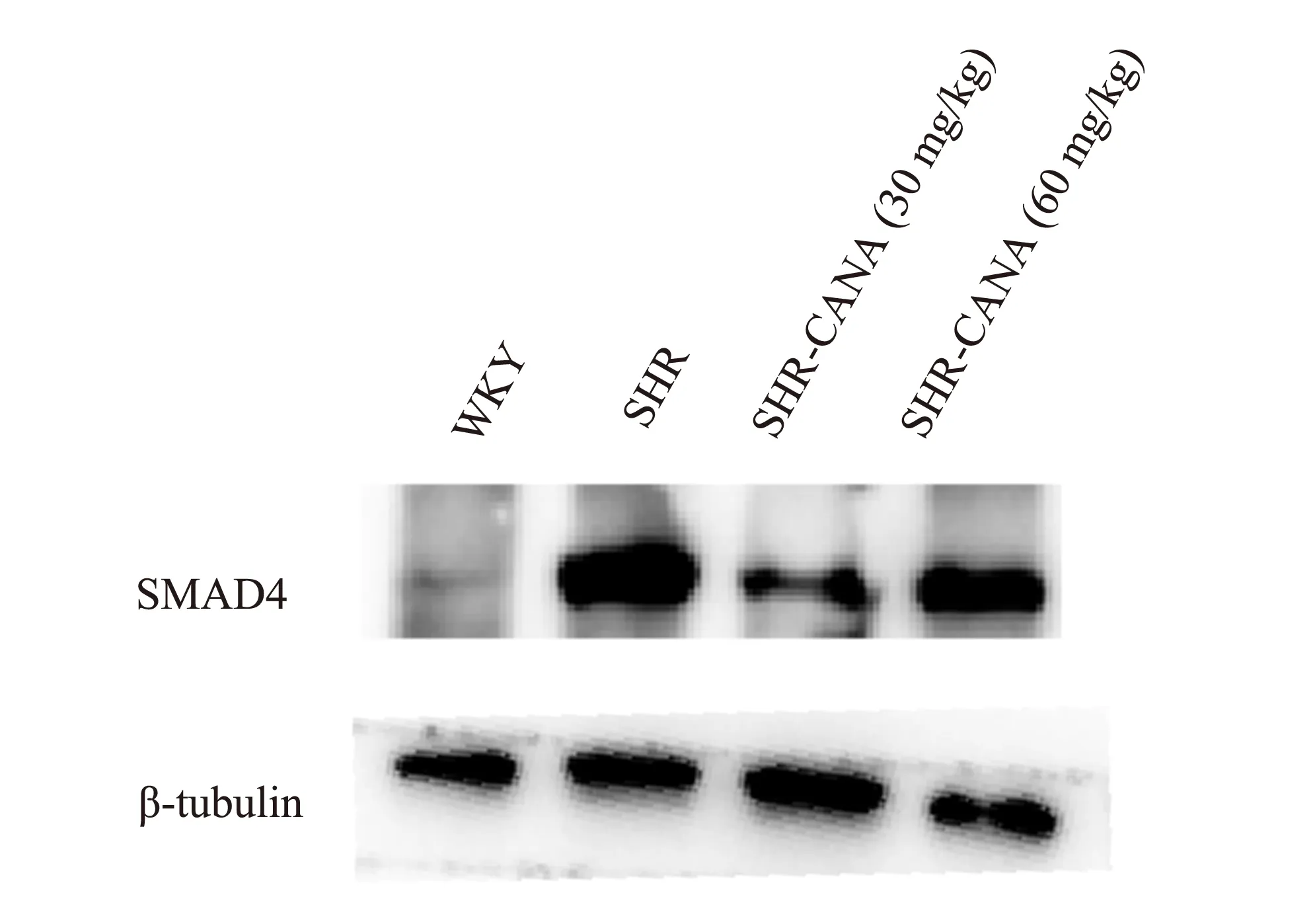
图5 各组心肌Smad4 的蛋白表达Fig 5 Protein expression of myocardial Smad4 in each group
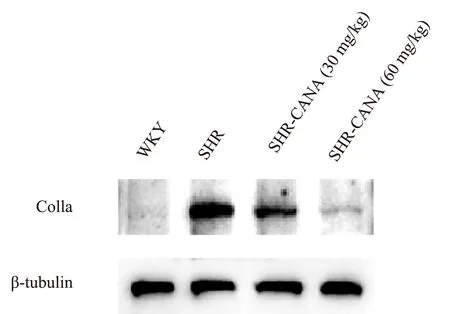
图3 各组心肌Col1a 的蛋白表达Fig 3 Protein expression of myocardial Col1a in each group
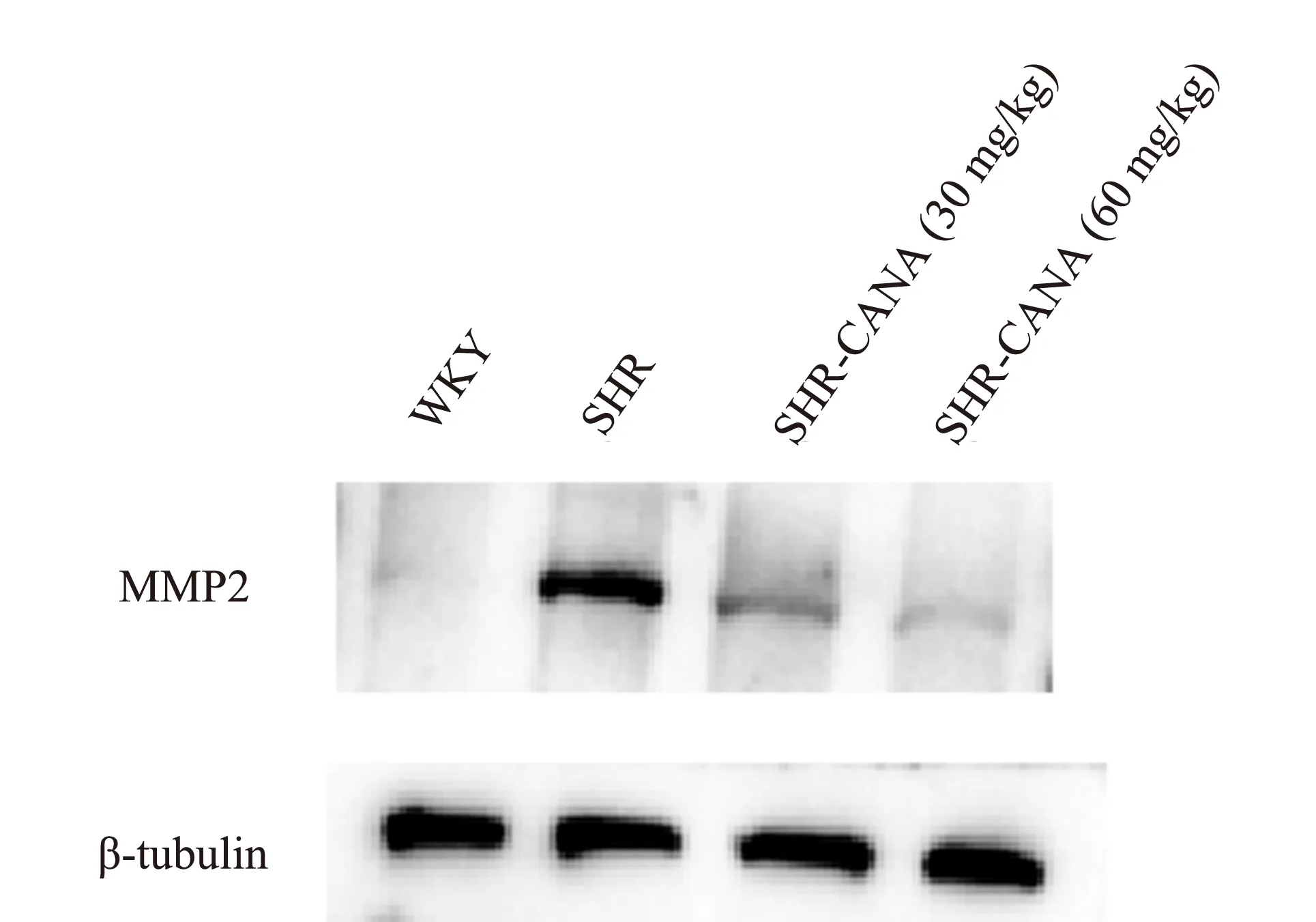
图4 各组心肌MMP2 的蛋白表达Fig 4 Protein expression of myocardial MMP2 in each group
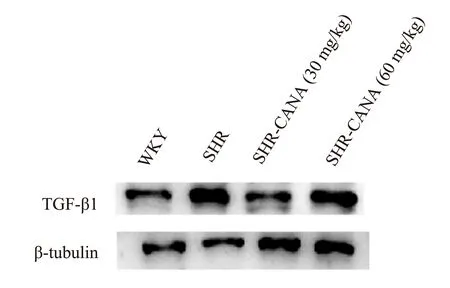
图6 各组心肌TGF⁃β1 的蛋白表达Fig 6 Protein expression of myocardial TGF⁃β1 in each group
表8 卡格列净对各组心肌组织AGTR1、AGTR2、肾素表达的影响(n=8,±s)Tab 8 Effects of canagliflozin on the expression of AGTR1,AGTR2 and renin in myocardial tissue in each group(n=8,±s)
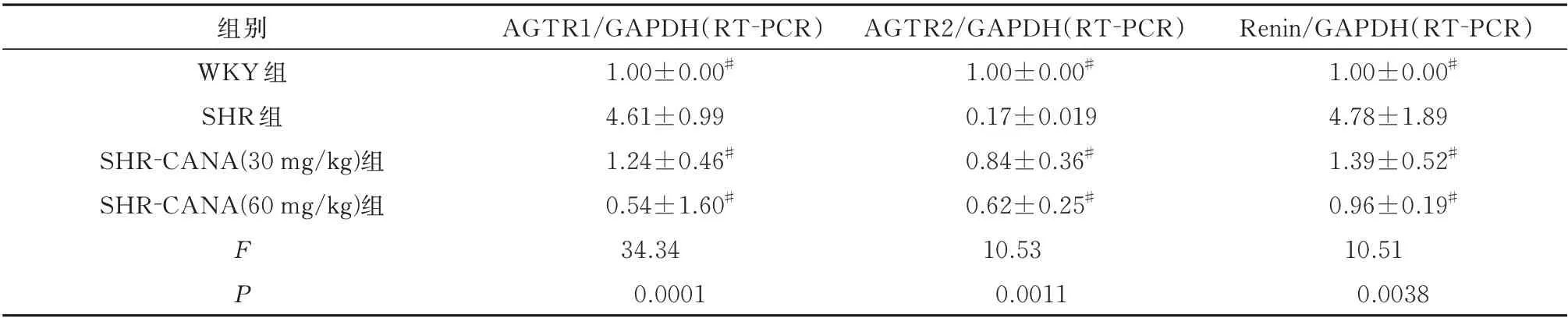
表8 卡格列净对各组心肌组织AGTR1、AGTR2、肾素表达的影响(n=8,±s)Tab 8 Effects of canagliflozin on the expression of AGTR1,AGTR2 and renin in myocardial tissue in each group(n=8,±s)
注:与SHR 组比较,#P<0.01,#P<0.05。
Renin/GAPDH(RT⁃PCR)1.00±0.00#4.78±1.89 1.39±0.52#0.96±0.19#10.51 0.0038组别WKY 组SHR 组SHR⁃CANA(30 mg/kg)组SHR⁃CANA(60 mg/kg)组FP AGTR1/GAPDH(RT⁃PCR)1.00±0.00#4.61±0.99 1.24±0.46#0.54±1.60#34.34 0.0001 AGTR2/GAPDH(RT⁃PCR)1.00±0.00#0.17±0.019 0.84±0.36#0.62±0.25#10.53 0.0011
3 讨论
本研究旨在探讨卡格列净对高血压引起的心脏重构的影响。卡格列净干预可减轻SHR 心肌肥厚、纤维化和心功能障碍。卡格列净下调了Col1a、Col3a、MMP⁃2、TGF⁃β1 和Smad4 等纤维化分子标志物的表达。研究证明卡格列净可抑制AGTR1 和Renin mRNA 表达,但上调了AGTR2 mRNA 的水平。这些结果表明,卡格列净可以改善SHR 的心室重构,这为卡格列净对心血管疾病的治疗提供了一个新的治疗靶点。
卡格列净最初用于控制血糖,也被发现具有心血管保护作用。CANVAS 试验表明卡格列净降低了2 型糖尿病患者心血管疾病死亡的风险[12,13]。降低心血管死亡率的机制包括降低血压、减轻体重、改善血管硬度、改善血糖和促进利尿。本研究表明,卡格列净治疗可以降低血压、体重和血糖。我们的结果与其他研究报道结果一致。最近的一项研究表明卡格列净治疗2 型糖尿病患者24 周后显著降低体重[21]。在高脂肪饮食诱导的肥胖小鼠中也可以观察到类似的结果,这些小鼠的脂肪量和白色脂肪组织重量都减少[22]。这种减少可能与卡路里损失的诱导有关[19]。与其他药物相比,卡格列净治疗可降低2 型糖尿病患者的收缩压和舒张压[23]。在用卡格列净治疗的非糖尿病大鼠中发现血压也降低[17]。一些研究表明卡格列净促进小鼠、大鼠和家兔对乙酰胆碱的血管舒张敏感性,这可能有助于解释卡格列净降低血压的作用[17,24,25]。卡格列净作为一种降糖药,可以降低糖尿病小鼠和大鼠的循环血糖浓度,但不能降低非糖尿病动物的血糖浓度[26,27]。本实验表明卡格列净治疗SHRs 的血糖水平降低,这是有争议的。这一差异可能与不同动物模型和不同剂量的卡格列净有关。
心肌肥厚的特点是心肌数量增加,心室厚度增加,心肌细胞大小增加,心功能受损,是心血管死亡的独立危险因素[3,4,28]。因此,减轻心肌肥厚对预防心血管疾病的进一步死亡至关重要。研究报道了SGLT⁃2i 在减轻心肌肥厚方面的有效性。Shi 等[29]观察到达格列净治疗后降低了主动脉横向收缩小鼠升高的HW/BW 比、左室直径、左室后壁厚度和左室射血分数。最近的一项研究报道,达格列净通过调节TGF⁃β1/Smad 通路改善Ang Ⅱ输注SD 大鼠的心肌肥厚和左心室功能[30]。在使用依格列净治疗的肥胖大鼠中,心脏重量和左心室体积的增加得到了改善[31]。同样,有研究表明卡格列净治疗3个月显著改善了2 型糖尿病患者的左心室舒张功能[14]。有报道称卡格列净对非糖尿病雄性大鼠心肌缺血再灌注损伤有保护作用,并可减轻糖尿病和非糖尿病心脏心肌梗死[17,26]。与之前的研究一致,本实验表明,与SHR 相比,卡格列净治疗SHR 显著降低了HW/BW 比、LVW/HW 比、心肌细胞大小、左室壁厚度、室间隔厚度和左室收缩期末容积。表明卡格列净可以改善心室重构。
心肌纤维化与心功能障碍密切相关[3,4,10]。众所周知,长期高血压可诱发心肌纤维化[3,4,10]。心肌纤维化的特点是胶原过度积累和细胞外基质降解,增加舒张强度,引起左室舒张功能损害[10]。胶原蛋白由成纤维细胞合成,是细胞外基质的主要成分。Ⅰ型胶原和Ⅲ型胶原分别占心脏胶原蛋白的80%和10%。慢性压力超负荷可促进胶原基因表达和胶原蛋白合成。多项研究表明SHR 心脏中Ⅰ型和Ⅲ型胶原的表达高于WKY[32,33]。高血压引起的心肌细胞外基质重构受基质金属蛋白酶(MMPs)调控。越来越多的研究表明,异常的基质金属蛋白酶活性可促进细胞外基质破坏和基质降解[34]。MMP2 在盐敏感的高血压大鼠和SHR 大鼠心肌组织中表达增加。有研究表明,MMP2 调节胶原合成和心脏基质重塑。MMP2 敲除可减少心肌肥厚并改善心肌纤维化,而MMP2 过表达可增强心肌肥厚和心肌纤维化[35,36]。本研究发现SHR 大鼠心脏组织中胶原沉积以及Ⅰ型胶原、Ⅲ型胶原和MMP⁃2中mRNA 和蛋白水平增加,卡格列净治疗后可使其减弱。研究提示MMP2 可能参与卡格列净在心脏重构中的保护作用。
TGF⁃β 信号通路在心肌重塑的发展中起着至关重要的作用[9]。作为纤维形成的主要介质,TGF⁃β1 已被证实在高血压大鼠的心脏组织中过度表达和激活[9]。许多研究表明TGF⁃β1 在心脏重塑中的重要性。例如,TGF⁃β1 在转基因小鼠中过表达可促进心肌肥厚和纤维化,而TGF⁃β1 缺乏的杂合小鼠心肌纤维化减弱[37,38]。TGF⁃β1 通过典型的Smad 依赖信号通路发挥促纤维化活性。TGF⁃β1与特异性TGF⁃β Ⅱ型受体结合后,受体调节的R⁃SMADs(SMAD2,SMAD3)被激活。R⁃SMADs与常见Smad4 结合形成复合物,复合物转运入细胞核并调控其下游基因表达[6,7,11]。最近的研究表明,TGF⁃β1 诱导体外培养的心肌成纤维细胞中Smad4的表达[39]。在慢性心肌梗死瘢痕和压力超载的小鼠心脏中TGF⁃β1 和Smad4 表达升高[3,40,41]。使用NLRP3 抑制剂MCC950 抑制TGF⁃β1 和Smad4 的上调,同时减轻心肌肥厚和纤维化[39]。同样,达格列净通过降低TGF⁃β1 的表达抑制血管内皮素诱导的肥大和纤维化[26]。与上述研究结果一致,本实验表明卡格列净可减少SHR 心肌组织中TGF⁃β1 和Smad 4 的表达,从而减轻高血压引起的病理性心脏重构。
有研究报道,肾素血管紧张素系统(RAS)与高血压引起的心肌重塑密切相关[3,6,7]。RAS 包括循环RAS 和组织RAS。越来越多的研究表明,组织RAS 可影响心脏,对病理性心脏重塑有更直接的影响[6,7]。较多的证据表明,Ang Ⅱ通过与AGTR1 相互作用可促进心脏重构,而AGTR2 被认为具有心脏保护作用[6⁃8]。有报道称,持续输注Ang Ⅱ诱导大鼠使心脏AGTR1 表达和AGTR2 表达减少,并伴有心肌肥厚、心肌纤维化和血压升高[42]。在高盐饲料喂养的大鼠中,发现Ang Ⅱ和AGTR1 在心脏中表达增加[8,43]。同样,SHR 心肌组织中肾素、AG⁃TR1、Ang Ⅱ表达上调,AGTR2 表达下调[44]。通过调节RAS 的表达可以逆转高血压引起的病理性心脏重塑。例如,缬沙坦通过调节AGTR1、AGTR2、ACE1 和ACE2 表达的表达,防止SHR 的心肌肥大和纤维化[45]。拟钙蛋白R568 通过调节肾素、AngⅡ、AGTR1 和AGTR2 的表达改善高血压诱导的心脏重构[44]。在本实验中,心脏组织中肾素、AGTR1表达增加,而AGTR2 表达减少。卡格列净可逆转其表达。这些发现表明卡格列净对SHR 心肌重构的有益影响是通过调节RAS 介导的。
综上所述,本研究表明卡格列净治疗通过调节RAS 和TGF⁃β1/Smad 信号通路减轻高血压所致心肌肥厚和纤维化。
作者贡献度说明:
李爱花:实验操作、指标检测,撰写论文;秦迎春、谢亦璘:协助实验造模;王青青:数据分析;严志强:实验设计,实验指导、论文修改、审阅。
本文无任何利益冲突。
