调强放疗联合小剂量甲磺酸阿帕替尼治疗原发性肝细胞癌合并梗阻性黄疸的疗效观察
2022-07-14刘莎韦燕原浩
刘莎 韦燕 原浩
原发性肝细胞癌(hepatocellular carcinoma,HCC)是我国常见的恶性肿瘤之一,通常诊断较晚,治疗效果以及预后不佳,占全球恶性肿瘤相关死亡原因第三位。黄疸是HCC 晚期并发症之一,常见原因有肝硬化或肿瘤细胞侵犯造成正常肝细胞的坏死、水肿等引起的肝细胞性黄疸;肝脏肿瘤侵及肝门区,或转移性淋巴结压迫胆管和胆管癌栓引起[1]。该类型患者大部分失去根治性手术机会,治疗上以姑息治疗为主,目前常用解除梗阻方法有介入治疗、手术切开引流以及放疗[2,3]。但是部分患者常常不能耐受或不愿接受介入治疗及手术切开引流的治疗方法,而单纯放疗效果有限。甲磺酸阿帕替尼是我国自主研发的高度选择性小分子靶向酪氨酸激酶抑制剂(TKI)。多项研究表明甲磺酸阿帕替尼在晚期HCC 治疗中疗效良好[4-6]。本研究回顾性分析采用调强放疗(intensity modulated radiation therapy,IMRT)联合小剂量甲磺酸阿帕替尼治疗20 例HCC 合并梗阻性黄疸患者的近期疗效及不良反应。现报告如下。
1 资料与方法
1.1 一般资料 收集2019 年1 月~2022 年1 月本院20 例有完整临床以及随访资料的HCC 合并梗阻性黄疸患者作为研究对象。所有患者根据计算机断层扫描(computed tomography,CT)、磁共振成像(magnetic resonance imaging,MRI)、内镜下逆行胰胆管造影术(endoscopic retrograde cholangiopancreatography,ERCP)结合临床诊断明确。初诊患者经外科会诊无根治性手术指征,不适宜或不愿行介入治疗的梗阻患者。其中男19 例,女1 例;平均年龄(53.00±7.30)岁;18 例有乙肝病史;PS 评分1 分4 例,2 分11 例,3 分5 例;16 例患者有3 个及以上肝脏肿瘤;肿瘤直接侵犯,或肝门区压迫15 例,胆管癌栓2 例,压迫并胆管癌栓3 例;所有患者的谷丙转氨酶、谷草转氨酶在正常或轻度升高(≤2 倍正常高值)。见表1。
表1 20 例患者的一般资料[n(%),]
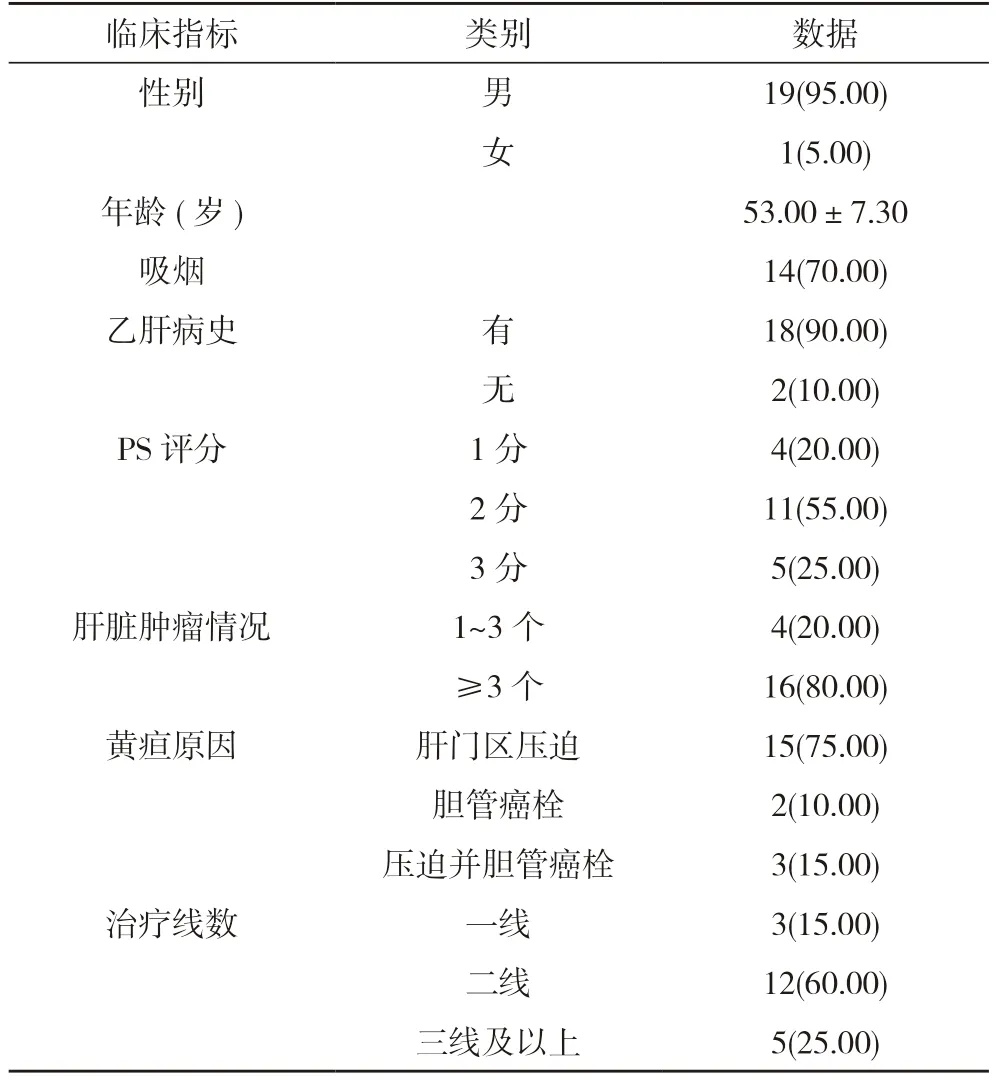
表1 20 例患者的一般资料[n(%),]
1.2 治疗方法 入院时伴有肝功能轻度受损患者,放疗的同时给予还原性谷胱甘肽和/或异甘草酸镁等药物降酶治疗。所有患者均接受调强适型放疗(intensitymodulated radiation therapy,IMRT),采用真空垫进行体位固定,CT 模拟定位,扫描范围为肝脏上缘上2 cm,下界为肾脏下缘。肿瘤靶区(gross tumor volume,GTV):结合CT 增强扫描、MRI、ERCP 检查综合评估,必须包括肝门区肿瘤、淋巴结以及胆管癌栓病灶;如肝脏肿瘤靠近肝门区,经评估剩余肝组织能代偿,则包括该部分的肝肿瘤,否则GTV 只包括肝门区域。给予总量46~50 Gy/23~25 F,常规分割(2 Gy/次,5 次/周)。同期使用甲磺酸阿帕替尼250 mg,1次/d,28 d为1个周期,一直服用至肿瘤进展或不可耐受。放疗开始前及放疗结束时,完善肝功能、胆红素、肾功能、血常规、尿常规等资料,并行CT、MRI 评估肿瘤情况。
1.3 观察指标及判定标准 观察患者的近期疗效及不良反应发生情况。治疗疗效果评价参照实体瘤疗效评价标准1.1 版(response evaluation criteria in solid tumor,RECIST1.1),分为完全缓解(complete response,CR)、部分缓解(partial response,PR)、疾病稳定(stable disease,SD)、疾病进展(progressive disease,PD);客观缓解率(objective response rate,ORR)=(CR+PR)/总例数×100%。疾病控制率(disease control rate,DCR)=(CR+PR+SD)/总例数×100%。按世界卫生组织(world health organization,WHO)抗癌药物毒副反应的0~4 级分度标准评价药物不良反应。
1.4 统计学方法 采用SPSS19.0 统计学软件对研究数据进行统计分析。计量资料以均数±标准差()表示,采用t检验。P<0.05 表示差异具有统计学意义。
2 结果
2.1 临床疗效 20 例患者均按计划完成放疗联合甲磺酸阿帕替尼靶向治疗。放疗结束后评估肿瘤情况,结果显示肝脏病灶CR 1 例(5.00%),PR 6 例(30.00%),SD 6 例(30.00%),PD 7 例(35.00%),ORR为35.00%,DCR 为65.00%。治疗后,患者总胆红素、直接胆红素均较治疗前明显下降,差异具有统计学意义(P<0.05)。见表2。中位PFS 为4.5 个月[95%CI=(4.28,4.72)]。见图1。
表2 20 例患者治疗前后总胆红素、直接胆红素水平比较(,μmol/L)
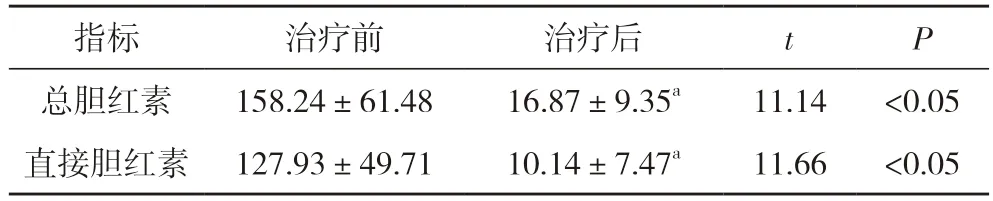
表2 20 例患者治疗前后总胆红素、直接胆红素水平比较(,μmol/L)
注:与治疗前比较,aP<0.05
2.2 不良反应 治疗期间出现最常见的不良反应有高血压(65.00%)、恶心呕吐(55.00%)、红细胞减少(50.00%)、血小板减少(35.00%)、中性粒细胞减少(30.00%)、蛋白尿(30.00%)、手足综合征(25.00%)及乏力(25.00%)。3 级不良反应主要为高血压,未出现4 级不良反应。不良反应经治疗均可控制。见表3。
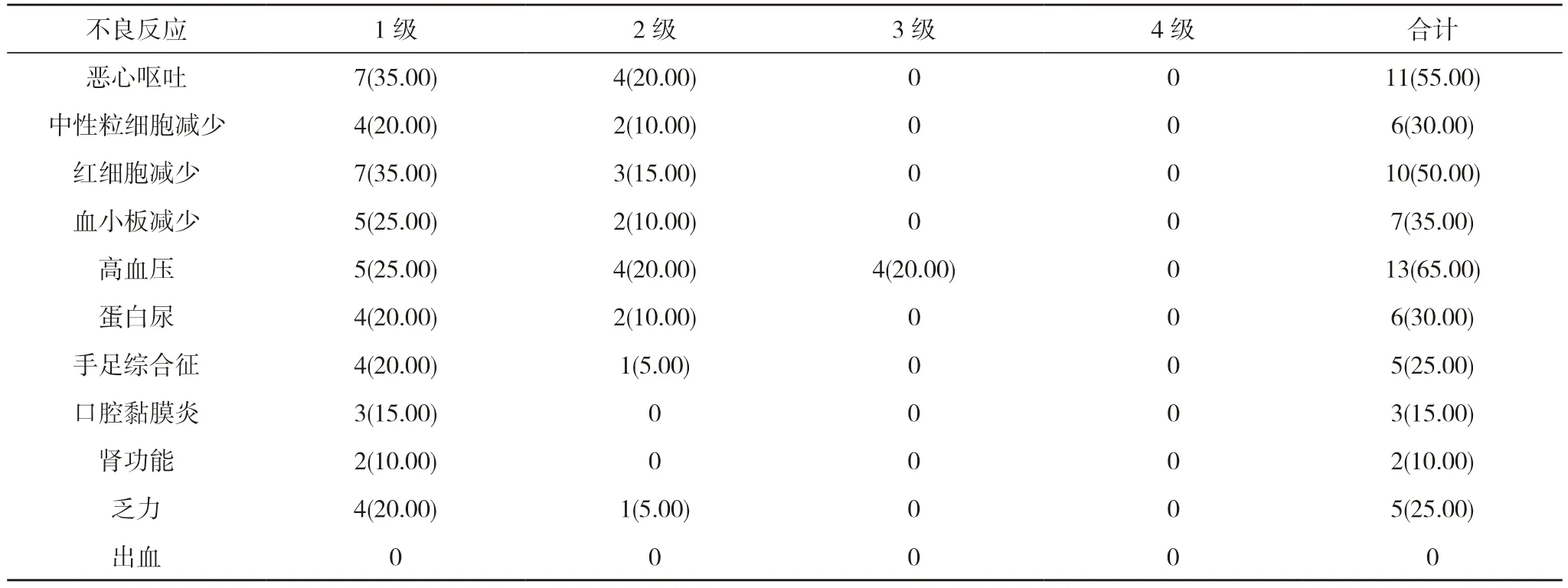
表3 20 例患者治疗期间的不良反应发生情况[n(%)]
3 讨论
HCC 在我国是常见的恶性肿瘤,梗阻性黄疸的出现提示预后不良,常见原因有肝细胞广泛坏死引起的以间接胆红素升高为主的肝细胞性黄疸,以及肝脏肿瘤侵及肝门区,或转移性淋巴结压迫胆管和胆管癌栓引起的以直接胆红素升高为主的梗阻性黄疸[7]。该类型患者预后被认为比门静脉癌栓差,可导致胆管炎、胆道出血等严重症状,并可导致肝衰竭,大部分失去根治性手术机会,以姑息治疗为主,常用解除梗阻方法有介入治疗、手术切开引流、放疗[8-10]。索拉非尼是晚期HCC 的标准一线治疗方法。Liang 第[11]的一项研究使用多模态分子成像技术,包括生物发光成像(BLI)、生物发光断层扫描(BLT)、荧光分子成像(FMI)、计算机断层血管造影(CTA),在体外和体内系统地研究和比较了阿帕替尼和索拉非尼在肝癌中的抗肿瘤和抗血管生成作用,并对两种药物的安全性和副作用进行了系统评价。结果发现,阿帕替尼在肝细胞癌中具有与索拉非尼相似的抗肿瘤和抗血管生成作用,且毒性较小。这些发现可能为阿帕替尼治疗HCC 患者提供临床证据。2020 年的ASCO 会议,公布了阿帕替尼二线治疗晚期肝细胞癌患者的随机双盲、平行对照、多中心Ⅲ期临床研究[12],并于2021 年5 月在Lancet Gastroenterol Hepatol 发表,这项研究将经过标准的一线治疗失败后的HCC 患者,按2∶1 比例随机入组,共纳入393 例患者(阿帕替尼组261 例,用药剂量750 mg,q.d.;安慰剂组132 例)。阿帕替尼组和安慰剂组中位PFS 分别为4.5 个月和1.9 个月;中位总生存期(OS)分别为8.7 个月和6.8 个月。与安慰剂相比,阿帕替尼显著延长中位OS 及PFS。临床上,对于晚期不可手术的HCC,多采用联合治疗,对于接受阿帕替尼联合TACE治疗的患者,有学者推荐口服剂量为500 mg,然而,部分患者,特别是老年患者以及肝功能欠佳患者,可能不能耐受这种剂量,有的患者不能连续服药,有的甚至不得不提前终止治疗。目前多项研究发现小剂量阿帕替尼在联合治疗恶性肿瘤方面在保证疗效的前提下,有更好的耐受性[13,14]。Xu 等[15]的研究显示,阿帕替尼联合卡瑞利珠单抗治疗晚期HCC 患者,推荐阿帕替尼用量为250 mg,不良反应主要为可控的转氨酶升高和高血压。本研究回顾性收集的患者一般状况欠佳,PS评分主要以2~3 分为主,同时伴有高胆红素血症,因此经过综合考虑,在联合放疗的过程中,采取阿帕替尼250 mg 的小剂量,在局部放射放疗解除梗阻的情况下,保证全身治疗,同时尽可能降低严重不良反应的发生风险,获得了比较理想的效果。结果显示ORR 为35.00%,DCR 为65.00%,中位PFS 为4.5 个月,该结果与相关研究相仿(ORR 为32.6%,DCR 为80.65%)[5,6]。血清总胆红素和直接胆红素水平是黄疸程度的最直接体现,能够一定程度反映胆道梗阻的情况,误差较小且易于测量,不会对患者造成额外的经济负担,因此将其作为评估梗阻缓解的指标进行定量分析。结果显示,治疗后,患者总胆红素、直接胆红素均较治疗前明显下降,差异具有统计学意义(P<0.05)。提示联合治疗有助于缓解梗阻,显著降低血清胆红素。
调强放疗联合小剂量阿帕替尼治疗的安全性及耐受性良好,出现的不良反应主要是恶心呕吐。恶心呕吐症状考虑主要与十二指肠受到射线累及照射有关。血液系统的毒性,除药物毒性及放疗不良反应外,可能与患者营养不良以及脾功能亢进有关。治疗过程中高血压发生率为65.00%,而达到3 级不良反应发生率为20.00%,这与甲磺酸阿帕替尼药物不良反应有关,这些患者经过降压治疗均可控制。但由于样本量较少,相对较高的高血压发生率是否与联合放疗相关尚需要进一步研究。
另外,本研究中GTV 结合CT 增强扫描、MRI,ERCP 检查综合评估。放疗范围包括肝门区肿瘤、淋巴结以及胆管癌栓病灶;如肝脏肿瘤靠近肝门区,若经评估考虑剩余肝组织能代偿,则包括该部分的肝肿瘤,否则GTV 只包括肝门区域,以保障患者肝脏照射在可耐受范围之内。为了尽量避免存在肝硬化基础疾病的患者在治疗期间发生急性肝衰竭,选择的患者转氨酶必须在正常或轻度升高(≤2 倍正常高值)水平。
本研究存在一些不足,主要为样本量较小,且为回顾性研究,放疗区域主要集中在肝门区域,对远隔的肝脏肿瘤照射不足,并且可能对二程放疗造成一定的影响。由于研究为回顾性分析,患者在放疗结束后行CT及MRI 进行疗效评价的时间存在差异,因此在临床疗效各方面的分析有一定局限性。如能进行前瞻性研究,增加样本量,筛选可能获益人群,将能为临床提供更好的参考。
目前关于甲磺酸阿帕替尼联合治疗的研究很多,包括联合化疗、放疗、介入治疗、免疫治疗等,许多研究证实了其获益[16],如何根据患者的病情进行个体化治疗需要更多的研究及系统的总结及指导。本研究亦为晚期肝癌,特别是体力评分较差,梗阻性黄疸明显但肝功能尚可患者的治疗提供了一种选择。
综上所述,调强放疗联合小剂量甲磺酸阿帕替尼治疗HCC 梗阻性黄疸患者,有助于解除胆道梗阻,降低血清胆红素,对肝脏原发灶有较好的客观疗效,安全性良好。
