钠插层的层状锰氧化物的制备及其电化学性能
2022-07-14黎少君王欣昱王桂玲陈俊明
黎少君, 王欣昱, 王桂玲, 陈俊明
(安徽科技学院 化学与材料工程学院,安徽 凤阳 233100)
超级电容器具有功率高,寿命长,安全,环保等优点,受到国内外广泛关注,但因其能量密度低、成本高等缺点使得超级电容的研究变得极为迫切[1-3]。电极材料作为影响电容器电容特性的一个重要因素[4],成为学者们研究的重点。
在早年前虽然人们发现二氧化钌作为电极材料具有较高的比容量,但是由于其材料价格昂贵,不利于大批量的开发利用,使得人们进行了新的研究,直到Goodenough等[5-7]首次报道非晶水和MnO2的超级电容特性,使得人们逐渐将目光投入到锰氧化物的研究中。二氧化锰材料因其具有多孔隙,易于人们做进一步探究,且材料本身价格低廉,具有高的理论比容量,资源丰富等优点,成为当下研究金属氧化物提高充放电比容量的优良选择。但是由于二氧化锰本身的电化学稳定性较弱,导电性较差,在高温下温度性控制不好,使得二氧化锰的实际比容量远远低于理论值的比容量,所以目前人们只能在具体的研究中通过掺杂来稳定二氧化锰的结构,巩固其稳定性,提高充放电比容量,从而获得高的比容量特性,来应用到工业生产当中[8-9]。
锰氧化物的结构主要是有一个共同的顶点和共面的MnO6八面体构架组成,其中锰氧化物在其内部的形态可分为一维链状、二维层状、三维网状的结构[10]。其中隧道状和层状结构的锰氧化物组成了从超微孔到介孔一个很大的孔状材料系列。层状锰氧化物因其具有特殊层状结构,可以通过在其层间插入离子或者分子,来提高电容特性[11]。
本课题研究主要从掺杂金属钠离子的探究入手,通过钠离子本身的结构具有微粒半径小,单质钠的导电导热性好,核外排布易失去一个电子达到稳定结构,可以进一步扩大层状锰氧化物的层间距,使得电荷内部交换能力增强,另外钠离子作为生活较为常见的材料,其价格便宜,资源丰富,有便于实际生活的批量运用[12]。
1 材料与方法
1.1 供试材料
1.1.1 药品及试剂 高锰酸钾(≥99.9%,国药集团化学试剂有限公司);无水硫酸钠(≥99.6%,国药集团化学试剂有限公司);无水乙醇(≥99.7%,国药集团化学试剂有限公司);乙炔黑(天一世纪化工产品有限公司);聚四氟乙烯(≥99.9%,广州市兴胜杰科技有限公司);氢氧化钾(≥85.0%,国药集团化学试剂有限公司);葡萄糖(≥99.9%,国药集团化学试剂有限公司)。
1.1.2 仪器 CT-3008W-5V3A-S4型充放电测试仪(深圳新威尔有限公司);XRD(Cu-Ka靶的日本电子Smart Lab);SEM(蔡司EVO18)及其配套EDS设备;法兰式水热釜(济南恒化科技有限公司);CHI660E型电化学工作站(上海辰华仪器公司)。
1.2 实验方法
1.2.1 样品制作 取0.79 g高锰酸钾溶于25 mL水中,加入1.8 g葡萄糖后搅拌10 min,加入25 mL无水乙醇,搅拌均匀加入1.8 g氢氧化钾结晶体,搅拌均匀之后掺杂入不同摩尔比例(相对于KMnO4)的(0%、30%、50%、65%、70%和80%)无水硫酸钠晶体,搅拌10 min至完全溶解,放入反应釜中在烘箱中180 ℃保温12 h,冷却至室温后减压过滤,将得到的沉淀物80 ℃烘干12 h,然后将样品400 ℃烧结4 h,得到最终产物。
1.2.2 极片制作 将活性物质(上述样品制作中的最终产物)∶乙炔黑∶PTFE按75∶20∶5的质量比例配制,将活性物质与PTFE先放入烧杯,加入少量无水乙醇,使其混合均匀,进行磁力振动,再将乙炔黑逐渐放入烧杯,与其混合均匀,将混合好的样品放入80 ℃恒温水浴锅中微沸破乳,当悬浊液变为黏稠状物质时,取出备用。
将该粘稠物涂抹在1 cm*1cm的泡沫镍上,制备成研究电极,之后烘干4 h。最后将烘干完成的极片用压片机压平,浸泡在6 mol/L的氢氧化钾溶液中6 h,等待测试。
1.2.3 材料测试 材料结构分析采用D-max-2500/PC型X-射线衍射仪(XRD),材料形貌分析采用日立S-4800场发射扫描电子显微镜(SEM)和日本Hitachi的HT7700型透射电子显微镜(TEM)。元素含量分析采用岛津EDX-8100型能量色散型X射线荧光分析仪(EDX),材料的电化学测试以制备好的活性物质电极为研究电极,铂片电极为对电极,Hg/HgO电极为参比电极,6 moL/L KOH为电解液,根据测试其的电容特性,做进一步探究。
2 结果与分析
2.1 样品XRD测试
图1是不同比例的钠离子掺杂下锰氧化物的XRD图像,该样品对应(PDF#39-1218)的锰氧化物Mn5O8,出现的三个主要的衍射峰是在2θ为18.11°、31.193°和36.696°处,对应晶面的分别为(100)(020)(400),并且可以发现在加入钠离子后没有出现新的衍射峰,说明钠离子没有单独成相[13]。并通过图像观察,在钠加入量为65%时,衍射峰出现略微的向低角度偏移,经EDX检测结果(表1)可知4个样品的Na+相对于锰的原子量分别为0%、9.56%、10.24%和16.37%,推测可能是由于钠离子的加入使层状锰氧化物的层间距加大,使衍射峰发生向左偏移[14-17]。
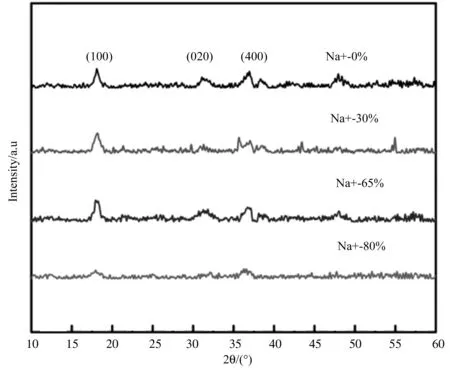
图1 不同摩尔含量钠掺杂量下的锰氧化物的XRD图谱

表1 不同摩尔含量钠掺杂量下各元素的原子含量百分比
2.2 样品SEM测试
如图2a、2b、2c、2d是不同比例的钠离子加入(0%、30%、65%、80%)下锰氧化物的SEM图像。通过图2a、2b、2c可以看到在低的钠摩尔比加入量下(0%~65%),产品均为规则的六边形片状结构,且在加入钠离子之后团聚现象下降,较未掺杂时更加蓬松,且在钠加入量为65%时,材料最蓬松。而在较多的钠离子掺杂量(图2d)片状结构不明显,团聚加剧,可见需要在适当的钠离子加入量下,对锰氧化物的层状结构有积极影响,过多时,反而会具有不利影响,具体原因在后续实验中将会继续探究。
2.3 样品的TEM测试
为了更好地分析在65%钠离子加入量下锰氧化物表观形貌,进行了TEM扫描测试,如图3a所示,材料表现较为规则的六边形片层结构,未出现片的破裂,片的大小约为300 nm。图3b是图3a中圆圈部分的局部放大图,通过此图可以更清楚地看到六边形片的表面状态,如图3c是六边形片的垂直方向,图像显示在65%钠加入下锰氧化物呈现六角形片状结构,片层厚度约为19.41 nm。如图3d发现六边形片的表面含有大量微孔,这些微孔既可以通过增大材料与电解液的接触面积来提高活性位点数量,又可以通过缩短离子的扩散路径来提高材料的倍率特性[18-20]。
2.4 样品电容特性研究
图4是电流为1 A/g时,不同钠离子掺杂量下样品的循环寿命曲线,通过图可以看到所有样品的循环稳定性都比较好,300圈循环后几乎没有容量衰减。尤其需要注意的是在钠离子加入量为65%时,具有最高的放电比容量约为206.062 F/g。为了更清楚地知道材料的循环稳定性,做了其长循环寿命曲线,结果如图4b所示,通过图4b可以看到1 000圈循环后,材料的放电比容量保持率仍能达到100%。图4b插图是电流密度在1 A/g时的充放电曲线,IR降为5.505 mV,说明此时材料内阻较小。这可能是由于钠掺杂增大了锰氧化物层间距,离子传输速度得到提高,使得放电比容量增加,当循环次数增加至1 000圈时,放电比容量始终稳定在一个较高值,说明总体表征性能良好,且未出现脱落现象,说明钠插层有效地提高了材料的电容特性[21-22]。

图3 加入65%钠的锰氧化物的不同放大倍数TEM图
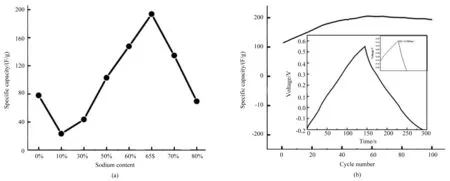
图4 (a)加入不同摩尔比例钠的锰氧化物的放电比容量图, (b)加入65%钠的锰氧化物的1 000次循环的放电比容量图(其中插图为在1 A/g电流密度下的充放电曲线图) Fig.4 (a) Discharge specific capacity diagram of manganese oxide doped with different molar ratios of sodium, (b) Discharge specific capacity diagram of manganese oxide doped with 65% sodium for 1 000 cycles
如图5a所示,不同比例的钠离子加入量(0%、30%、65%、80%)下样品在5 mV/s的扫描速度下的循环伏安曲线,循环伏安的电压范围为-0.2~0.55 V,涂覆的活性物质的质量约为3 mg。从图像可以看到,样品均表现较好的准矩形特征,在钠加入量为65%时,具有最大的矩形面积(即最大的比容量),在0.1~0.15 V时出现一个还原峰,对应在0.3~0.4 V时出现一个氧化峰,这可能是由于钠加入过程中增加了层与层之间的层间距,从而更加有利于电解液的进入,使得材料具有更加优良的赝电容特性。图5b是钠加入量为65%时,在5、10、20、50、100、200 mV/s的扫描速度下的循环伏安曲线,扫描范围为-0.2~0.55 V,通过图可以看出,在不同扫描速度下,在钠加入量为65%时呈现规则的准矩形特征,随扫描速度的增加准矩形的面积呈线性增加趋势,且在200 mV/s仍表现较好的准矩形特征,说明在钠加入量为65%时的样品具有良好的倍率特性[23]。
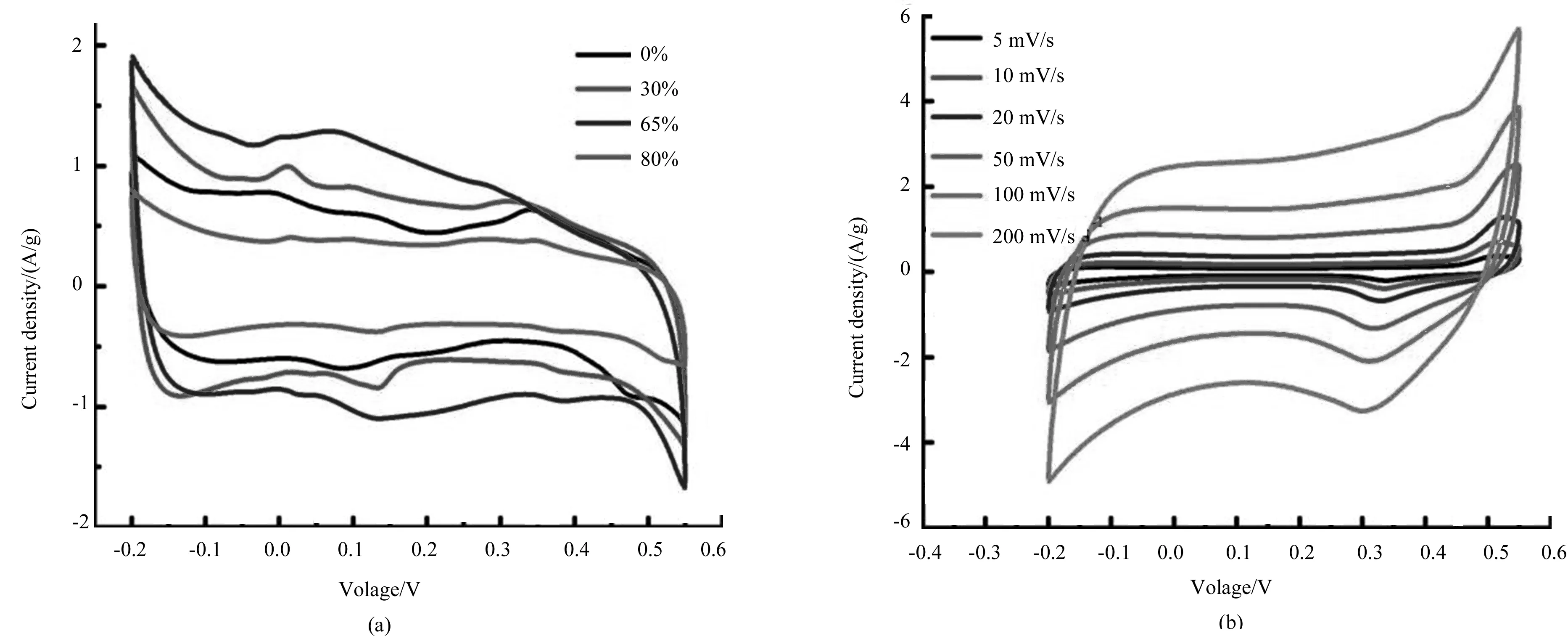
图5 (a)加入不同摩尔比例钠的锰氧化物的循环伏安曲线(扫描速率为5 mV/s), (b)65%钠离子加入量的锰氧化物在不同扫描速率下的循环伏安曲线 Fig.5 (a) Cyclic voltammetric curves of manganese oxide doped with different molar ratios of sodium (scan rate is 5 mV/s), (b) Cyclic voltammetric characteristics of manganese oxide doped with 65% sodium at different scan rates
如图6所示 钠加入量在0%、65%、80%时材料的交流阻抗谱图,可以观察到加入钠后,如小图高频区的未掺杂较钠掺杂为65%时的材料半圆直径并未发生较大的改变;在低频区的直线部分,可以观察到钠加入之后样品的直线斜率更靠近90°,更高的斜率对应更快的离子反应时间,说明钠插层能够增大层间距,可以使材料与电解液之间电荷转移阻力变小,提高材料的电容特性。而在较多的钠加入80%时,斜率增大,且电阻增大。说明掺杂过多的钠反而对电容特性具有不好的影响。在钠加入量为65%时,斜率最大,对应更小的溶液电阻,说明在此加入量下的材料的电容特性最好。
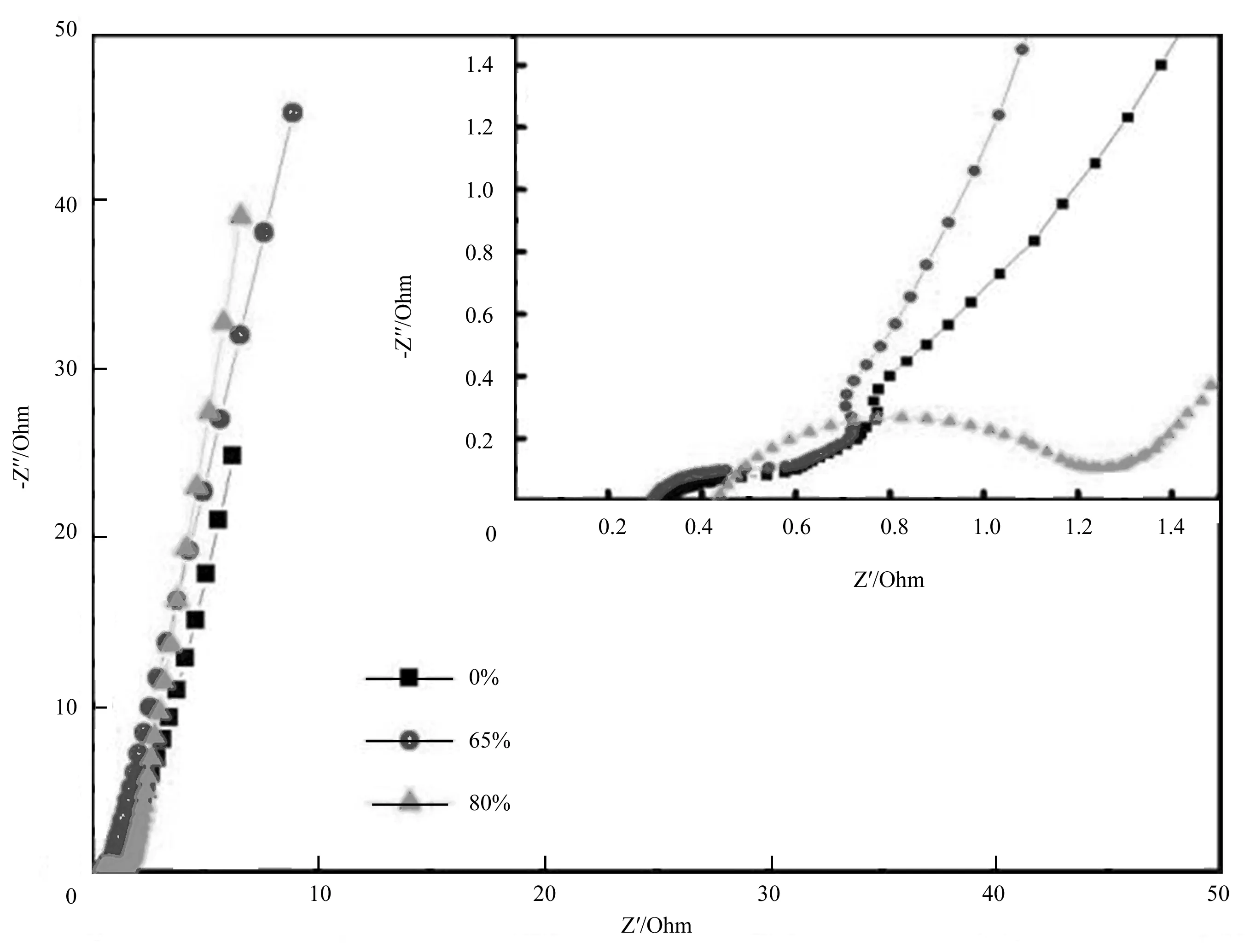
图6 加入不同摩尔比例钠的锰氧化物的电化学阻抗谱(EIS)
3 结论
本研究以高锰酸钾为氧化剂,葡萄糖为还原剂,水热结合低温烧结法制备钠掺杂于层状结构锰氧化物,通过对材料电容特性及性能表征的一系列探究,得到以下结论:
(1) XRD显示,材料在(100)晶面处呈现较好峰值,且在最佳钠含量下衍射峰(100)较未掺杂时左移,说明钠的掺杂增大了层状锰氧化物的层间距,有利于材料与电解液之间的电荷转移速度的提高。
(2) SEM显示,钠掺杂量为65%时材料微观形貌呈片层结构,团聚现象较未掺杂时下降,且微观表征蓬松。为了更为直观观察,测试了材料的表观形貌。通过TEM图像,更加直观地显示在钠掺杂为65%时,材料呈现规则的六边形片层结构,并显示片的大小约为300 nm,片层的厚度约为19.41 nm。
(3) 电容特性图像显示,当钠离子加入量为65%时,具有最优的放电比容量在1A/g电流密度下约为206.062 F/g,1 000圈后容量保持率仍达100%。CV图像显示,钠掺杂65%具有最大的矩形面积,且在高的扫描速度下具有良好的倍率特性,EIS显示,钠掺杂量65%时材料的斜率较未掺杂时更靠近90°,结果显示,在钠离子加入量为65%时钠掺杂具有较好的电化学特性。