4′-氯-7-[2-(哌嗪-l-基)乙氧基]异黄酮的合成及分析方法的建立
2022-07-14连孟强刘娅琛郭春燕
连孟强 刘娅琛 郭春燕
摘要:為解决天然大豆苷元(daidzein,DAI)抗肿瘤活性不足的问题,对DAI的4′位和7位进行结构修饰。首先,以间苯二酚和对氯苯乙酸为起始原料,经傅克酰基化、增碳关环反应制备4′-氯-7-羟基-异黄酮,将4′-氯-7-羟基异黄酮依次与二溴乙烷、哌嗪通过取代反应制备目标化合物4′-氯-7-[2-(哌嗪-l-基)乙氧基]异黄酮(3-(4-chlorophenyl)-7-[2-(piperazin-l-yl)ethoxy]-4H-chromen-4-one,CPEO-43),采用柱层析方法实现目标产物与杂质的分离。其次,通过FT-IR,MS,1H-NMR及13C-NMR确证结构。再次,通过MTT实验评价化合物CPEO-43对A549肺癌细胞和HCT116结肠癌细胞的抑制作用。最后,建立CPEO-43血浆样品的超高效液相色谱(ultra high performance liquid chromatography,UPLC)分析方法。结果表明,通过FT-IR,MS,1H-NMR及 C-NMR确证了所合成的化合物与目标化合物结构一致。10 μmol/L DAI对A549肺癌和HCT116结肠癌细胞的抑制率分别为4.421%和5.601%;而相同浓度的CPEO-43对A549肺癌细胞和HCT116结肠癌细胞抑制率分别为58.43%和72.03%,IC值分别为2.51 μmol/L和0.87 μmol/L。建立的UPLC方法无内源性物质干扰,在0.5~10 μg/mL范围内线性关系良好,日内精密度及日间精密度均小于10%,化合物CPEO-43的低、中、高浓度的血浆样品的回收率为92.98%~100.10%。化合物CPEO-43的抗肿瘤活性显著高于DAI,UPLC分析方法能简便快速地测定血浆中CPEO-43的含量,结果准确可靠,可为提高DAI的抗肿瘤效果提供理论依据,为药物临床检测提供方法基础。
关键词:药学其他学科;大豆苷元;大豆异黄酮衍生物;抗肿瘤活性;超高效液相色谱;核磁共振;质谱
中图分类号:R917文献标识码:A
DOI:10.7535/hbkd.2022yx03010
Synthetic and analytical method establishment of 3-(4-chlorophenyl)-7-[2-(piperazin-l-yl)ethoxy]-4H-chromen-4-one
LIAN Mengqiang LIU Yachen GUO Chunyan
(1.School of Pharmacy,Hebei North University,Zhangjiakou,Hebei 075000,China;2.School of Life Science,Hebei Normal University,Shijiazhuang,Hebei 050024,China)
Abstract:In order to solve the problem of insufficient antitumor activity of natural daidzein (DAI),the 4 'and 7 positions of DAI were modified.Firstly,3-(4-chlorophenyl)-7-hydroxy-4H-chromen-4-one was prepared from resorcinol and p-chlorophenylacetic acid by friedel crafts acylation,carbonization and ring closing reaction.The 3-(4-chlorophenyl)-7-[2-(piperazin-l-yl)ethoxy]-4H-chrome-4-one (CPEO-43) was synthesized by substitution reaction of 3-(4-Chlorophenyl)-7-hydroxy-4H-chromen-4-one with dibromoethane and piperazine.Column chromatography was used to separate the target product from impurities.Secondly,FT-IR,H-NMR,C-NMR and MS were used to identify the compounds.Thirdly,MTT assay was used to detect the inhibitory effect of compound CPEO-43 on A549 lung cancer cells and HCT116 colon cancer cells.Finally,an ultra high performance liquid chromatography (UPLC) method was established for the analysis of CPEO-43 plasma samples.The results show that the structure of the synthesized compound is consistent with that of the target compound confirmed by FT-IR,MS,1H-NMR and 13C-NMR.The inhibitory rates of DAI (10 μmol/L) on A549 lung cancer and HCT116 colon cancer cells are 4.421% and 5.601%,respectively.The inhibitory rates of the same concentration of CPEO-43 on A549 lung cancer cells and HCT116 colon cancer cells are 58.43% and 72.03%,respectively.The IC values of CPEO-43 are 2.51 μmol/L and 0.87 μmol/L,respectively.The established UPLC method has no interference from endogenous substances.The linear relationship is good in the range of 0.5~10 μg/mL.The intra-day precision and inter-day precision are less than 10%.The average recoveries of low,medium and high plasma samples of compound CPEO-43 are in the range of 92.98%~100.1%.The antitumor activity of compound CPEO-43 is significantly higher than that of DAI.The established UPLC assay method can easily and rapidly determine the content of CPEO-43 in plasma,and the results are accurate and reliable,provide a theoretical basis for improving the antitumor activity of DAI,and provide method basis for drug clinical testing.
Keywords:
other disciplines of pharmacy;daidzein;soybean isoflavone derivatives;antitumor activity;ultra high performance liquid chromatography;nuclear magnetic resonance;mass spectrum
癌症是全球第2大死亡原因,2018年约有960万人死于癌症,占死亡人数的1/6。肺癌、前列腺癌、结肠直肠癌、胃癌和肝癌是男性最常见的癌症类型,而乳腺癌、结肠直肠癌、肺癌、宫颈癌和甲状腺癌在女性中最为常见。肺癌和结肠直肠癌在男性和女性中都是最常见的癌症类型。研究表明,饮食富含异黄酮的食物可以降低许多癌症的发病率和死亡率[1-9]。人体中异黄酮的主要饮食来源是大豆和豆制品,大豆异黄酮的主要结构是以3-苯并吡喃酮为母核的化合物群[10-11],分为游离型的苷元和结合型的糖苷2种[12-13]。近年来,游离型苷元大豆苷元(daidzein,DAI)的生物活性,特别是抗癌活性引起了人们的极大关注[14-17]。DAI对A549肺癌细胞半数致死量(IC)为32.18 μmol/L[17]。大豆异黄酮在大豆中的含量为0.1%~0.5%,而游离型苷元仅占大豆异黄酮含量的5%~10%,仅仅依靠饮食富含异黄酮的食物抑制癌细胞的生长是不现实的。
基于DAI抗肿瘤活性不足的缺点,本研究旨在对DAI进行结构修饰,以提高其抗肿瘤活性。大豆异黄酮活性具有结构依赖性[11],从理论上分析,DAI的4′位和7位引入活性基团可以增加活性。因此,在4′位引入卤族元素Cl,在7位引入哌嗪基团,合成大豆异黄酮衍生物4′-氯-7-[2-(哌嗪-l-基)乙氧基]異黄酮(3-(4-chlorophenyl)-7-[2-(piperazin-l-yl)ethoxy]-4H-chromen-4-one,CPEO-43),通过体外细胞实验研究CPEO-43抗肿瘤活性,并建立CPEO-43的超高效液相色谱(ultra high performance liquid chromatography,UPLC)分析方法。
1仪器与材料
1.1主要仪器
核磁共振仪WIPM-NMR-400(中科牛津波谱技术有限公司);酶标仪SpectraMax25 (Molecular Devices);电子分析天平ME235P(德国Sartorius);AB Sciex QTRAP 4500液质联用仪(LC-MS,日本岛津);紫外可见分光光度计UV9100(北京莱伯泰科仪器股份有限公司);傅里叶红外光谱仪(德国Bruker);ACQUITY UPLC色谱仪(美国Waters)。
1.2材料
A549肺癌细胞和HCT116结肠癌细胞,河北北方学院药学系实验室保存。
SD雄性大鼠(250 g),购自北京华阜康,饲养温度为(25±2) ℃,湿度为(50±2)% 。
三氟化硼乙醚(批号 RH328089)、五氯化磷(批号 DX6RRR1A PCl),购自安耐吉;间苯二酚(批号 F2002009)、二溴乙烷(批号 F1808053)、4-氯苯乙酸(批号 B1826138),购自阿拉丁;哌嗪(批号 LMB0S39)、碘化钠(批号 LDB0S31),购自百灵威;碳酸钾、N,N-二甲基甲酰胺(DMF)、乙酸乙酯、石油醚等常规有机试剂,购自天津永大;DMEM 高糖培养基,购自Gibco公司;胎牛血清(FBS),购自ZATA公司;DAI,购自上海源叶生物科技有限公司;MTT试剂盒,购自Solarbio公司。
2实验方法
2.1化合物CPEO-43的合成与表征
2.1.1合成方法
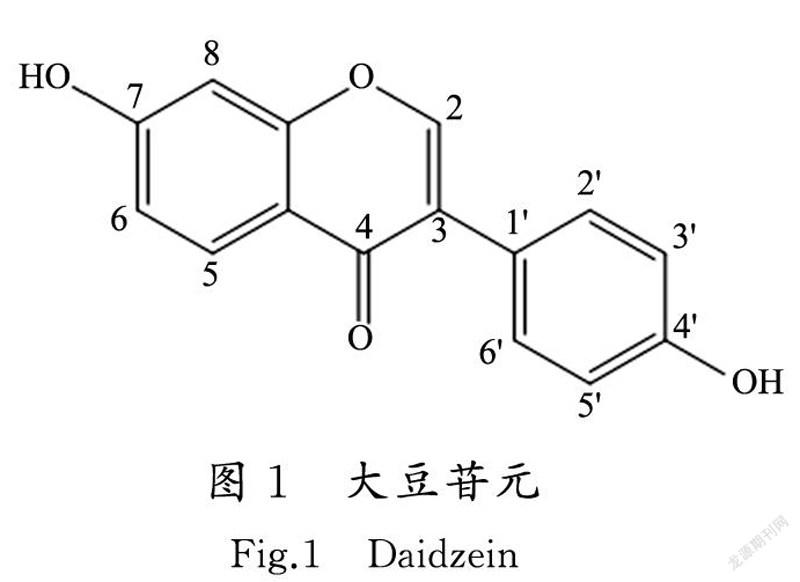
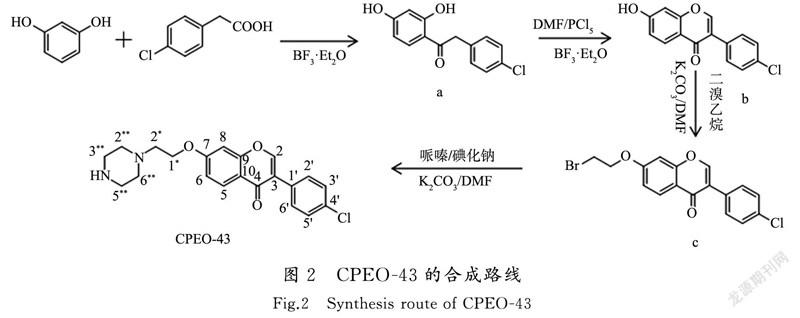
以天然DAI结构(如图1所示)为母核,对4′和7位进行结构优化,增加DAI的抗肿瘤活性。4′位引入Cl能够保证后续取代反应仅发生在7位,防止副反应发生,提高产率。另外,哌嗪是含氮杂环体系中的重要一员,环上的 N 原子可以参与生物体中氢键的形成,增加药物与受体的亲和力和选择性[18],因此在7位引入哌嗪增加了DAI的生物活性。合成过程中并未以DAI为起始原料,因为直接购买DAI成本较高,若从植物中提取,过程较为繁琐且收率较低[19-20],且以DAI为原料进行取代反应时,4′位及7位均可能发生取代反应,难以制备单一的4′-氯-7-羟基异黄酮(图2中b),进而影响后续中间产物4′-氯-7-溴乙氧基异黄酮和目标化合物CPEO-43的合成。因此,参照文献[21-22]设计了CPEO-43合成方案,如图2所示。
CPEO-43的合成:对氯苯乙酸在路易斯酸三氟化硼催化下形成C,具备较强的吸电子能力,与富电子基团间苯二酚发生傅克酰基化反应,生成脱氧安息香(图2中a)。化合物a反应溶液在DMF/PCl条件下生成中间产物4′-氯-7-羟基异黄酮(图2中b)。化合物b的酚羟基在碱性条件下生成氧负离子,溴代烷烃与氧负离子发生亲电取代反应,生成4′-氯-7-溴乙氧基异黄酮(图2中c)。再利用碘化钠作为催化剂,与化合物c反应,生成反应活性更强的碘取代物,碱性条件生成C,与哌嗪发生亲核取代反应,生成CPEO-43。使用柱层析方法,采用甲醇-二氯甲烷作为洗脱溶剂梯度洗脱,纯化化合物CPEO-43。具体过程如下。
4′-氯-7-羟基异黄酮的合成:将间苯二酚(10 mmol)和对氯苯乙酸(11 mmol)溶于三氟化硼乙醚(80 mmol)中,于85 ℃条件下磁力搅拌4 h,冷却,缓慢加入DMF(10 mL),生成脱氧安息香(图2中a)。向化合物a反应溶液中加入DMF(20 mL)/PCl(15 mmol)混合溶液,室温搅拌3 h,倒入沸腾的0.1 mol/mL HCl水溶液中,冷却、过滤、干燥得粗产物4′-氯-7-羟基异黄酮,再经乙醇重结晶纯化。
4′-氯-7-溴乙氧基异黄酮的合成:将化合物b(10 mmol)、碳酸钾(25 mmol)、二溴乙烷(52 mmol)加到DMF(50 mL)中。氮气条件下,80 ℃反应3 h,冷却后倒入冰水中,过滤、干燥得到粗产物4′-氯-7-溴乙氧基异黄酮,再经乙醇重结晶纯化。
CPEO-43的合成:将化合物c(10 mmol)、碘化钠(10 mmol)、哌嗪(12 mmol)、碳酸钾(35 mmol)加到DMF(100 mL)中,氮气条件下,60 ℃反应3 h,冷却后倒入冰水中,过滤、干燥得到化合物CPEO-43粗产物,再经二氯甲烷-甲醇梯度洗脱纯化(9∶1~3∶1)。
2.1.2化合物CPEO-43结构鉴定
通过FT-IR,MS,1H- NMR及C-NMR鉴定合成化合物CPEO-43的结构。取适量CPEO-43,加入溴化钾研磨后压片,在400~4 000 cm-1范围内测定红外吸收光谱。称取适量CPEO-43,加入DMSO氘代试剂,进行核磁共振氢谱及碳谱检测。
配制质量浓度约为5 ng/mL的 CPEO-43甲醇溶液,采用电喷雾离子源(ESI),以多反应监测模式(MRM)进行正离子(H)检测;喷雾电压为3 000 V;喷雾温度为500 ℃,m/z385.0→113.1(CPEO-43)进行质谱检测,观察样品溶液在m/z为385.0的离子片段下的吸收峰。
2.2化合物CPEO-43抗肿瘤活性实验
2.2.1细胞培养
A549肺癌细胞和HCT116结肠癌细胞用含10% FBS及1% 青霉素-链霉素(penicillin-streptomycin solution,PS)的DMEM高糖培养基,置于37 ℃,5% CO培養箱中培养,每2~3 d用胰酶消化液消化传代。
2.2.2MTT法检测细胞活性
实验分为溶剂组(以DMSO为溶剂)、阳性药对照组(以DAI为阳性对照药)、CPEO-43实验组和空白组(不加细胞,只加培养基)。取对数生长期的A549和HCT116细胞计数后均匀铺于96孔板,每孔8 000细胞,在37 ℃,5% CO细胞培养箱中培养24 h后,按照上述分组给药处理。
除空白组不含细胞外,其余每组加药之前含有相同数量的细胞,溶剂组、阳性药对照组、CPEO-43实验组中含有相同浓度的DMSO,终浓度为0.1%;阳性药对照组DAI终浓度为10 μmol/L;CPEO-43实验组设置8个浓度,CPEO-43终浓度分别为0.01,0.03,0.25,0.5,1,2,4,10 μmol/L。细胞给药后于培养箱中培养72 h,吸弃上清,加入90 μL新鲜培养液,加入10 μL MTT溶液,继续培养4 h,吸弃上清,加入110 μL Formazan溶液,置摇床上低速振荡10 min,使结晶物充分溶解,用酶标仪在波长490 nm处测定光密度值(optical density,OD),根据公式计算抑制率。抑制率%=(OD-OD)/(OD-OD)×100%。
2.3化合物CPEO-43的UPLC方法的建立
2.3.1色谱条件
ZORBAX Eclipse Plus C(4.6 mm×150 mm,5 μm)色谱柱;流动相为甲醇(A)-0.025%(体积分数)甲酸水溶液(B),流速:1 mL/min,柱温:35 ℃,进样量:5 μL。洗脱条件:0~2.5 min,46% A;2.5~8.0 min,46%~52.3% A;8.0~8.5 min,52.3%~59.5% A;8.5~12.0 min,59.5%~73% A;12.0~13.0 min,73%~46% A;13.0~15.0 min,46% A。检测波长:254 nm。
2.3.2标准溶液的配制
精密称取10 mg 化合物CPEO-43,加甲醇溶解,制成1 mg/mL的CPEO-43标准储备液,于-20 ℃下保存备用。临用时,用起始流动相稀释至所需浓度即可。
2.3.3血样采集
大鼠摘眼球取血,将血液采集至抗凝离心管中,摇匀,4 000 r/min离心10 min。
2.3.4血浆样品预处理
取血浆样品100 μL,置于离心管中,再加入900 μL甲醇,涡旋3 min,充分沉淀蛋白,再于4 ℃下以15 000 r/min离心10 min,取上清液,氮气条件下吹干,再用100 μL 50%甲醇水复溶,15 000 r/min离心10 min,取上清液,微孔滤膜过滤,待测。
2.3.5方法学考察
1)专属性考察
分别取大鼠空白血浆和含CPEO-43药物血浆,按“2.3.4”所述方法处理样品,进样分析,记录色谱图,考察血浆中内源性物质是否会干扰被测物质CPEO-43的测定。
2) 线性关系与定量限考察
取空白血浆100 μL,加入不同浓度的化合物CPEO-43,按“2.3.4”所述方法处理,制备CPEO-43标准系列溶液,按照上述色谱条件进样分析,记录峰面积。以质量浓度为横坐标,峰面积为纵坐标,进行线性回归。以信噪比10对应的CPEO-43浓度确定方法定量限。
3)准确度和精密度考察
参照《中华人民共和国药典》2020版第4部生物样品定量分析方法验证指导原则(以下简称指导原则)[23],配制定量下限0.5 μg/mL及低(1.00 μg/mL)、中(4.00 μg/mL)和高浓度(7.50 μg/mL)质控样品,每个浓度5个样本。按照上述色谱条件进样,连续测定3 d。准确度以测定值与质控样品标示值的差值表示,差值控制在±15%之内,定量下限准确度应在标示值的±20%范围内。同一批内低、中、高浓度的日内精密度的标准偏差RSD值和不同批的低、中、高浓度的日间精密度的RSD值均不得超过15%,定量下限的RSD值均不得超过20%。
4)提取回收率实验考察
取空白血浆100 μL,加入适量的化合物CPEO-43,按“2.3.4”项方法处理,制成终浓度分别为0.5,4.0,10.0 μg/mL的CPEO-43血浆样品,每个浓度平行制备5份,进样分析,记录峰面积A1;另取空白血浆,按“2.3.4”项方法处理。准确移取取上清液,加入适量化合物CPEO-43,使终浓度分别为0.5,4.0,10.0 μg/mL,旋涡混匀,氮气吹干。然后,加入100 μL 起始流动相复溶,微孔滤膜过滤,进样分析,记录峰面积A2。以A1与A2的比值进行回收率计算。
5)稳定性考察
参照3)方法制备定量下限0.5 μg/mL及低(1.00 μg/mL)、中(4.00 μg/mL)和高浓度(7.50 μg/mL)质控样品,分别于室温下放置8 h,4 ℃保存3 d和-20 ℃保存10 d,在上述色谱条件下检测,考察样品的稳定性。含量与初始值的偏差不得超过±15%。
2.4统计分析方法
用GraphPad Prism v8.0.2.263,计量资料数据以均数±标准差表示,计数资料以百分率表示,p<0.05为差异有统计学意义。
3结果与分析
3.1化合物CPEO-43的合成与表征
目标化合物的合成分为3步:1)间苯二酚和对氯苯乙酸在三氟化硼乙醚作用下生成脱氧安息香(a);2)a溶液在DMF/PCl催化下完成增碳反应生成中间产物b,产率为50%;3)化合物b在碱性条件下完成烷烃取代反应得到中间体c,产率为61%。化合物c与哌嗪反应得到含有哌嗪和异黄酮结构的化合物CPEO-43,产率为54%,总产率为 16.5%
CPEO-43制备过程中,中间产物b和c利用乙醇进行重结晶能够有效提纯,方法简单。但终产物CPEO-43通过乙醇重结晶后,产物混有杂质,结合终产物与其他杂质极性大小的差异,选择甲醇-二氯甲烷作为流动相进行梯度洗脱,可实现产物与杂质的有效分离。
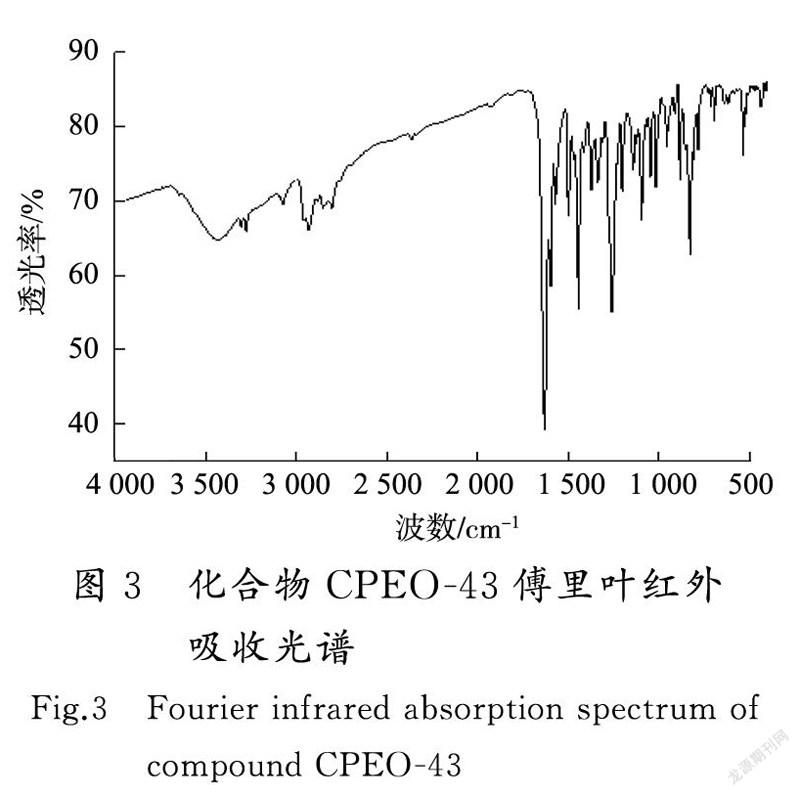
利用FT-IR鉴定化合物CPEO-43的官能团。如图3所示,化合物CPEO-43主要吸收峰如下:3 424 cm为NH的伸缩振动,1 627 cm为C=O的伸缩振动,1 335 cm为C-N伸缩振动,1 257 cm为=C-O-C伸缩振动,1 371 cm和1 201 cm为苯环的骨架振动产生的吸收峰,1 044,954,882,826 cm为苯环上的=C-H的弯曲振动所产生。
MS,H-NMR及C-NMR对化合物CPEO-43结构鉴定结果为:MS (CIHONCl):385 (M+H)+。1H-NMR(400 MHz,DMSO) δ 8.51(s,1H),8.01(d,J= 8.8 Hz,1H),7.62(d,J = 8.0 Hz,2H),7.49(d,J = 7.9 Hz,2H),7.20(s,1H),7.09(d,J = 8.9 Hz,1H),4.22(s,2H),2.68(s,6H),2.40(s,4H),1.21(s,1H)。13C-NMR(101 MHz,DMSO)δ 154.90(C-2),122.95(C-3),174.67(C-4),127.35(C-5),115.76(C-6),163.53(C-7),101.64(C-8),157.87(C-9),117.90(C-10),131.30(C-1′),131.09(C-2′,6′),128.61(C-3′,5′),133.01(C-4′),66.82(C-1′′),54.81(C-2′′), 57.54(C-2′′′,6′′′), 45.90(C-3′′′,5′′′)。
3.2化合物CPEO-43對癌细胞存活率的影响
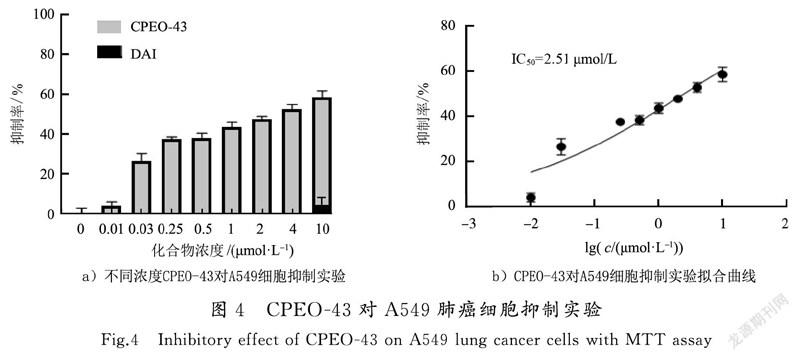
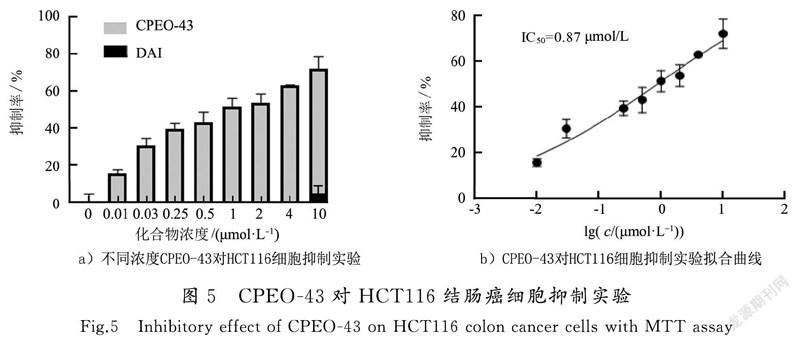
如图4和图5所示,与溶剂对照组相比,DAI对A549肺癌细胞和HCT116结肠癌细胞具有抑制作用,然而抑制率较低,结构优化后,CPEO-43对癌细胞的抑制作用显著增加。
由图4和图5可知,10 μmol/L DAI对A549肺癌和HCT116结肠癌细胞的抑制率分别为4.421%和5.601%;而相同浓度新合成的化合物CPEO-43对A549肺癌细胞和HCT116结肠癌细胞抑制率分别为58.43%和72.03%,该浓度下化合物CPEO-43对A549肺癌细胞和HCT116结肠癌细胞抑制率分别是DAI的13.2倍和12.9倍。表明化合物CPEO-43能够显著抑制A549肺癌细胞和HCT116结肠癌细胞生长,IC值分别为2.51 μmol/L和0.87 μmol/L。
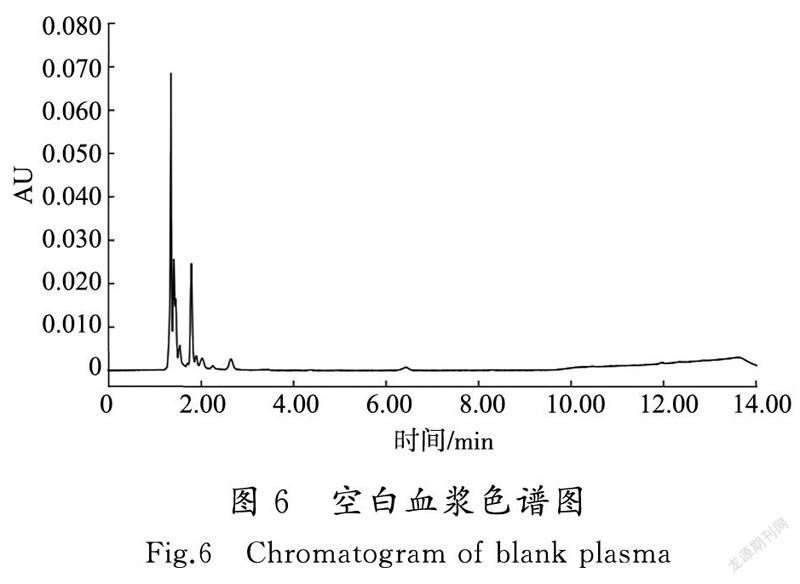
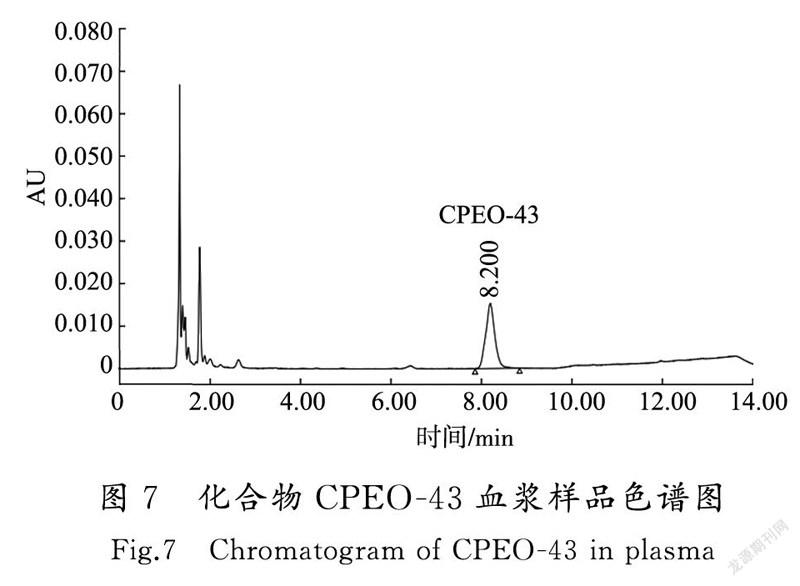
3.3化合物CPEO-43色谱分析专属性结果
如图6和图7所示,化合物CPEO-43的保留时间为8.2 min,峰形良好,无血浆杂质干扰。
3.4线性关系与定量限
以质量浓度(x,μg/mL)为横坐标,峰面积(y)为纵坐标进行线性回归: y=21 403x+356.08(R=0.999 9)。线性范围:0.5~10 μg/mL。利用信号噪音比值法确定定量限,信噪比为10时样品质量浓度为0.5 μg/mL。
3.5准确度和精密度
本方法的CPEO-43定量下限、低、中、高血浆样品的日内精密度和日间精密度RSD值分别为8.19%,3.27%,0.53%,0.53%和8.91%,5.90%,4.22%,2.35%,均小于《中华人民共和国药典》指导原则的15%。实测值与质控样本标示值的差值亦符合指导原则方法验证的要求。结果表明,本方法的准确度和精密度能够满足CPEO-43的分析要求。
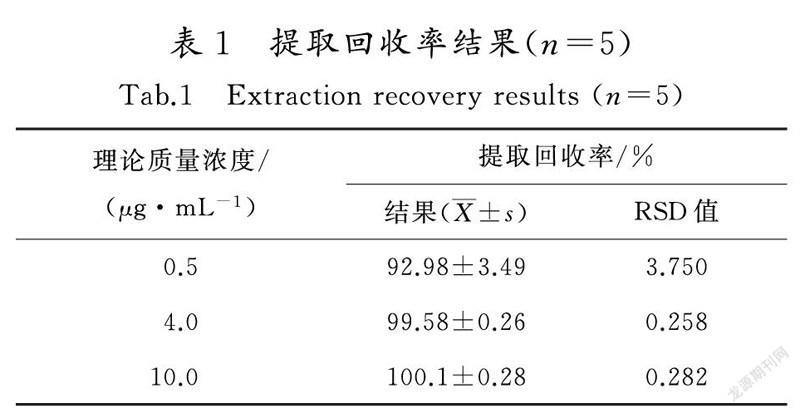
3.6回收率實验结果与分析
如表1所示,低、中、高3种质控浓度的样品的提取回收率在92%~100%,RSD值均小于5%,回收率满足分析要求。
3.7稳定性
将化合物CPEO-43低、中、高3个浓度质控样品于室温下放置8 h,4 ℃保存3 d和-20 ℃保存10 d后实验测得的各个浓度的含量与初始值相差均不超过10%,符合指导原则不超过±15%的要求,这表明该方法制备的样品在上述条件下是稳定的。
4结语
准确测定生物基质(如全血、血清、血浆、尿)中的药物浓度,对于药物和制剂的研发非常重要。本研究基于CPEO-43良好的抗肿瘤效果,建立了CPEO-43血浆样本的UPLC-UV分析方法。
甲醇和乙腈是液相色谱最常用的流动相试剂,甲酸、乙酸、三氟乙酸常作为调节剂来改善色谱峰形。选择甲醇-水-甲酸进行分析尝试,结果发现,流动相中含有甲酸后,能够降低色谱流出曲线的标准差,色谱结果更好。本研究考察了不同浓度甲酸对色谱峰形和保留时间的影响。甲酸体积比分别为0.1%,0.05%,0.025%时,CPEO-43 的峰形无明显变化,随着甲酸酸度的降低,保留时间由7.8 min延长到8.2 min。考虑酸度对色谱柱寿命的影响,因此选择0.025%的甲酸作为流动相进行色谱分析。
本研究所建立的UPLC分析方法在0.5~10.0 μg/mL线性关系良好,其准确度、精密度和稳定性均能满足要求。方法的定量限为0.5 μg/mL,CPEO-43能抑制A549肺癌细胞和HCT116结肠癌细胞生长,IC值分别为2.51 μmol/L和0.87 μmol/L。因此该分析方法的定量下限值能满足定量分析有效抗肿瘤药物浓度,可为药物临床检测提供方法基础。
本研究针对DAI抗肿瘤活性低的缺陷,在DAI的4′位引入卤族元素Cl,在7位引入哌嗪基团,进行结构修饰,成功全合成了CPEO-43,并显著提高了DAI抗肿瘤活性。但是,合成CPEO-43的工艺条件仍有待进一步优化,CPEO-43的抗肿瘤机制有待更为深入的研究。
参考文献/References:
[1]ZHAO Tingting,JIN Feng,LI Jiguang,et al.Dietary isoflavones or isoflavone-rich food intake and breast cancer risk:A meta-analysis of prospective cohort studies[J].Clinical Nutrition,2019,38(1):136-145.
[2]DOUGLAS C C,JOHNSON S A,ARJMANDI B H.Soy and its isoflavones:The truth behind the science in breast cancer[J].Anti-Cancer Agents in Medicinal Chemistry,2013,13(8):1178-1187.
[3]KUCUK O.Soy foods,isoflavones,and breast cancer[J].Cancer,2017,123(11):1901-1903.
[4]FRITZ H,SEELY D,FLOWER G,et al.Soy,red clover,and isoflavones and breast cancer:A systematic review[J].Plos One,2013,8(11):e81968.DOI:10.1371/journal.pone.0081968.
[5]QIU Shumin,JIANG Chongmin.Soy and isoflavones consumption and breast cancer survival and recurrence:A systematic review and meta-analysis[J].European Journal of Nutrition,2019,58(8):3079-3090.
[6]BASU P,MAIER C.Phytoestrogens and breast cancer:In vitro anticancer activities of isoflavones,lignans,coumestans,stilbenes and their analogs and derivatives[J].Biomedicine & Pharmacotherapy,2018,107:1648-1666.
[7]TAKAGI A,KANO M,KAGA C.Possibility of breast cancer prevention:Use of soy isoflavones and fermented soy beverage produced using probiotics[J].International Journal of Molecular Sciences,2015,16(5):10907-10920.
[8]ZIAEI S,HALABY R.Dietary isoflavones and breast cancer risk[J].Medicines,2017,4(2):18.DOI:10.3390/medicines4020018.
[9]ZHANG Hongyi,CUI Jie,ZHANG Ye,et al.Isoflavones and prostate cancer:A review of some critical issues[J].Chinese Medical Journal,2016,129(3):341-347.
[10]李紫微,曹庸,苗建银.大豆异黄酮及其苷元的研究进展[J].食品工业科技,2019,40(20):348-355.LI Ziwei,CAO Yong,MIAO Jianyin.Research progress of soy isoflavones and aglycones[J].Science and Technology of Food Industry,2019,40(20):348-355.
[11]CHADHA R,BHALLA Y,JAIN A,et al.Dietary soy isoflavone:A mechanistic insight[J].Natural Product Communications,2017,12(4):627-634.
[12]李硕,王建.大豆异黄酮临床应用的研究进展[J].大豆科学,2020,39(4):633-640.LI Shuo,WANG Jian.Research progress on the clinical application of soybean isoflavones[J].Soybean Science,2020,39(4):633-640.
[13]PIAO Yinzi,EUN J B.Physicochemical characteristics and isoflavones content during manufacture of short-time fermented soybean product (Cheonggukjang)[J].Journal of Food Science and Technology,2020,57(6):2190-2197.
[14]MONTALESI E,CIPOLLETTI M,CRACCO P,et al.Divergent effects of daidzein and its metabolites on estrogen-induced survival of breast cancer cells[J].Cancers,2020,12(1):167.
[15]SALAMA A A A,ALLAM R M.Promising targets of chrysin and daidzein in colorectal cancer:Amphiregulin,CXCL1,and MMP-9[J].European Journal of Pharmacology,2021,892:173763.DOI:10.1016/j.ejphar.2020.173763.
[16]LI Laifang,LIU Jun,WANG Xiaobo,et al.Microarray analysis of differentially expressed long non-coding RNAs in daidzein-treated lung cancer cells[J].Oncology Letters,2021,22(5):789.DOI:10.3892/ol.2021.13050.
[17]翟雨晴.大豆苷元誘导肺癌A549细胞凋亡及其相关机制的研究[D].大庆:黑龙江八一农垦大学,2021.ZHAI Yuqing.The Mechanism of Daidzein Induced Human Lung Cancer A549 Cells Apoptosis[D].Daqing:Heilongjiang Bayi Agricultural Reclamation University,2021.
[18]林玉萍,虎春艳,郑喜,等.新型4'-(N-取代-1-哌嗪基)查尔酮衍生物的合成及其抗肿瘤活性[J].有机化学,2017,37(1):237-241.LIN Yuping,HU Chunyan,Zheng Xi,et al.Synthesis and anti-tumor activities of novel 4'-(n-substitued-1-piperazinyl) chalcone derivatives[J].Chinese Journal of Organic Chemistry,2017,37(1):237-241.
[19]张月洁,兰韬,初侨,等.大豆异黄酮的制备技术与功能活性进展研究[J].食品安全质量检测学报,2020,11(17):5964-5970.ZHANG Yuejie,LAN Tao,CHU Qiao,et al.Progress in preparation technology and functional activity of soybean isoflavones[J].Journal of Food Safety & Quality,2020,11(17):5964-5970.
[20]NAN Guanjun,GAO Yuqiong,GUO Liying,et al.Solid-liquid extraction of daidzein and genistein from soybean:Kinetic modeling of influential factors[J].Preparative Biochemistry & Biotechnology,2018,48(10):946-953.
[21]LIU Chunming,WATT D S,FRASINYUK M S,et al.Cytisine-linked Isoflavonoid Antineoplastic Agents for the Treatment of Cancer[P].US:10188743,2019-01-29.
[22]潘星燕,陆云霞,姚军.高效液相色谱法测定芒柄花素磺酸钠有关物质[J].河北科技大学学报,2017,38(1):32-38.PAN Xingyan,LU Yunxia,YAO Jun.Related substance determination of formononetin by HPLC[J].Journal of Hebei University of Science and Technology,2017,38(1):32-38.
[23]国家药典委员会.中华人民共和国药典:四部[M].北京:中国医药科技出版社,2020.
