新型耐热含能钙钛矿化合物(C6H14N2)[Na(ClO4)3]的热分解行为
2022-07-13张俊林陈劭力邱丽莉祝艳龙王伯周
周 静,张俊林,丁 黎,陈劭力,邱丽莉,祝艳龙,王伯周
(1. 北京理工大学化学与化工学院,北京 102488;2. 西安近代化学研究所,陕西 西安 710065)
1 引言
耐热含能材料广泛应用于航天事业及深井爆破等领域[1-5]。迄今为止,已报道的耐热含能材料数量超过40 个,而能满足使用要求且具备工业化前景的不超过10 个[6],对于相关含能材料的热分解行为及耐热机理的解析则是评估其应用前景的关键。传统耐热含能材料主要基于共轭稳定化效应或氢键效应[7]。此外,成盐效应对耐热性能的提升作用在有机内盐含能材料中得到了证实[8-9]。与有机内盐型含能材料不同,含能钙钛矿属于有机-无机复合内盐型含能材料,结构新颖且合成方法简单,综合性能优异[10]。
新型含能钙钛矿化合物的典型代表(C6H14N2)[Na(ClO4)3]由陈小明等[11]首次报道,包括制备工艺、晶体结构和综合爆轰性能,其中结构研究表明,(C6H14N2)[Na(ClO4)3]中高氯酸根离子与钠离子分别充当了构建骨架的无机阴阳离子,而质子化的三乙烯二胺(DABCO)则充当了还原性有机离子。在含能钙钛矿热性质研究方面,本团队[12]围绕(C6H14N2)[NH4(ClO4)3]体系的热分解行为及热分解机理展开了研究,从机理角度提出笼状骨架对有机片段的锁定效应,结果显示(C6H14N2)[NH4(ClO4)3]热稳定性突出;郭学永等[13]发现CoFe-层状双氢氧化物衍生物会催化(C6H14N2)[NH4(ClO4)3]的分解,使其热分解温度降低;任慧等[14]则同时探索了(C6H14N2)[NH4(ClO4)3]热分解行为和燃烧行为,研究了该类材料的高能量释放效率。除了铵盐体系外,邓鹏等[15]通过热分析实验和动力学参数计算研究了(C6H14N2)[K(ClO4)3]的热分解行为与机理。本研究团队则进一步比较了不同盐类组成对钙钛矿分解行为的影响[16],得到了相似的结论,即含能钙钛矿类结构的热稳定性突出,且热行为主要由组成离子的种类决定。与其他含能钙钛矿相似,(C6H14N2)[Na(ClO4)3]在自身氧化还原反应过程中,有机阳离子与氧化性阴离子相互作用释放热能并对外做功;在受热分解过程中,无机阳离子与氧化性阴离子间的相互作用强度决定了骨架的热稳定性,对整体的耐热特性也至关重要[17]。初步研究表明(C6H14N2)[Na(ClO4)3]分解温度较高,但热解特性明显不同于(C6H14N2)[NH4(ClO4)3]及(C6H14N2)[K(ClO4)3]。针对(C6H14N2)[Na(ClO4)3]的系统的热分析研究与感度研究鲜有报道,而这些研究对含能钙钛矿热行为的理解以及(C6H14N2)[Na(ClO4)3]本身的应用研究具有重要意义。本研究以(C6H14N2)[Na(ClO4)3]为研究对象,以差示扫描量热-热重分析(DSC-TG)、动力学模拟计算、同步热分析-红外-质谱(DSC·TG-FTIR-MS)联用技术、原位红外技术、以及国军标法等实验与计算相结合的手段,全面探讨了(C6H14N2)[Na(ClO4)3]的热行为、热解机制、热感度及机械感度,为其在耐热含能材料中的应用提供了理论和实验依据。
2 实验部分
2.1 原料与仪器
原料:DABCO、高氯酸及高氯酸钠,化学纯,西安近代化学研究所。(C6H14N2)[Na(ClO4)3]制备按照文献报道方法完成[11]。
仪器:Q200 差示扫描量热仪(美国,TA)、60 SXR原位红外光谱仪(美国,Nicolet),YC-1C 型真空安定性试验仪、同步热分析-红外-质谱(DSC·TG-FTIR-MS)联用系统(由德国耐驰STA449F3、德国耐驰QMS403C 和布鲁克70vFTIR 组成)、ML-1 型撞击感度仪、WM-1 摩擦感度仪、爆发点测试仪。
2.2 实验
同步热分析-红外-质谱(DSC·TG-FTIR-MS)联用实验,样品量0.4 mg,温度范围40~600 ℃,铝坩埚,吹扫气为高纯氮气,吹扫速率50 mL·min-1,升温速率10 ℃·min-1。
DSC 实验,样品量0.4 mg,温度范围40~600 ℃,铝坩埚,吹扫气为高纯氮气,吹扫速率为50 mL·min-1,升温速率分别为2.5、5、10、20 ℃·min-1。
原位红外实验,样品量0.5 mg,升温速率10 ℃·min-1,分辨率4 cm-1,光谱捕获速率17.8 file·min-1,扫描速率16 scans·file-1,温度范围20~450 ℃。
真空安定性实验按照GJB772A-1997 方法501.1进行测试,实验温度(100±0.5)℃,恒温48 h。
撞击感度测定按照GJB772A-1997 方法601.2 进行测试,落锤重10 kg,药量50 mg,落锤高度25 cm;撞击感度用爆炸概率P1表示。
摩擦感度测定按照GJB772A-1997 方法602.1 进行测试,表压3.92 MPa,摆角90°,药量20 mg,摩擦感度用爆炸概率P2表示。
5 s 爆发点测试按照GBJ 772A-1997 炸药试验法606.1 完成,药量30 mg。
3 结果与讨论
3.1 (C6H14N2)[Na(ClO4)3]的热分解行为研究
在10 ℃·min-1下 对 产 物(C6H14N2)[Na(ClO4)3](图1)和原料DABCO 进行了热分解性能的研究,其中图2 为(C6H14N2)[Na(ClO4)3]的DSC-TG 结 果,图3为DABCO 的DSC 结果。由图2 可以看出,室温~500 ℃时(C6H14N2)[Na(ClO4)3]仅 有1 个 分 解 放 热峰,初始分解温度为287.4 ℃、分解峰温为354.9 ℃,对应失重量为80.1%。可见,(C6H14N2)[Na(ClO4)3]显示了优异的热稳定性,分解温度很高,明显高于黑索今(RDX,分解峰温208 ℃,DSC@5 ℃·min-1)、奥克托今(HMX,分解峰温276 ℃,DSC@5 ℃·min-1)、六硝基六氮杂异伍兹烷(CL-20,分解峰温224 ℃,DSC@5 ℃·min-1)等多数现役含能材料[18],也高于经典的耐热含能化合物六硝基砥(HNS,分解峰温320 ℃,DSC@5 ℃·min-1)[18],有望作为理想的耐热含能化合物。此外,由DSC 实验得到(C6H14N2)[Na(ClO4)3]的分解放热量为4227 J·g-1,说明其具有较强的能量释放能力。

图1 (C6H14N2)[Na(ClO4)3]结构Fig.1 Structure of(C6H14N2)[Na(ClO4)3]

图2 10 ℃·min-1下(C6H14N2)[Na(ClO4)3]分解的DSC-TG 曲线Fig.2 DSC-TG curves of(C6H14N2)[Na(ClO4)3]at the heating rate of 10 ℃·min-1
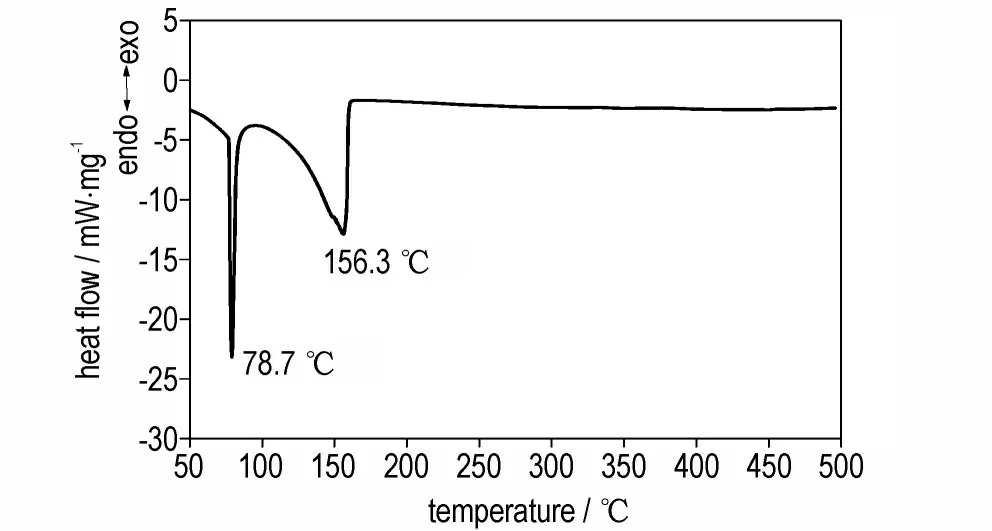
图3 10 ℃·min-1下三乙烯二胺分解的DSC 曲线Fig.3 DSC curve of DABCO at the heating rate of 10 ℃·min-1
图3 对比研究了有机组分DABCO 的热稳定性。在相同的实验条件下,三乙烯二胺在78.7 ℃处有1 个尖锐吸热峰,属于典型的相变吸热峰;而在此吸热峰之后出现的宽的吸热峰代表了DABCO 在持续加热条件下会发生缓慢挥发。但在质子化形成阳离子后,H2DABCO2+与(C6H14N2)[Na(ClO4)3]笼状骨架中的无机离子相互作用,有机组分的相变过程消失。但(C6H14N2)[Na(ClO4)3]在205.8 ℃存在1 个小的 吸热峰(图2),由于样品在此温度下没有熔化迹象,因此该吸热峰极有可能来源于笼状骨架内有机部分旋转所引发的晶型变化[12]。
3.2 (C6H14N2)[Na(ClO4)3]的热分解动力学研究
图4为(C6H14N2)[Na(ClO4)3]在2.5、5、10 ℃·min-1和20 ℃·min-1下 的DSC 曲 线。由 图4 可 以 看 出,(C6H14N2)[Na(ClO4)3]在2.5、5、10 ℃·min-1和20 ℃·min-1时对应的分解峰温分别为320.4、336.7、345.9 ℃和356.5 ℃。随着升温速率的增加,(C6H14N2)[Na(ClO4)3]的分解峰温明显向高温方向移动。表1 为不同升温速率下(C6H14N2)[Na(ClO4)3]的放热量,由表1 可见,随着升温速率的增加,(C6H14N2)[Na(ClO4)3]的分解放热量基本不变,综合考虑(C6H14N2)[Na(ClO4)3]的DSC 曲线上中仅含的1 个分解放热峰,初步判断(C6H14N2)[Na(ClO4)3]的 分 解 为 一 步 反 应。采 用Netzsch 动力学模拟软件中的Friedman 无模型方法[8],选择不同的分解深度α,以logα对1/T作图,通过曲线斜率计算得到了不同分解深度α下对应的活化能Ea及指前因子logA,结果如图5 所示。由图5 可以看出,在整个分解反应过程中活化能和指前因子基本不变,可见(C6H14N2)[Na(ClO4)3]的分解为一步反应,且反应过程中活化能Ea较高,计算值达到175 kJ·mol-1,也从理论角度解释了(C6H14N2)[Na(ClO4)3]具有较高热稳定性的原因。
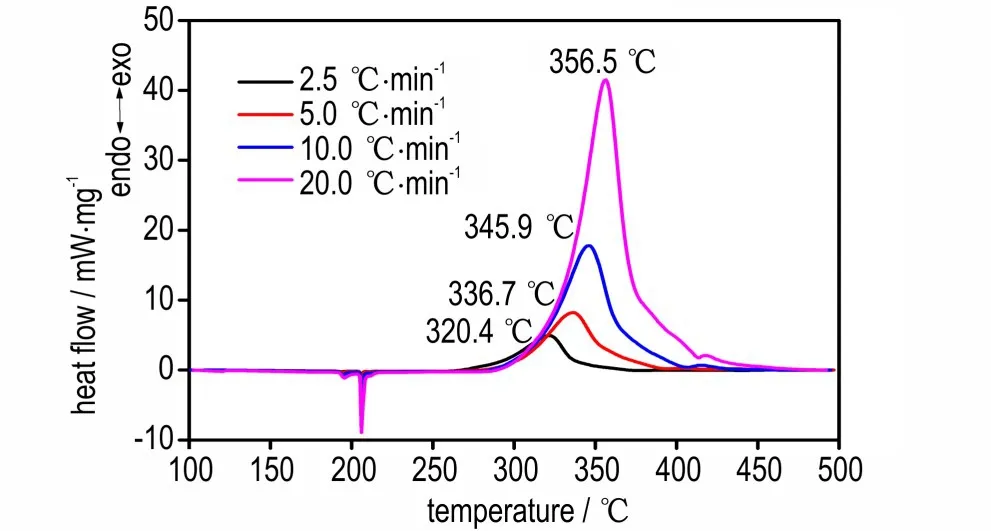
图4 不同升温速率下(C6H14N2)[Na(ClO4)3]下的DSC 曲线Fig.4 DSC curves of(C6H14N2)[Na(ClO4)3]at differentheating rates

表1 (C6H14N2)[Na(ClO4)3]在不同升温速率下的分解峰温和放热量Table 1 Decomposition peak temperature and heat release of(C6H14N2)[Na(ClO4)3]at different heating rates
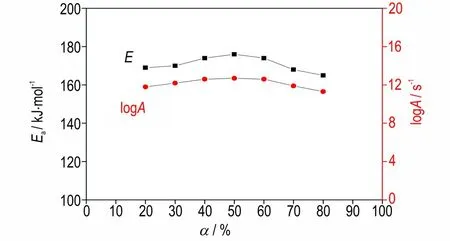
图5 (C6H14N2)[Na(ClO4)3]的分解活化能Ea随分解深度α 的变化Fig.5 Changes of the decomposition activation energy Ea of(C6H14N2)[Na(ClO4)3]with the decomposition depth α
3.3 基于分解产物的(C6H14N2)[Na(ClO4)3]热分解机理研究
(C6H14N2)[Na(ClO4)3]的 骨 架 是 基 于Na+和之间的库仑力作用所构建起的立体笼状骨架,有机阳离子H2DABCO2+被锁定在此笼状骨架中,(C6H14N2)[Na(ClO4)3]中的氧化性组分ClO4-和燃料组分H2DABCO2+间同样存在库伦力作用,这种复合的库仑力作用是三乙烯二胺体系在形成钙钛矿结构后稳定性大幅提升的主要原因。随着加热温度的升高,构成骨架的阴阳无机离子间的库仑力减弱,笼状骨架坍塌,导致有机阳离子与无机氧化性离子直接发生氧化还原反应,产生大量热量的同时释放出各种气相产物。同步热分析-红外-质谱(DSC·TG-FTIR-MS)联用系统可以在程序升温模式下加热样品,同时样品分解的气体产物通过管道实时输送至红外及质谱检测器,对样品分解的气相产物开展动态实时监测。图6 为10 ℃·min-1升温速率下气体分解产物对应的质谱,由图6 可以看出,(C6H14N2)[Na(ClO4)3]分解时对应的气体产物的质谱碎片m/z分别为17、18、27、30、36、44,基于元素组成分析可能的产物分别为NH3、H2O、HCN、NO、HCl、CO2·N2O。结合不同温度下气体产物对应的红外谱图(图7)可以看出,在初始分解温度287 ℃下,红外谱图中分 别 在2248、2329、2360 cm-1处有峰,此处红外谱图峰形与40 ℃时背景谱图中CO2的峰形明显不同,表明此时不仅有CO2,结合出峰位置和质谱碎片分析,287 ℃时(C6H14N2)[Na(ClO4)3]分解最先产生N2O。
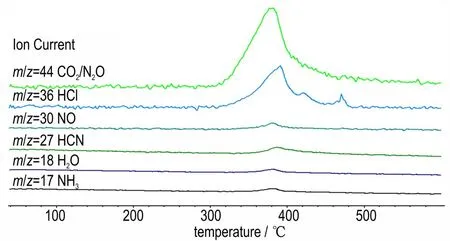
图6 10 ℃·min-1 下(C6H14N2)[Na(ClO4)3]分 解 的 气 体 产 物质谱图Fig.6 MS spectra of gaseous products of(C6H14N2)[Na(ClO4)3]at the heating rate of 10 ℃·min-1
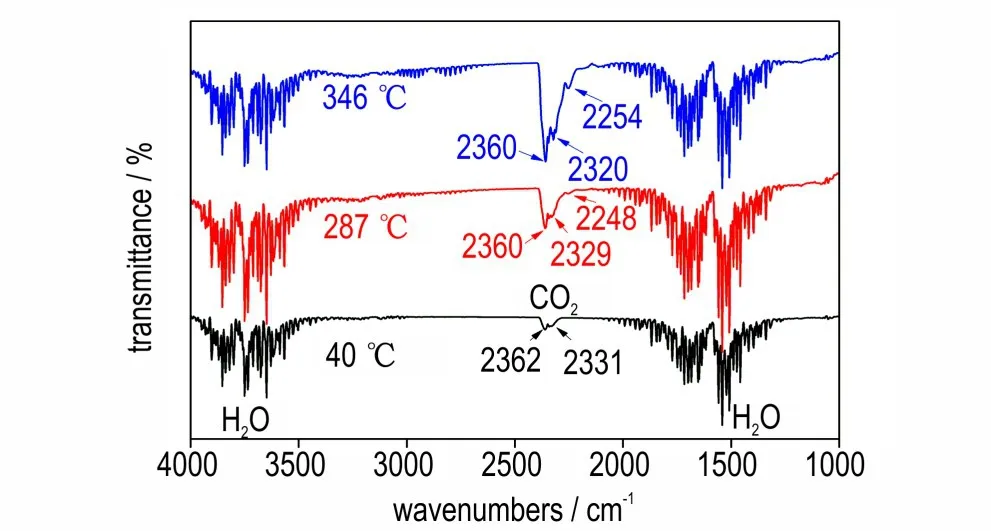
图7 10 ℃·min-1 下(C6H14N2)[Na(ClO4)3]不 同 温 度 下 的 气体产物红外图Fig.7 IR spectra of gaseous products of(C6H14N2)[Na(ClO4)3]at the heating rate of 10 ℃·min-1
为进一步阐明(C6H14N2)[Na(ClO4)3]分解机理,采用原位红外技术对比分析(C6H14N2)[Na(ClO4)3]及DABCO 受热分解的固相分解产物。.四联用技术研究了气相分解产物,需要进一步利用固相分解过程的监测与气相分解产物相互佐证。由于(C6H14N2)[Na(ClO4)3]在组成上可视为DABCO 体系与高氯酸体系的结合,通过分析比较(C6H14N2)[Na(ClO4)3]中H2DABCO2+组分与单一DABCO 的固相分解过程,可以进一步发掘(C6H14N2)[Na(ClO4)3]组分间的相互作用力。图8为(C6H14N2)[Na(ClO4)3]、DABCO 在10 ℃·min-1升温速率时不同温度下的凝固态体系的红外谱图,图9则是作为参照谱图的高氯酸铵的红外谱图,用于分析对比高氯酸根的红外分布。综合对比并分析图8a、图8b、图9 的红外峰形及位置发现:40 ℃时,DABCO在778、836、906、994、1060、1320、1459、1680、2249、2876、2944 cm-1和3417 cm-1位置红外吸收 峰明显,由于DABCO 的挥发性较强,当温度超过240 ℃时DABCO 的红外吸收极大削弱,而当加热到370 ℃时DABCO 的红外吸收峰彻底消失;40 ℃下1080 cm-1左右宽的红外峰信号为的吸收峰,而H2DABCO2+在1100cm-1左右的吸收峰多与的信号重叠,1423、1465 cm-1处的吸收峰也属于H2DABCO2+的红外吸收,随着温度的升高,H2DABCO2+的信号比的信号衰减更快,但H2DABCO2+在380 ℃时依然存在,说明笼状骨架中的有机分子首先分解,但与独立的DABCO 分 子 相 比,(C6H14N2)[Na(ClO4)3]分 子 中 的H2DABCO2+稳定性大幅提升,可见笼状骨架的锁定效应有效抑制了DABCO 体系的挥发逃逸并限制了其与氧化性组分的直接相互作用,对比DABCO 本身,这种对有机组分的锁定效应保证了DABCO 结构在自身氧化还原前不会发生逸出;ClO4-的信号在约350 ℃时开始减弱,说明此时骨架开始逐步碎裂,温度继续升高导致笼状骨架所依赖的库仑力已无法维持,而有机组分则会与氧化性ClO4-发生氧化还原反应,释放大量热量和气相产物,热量释放和气相产物可以通过上述DSC 以及DSC·TG-FTIR-MS 联用技术进行监测。通过各类实验结果的比较,可以得出以下结论:加热条件下有机阳离子H2DABCO2+先于笼骨架被激活;当有机阳离子H2DABCO2+与ClO4-之间的相互作用强到足以破坏笼状骨架时,触发氧化还原反应,充当燃料组分的有机结构被氧化,形成氮氧化物等气相产物,而被还原为HCl。
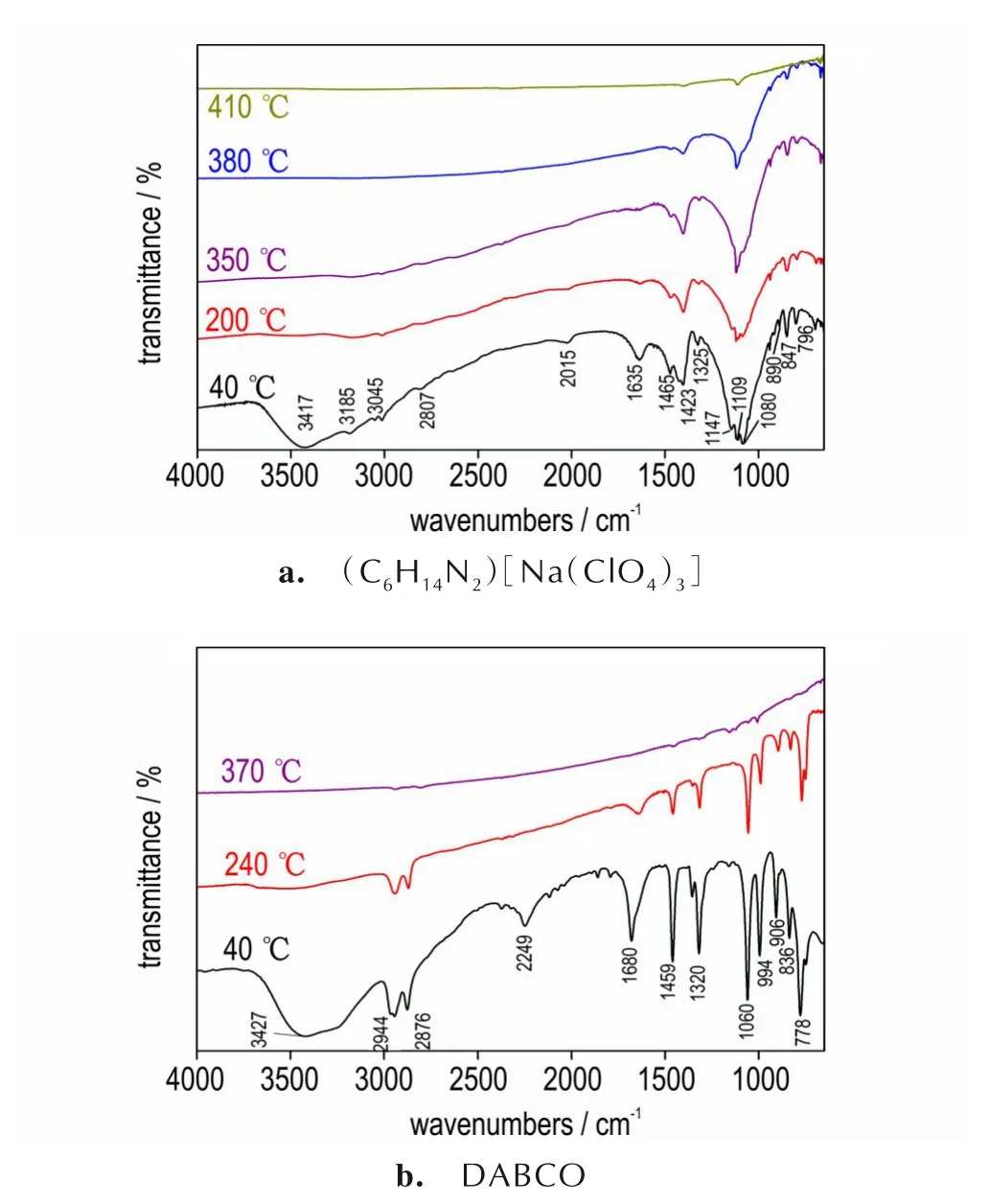
图8 10 ℃·min-1下(C6H14N2)[Na(ClO4)3]及三乙烯二胺不同温度的凝固态体系的红外谱图Fig.8 IR spectra of condensed products of(C6H14N2)[Na(ClO4)3]and DABCO at the heating rate of 10 ℃·min-1
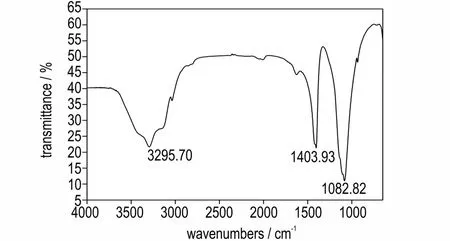
图9 高氯酸铵的红外谱图Fig.9 IR spectra of NH4ClO4
3.4 (C6H14N2)[Na(ClO4)3]的安全性
根据GJB772A-1997 中,采用真空安定性方法和5 s 爆发点测试对(C6H14N2)[Na(ClO4)3]的热感度进行了初步探索,并研究了其安全性能。(C6H14N2)[Na(ClO4)3]的5 s 爆发点233 ℃,真空安定性实验结果表明,(C6H14N2)[Na(ClO4)3]在100 ℃下加热48 h,放气量约0.04 mL·g-1,远远小于方法的判据2 mL·g-1[19],说明(C6H14N2)[Na(ClO4)3]的 热 安 全 性 良 好。传 统RDX 与HMX 的 撞 击 感 度 及 摩 擦 感 度 均 为100%[20],(C6H14N2)[Na(ClO4)3]撞击感度P1为32%,摩擦感度P2为80%,机械感度水平低于RDX、HMX 等代表性现役含能化合物,具有较好的安全性。
4 结论
(1)本研究对新型含能钙钛矿(C6H14N2)[Na(ClO4)3]的热分解热行为、分解动力学、分解机理以及安全性等进行了全面的研究探讨。
(2)(C6H14N2)[Na(ClO4)3]具 有 优 异 的 热 稳 定性,属于耐热含能结构,其分解放热量为4227 J·g-1,能量释放能力强。
(3)采用Friedman无模型方法计算,(C6H14N2)[Na(ClO4)3]整个分解反应过程中活化能和指前因子基本不变,(C6H14N2)[Na(ClO4)3]的分解为一步反应,且反应过程中活化能为175 kJ·mol-1。
(4)加热条件下有机阳离子H2DABCO2+先于笼状骨架被激活。当有机阳离子H2DABCO2+与ClO4-之间的相互作用强到足以破坏笼状骨架时将触发氧化还原反应,充当燃料组分的有机结构被氧化形成氮氧化物等气相产物,而ClO4
-被还原为HCl。(5)(C6H14N2)[Na(ClO4)3]撞 击 感 度P1为32%,摩擦感度P2为80%,机械感度水平低于RDX、HMX 等代表性现役含能化合物。
