超声胃镜引导下穿刺引流治疗经胃保胆术后膈下脓肿1例
2022-07-12赖际霞马明刘妍陈凤莉张鸣青
赖际霞,马明,刘妍,陈凤莉,张鸣青
经胃自然腔道内镜手术(trans-gastric nature orifice transluminal endoscopic surgery,TG-NOTES)具有无体表疤痕、创伤小、恢复快等优势[1]。随着内镜技术的发展,其临床应用越来越广泛,尤其是应用于保胆术。NOTES成功的关键是术后腹腔感染的防治,腹腔感染常表现为腹膜炎、腹腔积液、菌血症,膈下脓肿较为少见,多继发于胆漏、入路口漏[2]。目前临床上膈下脓肿的治疗方法有药物治疗、经皮穿刺引流术、外科清创术等[3-4]。近期我院1例患者TG-NOTES保胆术后1 d并发左膈下脓肿,查胃镜、腹部CT未见消化道瘘,应用超声内镜(endoscopic ultrasound, EUS)引导下穿刺引流成功治愈,现报道如下。
1 病历资料
患者女性,69岁,2018年7月2日因“剑突下闷痛3年余”入院,行腹部彩超提示胆囊息肉(10 mm×12 mm);上腹部CT平扫未见明显异常(图1A);诊断:胆囊息肉。该患者胆囊息肉直径>10 mm,具有手术指征,完善术前相关检查,无手术禁忌症,于2018年7月3日在全麻下行TG-NOTES保胆胆囊息肉摘除术,术后诊断:胆囊息肉。术后第1天出现发热,最高体温达38.9 ℃,无腹泻,无反酸、嗳气,精神、睡眠尚可,肛门已排气,无排便。查体:腹肌软,上腹部、右下腹压痛,无反跳痛。查炎症指标明显升高,考虑可能并发腹膜炎,予“头孢哌酮钠舒巴坦钠”联合“奥硝唑”抗感染治疗。此后间断发热,呈不规则热型,查体左下肺呼吸音弱,左肋下压痛,余无明显阳性体征。遂完善胸腹部CT(图1)提示:双侧胸腔积液,左侧较明显,左侧肺不张;胃窦前壁及胆囊壁可见金属密度(止血夹),脾周少量积液;左膈下见大片状液性密度影,CT值约20 HU,周围形成包裹,内壁光滑,壁薄,增强呈环形强化,其内伴散在小气泡,并可见气-液平,脾脏呈受压推移改变。结合患者症状、体征、手术史及胸腹CT检查结果,明确诊断为“TG-NOTES保胆术后隔下脓肿”。拟行经皮穿刺引流术,但体表超声左侧腹未探及适合穿刺路径。向患者及其家属交代病情,建议其行EUS引导下穿刺引流治疗,均表示知情同意。遂于2018年7月20日行EUS引导下穿刺引流术(图2),术程如下:肝、胃、脾间隙、胰尾附近探及低回声区(图2B),范围约5.2 cm×3.6 cm,内回声不均匀,见散在高回声光点漂浮,近胃壁侧见少许液性暗区,CDFI示病灶内未探及明显血流信号。在EUS引导下19 G COOK穿刺针刺入脾胃间隙病变内,穿刺部位为胃体中段前壁,负压抽吸阻力明显,抽出约2 mL淡绿色脓液。交换置入斑马导丝进入脓腔,囊肿切开刀沿斑马导丝切开胃壁及脓肿壁,见黄绿色脓液流入胃腔,沿斑马导丝置入鼻脓肿引流管及双猪尾巴管(图2C),经鼻脓肿引流管抽取15 mL脓液送检病原微生物培养,脓液培养提示肺炎克雷伯杆菌感染,三代头孢敏感。术后经引流管予生理盐水反复冲洗脓腔,引流出约450 mL灰绿色脓液,并继续予“头孢哌酮钠舒巴坦钠”联合“奥硝唑”抗感染治疗。引流术后第3天体温恢复正常,复查炎症指标较前下降。引流术后7 d复查EUS(图2D),脓肿明显吸收。
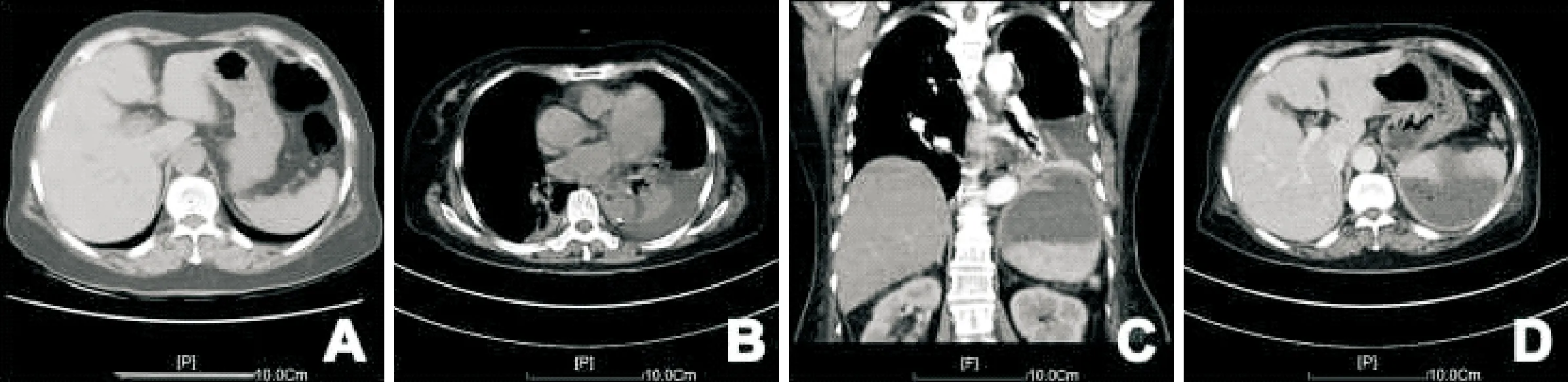
图1 EUS穿刺引流术前胸腹CT检查 A:保胆胆囊息肉摘除术前,上腹部CT平扫未见明显积液;B:双侧胸腔积液,左侧较明显,左侧肺不张;C(冠状面)、D(横断面):左膈下见大片状液性密度影,CT值约20 HU,周围形成包裹,内壁光滑,壁薄,增强呈环形强化,其内伴散在小气泡,并可见气-液平,脾脏呈受压推移改变

图2 EUS穿刺引流术中及术后图像 A:穿刺部位内镜所见;B:穿刺部位EUS所见;C:置入鼻脓肿引流管;D:穿刺置管7 d后脓肿明显吸收
2 讨论
TG-NOTES保胆术常见的并发症之一是腹腔感染,与腹腔镜手术及开腹手术不同,对于TG-NOTES而言,实现无菌操作要困难很多,细菌可经由口腔、食道及胃感染腹腔,因此在TG-NOTES发展的早期,预防感染一度被认为是阻碍其发展的最主要因素。目前临床上有多种预防感染的方法,如预防性静脉用抗生素、口腔消毒、使用无菌套管、洗胃以及腹腔灌洗等等[5-7]。有研究表明,高水平的设备消毒、术前胃腔灌洗、充分的腹腔灌洗以及严格使用无菌套管的TG-NOTES的污染水平与腹腔镜手术相当[8]。腹腔感染表现形式多样,可以表现为腹膜炎、腹腔积液、菌血症、膈下脓肿、脓毒血症等。其中,膈下脓肿较为少见,通常继发于胃漏、胆漏等,也有腹腔冲洗不充分、胃腔灌洗不严格等引起膈下脓肿的可能,但极为少见[2]。肺炎克雷伯杆菌是消化道的定植菌,一般不引起感染,只有在机体免疫力差和或细菌移位于腹腔时才会造成感染[9]。
此例患者行TG-NOTES保胆术,术后第1天出现发热,后明确并发左膈下脓肿,脓液培养提示肺炎克雷伯杆菌感染。术中严密地闭合了胃壁切口,术后复查胃镜未见胃漏,腹部CT未见膈下游离气体,排除了胃壁切口闭合不严密或者金属夹过早脱落,术后肺炎克雷伯杆菌经其移位腹腔引起感染的可能。术中采用的是金属夹内镜下缝合胆囊切口,术后复查腹部CT未见胆囊周围游离气体,EUS下未见胆囊底部积液,且脓肿位于左膈下,故排除胆漏引起膈下脓肿的情况。TG-NOTES保胆术采用左侧卧位,腹腔冲洗液易集聚于左侧膈下,术后平卧位,左侧膈下也是低位,而膈下脓肿也位于左侧,与之一致,因此该患者并发左膈下脓肿的原因考虑为洗胃不够充分,残留的肺炎克雷伯杆菌在TG-NOTES保胆术中移位至腹腔,后续的灌洗未将这部分细菌冲洗、吸引完全。这给我们带来了启示:虽然2 L的生理盐水与聚维碘酮洗胃的效果相当,但是为了尽可能地实现无菌,可以考虑先用生理盐水洗胃,然后聚维碘酮洗胃,最后再次用生理盐水洗胃。除此之外还应进行充分的腹腔灌洗、吸引,必要时可变换体位,避免冲洗液集聚。
膈下脓肿多位于胃脾间隙,位置深,有脓肿壁,药物难道到达,通常抗感染治疗效果欠佳,需要进一步行穿刺引流术或是外科清创术[10-12]。因为外科清创术创伤大、风险高,目前临床上多采用CT或超声引导下经皮穿刺引流术治疗膈下脓肿[3,13-14]。经皮穿刺引流术具有创伤小、恢复快、成功率高等优势,但同时也具有一定的局限性。CT定位非实时可视,无法动态监测穿刺针的穿刺路径,无法显示血管血流,存在出血的风险。体表超声定位相对CT而言具有一定的优势,穿刺针头实时可视,能够显示血管血流,降低出血的风险,但是体表超声不能清楚地描绘介入组织,再加上肠内气体的覆盖,有时针道很难显示。EUS拥有更高的空间分辨率,比体表超声和CT显示更多的细节和解剖结构,且能够实时、清晰、高度一致地显示穿刺针,避免误穿血管和肠道气体干扰。目前在临床上应用EUS引导进行各种内镜下诊疗越来越广泛、成熟,比如用于辅助穿刺引流胰周积液(包括胰腺炎、脓肿和假性囊肿)[15-16],EUS-FNA穿刺活检胰腺囊肿或肿物[17-20]及用于辅助穿刺引流肝、脾、乙状结肠、直肠周围和盆腔脓肿等[21],均具有较高的成功率。在一项Meta分析中指出,EUS辅助穿刺引流治疗胰腺假性囊肿与经皮引流术相比成功率、副反应发生率没有明显差异,而住院时间、费用、术后恢复等EUS更具有优势[22]。也有应用EUS引导下穿刺引流治疗腹腔镜术后并发膈下脓肿的个案报道[23]。
本例患者膈下脓肿位于胃脾间隙,位置较深,本拟行经皮穿刺引流术,但体表超声于左侧腹探查未探及适合穿刺路径,而EUS在解剖位置上具有优势,经其定位,找到胃壁与脓腔之间合适的穿刺路径,在其辅助之下经胃穿刺引流置管成功。术后脓液黏稠,不易引流,予生理盐水反复冲洗并抗感染治疗,症状、体温及炎症指标下降均提示治疗效果可,有效地减轻了病人的痛苦,缩短了住院时间。
总而言之,EUS引导下穿刺引流治疗膈下脓肿能明显缩短穿刺距离,避开腹腔脏器、血管,是安全、微创、有效的,较外科清创术具有创伤小、恢复快的优势,较CT或超声引导下经皮穿刺引流术具有分辨率高、视野好、解剖位置好等优势。临床上,经胃保胆术后出现膈下脓肿可考虑采用EUS引导下穿刺引流治疗。
