血浆表皮生长因子受体基因突变检测质控品的制备及性能评价*
2022-07-12潘志文来茜田珊徐笑红中国科学院大学附属肿瘤医院检验科病理科杭州310022
潘志文,来茜,田珊,徐笑红(中国科学院大学附属肿瘤医院.检验科,.病理科,杭州310022)
近年来,肺癌精准治疗得到广泛应用。小分子酪氨酸激酶抑制剂(tyrosine kinase inhibitor, TKI)能靶向抑制突变的表皮生长因子受体(epidermal growth factor receptor, EGFR)基因活性,EGFR突变的晚期非小细胞肺癌(non small cell lung cancer, NSCLC)患者接受TKI治疗后,可明显获益[1-2]。EGFR突变检测已成为肺癌靶向治疗的必需基因检测项目。对EGFR突变情况进行检测,可较好地预测EGFR-TKI的疗效,监测疾病的进展,并可发现EGFR-TKI是否耐药,从而及时调整治疗方案[3-5]。EGFR突变的检测方法仍以组织标本检测为金标准,同时,细胞学及外周血EGFR突变检测亦得到良好发展。由于组织标本获得途径和次数有限以及肿瘤组织的异质性,血浆检测越来越受关注,已成为肿瘤伴随诊断的主要发展方向。开展基因突变检测必须有规范的质量控制,室内质量控制和室间质量评价都需有适宜的质控品。为满足分子实验室质量控制的要求,本研究自制模拟临床样本的EGFR基因突变检测质控品并进行性能评估。
1 材料与方法
1.1仪器及试剂 LightCycler 480扩增仪(美国罗氏公司),NanoDrop分光光度计(美国ThermoFisher公司);EGFR基因突变检测试剂盒(厦门艾德公司),石蜡组织DNA提取试剂和血浆DNA提取试剂盒(德国Qiagen公司)。
1.2血浆EGFR质控品准备 (1)收集中国科学院大学附属肿瘤医院经病理确诊为肺癌的多份手术标本,由分子病理检测确认有EGFR 19del、L858R突变、T790M突变阳性的福尔马林固定石蜡包埋(formalin-fixed and parrffin-embeded,FFPE)蜡卷,每份组织取15张蜡卷,其第1、2张切片和最后2张切片均由病理医生确认肿瘤细胞>500个以上,用石蜡组织DNA提取试剂提取DNA,用分光光度计检测其浓度;(2)准备无溶血、无黄疸、无脂浊,HBsAg、HCV、人类免疫缺陷病毒(HIV)及梅毒阴性的正常人血浆,将血浆于65 ℃灭活10 h,1 500 r/min离心10 min,去除沉淀物;(3)将标本DNA与血浆混合,提取DNA并进行PCR扩增,根据PCR扩增曲线,配制成检测下限2~4倍的EGFR突变DNA浓度的血浆溶液;(4)分装到1 mL的EP管中,每支0.5 mL,-80 ℃冻存;(5)标本获取均由医院伦理委员会讨论通过(伦理批件号IRB-2022-66)。
1.3血浆质控品DNA提取及突变检测 用血浆DNA提取试剂盒提取自制血浆质控品DNA,按试剂说明书进行操作。用分光光度计测定浓度和纯度后,用LightCycler 480扩增仪和血液EGFR突变检测试剂盒检测突变状况。PCR扩增后,对质控品循环阈值(cycle threshold,Ct)值进行统计和分析。
1.4统计学分析 用SPSS 16.0软件进行。用两样本t检验进行均一性分析,以P<0.05为差异有统计学意义。
2 实验与结果
2.1均一性评价 参照CNAS-GL03《能力验证样品均匀性和稳定性评价指南》中关于均一性的评价要求,分别抽取19del、L858R突变、T790M突变的自制质控品各10支,每支重复测定2次。第1轮按1→10的顺序检测,第2轮按10→1的顺序重复测定,记录两轮检测的Ct值结果并计算平均值,两轮检测结果间差异均无统计学意义(P值>0.05),表明样品均一性较好。见表1。

表1 自制血浆EGFR突变质控品均匀性评价结果(Ct值)
2.2稳定性评估 按照CNAS-GL03中稳定性检验“5.2.2 两个平均值之间的一致性”方法进行评价。随机取19del、L858R突变、T790M突变的自制质控品各1瓶,每瓶重复检测2次,将得到的Ct均值作为初始均值,再分别于第2、4、6、8、10、12个月随机各抽取1瓶-80 ℃保存的自制质控品,按同样方法进行检测,分别取其平均Ct值,观察Ct值变化情况。自制质控品保存第2、4、6、8、10、12个月检测结果的Ct值见图1,结果显示19del、L858R和T790M突变的Ct值变异系数分别为1.3%、1.8%和1.3%,均小于5%,检测结果的稳定性较好,见表2。

图1 19del、L858R和T790M突变质控品检测Ct值变化曲线
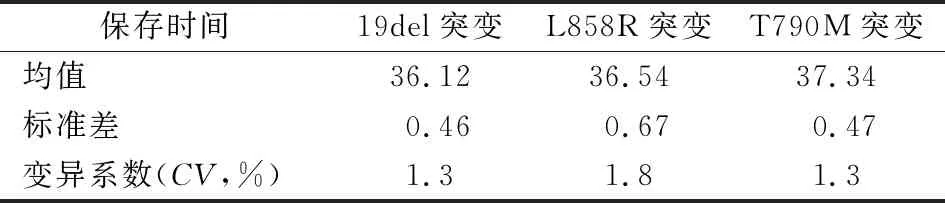
表2 自制EGFR 突变质控品稳定性检测结果(Ct值)
2.3准确性评估 选取自制质控品共测定10次,检出10次,阳性符合率均为100%,准确性较好。
3 讨论
目前,临床的分子诊断相关检测越来越多,项目繁多,方法多样,人员水平参差不齐,检测主体层次不一,质量意识强弱不一,缺乏统一规范的质量监控体系,质量令人担忧。为此,建立实验室质量管理体系,采取规范的质量管理措施刻不容缓。分子诊断质控品有其特殊性:没有国家级标准品;不能自动化和标准化,随机差异大;诊断方法多样,如Sanger测序、ARMS-PCR法,dd-PCR法、二代测序法(NGS)等,检测结果五花八门[6-8]。Liu等[9]研究中,自制5个EGFR血浆和石蜡组织的检测质控品,并发给8家单位NGS盲测,其中,19del Plasma-Q0有3家未检出,Plasma-Q1有1家未检出,Plasma-Q2有2家未检出,FFPE-Q1有1家未检出。由于分子检测诊断方法更新换代快,决定了检测质量控制的复杂性和持续更新的必要性。
然而,无论使用何种检测方法,运用质控品进行全流程的质量监管,是保证检测结果准确的必不可少的措施。目前,EGFR突变临床检测中,缺少用于质量控制的全程实验用的质控品。因此,为确保检测结果的准确性和可靠性,本研究利用病理剩余组织提取EGFR突变的DNA,混合正常人血浆,稀释成低浓度后配制成EGFR常见突变位点的质控品,与常规检测标本性状相同、DNA提取操作同步,可完整监控DNA提取过程,真实反映提取操作过程是否合格;同时,在扩增反应上,通过质控品的扩增曲线、阴性和阳性对照扩增曲线,可监测每日检测的稳定性,克服了组织标本的异质性,均一性好;在对自制质控品进行每月1次检测中显示,在1年内3种阳性突变质控品检测Ct值差异无统计学意义,可良好地应用于实验室自建检测(LDTs)的性能确认,符合室内质量控制的管理要求。更长时间的保存是否会影响质控品的稳定性,还有待继续研究。自制质控品定性结果准确性达100%。
分子病理中突变组织的DNA含量较高,在制备过程中,稀释倍数较高,可一次制备的质控品量大,减少了不同制作批间的差异,可保证半年到一年的用量。本研究中EGFR阳性质控品制备方法简单,成本低廉,均一性好,结果稳定,使用方便,利于LDTs项目的质量控制,也适合基层医疗机构实验室的推广和应用。
