妊娠期肝内胆汁淤积症患者血清25-羟基维生素D3甘胆酸和总胆汁酸水平与不良妊娠结局的关联性研究
2022-07-08黄玉林李伟清利惠婵黄洪萍
黄玉林, 李伟清, 利惠婵, 黄洪萍
妊娠期肝内胆汁淤积症(intrahepatic cholestasis of pregnancy,ICP)是一种妊娠期独特的肝脏疾病,是一种可逆的胆汁淤积形式,主要见于妊娠中晚期,以出现不明原因的瘙痒、胆汁酸升高和(或)肝功能异常为主要临床特征[1-2]。由于地域和种族的差异性,文献报道的ICP发病率为0.8%~12%[3]。临床试验和观察性研究的证据均显示,当孕妇的血清胆汁酸浓度高于实验室界定的临界上限值后,其疾病的严重程度与围产期不良妊娠结局风险增加相关,如死产、早产、羊水胎粪污染、胎儿窘迫、胎儿窒息等[2,4]。尽管ICP是一种良性疾病,在分娩后大多会自行消退,但ICP发生的病因尚未完全清楚[5-6]。此外,在肝脏参与代谢的一些维生素,如维生素D等,也被证明在胆汁淤积和肝硬化等肝病中起着保护作用[7],其在肝脏中可被羟基化为25-羟基维生素D3[25-hydroxyvitamin D3,25(OH)Vit D3]。25(OH)Vit D3是体内维生素D的主要储存和循环形式,已有文献报道低水平25(OH)Vit D3与ICP的发病有关[3]。本研究旨在调查ICP孕妇体内甘胆酸(cholyglycine,CG)、总胆汁酸(total bile acid,TBA)、肝酶和25(OH)Vit D3的水平及其与ICP疾病严重程度和围产期不良妊娠结局的关联性。
1 对象与方法
1.1研究对象 选择2019年1月至2020年4月我院妇产科收治的ICP孕妇153例(ICP组),另选择同期产检且无妊娠并发症的健康孕妇153名(健康对照组)。ICP的诊断标准参照中华医学会妇产科学分会产科学组发布的《妊娠期肝内胆汁淤积症诊疗指南(2015)》[8],轻度ICP 114例(轻度ICP组):(1)TBA水平为10~40 μmol/L;(2)临床症状以轻度皮肤瘙痒为主,无明显其他症状。重度ICP 39例(重度ICP组):(1)TBA水平≥40 μmol/L;(2)伴随严重皮肤瘙痒;(3)伴有其他情况如合并妊高症、复发性ICP、曾因ICP致围产儿死亡者。本研究只纳入单胎ICP和非人工授精妊娠者。ICP组和健康对照组孕妇年龄、分娩后的体质量指数(body mass index,BMI)比较差异无统计学意义(P>0.05)。ICP组新生儿体质量大于健康对照组,差异有统计学意义(P<0.05)。见表1。
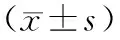
表1 两组一般资料比较
1.2检测方法 孕妇在妊娠期出现皮肤瘙痒、黄疸时抽血测定TBA、CG、肝酶和25(OH)Vit D3水平。对于无皮肤瘙痒和黄疸的孕妇,则常规在孕32~34周测定TBA、CG、肝酶和25(OH)Vit D3水平。CG和TBA采用Cobas8000 c702仪器进行检测,试剂购自美康生物科技公司,其正常参考值范围分别为0.0~2.7 mg/L和0.0~10.0 μmol/L。丙氨酸氨基转移酶(alanine aminotransferase,ALT)、天门冬氨酸氨基转移酶(aspartate aminotransferase,AST)、γ-谷氨酰基转移酶(gamma-glutamyltransferase,GGT)检测采用罗氏Cobas8000 c702仪器进行,试剂购自罗氏公司,ALT、AST、GGT的正常参考值范围分别为9~50 U/L、8~40 U/L和10~60 U/L。25(OH)Vit D3采用罗氏Cobas e411仪器进行检测,试剂购自罗氏公司。25(OH)Vit D3充足定义为≥75 nmol/L,不足定义为50 nmol/L≤25(OH)Vit D3<75 nmol/L,缺乏定义为<50 nmol/L。仪器在检测样本前均进行定标,样本的变异系数在可控范围内,确保检验质量。
1.3不良妊娠结局资料收集 收集研究对象不良围产结局信息,包括早产、产后出血、羊水胎粪污染、小于胎龄儿(体重低于同胎龄儿平均体重的第5百分位)[9]、1 min和5 min Apgar评分<7分、低出生体重儿(出生体重<2 500 g)、新生儿黄疸和新生儿窒息等,并收集其实验室检查结果,用于综合性评价分析。
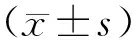
2 结果
2.1三组生化指标检测结果比较 轻度ICP组和重度ICP组CG、TBA、ALT、AST、GGT水平均显著高于健康对照组(P<0.05)。健康对照组25(OH)Vit D3水平均显著高于轻度ICP组和重度ICP组(P<0.05)。重度ICP组的CG、TBA、ALT、AST、GGT水平均高于轻度ICP组,25(OH)Vit D3水平低于轻度ICP组,差异有统计学意义(P<0.05)。见表2。

表2 三组生化指标检测结果比较[M(P25,P75)]
2.2三组25(OH)Vit D3评定情况比较 轻度ICP组和重度ICP组25(OH)Vit D3不足和缺乏情况高于健康对照组,差异有统计学意义(P<0.05)。见表3。

表3 三组25(OH)Vit D3评定情况比较[n(%)]
2.3CG、TBA与25(OH)Vit D3水平的相关性分析结果 孕妇外周血的CG、TBA水平与25(OH)Vit D3水平均呈负相关(r=-0.611,P=0.000;r=-0.489,P=0.000)。见图1,2。

图1 CG与25(OH)Vit D3水平相关性分析散点图
2.4ICP组与健康对照组的不良妊娠结局比较 ICP组医源性早产、自发性早产、羊水胎粪污染、低出生体重儿等不良妊娠结局的发生率均高于健康对照组,分娩孕周小于健康对照组,差异有统计学意义(P<0.05)。见表4。

图2 TBA与25(OH)Vit D3水平相关性分析散点图

表4 ICP组与健康对照组的不良妊娠结局*比较
3 讨论
3.1ICP孕妇CG、TBA和肝酶水平显著高于健康对照组 本研究结果显示,ICP孕妇的CG、TBA和肝酶水平高于健康孕妇,与国内大部分研究结果[10-11]一致。胆汁酸是肝脏胆固醇代谢的最终产物,在肝脏中形成,主要与甘氨酸和牛磺酸结合,然后分泌到胆汁中。ICP患者的胆汁酸盐从肝脏到胆囊的运输被破坏后会导致胆汁酸盐从肝细胞代偿性运输至血液中,导致ICP孕妇与健康孕妇的胆汁酸谱具有差异。CG是胆汁酸主要的缀合形式之一,当运输途径被破坏后,主要分泌至血液中,与其他的胆汁酸一起汇总成TBA,导致ICP患者血液中的TBA水平迅速增高。上述研究提示一旦发生胆汁酸盐转运途径的障碍,ICP孕妇体内的CG和TBA均可快速升高,因此联合检测CG和TBA对于鉴别诊断重度ICP比检测单个胆汁酸水平更加实用[11-12]。本研究结果显示,ICP孕妇血清ALT、AST和GGT水平显著高于健康孕妇。血清肝酶水平升高是肝细胞损伤的指标。研究显示,ICP孕妇体内ALT、AST和GGT的水平会随着时间的推移而逐渐增加,重度ICP孕妇的上述三种肝酶水平高于轻度ICP孕妇[13-14],且高水平的肝酶和TBA是预测不良妊娠结局的最佳生物标志物[14-15],表明ICP孕妇由于肝细胞受损,胆汁盐运输途径障碍,导致了孕妇胆汁淤积、肝功能异常,进而导致肝脏内分泌功能下降和肝脏的毒素降解能力下降,形成恶性循环,对围产期预后产生不良影响。
3.2ICP孕妇25(OH)Vit D3与CG和TBA水平呈负相关影响妊娠结局 文献报道,肝脏是25(OH)Vit D3储存和代谢的重要场所,25(OH)Vit D3在调节肝脏和肠内胆汁酸的排泄中起着重要的作用,可调控胆汁酸稳态[15]。一旦发生肝脏疾病,则常导致25(OH)Vit D3缺乏[16]。也有文献报道25(OH)Vit D3在细胞的免疫活化和增殖中起着免疫调节的作用,在胆汁淤积症患者体内,25(OH)Vit D3可通过调节B细胞和T细胞的功能来调节患者体内的促炎免疫反应[17]。此外,胆汁中的胆汁酸对维生素D受体(vitamin D receptor,VDR)具有高亲和力,它可与25(OH)Vit D3竞争维生素D受体[17]。小肠内维生素D受体缺乏,导致胆汁淤积严重,加重肝脏细胞毒性[18]。此可解释为何胆汁淤积性肝病中胆汁酸增加,伴随25(OH)Vit D3水平的降低。本研究发现ICP孕妇25(OH)Vit D3与CG和TBA水平之间存在显著的负相关,此与相关文献报道[19]一致。ICP是孕妇良性疾病,但与不良妊娠结局发生具有关联,研究报道子痫前期患者血清和胎盘组织中25(OH)Vit D3代谢受损与早产之间存在着统计学关联,此为ICP、25(OH)Vit D3与不良妊娠结局发生的病理生理学提供了一些重要的间接证据[20]。此外,25(OH)Vit D3可改善胎盘炎症细胞的浸润,对感染性早产有一定的保护作用[21],间接证明了低水平25(OH)Vit D3与不良妊娠结局存在关联。
3.3高水平的TBA和低水平的25(OH)Vit D3导致不良妊娠结局的发生 本研究结果显示,ICP孕妇发生不良妊娠结局的风险高于正常妊娠组,且25(OH)Vit D3缺乏和不足情况在重度ICP组的表现尤为明显。有研究结果显示高水平的TBA和低水平25(OH)Vit D3在此过程中起着关键的作用。孕妇的胆汁酸和毒素会通过胎盘循环转移到胎盘,导致早产、宫内窘迫甚至胎儿窒息等情况发生[22]。而ICP孕妇体内高水平的胆汁酸,尤其是CG,可能会使胎盘绒毛萎缩[22],从而导致胎盘滋养细胞浮肿,绒毛腔明显减少,进而导致胎盘绒毛腔中的母体血流量显著减少,发生胎儿缺氧和宫内窘迫等风险增加[22]。有研究显示,当TBA的截断值为34 μmol/L时,可有效预测早产、入住新生儿重症监护室(neonatal intensive care unit,NICU)的风险。而34周前诊断为ICP的孕妇,与34周后诊断为ICP的孕妇相比,其发生羊水胎粪污染和胎儿窘迫的发生率更高[23]。另国外的研究显示,有羊水胎粪污染、ICP孕妇的25(OH)Vit D3水平远低于健康、无羊水胎粪污染孕妇[24],表明高水平的TBA和低水平的25(OH)Vit D3容易导致羊水胎粪污染、早产等不良妊娠结局的发生[25]。
综上所述,ICP孕妇体内CG、TBA和肝酶水平升高,以及25(OH)Vit D3水平降低,对围产期妊娠结局产生不良影响。关于治疗ICP的同时加入维生素D对降低不良妊娠结局风险的作用,值得进一步探讨。
