钨基抗肿瘤纳米药物在肿瘤诊疗一体化中的应用
2022-07-07谢佳妮徐琦琦吕明珠刘成辉
雍 媛,谢佳妮,徐琦琦,吕明珠,王 欢,刘成辉
(1. 西南民族大学化学与环境学院,四川成都 610041;2. 成都大学食品与生物工程学院,四川成都 610106)
近年来,癌症作为人类死亡率最高的恶性肿瘤之一,对人类的生命健康造成了严重的威胁.据2012 年国际癌症研究中心对近5 年的诊断数据进行调查分析显示:全球有1 410 万例新发癌症患者,820 万例死于癌症,3 260 万例癌症患者正与癌症作斗[1-2].因此,亟需开发有效的新型药物和治疗方式,以有效消除癌症对社会、家庭和病人产生的巨大压力和痛苦.
目前,临床上治疗癌症的方法有许多种,大体上分为两种:传统法和新型法.传统治疗方法主要包含:手术治疗、放疗、化疗等,其中放射治疗因其具有适用范围宽、治疗效果好等优点,成为癌症治疗的一种最常用且最有效的手段.其主要原理是利用穿透力极强的高能电离辐射(比如:X-射线,γ-射线)直接作用于体内生物大分子或间接促使体内水分子发生电离,产生大量的具有细胞毒性的活性氧物质(Reactive Oxygen Species,ROS)来诱导单链或多链DNA 产生损伤作用,最终实现癌细胞分裂和肿瘤生长的抑制[3]. 近年来,随着纳米技术的迅猛发展,一些新型的治疗方法也迅速发展起来,主要包括:光动力治疗、光热治疗、基因治疗、免疫治疗及生物治疗等. 其中,光动力治疗和光热治疗作为光治疗的两种典型方式,其主要原理是利用光吸收试剂在光照射下产生大量的ROS来选择性杀死肿瘤细胞的一种治疗方式[4].虽然这些治疗方式在一定程度上均对肿瘤细胞的生长具有抑制作用,但是单一的治疗手段往往使癌症的治疗效果不彻底,从而引起复发使癌症的治疗面临巨大挑战.因此,如何彻底地杀死肿瘤细胞,并有效提高癌症的治疗效果是临床上亟待解决的重要科学问题.
为了解决这一难题,临床上将两者或两者以上的治疗方式结合在一起,形成综合治疗模式,这将成为治疗癌症的必然趋势. 与单一治疗模式相比,综合治疗具有以下优势:(1) 实现优势互补,达到更好的治疗效果;(2) 减少单一治疗模式所引起的毒副作用;(3) 降低依赖性,增强靶向性;(4) 最终实现1 +1 >2的效果.因此,如何选择合适的综合治疗方法并尽可能降低对正常组织的毒副作用,同时能够实现肿瘤细胞的有效抑制并显著提高癌症的治疗效果,在临床上具有十分重要的科学意义. 为此,随着纳米科学和纳米技术在生物医学领域的快速发展,纳米药物的出现为肿瘤的综合治疗提供了新的重大机遇[5]. 一方面:纳米药物本身可以作为药物或者药物载体负载多种其他治疗药物进入生物体内,实现联合治疗作用;与此同时,纳米药物还可以利用自身优异的物理化学性能,响应外界光、电、磁、热等刺激,将药物治疗与物理治疗有机结合在一起,充分利用医疗资源,实现协同增效.更重要的是,现代新型纳米药物系统可以将药物和成像功能集于一体[6],利用纳米材料的高渗透和高滞留效应(EPR 效应)将药物精准送达到病变部位,同时实现肿瘤的早期诊断和治疗.
为此,钨基抗肿瘤纳米药物可以作为一种优异的诊疗一体化试剂应用于癌症的早期诊断和有效治疗.其主要原因是其含有W 高原子序数原子,对X-射线吸收能力强,而且具有较高的光热转化效率,尺寸小易代谢等一系列优异性能.本文结合钨基抗肿瘤纳米药物在肿瘤诊疗一体化中的优势和潜能,概括了钨基抗肿瘤纳米药物的主要类型,简述了钨基抗肿瘤纳米药物在肿瘤诊疗一体化中的应用,并归纳了钨基抗肿瘤纳米药物综合治疗的主要方式和机制.最后总结和展望了钨基抗肿瘤纳米药物在生物医学领域面临的挑战和发展前景.
1 肿瘤的诊疗一体化概述
1998 年,John Funkhouser 作为药理学首席执行官首次提出了“诊疗一体化”一词作为“影响某种疾病状态的治疗或治疗的能力”的概念,随后“诊疗一体化”便作为一种新型的个性化治疗策略广泛应用在生物医学领域(图1)[7].其主要原理是通过新型的药物合成技术制备出同时具有成像和治疗功能的多功能智能药物,在诊断过程中阻止肿瘤的进一步发展,从而使肿瘤的后续治疗变得更加敏感. 近年来,纳米技术的快速发展为同时实现肿瘤的诊断和治疗提供了新的重大机遇,在肿瘤“诊疗一体化”中显示出广泛的应用前景.
图1 基于纳米药物的肿瘤诊疗一体化Fig.1 Integration of nanomedicine for oncology diagnosis and treatment
一方面,许多智能纳米药物利用自身优异的理化性能,可以作为造影剂或治疗试剂,对肿瘤实现诊断或者治疗.例如:先前许多被报道的含钆、铁或锰元素的高分子纳米材料自身具有单电子结构,将其注入肿瘤组织中,在外界磁场作用下作为造影剂应用于肿瘤的MRI 成像[8-9]. 另一方面,纳米药物还可以作为载体,利用自身尺寸小、比表面积高和活性强等特性,通过物理吸附或化学键合等方式将外界具有CT、MRI和PA 等成像功能的造影试剂或化疗、放疗、基因治疗、免疫治疗等药物同时运输到肿瘤部位,实现肿瘤早期的多模态诊断或有效治疗. 更重要的是,纳米药物自己本身还可以作为“诊疗一体化”试剂,将多模态成像和治疗功能集于一体,同时实现肿瘤的早期诊断和有效治疗,提高肿瘤靶向治疗的同时降低药物毒副作用.
2 钨基抗肿瘤纳米药物的诊疗一体化应用
为了提高肿瘤的治疗效果,可以将智能纳米药物作为诊疗一体化试剂用于实现肿瘤的早期诊断和治疗,阻止肿瘤转移并促进肿瘤的有效抑制. 诊疗一体化试剂是指可同时实现肿瘤的早期诊断,并能够利用自身优异的理化性能用于肿瘤的有效治疗、实现肿瘤个性化和具体化治疗的物质. 一般来说,理想的诊疗一体化试剂应该具备以下几个特征:(1) 诊疗一体化试剂不仅需要同时具有成像和治疗的功能,而且还需要拥有良好的生物相容性,以保证药物进入生命体后对人体正常健康组织和器官损害小;(2) 诊疗一体化试剂还需要合成方法简单、结构单一,以降低复杂且繁琐的合成过程所带来的高昂经济成本;(3) 诊疗一体化试剂还必须具备尺寸小、易代谢,保证有效浓度的体内药物用于实现肿瘤的成像和治疗,同时这些药物还需及时通过肾脏等器官排泄出去,以减少对其他正常组织和器官所带来的毒副作用;(4) 为了提高肿瘤的靶向性治疗,需要诊疗一体化试剂对肿瘤细胞和正常细胞具有特异性识别功能. 因此,随着纳米科技的发展,新出现的结构独特、性能优异的钨基纳米药物可以作为优良的诊疗一体化试剂用于肿瘤的诊断与治疗应用.下面对相关文献中用作诊疗一体化试剂的钨基纳米材料进行总结,按照材料成分、结构、物理化学性能及诊疗一体化应用等方面进行简要分类,主要概括为以下几种:
2.1 含钨过渡金属硫族化合物
二维晶体是一种只有一个或几个原子厚度,横向尺寸为纳米或亚微米的新型纳米材料[10-11].在用于生物传感和生物成像的各种纳米材料中,二维纳米材料因其独特的结构和光、电、磁、力、热等性能而受到人们的广泛关注,比如:可调的带隙结构[12],超高的比表面积[13],灵敏的光响应[14-16],独特的电性能[17],良好的柔韧性和加工性能等[18-20].自从2004 年Geim 和Novoselov 成功制备单层石墨烯后[21],二维纳米材料得到了迅猛的发展,尤其是以二维过渡金属硫族化合物(TMDCs)为代表. TMDCs 通常是由过渡金属元素(通常表示为M)和硫族元素(通常用X 表示)所组成的导体、半导体和绝缘体[22-24].具有种类繁多,性能可调,生物相容性好,新陈代谢快,原料丰富,制备方法简单,易于批量生产等特点[25]. 与此同时,它们还具有优异的光热性能和荧光特性,快速的异质电子转移以及高密度的电子态,使得它们广泛应用于生物医学领域,尤其是肿瘤的诊断和治疗.
二硫化钨作为一种典型的过渡金属硫族化合物,其对应的纳米尺度的化合物可以通过研磨、机械剥离或超声破碎法制备而得到.二硫化钨纳米药物具有窄的带隙结构(1.35 eV),在紫外、可见和近红外光区具有较强的吸收,因此,二硫化钨纳米药物可作为一种良好的光热吸收试剂应用于肿瘤的光声成像和光热治疗,这是因为热转化效率η 与温度T 及能量Q 存在以下关系:
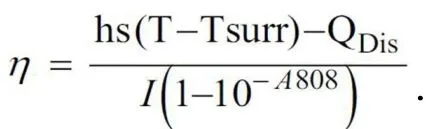
其中,T 和Tsurr分别是纳米材料溶液被近红外光照射之后的实际温度及室温,I 为近红外光入射强度,A808是指材料在近红外光808 nm 处的吸收,因此,材料在近红外光区的吸收以及入射光强度会对热转化效率η 造成显著的影响,所以,在近红外光区具有强烈吸收的材料具有更高的热转化效率[26].与此同时,二硫化钨纳米药物中含有高原子序数的W 原子,对X-射线吸收能力强.可以与高能电离辐射作用产生光子、康普顿电子、正负电子对以及俄歇电子等放射粒子,直接或间接引起细胞内DNA 损伤,实现CT 成像和放射治疗作用. 更重要的是,一些二硫化钨纳米药物具有超小的尺寸和良好的生物相容性,进入生物体后,在体内具有较长的血液半衰期,而且可以通过肾脏迅速排出体外,减少在体内长期蓄积对正常组织所带来的毒副作用. 因此,二硫化钨纳米药物可以作为一种优良的诊疗一体化试剂替代品应用于肿瘤多模式成像和治疗.
近年来,Gu 课题组发现经 PEG 修饰过的 WS2(WS2-PEG)量子点对近红外光和X-射线吸收均比较明显,在808-nm 近红外光和 X-射线共同作用下,WS2-PEG 量子点不仅表现出CT/PA 双模式成像功能,而且还产生明显的光热效应,同时表现出放射增敏效果(图2)[27]. 在细胞和活体层次证实WS2-PEG同时采用808-nm 近红外光和-射线处理后,细胞内部产生大量的活性氧物质,用于阻止细胞生长和抑制肿瘤,作为诊疗一体化试剂实现CT/PA 双模式成像介导的光热/放射协同治疗[27]. 此外,Liu 团队[28]进一步构建了在WS2中掺杂Gd,形成WS2@Gd-PEG,其中Gd 原子含有7 个单电子结构,在外界磁场作用下表现出优良的MR 成像效果,同时,W 和Gd 原子均具有高的原子序数,具有强的X-射线吸收能力,且WS2在近红外光区吸收较强,因此,在外界X-射线和近红外光共同作用下,可以实现PA/CT/MR 三模式成像,且WS2@Gd-PEG 通过吸收大量的近红外光和X-射线,采用光热转换和物理放射增敏的作用产生大量的ROS,有效地实现PA/CT/MR 三模式成像介导的光热/放射联合治疗.在此基础之上,Liu 课题组[29]进一步通过自组装作用将氧化铁纳米粒子(IONPs)吸附在WS2纳米片表面,然后再涂上二氧化锰(MnO2),并在其表面接枝上聚乙二醇(PEG),形成WS2-IO/S@MO-PEG 纳米材料.获得的WS2-IO/S@MO-PEG 纳米材料对pH 值高度敏感,其中IONPs 可作为pH 惰性T2对比剂探针,MnO2可作为pH 敏感T1 对比剂探针,从而导致WS2-IO/S@MO-PEG 纳米材料实现肿瘤pH响应性MR 成像功能. 同时,利用WS2纳米片对近红外光和X-射线强的吸收,实现癌症的光热治疗和反射治疗,并且MnO2能够分解肿瘤内源性H2O2和缓解肿瘤缺氧的能力,进一步克服乏氧导致的放疗抵抗.因此,WS2-IO/S@MO-PEG 纳米材料可作为一种优良的诊疗一体化试剂应用于肿瘤微环境pH 响应的MR成像和光热/放射治疗.
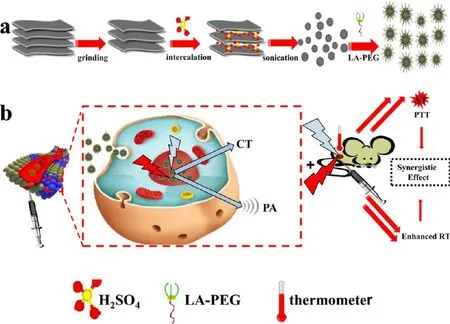
图2 WS2量子点作为诊疗一体化试剂应用于肿瘤的诊断和治疗Fig.2 Application of WS2 QDs as diagnostic and therapeutic integrated reagents for tumor diagnosis and treatment
2.2 含钨多金属氧酸盐纳米药物
多金属氧酸盐(Polyoxometalates,POMs)是一种重要的无机纳米团簇分子,拥有类似于“三明治”结构,由中心的过渡金属原子或稀土元素与两侧的含氧配体连接而成.许多杂原子,比如:Gd,Mn 和 Cu 等可以嵌入到多金属氧酸盐框架结构中,以赋予多金属氧酸盐具有各种独特的电学结构和优异的物理化学性能,这些纳米团簇在分析学[30-31]、磁学[32-33]、光学[34]和催化领域[35-36]具有广泛的应用,尤其是在生物医学领域表现出巨大的应用潜能. 近年来,大多数POMs 在体内和体外均表现出显著的抗肿瘤、抗菌和抗糖尿病等生物活性,且具有成像功能. 例如:顺磁性稀土元素Gd3+,能够很容易地嵌入到多金属氧酸盐的框架结构中形成新分子,这些含钆元素的多金属氧酸盐已经被证实可作为一种有效的MR 造影剂,并且比常用的商用的MR 造影剂的造影性能优异[37],是因为它们具有较大的分子量以及刚性结构.
含钨多金属氧酸盐(W-POMs)纳米药物作为POMs 中的一种,通常表现出尺寸小,水溶性好,易代谢等特点,因此利于其作为纳米药物或药物载体应用于生物医学领域. 同时,W-POMs 纳米药物中同时含有高原子序数W 和过渡金属原子或稀土元素,在外界X-射线照射下,表现出强的X-射线衰减能力,因此可应用于肿瘤的CT 成像和放射治疗. 此外,氧化型W-POMs 纳米药物还可以利用自身特殊理化性能从氧化还原作用、酸性应激、内源性巯基的耗竭等途径与肿瘤微环境中的活性物质 (如GSH、H2O2等) 产生一系列生化反应,实现肿瘤微环境调控.更重要的是,在肿瘤微环境应激作用下,产物还原型W-POMs 纳米药物通常表现出较强的近红外光吸收和较大的尺寸,实现肿瘤原位的自聚集,增强药物在肿瘤部位的蓄积,并具有高效的光热转化效率,从而激发出其光声成像和光热治疗的作用,实现肿瘤诊疗一体化. 值得一提的是,肿瘤微环境在W-POMs 纳米药物的调控作用下,对外界X-射线和近红外光刺激表现出更为敏感的性质,从而提高W-POMs 纳米药物的抗肿瘤性.
Gu 课题组首次报道了多钨酸钆 (GdW10) 经牛血清白蛋白(BSA)修饰之后,形成的GdW10@BSA 纳米团簇可作为一种超小的诊疗一体化试剂应用于肿瘤的诊断和治疗(图3)[38].其主要原因是:含有高原子序数Gd 和W 原子的GdW10@BSA 纳米团簇不仅表现出对X-射线较强的吸收作用,而且被还原之后形成的还原型多钨酸钆对近红外光的吸收也明显增强.后续进一步证实其优良的光热转化效应对细胞可产生明显的杀伤作用,且强的X-射线衰减能力这一特性促使GdW10@BSA 纳米团簇同时具有CT 成像和放射治疗功能,实现CT 成像介导的光热和放射治疗.更重要的是,超小的GdW10@BSA 纳米团簇可通过肾脏迅速排出体外,减少体内长期蓄积产生的毒副作用.
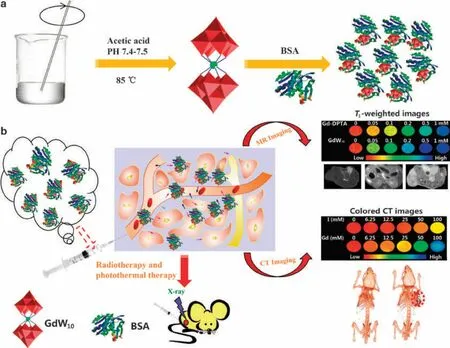
图3 GdW10@BSA 纳米团簇的诊疗一体化应用Fig.3 Application of GdW10@ BSAnanoclusters for diagnosis and treatment integration
在此基础之上,Chen 及其合作者[39]进一步利用EDC 反应将二维Ti3C2MXene 纳米片与含钨多金属氧酸盐 (GdW10) 复合在一起,形成GdW10@Ti3C2复合纳米片[39]. 实验证实GdW10@Ti3C2复合纳米片可同时作为MR 和/或CT 成像造影剂,用于指导后续肿瘤的治疗,是因为该复合物中含有大量的Gd 和W 高序数原子.同时,GdW10@Ti3C2复合纳米片在肿瘤光热治疗方面显示出巨大的潜力. 而且在细胞和活体层次,GdW10@Ti3C2复合纳米片均被证实具有高的生物相容性,这些优异的物理化学性能为后续实现其临床医学转化提供了可能.
2.3 其他含钨纳米药物
与二硫化钨类似,硒化物、氧化钨及钨青铜等钨基纳米药物也可以作为优良的诊疗一体化试剂应用于生物医学领域[44].一方面,大多数这些纳米药物表现出尺寸小,易代谢,具有良好的生物相容性和稳定性,进入生物体后不会引起明显的毒副作用. 与此同时,这些纳米药物也具有较窄的带隙结构,对可见和近红外光表现出较强的吸收能力,从而能在光声成像和新型的光热治疗这一领域具有巨大的应用潜能.而且,这些纳米药物均含有钨原子,利用高原子序数原子对X-射线吸收较强的这一性能,这些纳米药物进入生物体内,一旦暴露在外界X-射线下,均可载体内产生大量的康普顿电子和俄歇电子等二次粒子,直接或间接与体内DNA 作用,导致DNA 单链或双链产生损伤,从而引起肿瘤细胞凋亡.并且,这些纳米药物还可以利用自身尺寸小、比表面积大和活性高等优势,将其他成像试剂和治疗药物负载进入体内,通过本身较高的生物膜屏障穿透性、较强的组织器官靶向性和优异的缓释、控释等性能,实现肿瘤的多模态成像和联合治疗,关于这些钨基纳米药物在诊疗一体化方面的应用较多,本文不再展开论述,请感兴趣的读者参考以下文献[40-45].
3 总结与展望
虽然钨基抗肿瘤纳米药物作为诊疗一体化试剂具有许多独特的优势,比如:均含有高原子序数W 原子,对X-射线具有强的衰减能力;绝大部分在近红外光区具有较强的吸收,同时利用自身光热转换性能实现高的光热转化效率;此外,许多钨基纳米药物还含有其他一些重要的过渡金属元素或重要组成部分,因此不仅可作为诊疗一体化试剂,同时还可以应用于肿瘤的综合治疗;以尺寸小、易代谢;更重要的是,大部分这些纳米药物具有尺寸小、易代谢生物相容性良好等特点,为实现癌症的早期诊断和有效治疗提供了可能.然而,钨基纳米药物的研究仍处于起步阶段,既充满潜力又有许多问题需要进一步解决.
(1)需要深入研究钨基纳米药物的长期稳定性和生物安全性.目前,基于钨基纳米药物的诊疗一体化研究大多只关注于其应用性能.其生物相容性通常是简单通过几天的细胞活力测定来研究的,基于钨基纳米药物对细胞增殖和细胞功能的影响尚不清楚. 此外,还应进一步深入研究钨基纳米药物长期在生物体内的运动、代谢、分布、停留时间、降解和生理毒性等.含有高原子序数过渡金属元素的钨基纳米药物是否对免疫和生殖系统有毒副作用,目前还没有系统性研究.
(2)在临床中,不同影像学,如PET/MRI 成像正在进行有效的结合. 因此,开发和构建适用于多模态成像和治疗的造影剂将是十分有必要的.钨基纳米药物还没有广泛应用于PET 成像,但临床PET/MRI 成像需要的纳米成像探针不仅应该具有MRI 成像功能,而且也应该拥有PET 成像性能.
(3)未来的诊疗一体化方法应考虑到癌症研究的多个方面,以满足针对性较强的实际临床应用,这不仅要求成像诊断本身应该从传统的“解剖成像”发展到“分子成像”,而且治疗也应该针对每一个源于特定基因突变组的癌症病例.
(4)目前大多数钨基纳米药物作为诊疗一体化试剂已经应用于肿瘤的综合治疗,仅仅从表面研究其综合治疗效应,但是其协同治疗机制的研究还相对较少.这不仅需要深层次明确钨基纳米药物的综合治疗机制,为解释生物效应应用提供依据;同时也有助于进一步理解钨基纳米药物、多模式成像与肿瘤联合治疗之间的相互作用,进而为改进钨基纳米药物的结构和性能、降低生物毒性、拓展和发现新的应用领域等提供指导性意见.
