杭州市临床试验机构“院外CRC”的工作现状调查与思考
2022-07-06徐叶偲许鸣
徐叶偲 许鸣
(1.浙江大学医学院附属邵逸夫医院临床试验机构;2.浙江大学医学院附属邵逸夫医院伦理委员会)
临床试验是指以人体为对象,为了确定试验药物的疗效与安全性的系统性试验。根据国家药监局药品审评中心的药物临床试验登记与信息公示平台的数据显示,截至2022年3月14日平台登记的我国药物临床试验项目总数为16120项,其中2021年公示的项目有3276项。我国自2003年GCP法规施行以来,对试验中的伦理、研究者职责、试验质量等方面都提出了具体要求。在我国临床试验项目庞大基数和国家对试验质量要求越来越严格的背景下,CRC职业应运而生,它解决了研究医生因医务工作繁忙无法及时完成试验中繁琐的非医学判断工作的问题。CRC经主要研究者授权在试验中协助研究者进行一些事务性工作,其工作内容涉及试验全过程,CRC是试验的参与者、协调者[1]。CRC可以帮助研究者及时发现和解决问题,减少工作失误,其重要性使其职业地位日益稳固[2]。CRC的工作质量很大程度上影响着整个临床研究的质量,加强CRC的管理,是试验机构质量管理的一项重要内容[3]。现阶段我国CRC聘用方式通常分为院内CRC、院外CRC。前者与临床试验机构(即医院,简称“机构”)签订人事合同,属医院员工;后者为SMO(site management organization,临床试验现场管理组织)派遣到机构承担临床试验相关工作的人员。基于人事编制、职称晋升等限制,院外CRC服务外包模式在我国较为普遍。目前,大部分机构尚无健全的CRC管理制度,缺乏完善的监管方法[4]。如何科学化管理院外CRC考验着机构的水平。本文拟通过调查在杭州市临床试验机构工作的院外CRC的工作现状,试图去发现相关管理问题并提出相关措施。
一、资料与方法
笔者于2022年3月从27家位于杭州市的试验机构中抽取了两百多位院外CRC进行了问卷调查,问卷包括了其人口学特征、职业背景、工作量、工作中面临的问题。本次调查采取无记名填写方式,并向其保证对问卷资料进行保密。在取得其知情同意后,以问卷形式发放调查问卷。问卷回收后,对调查问卷进行核对和统计分析。
二、问卷调查结果
(一)被调查者基本情况
共发放问卷270份,最终回收有效问卷244份(有效回收率90.37%),其中女性CRC占89.34%;以90后年龄段为主;超过一半是药学专业,其次是护理学专业,约占三分之一;超过七成是本科学历;超六成通过了国家四六级英语考试。CRC需要较好的英文水平和专业背景,需要协助研究者录入电子病例报告表,且CRC的工作内容较为复杂细致,年轻女性更愿意从事该工作。本研究样本的人口学特征如表1。

表1 被调查者人口学特征
超六成被调查者工作年限在3年以下;有跳槽经历的约占四成;约七成被调查者每月到手收入不足一万;超六成被调查者对收入不满意;有跳槽经历的约占四成;超过三成表示可能会离开当前的公司。这些数据反映了杭州市院外CRC较大的流动性。促使CRC离职的因素占比最大的是薪资因素(占85.25%),其次是因为晋升受限(占69.67%),工作量大的因素占50%。被调查者的职业背景如表2。
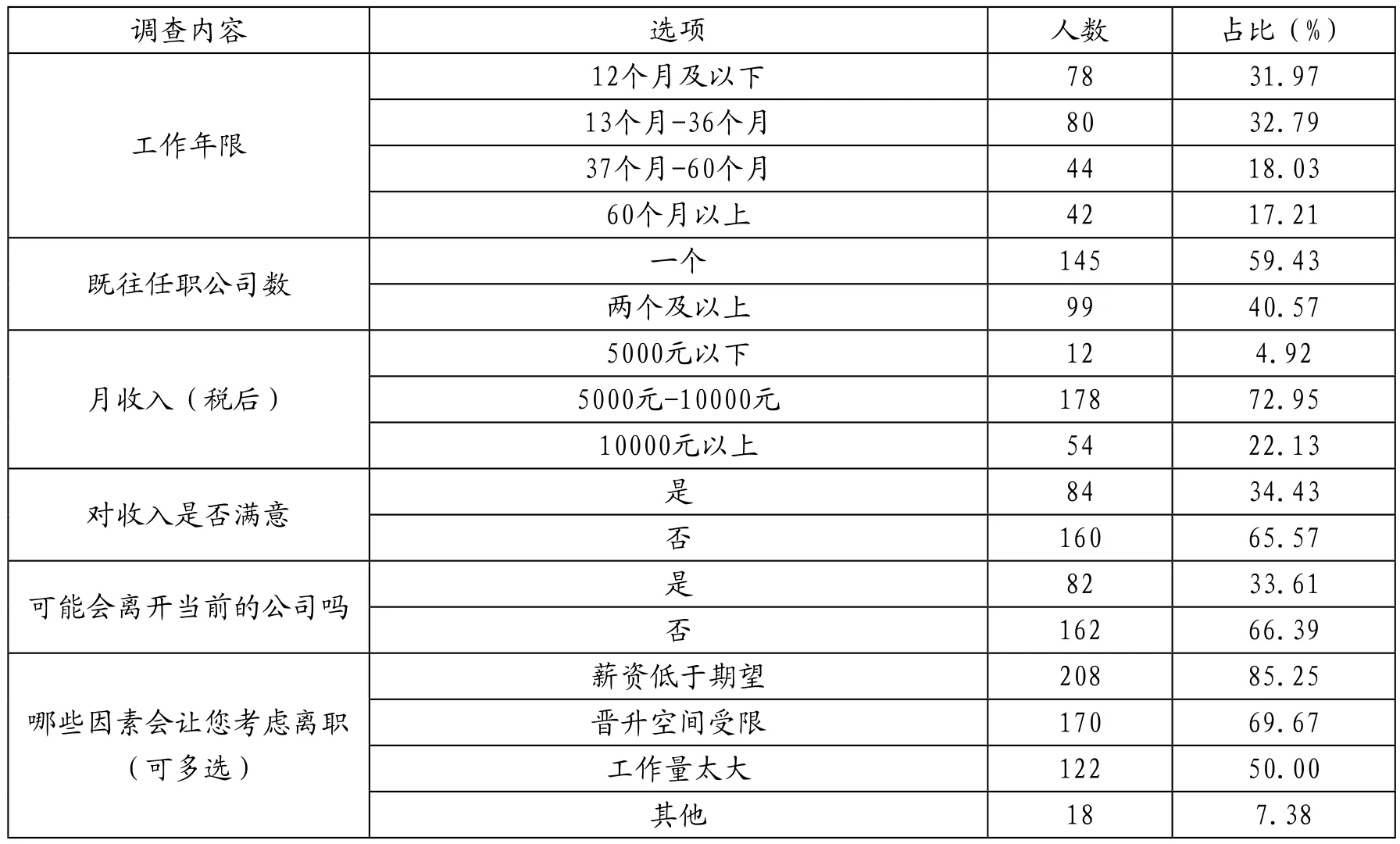
表2 被调查者的职业背景
(二)被调查者工作情况调查
在244位被调查者中,CRC仅负责一家机构项目的占68.85%,负责两家及以上的占31.15%;同时只承接一个项目的仅占9.02%,其余CRC均同时承接2个及以上的项目,甚至有24.59%的CRC同时负责6个及以上的项目;仅3.28%的CRC从不加班,超过三成的CRC表示经常加班甚至每天加班。以上数据可见其工作强度普遍较大。被调查者的工作量如表3。

表3 被调查者的工作量情况
CRC的工作地点在试验机构,超过三成的被调查者认为在医院工作无归属感;仅59.02%的试验机构对CRC的工作有进行考核;仅七成试验机构对其有进行培训。没有固定工作场所和工位、项目相关方不配合自己工作占六至七,是成被调查者认为工作中最困难的地方,超过三成被调查者认为工作的阻碍部分来自于受试者对自己不任性。被调查CRC工作中面临的问题调查结果如表4。

表4 被调查者工作中面临的问题
三、讨论和建议
(一)院外CRC存在的问题
CRC服务外包的模式在一定程度上影响了CRC队伍的稳定性:(1)试验机构被动接受院外CRC,院外CRC对医院工作流程不了解,对医技部门的协调工作心余力绌,不容易得到研究者的重视和相关部门的配合,容易造成院外CRC流动。(2)院外CRC的人事关系不在试验机构,不属于医院员工,不容易得到受试者信任,从而难以对医院有归属感[5]。(3)调查发现院外CRC普遍工作量较大、薪资普遍不高,加上国内没有统一针对CRC的执业评定体系,这些因素加剧了院外CRC的流动性。
此外,院外CRC作为临床试验的一线执行者,其工作环境较为艰辛,由于大部分医院用房紧张,导致大多数院外CRC没有专门的办公场地、工位所。
(二)对院外CRC管理的一些建议
1.CRC聘用及备案管理
CRC由SMO公司委派至试验机构工作,这就要求机构建立起相关管理机制。一方面,机构要甄选提供CRC服务的SMO公司[6],因为市场上SMO公司众多,层次不齐。申办方、SMO公司与机构签署CRC服务三方协议,申办方委托SMO指派CRC到试验机构提供临床研究协助服务,并由申办方支付CRC费用。为防止利益冲突,不允许申办方直接聘用CRC。另一方面,机构应对CRC实行备案管理,要求其开展工作之前向机构办提供公司派遣函、简历、身份证复印件、GCP证书以及主要研究者对CRC在项目中的授权书。
2.CRC培训和考核
CRC在工作中需要掌握临床试验的技能及相关管理工具,因为试验项目从启动到关闭,需要经历繁琐复杂的流程。面对未知的药物不良反应,有专业培训经历的CRC是降低试验风险的一个要素。除了SMO对CRC基本的GCP法规培训,机构也应承担起CRC培训的担子,比如对其进行医院临床试验相关流程的培训,熟悉机构相关工作程序可避免不必要的错误。CRC的工作场所涉及病区、手术室、生物样本库等物理空间,为提高其自我保护能力,机构可以对其做医院感染管理、出入手术室规则、生物安全等内容的培训,落实个人防护措施。此外,机构还可以每月开展CRC座谈会,报告项目进度,反馈分析日常工作中发生的问题,持续改进质量。关于对CRC的考核,仅在入职前对其做资质的审核,无法考察其工作效率和质量。而研究者作为接触CRC最频繁的人员,最有资格给CRC的工作情况进行评价。因此,试验机构可结合日常项目质控情况、研究者评价,综合评定CRC的工作表现,如发现其工作质量较差,机构有权提出更换人员。
3.为CRC提供良好的工作环境
试验机构应以人为本[7],将院外CRC当成本院员工一样去管理,为其配备工作服、工作牌,协调相关部门给予其良好的工作条件,给予其在医院工作的归属感。建议有条件的试验机构尽可能为院外CRC提供专门的办公区域,不仅可以提高其工作效率,而且有利于试验机构统一管理人员。
4.重大突发公共卫生事件下的CRC管理
在重大突发公共卫生事件响应下,为保障院外CRC安全,机构应制定相关政策,制定应急情况下的各类预案,如重大突发公共卫生事件下临床研究人员现场访视工作原则及防护须知、院外CRC工作指引等。对来院的CRC实行预约登记、分时段办公制度,进行人流控制,并为其提供充足的防护物资,如口罩、防护服、护目镜、乳胶手套、消毒液等,保障其人员安全。
5.优化CRC工作流程
试验机构使用临床试验电子管理系统,信息化系统充分显示了方便、实时、低人力成本等优势[5],CRC等临床试验相关人员可以在线向机构和伦理委员会递交临床试验相关资料,极大提高了其工作的便捷性,降低院内感染风险。
四、小结
本次调研发现,杭州市院外CRC的工作现状受多方面影响,这些因素影响了其对机构的归属感和工作的主观能动性。CRC对于临床试验至关重要,科学地、人性化地管理院外CRC,建立起完善的院外CRC管理体系,才能促进临床试验项目的质量和进度。
