CoFe2O4@CSC材料的合成及其对水样中拟除虫菊酯类杀虫剂的磁固相萃取
2022-07-06李小路吕思颖郑小妮赖嘉豪崔世海
李小路,吕思颖,郑小妮,赖嘉豪,杨 静,崔世海
(1.南京师范大学化学与材料科学学院,江苏省生物医药功能材料协同创新中心,江苏省生物功能材料重点实验室,江苏 南京 210023) (2.江苏环保产业技术研究院股份公司,江苏 南京 210019)
作为重要的人工合成杀虫剂,拟除虫菊酯具有高效、广谱等特性,在我国农业生产中有广泛的应用. 研究表明,虽然环境水体中拟除虫菊酯类物质的浓度相对较低[1-3],但其对水生动物(如鱼类)具有较高的毒性,人体长时间的暴露亦会导致肌肉痉挛、呼吸衰竭等不良症状. 因此,开发拟除虫菊酯类农药的痕量检测方法具有重要的理论与应用意义.
与其他处理技术相比,固相萃取技术(SPE)可减少有害有机溶剂的使用,简化繁琐的样品洗脱步骤,易于实现自动化,并可对样品中的痕量化合物进行高倍的富集. 另一方面,由于固相萃取过程的扩散和传质速率有限,萃取过程的平衡时间通常较长. 磁固相萃取(magnetic solid phase extraction,MSPE)与传统的SPE技术不同,这种微纳米颗粒可完全暴露于待测体系,并与之充分接触,能够在短时间内从大体积的待测体系中吸附和萃取待测物质. 此外,磁性颗粒易于通过外加磁场从待测体系中分离和收集,避免了繁琐的过滤或离心过程. 常用的磁性载体有四氧化三铁和铁酸钴等,具有极高的磁性和稳定性,其表面可用吸附材料改性. 常用的吸附材料包括碳纳米管、C3N4、石墨烯、金属有机框架和生物质材料等[4-9],其中生物质材料来源广泛、理化性质稳定、比表面积较大,且能较好地吸附水体中的有机污染物. 本文拟采用甘蔗皮为碳源,以CoFe2O4为磁核、NaHCO3为致孔剂制备CoFe2O4@CSC碳化材料,选取甲氰菊酯(fenpropathrin,Fenp)、联苯菊酯(bifenthrin,BFT)、溴氰菊酯(deltamethrin,DMT)和高效氯氟氰菊酯(lambda-cyhalothrin,L-CHT)为目标污染物,探讨MSPE过程中的外界因素对样品回收率的影响,建立痕量拟除虫菊酯类物质的样品预处理方法,并应用于实际水样的检测.
1 实验方法
1.1 主要试剂及仪器
六水合氯化铁(III),六水合硝酸钴(II),氢氧化钠,碳酸氢钠,无水乙醇(EtOH),氨水(25%),盐酸(37%),氯化钠,甲醇,丙酮,乙腈,均来源于国药集团化学试剂有限公司;甲氰菊酯,高效氯氟氰菊酯,溴氰菊酯,联苯菊酯,均来源于上海市农药研究所;以上药品均为分析纯. 实验中所使用纯净水均产自杭州娃哈哈集团有限公司. 实际环境水样主要包括长江水、玄武湖水、自来水,所有采集样品均进行过滤预处理.
超声波振荡器HT-500A,梅特勒-托利多仪器有限公司;管式炉OTF-1200X,合肥科晶材料技术有限公司;透射电子显微镜H-7650,日本Hitachi公司;扫描电子显微镜S-3400N II,日本Hitachi公司;红外光谱仪Tensor 27,德国布鲁克公司;热重分析仪STA449F3,德国Netzsth公司;XRD粉末衍射仪X’TRA,美国赛默飞世尔科技有限公司;BET测试仪ASAP 2050,美国微电子仪器有限公司;振动样品磁强计VSM 7404,美国Lake Shore公司;高效液相色谱仪Waters 1525,美国沃特世公司.
1.2 实验步骤
1.2.1 CoFe2O4纳米颗粒的制备
CoFe2O4材料的合成基于文献[10]报道并略作改进. 在30 mL纯水中依次加入20 mmol FeCl3·6H2O及10 mmol Co(NO3)2·6H2O,并调节体系pH至12. 在105 ℃下烘干10 h后转移至管式炉中,在升温速率为5 ℃/min及氩气保护下于400 ℃热解4 h. 冷却至室温后洗涤并干燥,即可得到CoFe2O4纳米颗粒.
1.2.2 CoFe2O4@CSC复合材料的制备
将清洁的甘蔗皮于110 ℃下热处理24 h后研磨成粉末备用. 分别取一定质量的CoFe2O4、甘蔗皮粉和NaHCO3(0.5 g)混合均匀后于500 ℃氩气环境下碳化. 冷却至室温后以纯水及乙醇交替洗涤并干燥,所得产品即为CoFe2O4@CSC复合材料. 其中,CoFe2O4与甘蔗皮粉的质量比为0.5∶1、1∶1及2∶1,相应制备所得材料命名为CB0.5、CB1及CB2,未添加CoFe2O4合成的材料为CSC.
1.3 磁固相萃取实验
在拟除虫菊酯溶液中加入适量CoFe2O4@CSC材料,超声至吸附平衡后,在外加磁场作用下分离吸附剂并进行洗脱,应用HPLC对洗脱液进行分析检测,计算污染物回收率. 仪器色谱条件为:检测波长:220 nm;流动相(体积百分比):乙腈∶水=80∶20;流速:1.0 mL/min;进样量:20.0 μL;柱温:30 ℃.
2 结果与分析
2.1 形貌分析
材料的电镜图如图1所示,其中A、B、C分别为CoFe2O4、CSC及CB1材料的TEM图,D、E、F为相应的SEM图. 图1(B)结果显示,甘蔗皮在热解后形成多孔结构,其致孔原理为:NaHCO3在高温下会分解为Na2CO3、H2O和CO2,H2O和CO2能起到物理活化活性炭的作用,碳酸钠可以和生物质炭继续反应生产CO. 图1(C)中,由于CoFe2O4的复合,CB1材料的介孔较CSC有所减少. 此外,SEM图(图1(E)、(F))均可明显观察到两种材料表面分布着较为均匀的孔隙.

图1 CoFe2O4(A)、CSC(B)和CB1(C)的TEM图;CoFe2O4(D)、CSC(E)CB1(F)的SEM图Fig.1 TEM images of CoFe2O4(A),CSC(B)and CB1(C);SEM images of CoFe2O4(D),CSC(E),CB1(F)
2.2 XRD分析
图2(A)为材料CSC、CoFe2O4及CB1的XRD. 结果表明,CSC在2θ为26.475°处出现的衍射峰可归结为无机碳材料的(002)晶面. CoFe2O4在2θ为30.084°、35.437°、43.058°、56.973°和62.585°处的衍射峰分别对应于(220)、(311)、(400)、(531)和(511)晶面(JCPDS卡22-1086). 而CB1复合材料中同时显示了CoFe2O4及CSC的特征峰,表明复合材料的成功合成.

图2 CoFe2O4、CSC和CB1的XRD图(A)、红外光谱图(B)及热重曲线(C)Fig.2 XRD patterns(A),infrared spectra(B)and thermogravimetric curves(C)of CoFe2O4,CSC and CB1
2.3 FT-IR分析

2.4 热稳定性分析
材料在N2气氛的TG图如图2(C)所示. CoFe2O4材料在30~1 200 ℃之间少量的质量损失可归因于材料表面的水分挥发. CSC的质量变化主要分为两个阶段,其中,30~400 ℃之间的质量损失归因于物理吸附水的消耗[11];在400~900 ℃范围内较大的质量损失是由于生物炭材料部分碳元素转化为CO2;温度超过900 ℃时,其结构趋于稳定. CB1的TG曲线与CSC类似,但由于复合材料中CSC的质量分数相对较低,其质量损失相对较低. 所以,CB1在400 ℃下具有良好的热稳定性.
2.5 BET分析

表1 BET实验理化参数Table 1 Physico-chemical parameters derived from BET experiments
材料的BET结果如图3所示. 其中,图3(A)为CoFe2O4和CB1的N2吸脱附曲线图,(B)为对应的孔径分布图. 图3(A)中,CoFe2O4和CB1均为带有H3滞后环的Ⅱ型等温线,为典型的介孔材料[16]. 材料CB1的比表面积明显增大,平均孔径在30 nm左右. 基于Barrett-Joyner-Halenda(BJH)方法所计算的材料理化参数见表1,其中SBET、Vpore及Rpore分别为比表面积、孔体积与孔直径.
2.6 磁性分析
磁性是磁固相萃取所使用材料的重要特征,在实际应用中,足够的磁性可确保材料快速从体系介质中分离. 图3(C)表明CoFe2O4和CB1材料均存在磁滞回线,即所制备复合材料均具有一定的铁磁性[10]. 与CoFe2O4相比,CB1的磁性强度有所下降,归因于材料中CoFe2O4质量分数的下降.

图3 CoFe2O4和CB1的N2吸脱附曲线(A),孔径分布(B)和磁化曲线(C)Fig.3 N2 adsorption and desorption curves(A),pore size distribution(B)and magnetization curves(C)of CoFe2O4 and CB1
2.7 MSPE条件的优化
2.7.1 材料的最佳选择
取浓度均为0.02 mg/L的100.0 mL Fenp、L-CHT、DMT和BFT混标溶液各3份,分别加入40 mg CB0.5、CB1及CB2复合材料进行磁固相萃取实验,并用2 mL乙腈洗脱,测定目标污染物的回收率,结果如图4所示.
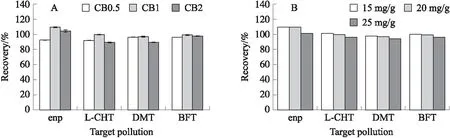
图4 3种材料对4种菊酯类农药的回收率(A)以及CB1对4种不同浓度菊酯类农药的回收率(B)Fig.4 Recoveries of four pyrethroid pesticides with three composites(A),and the recovery of CB1 to four different concentrations of pyrethroid pesticides(B)
图4(A)表明CB1复合材料对4种拟除虫菊酯均具有最高的回收率,分别为100.44%、99.74%、96.82%及99.22%. 而CB2及CB0.5材料较CB1均有所降低. 图4(B)为CB1对浓度分别为15、20和25 mg/L的4种菊酯类农药的回收率,表明随着浓度的升高,回收率略有下降,但仍保持在90%以上.
2.7.2 条件实验
图5(A)显示随着材料投加量的增加,目标分析物的回收率亦有所增加. 当CB1投加量达到40 mg时,回收效果最好. 继续增加复合材料用量,其回收率有所下降,可能是由于材料的聚集导致吸附位点的降低[17]. 因此,复合材料投加量的最佳实验条件为40 mg.
图5(B)显示4种目标污染物的回收率均在中性体系中达到最佳. 这主要是因为分子结构中均含有酰氧基官能团,可在酸性或碱性条件下发生水解,导致其表面带有电荷. 此外,体系中的OH-亦会与目标物在CB1碳化材料上发生竞争性吸附[13].
磁固相萃取速率的快慢是决定该方法能否在实际分析检测中应用的重要参数. 图5(C)表明,当吸附时间达到10 min时,Fenp、L-CHT、DMT及BFT 4种杀虫剂在CB1材料表面均已达到吸附-解吸平衡.
吸附目标污染物的复合材料能否被成功洗脱及材料的稳定性能对磁固相萃取技术尤为重要. 图5(D)表明,4种洗脱剂中,使用乙腈时Fenp、L-CHT、DMT和BFT的回收率分别达到100.44%、99.74%、96.82%及99.22%. 图5(E)表明,富集因子,即富集倍数为50时,回收率最高. 图5(F)表明CB1经6次循环使用后,样品回收率仍能分别达到95.37%、89.61%、91.74%及90.11%,表明CB1具有良好的重复使用性和结构稳定性.
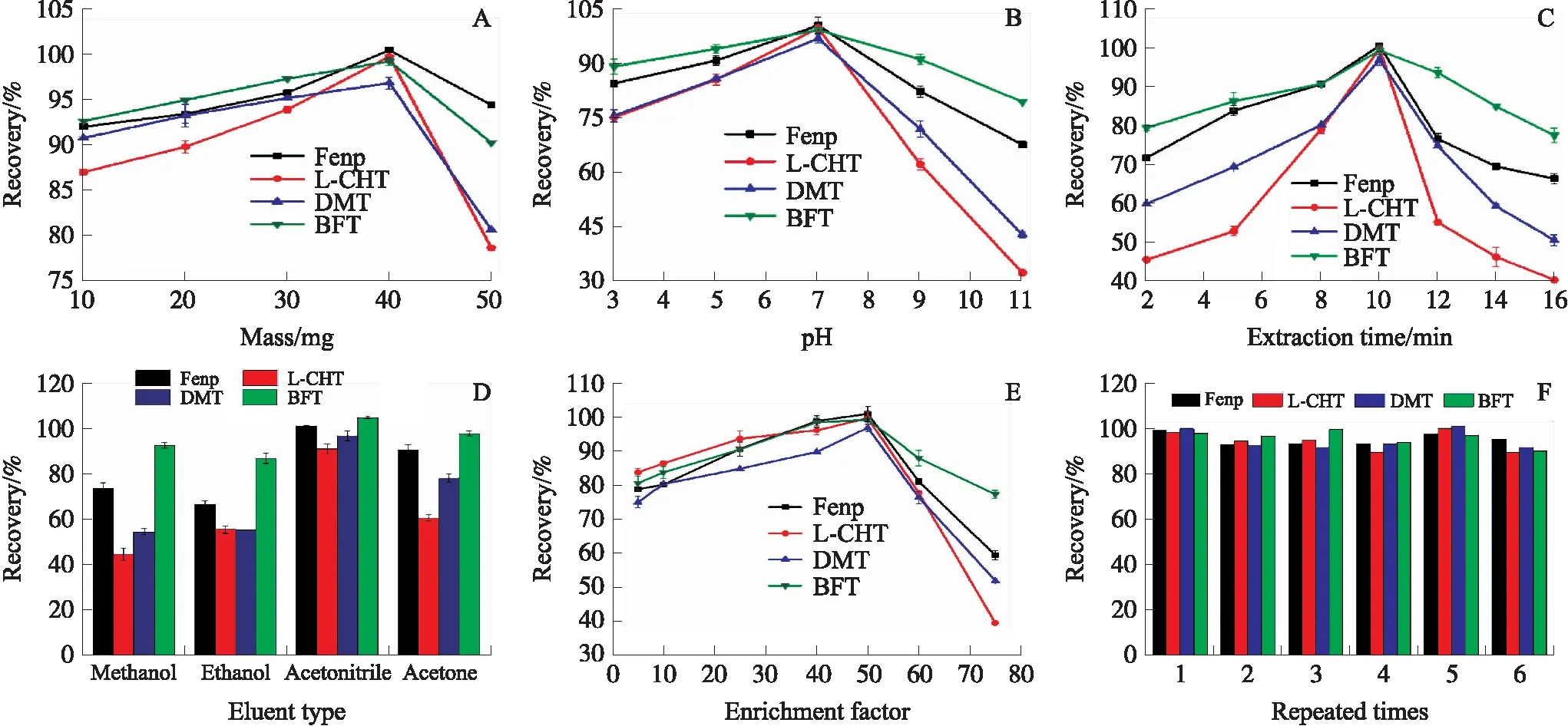
图5 投加量(A)、pH(B)、吸附时间(C)、洗脱剂种类(D)和富集因子(E)对4种拟除虫菊酯农药的影响以及可重复利用性(F)Fig.5 The effect of dosage(A),pH(B),adsorption time(C),eluent type(D),and enrichment factor(E) on four pyrethroid pesticides and their reusability(F)
2.8 环境水样检测
分别取长江水、玄武湖水和自来水,应用经方法验证和条件优化后的MSPE方法对实际水样进行检测,结果如表2所示.
表2数据显示,所采集的3种实际水样中均未检出目标污染物. 分别在实际样品中进行加标分析,加标浓度分别为2 μg/L、4 μg/L,此时Fenp、L-CHT、DMT和BFT的回收率在88.69~99.96%之间,相对标准偏差(RSD)为0.89%~3.64%,表明所建立的MSPE方法具有良好的准确性、稳定性和可靠性.
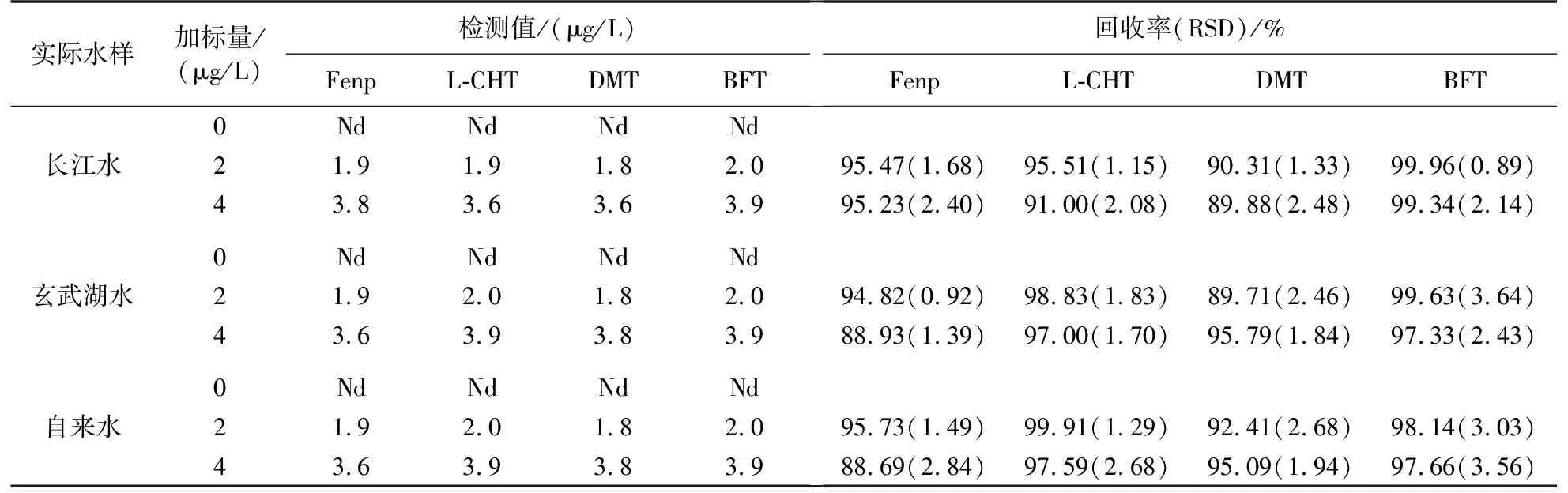
表2 环境水样中4种拟除虫菊酯类杀虫剂的检测结果Table 2 Analytical results of 4 insecticides in water samples
3 结论
本文通过热解法制备了CoFe2O4@CSC复合材料,并将其应用于水体中4种拟除虫菊酯类杀虫剂(Fenp、L-CHT、DMT、BFT)的磁固相萃取,系统研究了材料投加量、吸附时间、洗脱溶剂、体系pH及富集因子对萃取效果的影响,并将优化后的实验方法应用于环境水样的实际检测. 所得结论如下:
(1)所制备的CoFe2O4@CSC复合材料具有明显的介孔结构,其孔径约为30 nm. 当CoFe2O4与CSC的质量比为1∶1时,其萃取效果最佳;
(2)磁固相萃取的最佳条件为材料使用量40.0 mg、体系pH为7.00、平衡吸附时间10 min、选用乙腈为洗脱剂,此时目标分析物回收率可达到100.44%、99.74%、96.82%及99.22%;此外,CB1材料具有良好的稳定性,经6次循环使用,其磁固相萃取效果无明显下降;
(3)环境水样的实际检测结果表明所建立方法具有良好的准确度与可靠性.
