铜镍合金在海水冲刷条件下的腐蚀行为与机理研究进展
2022-07-05曹青敏石泽耀张赪栋蹇冬辉
曹青敏,刘 岩,刘 斌,石泽耀,张赪栋,蹇冬辉
(北京化工大学材料科学与工程学院 材料电化学过程与技术北京市重点实验室,北京 100029)
1 前 言
海洋的腐蚀环境是极其复杂的,金属及合金在海洋中的腐蚀同时受到多方面因素的影响,主要包括材料因素和环境因素2个方面。材料因素包括合金成分、微观组织、初始表面状态和腐蚀产物膜等,环境因素包括温度、pH、杂质离子、硫化物和流速等。另外,海洋中的微生物群落也可能牢固地附着在金属表面,形成一层生物膜,生物膜的腐蚀作用会损坏设备,导致生产损失和维护成本的增加[1, 2]。因此,金属在海洋环境中的腐蚀比在一般环境中更为严重,造成了大量的资源浪费。调查表明,每年由于海洋腐蚀造成的经济损失,全球共计高达6000~12 000亿元,占国民生产总值的2%~4%[3]。
铜镍(Cu-Ni)合金具有优异的耐海水腐蚀、防污、防海洋生物附着能力,被广泛应用于海洋工程领域,尤其是滨海电站的换热器及其他舰船用的冷凝管道,至今已有数十年的应用历程[4]。随着人们对海洋材料的性能、腐蚀年限要求越来越高,传统的Cu-Ni合金已经不能满足海洋工程对材料防腐蚀性能的需求。国内外的专家学者们不断对Cu-Ni合金进行着深入的研究,但由于涉及的因素多种多样,对于海水中Cu-Ni合金的腐蚀规律目前还没有系统的研究。因此,对已有的研究成果进行整理与分析,提炼存在的问题,对进一步的研究十分必要。
本文将综述国内外对Cu-Ni合金腐蚀行为的研究进展,从材料因素和环境因素2个方面,阐述Cu-Ni合金腐蚀行为的影响因素,分析Cu-Ni合金在海水冲刷条件下的腐蚀机理,并提出问题与建议。此外,还对国内Cu-Ni合金在海洋工程领域的研究及应用进行了展望。
2 材料因素对腐蚀行为的影响研究
2.1 合金成分
纯铜的耐海水腐蚀能力较差,添加Ni元素可以提高其腐蚀电位和钝化能力,从而增强合金的耐腐蚀性能。Ni和Cu元素可以无限固溶,在常温下形成Cu-Ni合金的α单相固溶体[5],其二元相图如图1所示[6]。随着Ni含量的增加,Cu-Ni合金耐腐蚀性能逐渐增强,Crousier等[7]用电化学方法研究了Ni含量对Cu-Ni合金耐蚀性的影响,发现随着Ni含量增加,合金的钝化电流密度减小,腐蚀速度降低。相关研究表明,Ni在一定程度上可以改善铜合金表面钝化膜的防腐蚀性能,其机理是Ni2+进入Cu+的空缺位置,增加了Cu2O膜的离子阻力,导致一个阳离子空位消失,从而增大了电子阻力。Ni2+能大量地存在于Cu2O的点阵结构中,并且不影响Cu2O结构,但是当Ni含量高于40%时(质量分数,下同),钝化膜的防腐蚀性能将降低[8]。

图1 铜镍合金二元相图[6]Fig.1 Copper-nickel alloy binary phase diagram[6]
在Cu-Ni合金中添加不同量的Fe对耐蚀性的影响效果不同,有许多学者做了相关研究。Efird等[9]通过静态和动态海水腐蚀试验研究了Fe含量对Cu-Ni合金耐蚀性的影响,结果发现,添加0.5%~2.0%的Fe可以显著提高Cu-Ni合金的耐冲刷腐蚀性能。Zubeir[10]报道了Fe含量对90Cu-10Ni合金腐蚀性能的影响,结果表明,Fe的含量大于2.0%时,将会导致富Ni-Fe相的连续沉淀析出,在海水中形成黑色、疏松、易脱落的薄膜,致使合金的耐腐蚀性能变差。姜雁斌等[11]的研究发现,随着合金中Fe含量的提高,合金腐蚀速率呈现先减小后增大的趋势,如图2所示。因此,目前在工程中应用的Cu-Ni合金,Fe的添加量通常在0.5%~2.0%之间。
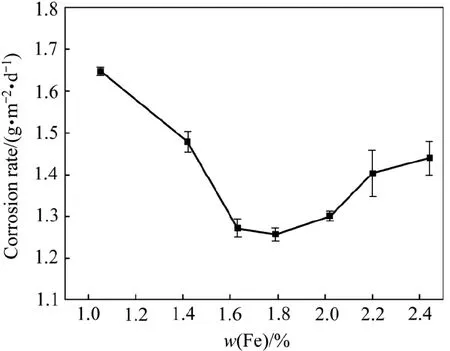
图2 B10铜镍合金腐蚀速率随Fe含量变化[11]Fig.2 The corrosion rate of B10 alloy varies with Fe content[11]
当合金中Fe的含量较低时,Mn可以在一定程度上替代Fe,同时还有消除多余碳的作用,提高了合金的耐蚀性[12]。目前应用最普遍的合金如BFe10-1-1和BFe30-1-1等,具有很强的抗冲刷腐蚀性能,其中的Mn和Fe的质量都是以1∶1的比例加入的。Mn还能与Ni共同作用,使合金的微观组织结构更加稳定。Saud等[13]利用拉伸实验和电化学实验研究了Mn含量对Cu-Al-Ni合金性能的影响,发现当合金中的Mn添加量为0.7%时,合金的力学性能和耐蚀性能都达到最优,而Mn含量的继续增加反而会使合金的耐蚀性降低。
美国海军在给Cu-Ni合金中添加Fe和Mn元素的基础上,还添加了0.5%的Cr元素,发明了一种新型合金并广泛应用。研究表明,此类合金的耐海水冲刷腐蚀性能明显优于B10和B30合金[14]。国内外学者研究了Cr元素的添加量对Cu-Ni合金各方面性能的影响。Anderson等[15]探究了不同Cr含量对Cu-Ni合金抗冲击腐蚀性能的影响,结果表明,当Cr元素的添加量大约为0.5%时可以提高合金的耐冲击腐蚀性能。Jeon等[16]研究了在pH=1.2的酸性氯化物溶液中Cu-6%Ni-4%Sn-x%Cr合金的腐蚀特性随Cr含量的变化,发现Cr的添加可以减少富Sn的沉淀,防止局部腐蚀的发生。李晓娜等[17]认为,Ni-Cr的同时加入可以明显抑制铜合金在800 ℃以下的中温氧化,但合金的抗高温氧化性能与Cr和Ni的质量比有密切联系,较高的比例才能提高铜合金的抗高温氧化能力。由此可见,添加的Cr元素会与其他合金成分共同作用,对合金的耐冲刷、耐冲击、抗高温氧化性能均有不同程度的提升,值得继续对该元素的作用进行深入研究。
Al元素对Cu-Ni合金具有强化作用,可以促进合金表面形成坚韧、致密的保护膜,降低表面活性,使合金的机械强度大幅提高,增强合金的抗冲蚀性能,从而提高合金的耐蚀性[18]。
稀土对铜及铜合金的作用主要有净化、微合金化、改善机械加工性能以及提高耐蚀性。因此许多研究者在Cu-Ni合金中加入少量的稀土元素对其进行改性,以提高Cu-Ni合金的耐蚀性[19, 20]。关于稀土改善铜及铜合金耐蚀性的机理,主要有以下5种解释:① 稀土元素能在合金表面形成极薄且致密的腐蚀产物膜,增大了腐蚀进行时的传质过程阻力[21];② 稀土在晶界上的分布会阻碍镍、铁、氧等元素的扩散,降低成分偏析的出现,使合金的成分和组织均匀化[22];③ 缩小了铜及铜合金的结晶温度范围,减轻了枝晶偏析[23];④ 稀土元素能提高铜及铜合金的腐蚀电位[24];⑤ 稀土净化基体后杂质减少,从而减少腐蚀微电池的数目和腐蚀电势梯度,提高了合金的耐蚀性[25]。
2.2 微观组织
Cu-Ni合金的组织均匀性会显著影响其耐蚀性,这是由于合金成分的相互作用会影响偏析程度,具体表现为合金中镍元素的偏析,从而降低其耐冲刷腐蚀性能[11]。甘春雷等[26]研究了连续柱状晶组织和普通铸造多晶组织的BFe10-1-1合金耐蚀性,测试结果表明,前者的微观偏析程度较小,成分更加均匀,能够有效避免局部腐蚀的发生,同时腐蚀产物膜阻抗较大,耐蚀性提高。孔小东等[27]的研究也证明了微观组织和夹杂物的差异对铜合金的耐腐蚀性能有重要影响。
关于晶粒尺寸对Cu-Ni合金耐蚀性的影响,目前学界的看法还存在一定分歧。曹中秋等[28]研究了不同晶粒尺寸的Cu-Ni合金在酸性含氯介质中的电化学性能,结果发现,晶粒细化后晶界所占的总面积相对增加,而晶粒内部的原子能量通常小于晶界处的原子能量,因而晶界处原子反应活性较强,参与腐蚀的活性原子增加,使得腐蚀加速,且优先在晶界处发生腐蚀。Tan等[29]通过对6种不同使用寿命的Cu-Ni合金的研究,认为提高Cu-Ni合金耐蚀性的有效方法是获得较大的晶粒和较宽的晶粒尺寸分布。
综合前人的研究,要增强合金的耐蚀性,其晶粒尺寸应该控制在一个合适的范围内,因此还需做进一步的研究以确定具体尺寸范围,同时,合适的晶粒尺寸还可以满足材料的力学性能和成形性能要求。
2.3 初始表面状态
由于Ni和Cu元素可以无限固溶,可在常温下形成单相固溶体且均匀性较好,但由于金属表面以及金属-海水界面处物理化学性质的微观不均匀性,导致金属与海水接触界面的电极电位不均匀,易在活性点形成微腐蚀电池,造成局部腐蚀[30]。因此,点蚀是Cu-Ni合金在海洋环境中较为常见的腐蚀类型,而点蚀的情况与材料的初始表面状态有关。原始表面膜指金属通过热处理工艺形成的膜层,腐蚀产物膜指金属在腐蚀环境中形成的膜层。Cu-Ni合金原始表面膜中的镍富集和镍的充分氧化可以增强合金的耐蚀性,而表面膜层中残留的游离态碳会使Cu-Ni合金腐蚀更加严重,原始膜层中非游离态的碳则对合金的耐蚀性影响不大[31];另外,材料的表面粗糙度越高,在表面越容易形成湍流,冲刷腐蚀也就越严重。
2.4 腐蚀产物膜
Cu-Ni合金在海水环境中具有优异的耐腐蚀性能,不仅由于自身电位较正,不易发生腐蚀反应,更由于其表面形成的致密的腐蚀产物膜阻隔了金属基体与腐蚀环境的接触,从而降低了腐蚀速率。
目前,学术界公认的Cu-Ni合金在海洋环境中的腐蚀产物膜,是一种双层结构模型[32]。模型的内层为致密的Cu2O膜,可以保护合金免于腐蚀,这是铜镍合金在海水中具有良好耐蚀性的主要原因;外层为二价铜的化合物(Cu(OH)2、CuO、Cu2(OH)3Cl、CuCl2或CuCO3·Cu(OH)2)产物膜,外层膜疏松多孔,对基体不具有保护性[33, 34]。Ma等[35]还发现产物膜中有金属镍的存在,随着膜层深度的增加,镍的氧化态(NiO和Ni(OH)2)逐渐减少,而镍金属单质增加。在膜的内层中检测到的NiO/Ni(OH)2对内层的较高电阻有很大贡献,Ma等认为腐蚀产物膜在海水中的形成过程可以分为5个阶段,如图3所示。

图3 90/10(B10)铜镍合金在海水浸泡环境下的腐蚀产物膜形成过程示意图[35]:(a) 浸泡初期,铜溶解形成CuCl2,Cu2O再沉淀;(b) 浸泡中期,Cu2O被氧化并形成非保护性的Cu2(OH)3Cl;(c) 浸泡中后期,阳离子空位及电子空穴的产生、扩散,Cu2O薄膜开始向内生长;(d) 浸泡中后期,向内生长的Cu2O膜增厚,纯铜晶粒再沉积;(e) 浸泡后期,向内生长的Cu2O薄膜变厚,薄膜内层形成NiOFig.3 Schematic diagram of corrosion product film formation process of 90/10 copper-nickel alloy in seawater immersion environment[35]: (a) at the early stage of the immersion, dissolution of copper to form CuCl2 and reprecipitation of Cu2O; (b) at the middle stage of the immersion, oxidation of Cu2O and formation of nonprotective Cu2(OH)3Cl; (c) at the mid-to-late stage of the immersion, generation and diffusion of cation vacancies and electron holes and start-up of inward growth of Cu2O film; (d) at the mid-to-late stage of the immersion, thickening of the inward-growing Cu2O film and redeposition of pure copper grains; (e) at the late stage of the immersion, thickening of the inward-growing Cu2O film and formation of NiO in the inner layer the film

2Cu+H2O↔Cu2O+2H++2e-
(1)
(2)
(3)
North等[37]用铜基合金上的Cu2O膜的不良半导体特性解释了Cu-Ni合金相较于纯铜的耐蚀性优势。他们猜想镍和铁掺入Cu2O膜中,占据了阳离子空位,降低了阳离子空位浓度,从而提高了耐蚀性,这一说法被许多人所接受。但是Burleigh等[38]认为,将氧化镍(NiO)和赤铁矿(Fe2O3)代替Ni2+和Fe2+/Fe3+添加到Cu2O中并不会消除阳离子空位,但会产生新的空位,如式(4)和式(5)所示:
(4)
(5)

根据在氧恒定压力下阳离子空位浓度与电子空穴浓度之间的关系式(6)和式(7),阳离子空位浓度的增加必然会导致电子空穴浓度的降低。因此,镍和铁改善钝化膜耐冲刷腐蚀性能的方式可能与电子空穴的减少有关,从而导致电子电阻率增加。
(6)
(7)

3 环境因素对腐蚀行为的影响研究
3.1 温度
温度对铜镍合金的影响机制在于:腐蚀反应的氧扩散速率、阴阳两极反应速率都会随着环境温度的变化有较大波动,从而使合金的腐蚀速率随之发生改变;另外,较高的温度还适宜海洋中微生物的繁殖,加速微生物腐蚀。但是海水温度升高又会使海水中的溶解氧含量降低,同时加速保护性钙质水垢在合金表面的生成,减慢阴极还原反应的进行,使得腐蚀速率降低。由此可见,温度对铜镍合金在海洋环境中腐蚀速率的影响是多方面综合作用的,实验条件的不同可能会导致研究结果各不相同。Melchers[39]对现有的90/10铜镍合金浸泡腐蚀数据的分析表明,样品最初浸泡时的温度会对其长期腐蚀行为产生较大影响,最初浸泡温度在18~28 ℃之间时,90/10铜镍合金表现出更好的耐蚀性。杜孟孟等[40]利用电化学测试手段研究了2种铜镍合金在20~80 ℃时的腐蚀性能,发现BFe10-1-1合金在40 ℃时腐蚀速率最小,这是传质速度和溶解氧含量综合作用的结果,且2种合金在较高温度下均会在表面迅速生成腐蚀产物膜,达到稳定状态。
3.2 pH值
海水的pH值一般为8.1~8.3,偏弱碱性。铜合金在海水中会发生钝化,在表面形成Cu2O钝化膜,对基体有保护作用,但钝化膜在酸性条件下会溶解。Efird[41]发现当海水介质的pH值≥9时,铜合金表面会形成CuO膜,当pH值>13时,CuO膜将会溶解,并推导出了电位-pH图(如图4)。罗宗强等[42]研究了pH值对Cu-17Ni-3Al-x铜合金腐蚀的影响,发现在3.5%的NaCl溶液中,环境pH值越高(pH=3~12),合金越易形成致密的腐蚀产物膜,腐蚀速率越低。
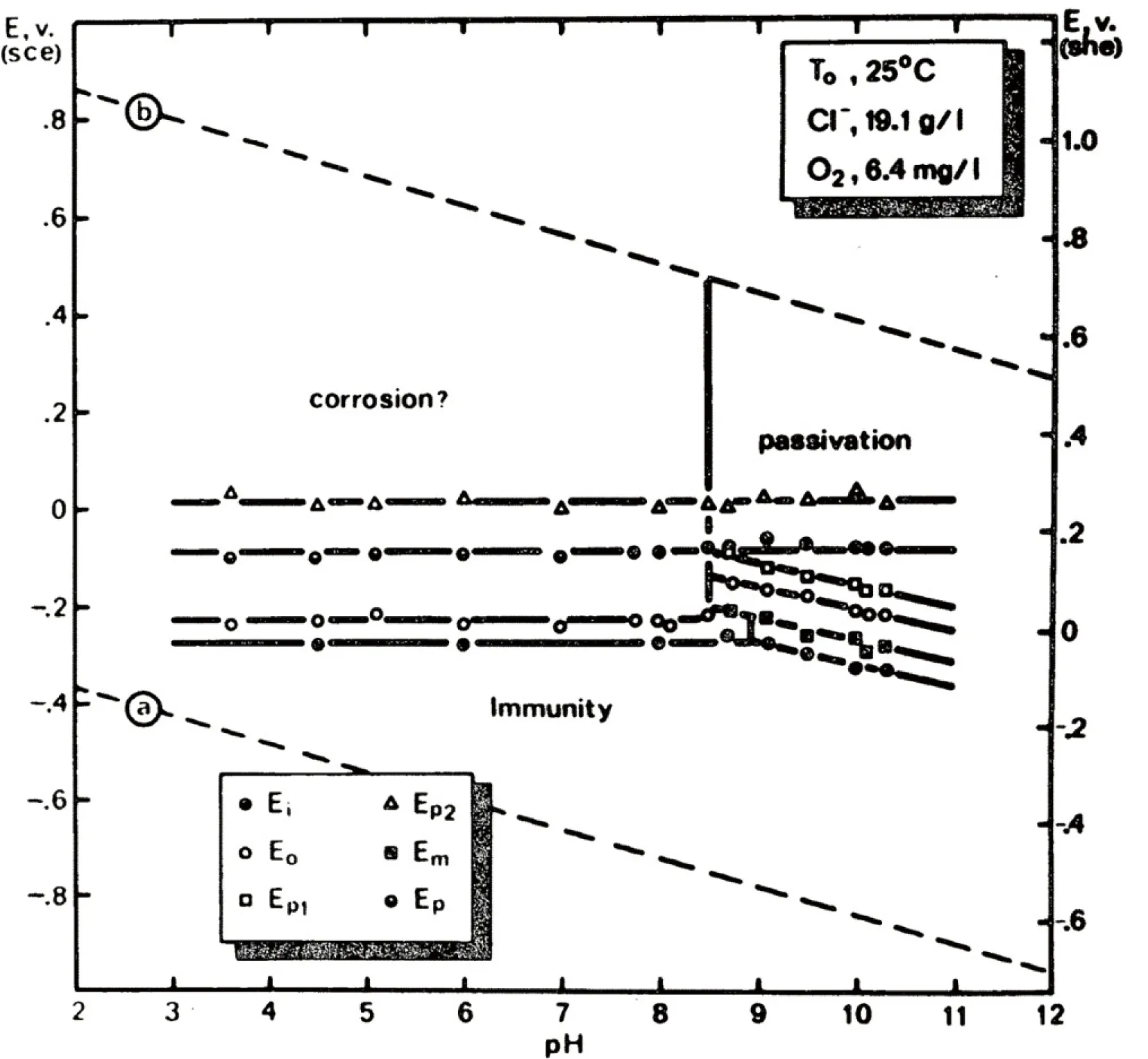
图4 90/10铜镍合金在25 ℃下的电位-pH图[41]Fig.4 Potential-pH diagram of 90/10 copper-nickel alloy at 25 ℃[41]
3.3 氯离子
海洋环境是高盐环境,因此氯离子(Cl-)对合金的腐蚀影响不可忽视。Cl-会对合金产生腐蚀的主要原因是其与铜合金表面的氧化亚铜膜发生反应,生成可溶或微溶的氯化物,从而引起合金发生点蚀[43]。研究表明,Cl-主要通过以下几个方面对合金材料造成腐蚀破坏[44]:① Cl-会渗透到腐蚀产物膜内,对膜的结构造成破坏;② Cl-的吸附容易抑制腐蚀产物膜的形成及修复;③ Cl-的吸附在腐蚀产物膜上形成强电场,加速基体的溶解。
对于Cl-对Cu-Ni合金腐蚀速率的影响,研究者们做了许多研究。常钦鹏等[45]发现在含Cl-的环境中B30 Cu-Ni合金表面氧化膜会发生点蚀,并且随着环境中Cl-浓度的增大,腐蚀速率逐渐增大。Badawy等[46]的研究结果表明,当Cl-浓度低于0.3 mol/L时,Cu-Ni合金的腐蚀速率会随着Cl-浓度的升高而升高;当Cl-浓度达到0.3 mol/L时,CuCl经过反应和水解生成致密的Cu2O层,保护基体免于腐蚀,腐蚀速率降低。Verma等[47]也表示,Cu-Ni合金在含氯介质中腐蚀形成的主要腐蚀产物为CuCl、CuCl2和Cu2O。Cl-浓度还会影响镍含量与腐蚀速率的关系,Milošev等[48]研究了Cu-xNi(x=10%~40%,质量分数)合金在碱性溶液(pH=9.2)中的腐蚀行为,该溶液含有不同浓度的NaCl(0.01~2.0 mol/L),发现存在一个临界Cl-浓度,低于该浓度时,镍含量越低,对局部腐蚀的抵抗力越大;高于该浓度时,镍含量越高,对局部腐蚀的抵抗力就越大。
3.4 硫化物
硫化物在海洋中的存在形式多种多样,如工业废水的排放、腐烂的海洋生物、硫酸盐还原菌等,这些因素都会导致海水介质中硫化物的产生,因此其对金属的腐蚀影响相对比较复杂。Cu-Ni合金对S2-特别敏感,S2-可以与腐蚀过程中产生的Cu+结合生成Cu2S,Cu2S是一种硬而脆的腐蚀产物,它可以附着在合金表面但粘附力较小,加上腐蚀产物膜的结构较为疏松,Cu2S在流动介质中极易产生脆性剥落,进而降低合金的耐蚀性[49]。
硫化物的存在会使Cu-Ni合金腐蚀电位向活化方向移动。在活化电位时,阴极反应主要依赖于氢离子的还原,在海水含氧量很低时腐蚀依然可以进行。Kong等[50]采用一系列电化学方法研究了硫化物浓度对含厌氧氯化物溶液中铜腐蚀的影响,认为在缺氧环境下,硫化物浓度对耐蚀性有显著影响,形成的钝化膜同时包含Cu2S和CuS。随着硫化物浓度增加,钝化膜厚度减小,并形成多孔的外层,其对基体没有保护作用,导致合金耐蚀性降低。
目前已发现有些物质可以减小硫化物对Cu-Ni合金腐蚀的危害。5-(3-氨基苯基)四唑(APT)可作为混合抑制剂,在没有APT的情况下,海水和硫化物污染的海水中都存在CuO、Cu2O、CuCl、CuS和Cu2S,然而,在APT膜存在的情况下,上述产物完全不存在[51]。苯并三唑(BTAH)可以抑制Cu10Ni合金在被硫化物离子污染的盐水中的腐蚀,研究表明,BTAH的存在会降低腐蚀速率和腐蚀产物膜的生成量,同时可以说明腐蚀产物膜越薄,合金的腐蚀速率越低,即对合金基体的保护性越高[52]。
3.5 流速
Cu-Ni合金耐海水冲刷腐蚀性能较好,但是存在一个临界流速,一旦海水超过该流速,则腐蚀速率急剧增大,如图5所示[53]。一般认为,海水流速对Cu-Ni合金腐蚀过程的影响机制为:流动的海水在合金表面产生剪切力,流速越大剪切力越大[54],当表面产生的剪切力超过表面钝化膜与合金基体的结合力时,钝化膜就会与基体分离,从而腐蚀速率变大,这个海水流动的临界速度就被称为材料在该介质中的临界流动速度。当海水流速增大时,传质系数随之增大,会促使电化学反应加速,加快腐蚀性物质到达材料表面,加速腐蚀;当海水流速过大时,还会在合金表面形成湍流产生气泡,造成空泡腐蚀。吴成红等[55]则得到了相反的结论,认为流速增大可以冲刷掉金属表面的腐蚀性物质,减少局部腐蚀的发生,同时可以促进钝化剂到达金属表面,增强钝化能力,从而保护金属。因此,海水流速对Cu-Ni合金腐蚀速率的影响,目前的研究尚没有达成一致,有待于进一步深入研究。
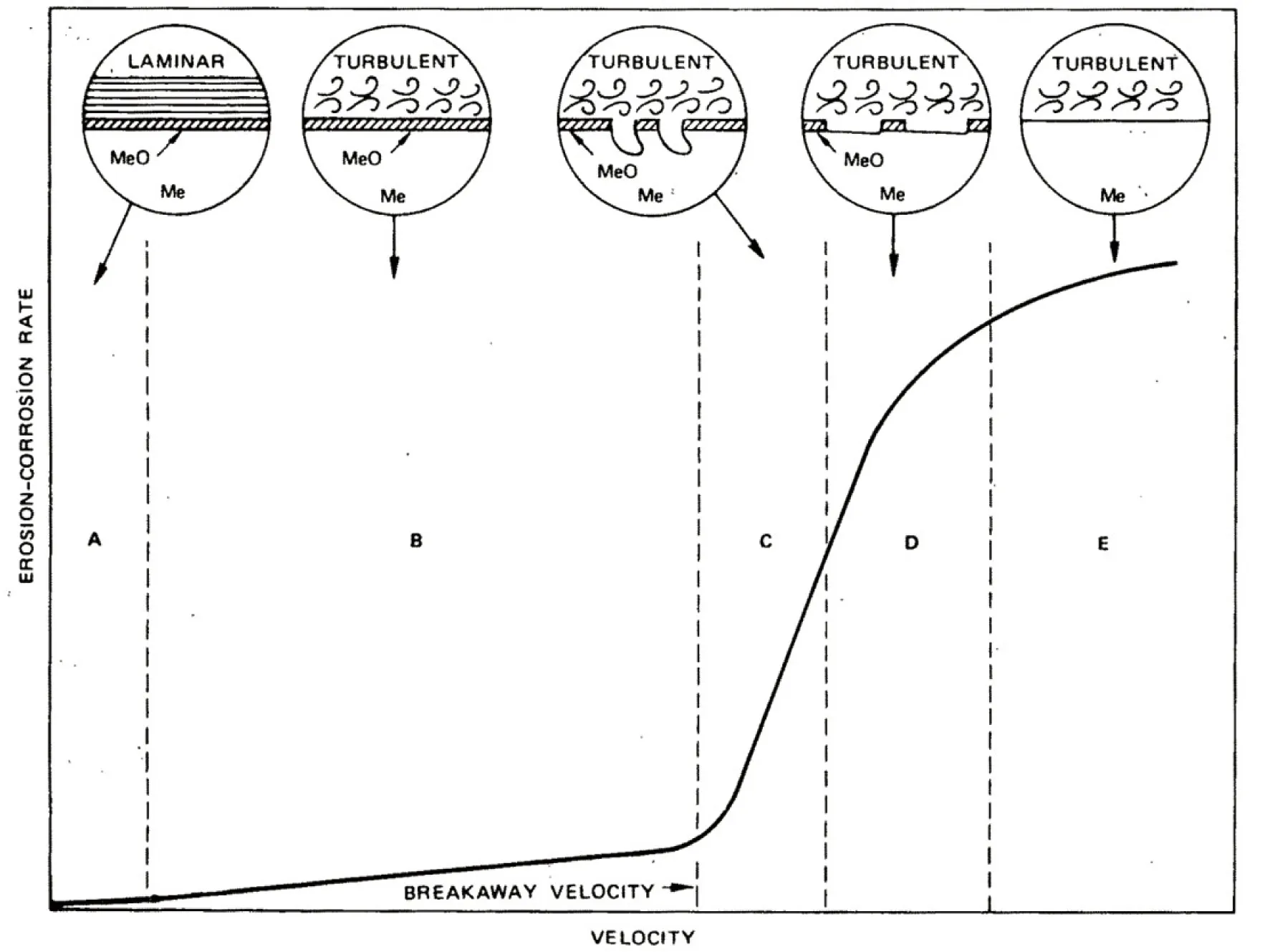
图5 冲刷腐蚀速率随流速变化示意图[53]Fig.5 Schematic of the changes in erosion-corrosion mechanism as velocity is increased[53]
4 Cu-Ni合金在海水冲刷条件下的腐蚀机理研究
研究表明,由于铜的电位较低,在海水中很难被直接氧化,而且在其表面会生成一层氧化产物膜,阻碍腐蚀过程的进行,因此Cu-Ni合金在海洋环境中表现出良好的耐蚀性[56, 57]。North等[37]是最早将Cu2O膜的半导体性质和Cu-Ni合金的耐蚀性联系起来的学者。他们认为Cu-Ni合金的耐蚀性能够优于纯铜,是因为Cu-Ni合金中的镍以掺杂离子的形式溶解在Cu2O膜中,与亚铜离子溶解后形成的阳离子空位相结合,降低了膜层中的阳离子空位浓度和电子电导率,增加了膜层电阻,从而改善了合金的耐蚀性[58]。以上过程可用式(8)表示:
(8)
一些研究者认为,Cu-Ni合金在海洋环境中浸泡后,在其表面形成了致密的Cu2O保护膜层,该膜层能与基体牢固地结合在一起,有效保护基体,阻止合金进一步被腐蚀[59-61]。然而单纯的Cu2O产物膜层实际上存在大量缺陷,研究者在Cu2O产物膜中发现了少量Ni和Fe的氧化物,证明了是Ni和Fe的氧化物填充了产物膜中的缺陷,增加了产物膜的致密性,才能提升合金的耐蚀性。
冲刷腐蚀是材料受到流体冲刷和环境腐蚀协同作用的结果,比单一地受到冲刷或腐蚀作用要严重[62]。冲刷腐蚀的交互作用机制主要可以概括为以下2个方面[63]。
一方面是冲刷对腐蚀的影响。首先,冲刷能促进传质过程,加速去极化剂(如O2、CO2等物质)到达合金表面,以及腐蚀产物从表面剥离。其次,冲刷会破坏合金表面的钝化膜,并促使新的钝化膜形成,若表面膜的自修复速率小于被冲刷破坏的速率,那么该材料的耐冲刷腐蚀性能较弱,会发生较为严重的冲刷腐蚀。因此,合金的耐冲刷腐蚀性能受到其能否形成稳定的表面膜,以及表面膜再修复能力的直接影响。所以,要提高合金的耐冲刷腐蚀性,可以从研究如何提高合金表面钝化膜的力学性能入手。再者,冲刷作用还会使材料发生变形,使位错发生滑移、塞积,局部的能量增大,形成应变电池。当腐蚀环境中存在固体时,冲刷过程还会在材料表面留下大小不一的冲蚀坑,增大合金比表面积,进一步加剧腐蚀过程。
另一方面是腐蚀对冲刷的影响。腐蚀会发生在材料表面,使表面凹凸不平,从而加剧冲刷的效果,尤其是在材料的缺陷处和相界面处,由冲刷造成的局部腐蚀更为严重。腐蚀在材料表面作用后还会破坏材料表面结构,溶解材料表面的加工硬化层,使其更加容易折断和脱落。材料因腐蚀在表面形成的氧化物膜层在强的冲刷作用下易被冲去,使腐蚀速率增大。
对于冲刷腐蚀的过程及机理,目前学界观点比较一致[64, 65],铜合金的冲刷腐蚀过程如图6所示。冲刷腐蚀的总失重T可以通过式(9)表示[66]:
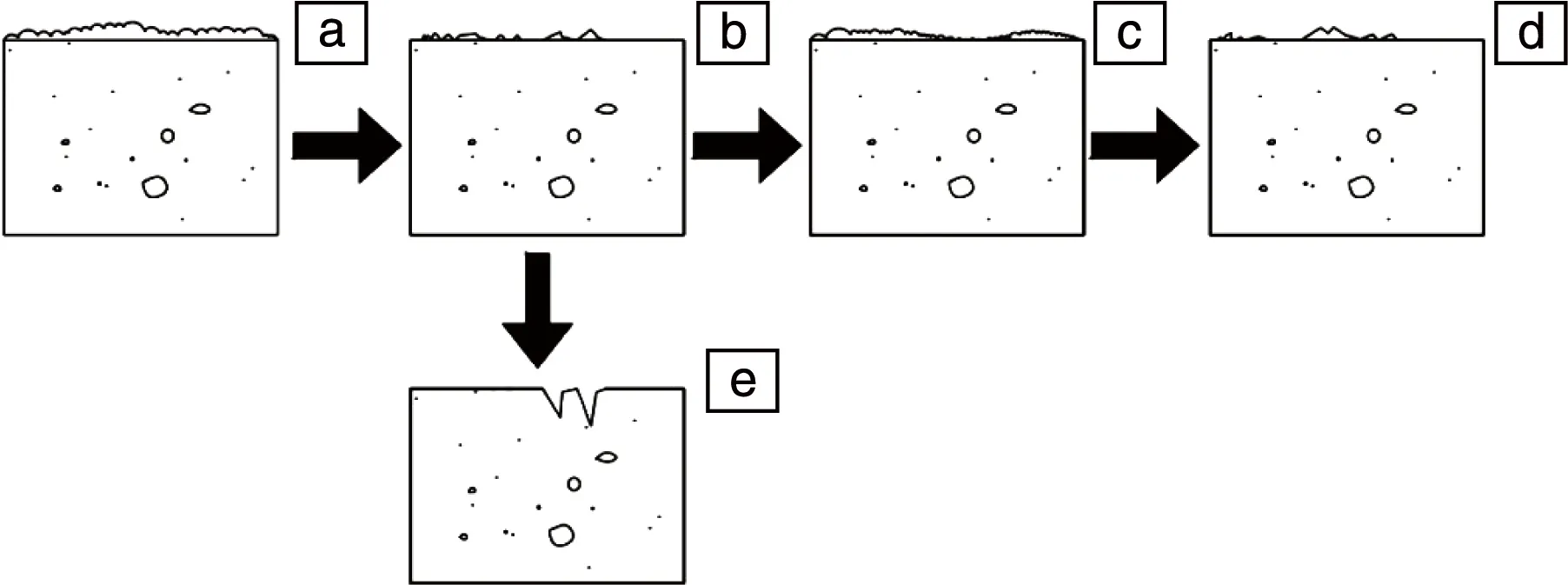
图6 铜合金冲刷腐蚀过程[65] :(a) 冲刷腐蚀初期,(b) 冲刷腐蚀破坏铜合金表面钝化膜,(c) 钝化膜再形成,(d) 钝化膜再被破坏,(e) 表面腐蚀层与内部缺陷联通Fig.6 Copper alloy erosion-corrosion process[65]:(a) in the early stage of erosion corrosion, (b) erosion corrosion damage the passivation film on the surface of copper alloy, (c) the passivation film is re-formed, (d) the passivation film is destroyed again, (e) the surface corrosion layer is connected to internal defects
T=C0+E0+Ce+Ec
(9)
其中,T是冲刷腐蚀的总失重;C0是纯腐蚀的失重;E0是纯冲刷的失重;Ce是冲刷对腐蚀的影响导致的失重;Ec是腐蚀对冲刷的影响导致的失重。
5 存在问题与解决途径
基于以上关于Cu-Ni合金在海水冲刷条件下的腐蚀行为与机理研究现状,对目前存在的主要问题和解决途径分析如下。
一是国内对于Cu-Ni合金的研究主要集中在B10、B30及部分多元合金,而针对更苛刻条件下对合金性能要求更高的材料设计研发工作相对较少。针对此方面的问题,可以通过对合金表面进行改性处理或添加合金元素(如稀土元素)的方式,增强其耐蚀性。另外,还可以调整Cu-Ni合金的晶粒尺寸,以满足材料耐蚀性、力学性能以及成形性能的要求,并深入研究各种合金元素对耐蚀性的影响机理,形成我国完整的海洋环境用Cu-Ni合金材料体系,为将来Cu-Ni合金在海洋与船舶工程领域的应用提供技术基础。
二是对于Cu-Ni合金腐蚀产物膜Cu2O的生成方式,以及其提高耐蚀性的机理方面,尚没有形成统一的认识和理论。另外,关于海水流速对Cu-Ni合金在海水中耐冲刷腐蚀性能的影响方面,也存在一定的分歧。针对此方面问题,可以综合运用新仪器新方法,如声发射技术、原位观测技术、腐蚀仿真计算,对以上问题进行更深入的研究,同时可采用理论计算与实验验证相结合的方法,探讨前人研究结果不同的原因,并得到更有力的证据和结论,进而不断完善对以上分歧和争议内容的认识和理解,逐渐达成一致。
三是针对Cu-Ni合金在海水冲刷条件下的腐蚀行为与机理研究手段方面,还有待于进一步拓展。目前,主要有原位电化学测试、腐蚀失重、表面形貌观察等研究方法,相较于海洋Cu-Ni合金的应用与发展需求而言,略显不足。近年来,随着计算机仿真技术的迅猛发展,研究者[67, 68]开始使用计算机软件平台开展冲刷腐蚀的仿真计算。通过腐蚀模型的建立,模拟冲刷腐蚀过程,并基于以往的相关腐蚀试验数据建立数据库并开展分析,能够更加全面地研究温度、流速等因素对合金腐蚀行为的综合影响,得到更为丰富的腐蚀过程信息,因而可以为Cu-Ni合金在海水冲刷条件下的腐蚀行为与机理研究提供一种更为直接、有力的技术手段。
四是在实际应用中,由于材料工件的形状复杂多样,其受到的腐蚀作用和形式也可能更为复杂,而在此方面尚缺乏针对Cu-Ni合金构件在实际工程应用环境中的腐蚀行为研究。因此,应加强对特殊结构形状的Cu-Ni合金冲刷腐蚀的试验研究,重点关注因构件结构形状带来的海水流态变化,及其对Cu-Ni合金冲刷腐蚀行为的影响,并开展特殊部位多重因素(冲刷速度、海水流态、冲击力、侵蚀性离子等)综合作用对腐蚀影响的分析研究,从而可以针对不同部位的腐蚀情况,有针对性地选择不同的材料或采取不同的防护措施。
6 展 望
近年来,我国已将发展海洋经济与科技提升到了前所未有的战略高度,作为海洋工程的主要材料之一,铜镍(Cu-Ni)合金因其优异的综合性能,在海洋工程领域的应用越来越广泛。在Cu-Ni合金海洋腐蚀行为研究方面,鉴于传统Cu-Ni合金的相关研究已基本趋于成熟,当前世界各国将研究重点更多地聚焦在海洋用新型Cu-Ni合金的研制开发,以及针对侵蚀性离子、流速、流态、温度等多因素耦合条件下Cu-Ni合金腐蚀行为与机理研究方面。相比较而言,国内在新型海洋用Cu-Ni合金材料的研究与应用方面与国外还有一定差距,尤其是尚未建立较为系统且全面的海洋环境用Cu-Ni合金材料体系,难以满足发展海洋战略强国的技术需要。因此,未来应着力加强新型耐超高流速、复杂流态海水冲刷Cu-Ni合金材料的研制开发,尽快缩小在海洋用Cu-Ni合金材料研究与应用方面与国外的差距,逐渐完善相关技术基础理论和材料技术体系,做好海洋用Cu-Ni合金材料应用的技术储备,从材料应用角度为我国海洋工程领域的发展提供有力支撑。
