聚酰胺6微塑料对土壤吸附磺胺甲恶唑的影响
2022-07-04江长松彭艳芳罗翠莲黄亮亮邹小明
江长松,彭艳芳,罗翠莲,周 琪,黄亮亮,邹小明
聚酰胺6微塑料对土壤吸附磺胺甲恶唑的影响
江长松1,彭艳芳2,罗翠莲2,周 琪2,黄亮亮1,*邹小明2
(1.桂林理工大学环境科学与工程学院,广西,桂林 541004;2.井冈山大学生命科学学院,江西,吉安 343009)
微塑料(MPs)和磺胺类抗生素(SAs)在农田土壤中普遍共存,且MPs和土壤均可吸附SAs,但不清楚MPs如何影响土壤对SAs的吸附。为此,本研究选择南方红壤区农田土壤探究了聚酰胺6微塑料(PA6)对土壤吸附磺胺甲恶唑(SMZ)特性的影响。结果表明,土壤和土壤+PA6对SMZ的吸附在24 h内达到平衡,动力学能用双常数方程较好地拟合(R≥ 0.968),Freundlich模型能很好地描述吸附等温线(R≥ 0.998);土壤吸附SMZ受土壤pH和腐植酸(HA)浓度的影响,碱性土壤和低HA浓度土壤有利于SMZ的迁移;PA6对土壤吸附SMZ有显著影响,表现为土壤中PA6含量占比越高其促进作用越大,且不受老化过程影响。本研究能为评估MPs和SAs的土壤生态风险提供科学依据。
微塑料;聚酰胺6;土壤;磺胺甲恶唑;吸附
磺胺类抗生素(SAs)是一类广谱类抗生素,由于其价格低廉、化学性质稳定和高效等特点而被广泛使用[1]。但被人体和畜禽消化吸收后,大约30% ~ 90% 以原型或代谢物的形式排放,然后通过粪肥施入、污泥堆肥和污水灌溉等方式进入土壤[2]。进入土壤中的SAs会对动植物产生毒性作用和诱导生成抗生素抗性基因,进而危害陆地生态系统[3]。同时,SAs在土壤中往往与其它污染物普遍共存,且土壤中的其它污染物会通过影响SAs的迁移,进而影响其危害作用[4]。例如,Jiang等[5]研究了土壤对二元系统中磺胺嘧啶(SD)和金霉素(CTC)的吸附,发现CTC会竞争土壤对SD的吸附位点,促进SD在土壤中迁移,进而提升SD在土壤中的环境风险。因此,研究其它污染物对SAs在土壤中吸附的影响具有重要意义。
微塑料(MPs)作为一类新型污染物,在土壤环境中无处不在,其含量是水体环境中的4到23倍[6]。MPs不仅能与陆地生态系统中的生物群落相互作用,引发生态危害;还能通过对其它污染物的吸附效应,进而影响其在土壤环境中迁移[7-8]。研究表明,MPs对不同污染物在土壤中的迁移可能存在着不同的影响。例如,聚苯乙烯和聚氯乙烯对土壤中噻虫啉迁移的几乎无任何影响[9];聚乙烯(PE)会促进金属离子在土壤中迁移[10-11]。但MPs对土壤吸附SAs的影响如何,尚不清楚。
聚酰胺塑料(PAs)作为一种广泛使用的工程塑料,在土壤环境中经常检测到其微米级残留[8]。研究表明,PAs相对于其它MPs对SAs具有更大的吸附能力[12]。因此,本研究选择了PA6和SMZ作为代表性MPs和SAs。探究了(1)PA6对土壤吸附SMZ过程、能力和机理的影响;(2)PA6在其他因素条件下(不同PA6占比、pH值、HA浓度和老化)对土壤吸附SMZ的影响。
1 材料与方法
1.1 实验材料
PA6(纯度≥99%)购自东莞兴旺塑胶原料有限公司,过100目筛后,根据Jiang等的老化方法[13],使用紫外辐射(UV)和紫外辐射+过氧化氢(UV + H2O2)老化PA6;SMZ(纯度>98%)和色谱级乙腈购自阿拉丁试剂(上海)有限公司;其他试剂均为分析纯,实验用水为三级水。
以江西红壤区(中科院地理科学与资源研究所千烟洲红壤丘陵综合开发试验站,江西吉安市泰和县)农田土壤为研究对象。采集0~20 cm的表层土壤,放置于实验室自然条件下风干,碾碎后过100目筛备用,基本理化信息如表1所示。
表1 土壤的基本理化性质
Tbale 1 Basic physical and chemical properties of soil

pH值有机质(g/kg)全氮(g/kg)全磷(g/kg)全钾(g/kg)阳离子交换总量 (cmol/kg)机械组成(%) 粘粒粉粒砂粒 5.8221.121.280.5111.126.6225.8743.9430.19
1.2 实验方法
参考Pan和Chu的研究[14],采用恒温水平振荡法,选择固液比为1:5,一式两份地进行吸附动力学、吸附等温线和其它因素影响的吸附实验。
1.2.1 吸附动力学
称取20 g样品(土壤、土壤+2% PA6)于250 mL锤形瓶中,以0.01 mol/L的CaCl2溶液作为电解质,加入100 mL质量浓度为6 mg/L的SMZ溶液。样品置于水平恒温震荡器(温度25℃,转速为180 rpm)中振荡,分别在0、0.1、0.25、0.5、1、2、4、8、12、16、24、36、48 h后取出样品过0.22 μm滤膜,得到SMZ滤液进行测定分析。
1.2.2 吸附等温线
称取2 g样品(土壤、土壤+2% PA6)于15 mL离心管中,以0.01 mol/L的CaCl2溶液作为电解质,分别加入10 mL质量浓度分别为0、1、2、4、6、8、10 mg/L的SMZ溶液,每个浓度设置不加样品的空白对照。样品置于水平恒温震荡器(温度25℃,转速为180 rpm)中振荡24 h,达到平衡后取出样品于4000 rpm下离心5 min,取上清液过0.22 μm滤膜,得到SMZ滤液进行测定分析。
1.2.3 其它因素的影响
称取2 g样品于15 mL离心管,以0.01 mol/L的CaCl2溶液作为电解质,加入10 mL质量浓度为6 mg/L的SMZ溶液,调变PA6占比(0%,0.5%,1%,2%,5%,10%)、溶液pH(3,5,7,9,11)、HA浓度(0 mg/L,5 mg/L,10 mg/L,20 mg/L,50 mg/L,100 mg/L)和不同老化MPs(原始PA6,UV老化PA6,UV+H2O2老化PA6)。将样品置于水平恒温震荡器(温度25℃,转速为180 rpm)中振荡24 h,达到平衡后取出样品于4000 rpm下离心5 min,取上清液过0.22 μm滤膜,得到SMZ滤液进行测定分析。
1.2.4 磺胺甲恶唑的测定
参考Wu等[15]的操作方法,SMZ滤液使用高效液相色谱(HPLC,日本岛津,LC-20AD)和C18反向色谱柱(250 mm × 4.6 mm,5 μm,日本岛津)于268 nm波长下检测。流动相为乙腈:0.1%甲酸=3:7(V/V),流速为1 mL/min,柱温28℃,进样体积20 μL。SMZ的标准曲线方程为y = 88367x + 2950.6,其回收率为98%。
1.3 分析方法
样品对SMZ的吸附量使用式1进行计算:
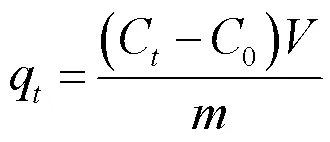
式中,q为样品在时刻对SMZ的吸附量,mg/kg;C和C分别为SMZ初始和时刻残留的质量浓度,mg/L;为SMZ溶液的体积,L;为样品的质量,kg。
土壤对有机污染物的吸附动力学研究通常使用Elovich方程、双常数方程和抛物线扩散方程拟合[16],其表达式分别如式2、式3和式4所示:
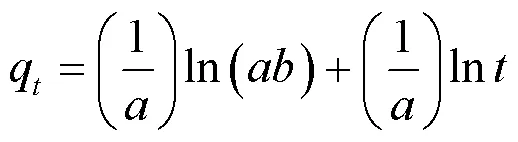
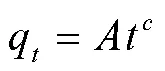
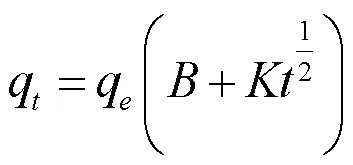
式中,q为24 h时样品对SMZ的平衡吸附量,mg/kg;为样品吸附SMZ的时间,h;a, b, c, A, B, K为常数。
linear模型和Freundlich模型被用于描述土壤和土壤+PA6对SMZ的吸附等温线,其表达式分别如式5、式6所示:
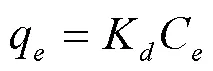
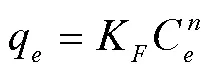
式中:K为SMZ在样品上的分配系数,L/kg;C为平衡时SMZ残留的浓度,mg/L;K为Freundlich吸附常数,L/kg;表示吸附强度。
2 结果与分析
2.1 吸附动力学
土壤和土壤+PA6对SMZ吸附量随时间变化的曲线如图1所示。从图1可知,吸附过程明显分为3个阶段,第一阶段(0- 4 h)土壤和土壤+PA6对SMZ的吸附量分别达到了平衡吸附量(24 h)的65.17%和65.57%,为快速吸附阶段;第二阶段(4 - 24 h)吸附速率相对于第一阶段明显减弱,为慢速吸附阶段;第三阶段(24 – 48 h)吸附量基本保持不变,为平衡吸附阶段。2种样品对SMZ的吸附均在24 h内达到平衡,土壤和土壤+PA6的平衡吸附量分别为8.13 mg/kg和12.17 mg/kg,表明PA6的添加促进了对SMZ的吸附。
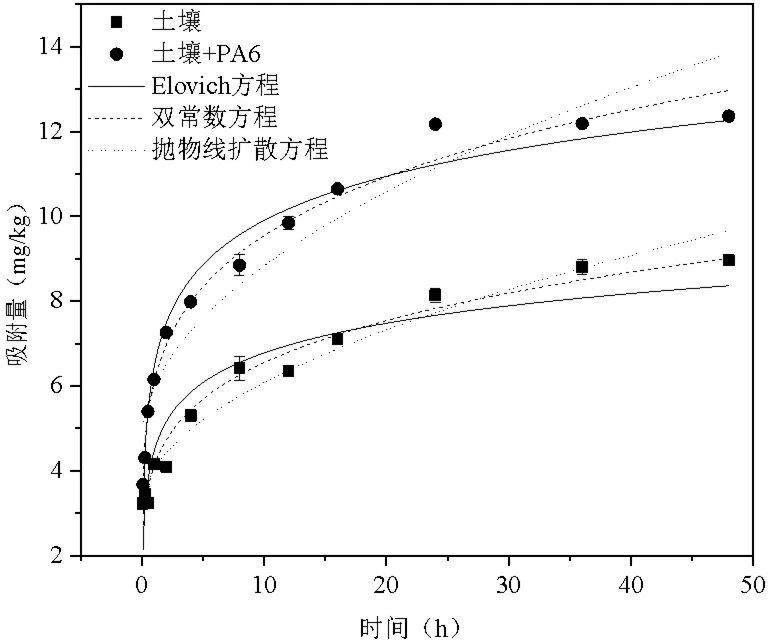
图1 土壤和土壤+PA6对SMZ的吸附动力学
为进一步明确土壤和土壤+PA6对SMZ的吸附过程,Elovich方程、双常数方程和抛物线扩散方程被使用去拟合吸附动力学数据,结果如表2所示。从表2可知,3种方程均能较好地拟合(R≥0.900),双常数方程的拟合度最高(R≥0.968)。双常数方程是修正的Freundlich方程,常被用来描述吸附剂表面能量分布的非均质性,其中A值越大,吸附能力越强[17]。因此,结果表明反应是一个复杂的动力学过程,反应速率呈幂函数指数级增长[18];土壤被PA6污染后,对SMZ的吸附能力增强。
表2 Elovich方程、双常数方程和抛物线扩散方程拟合参数
Table 2 Parameters for the fitted Elovich equation, double-constant equation and parabolic diffusion equation
样品Elovich方程 双常数方程 抛物线扩散方程 abR2 AcR2 BKR2 土壤0.99082.780.900 4.100.2030.968 0.3780.1170.965 土壤+PA60.665108.530.973 6.090.1960.985 0.3800.1090.912
2.2 吸附等温线
吸附等温线通常被用于描述平衡状态下吸附剂在吸附质和水溶液中的分配,同时揭示吸附质和吸附剂之间的相互作用[19]。一般认为,Freundlich模型能够比较好地拟合土壤对有机污染物的吸附数据,适用浓度范围较宽[17];linear模型求出的常数可以定量地描述吸附质在吸附剂和水溶液中的分配比。土壤和土壤+PA6对SMZ的吸附等温线如图2所示。从图2可知,随着SMZ浓度的增大,土壤和土壤+PA6吸附SMZ的量增多,且吸附能力均为土壤+PA6 >土壤。
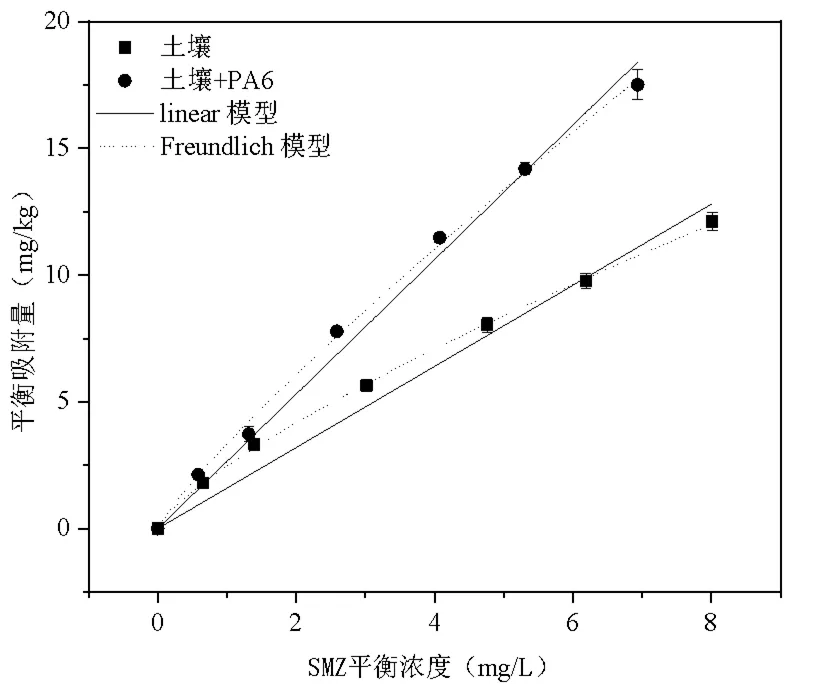
图2 土壤和土壤+PA6对SMZ的吸附等温线
为进一步明确其吸附机理,linear模型和Freundlich模型被使用去拟合吸附等温线数据,拟合结果如表3所示。从表3可知,linear模型和Freundlich模型均能很好地拟合土壤和土壤+PA6对SMZ的吸附等温线数据(R2>0.950),Freundlich模型(R≥0.998)相对于linear模型(R≥0.974)拟合度更高,土壤和土壤+PA6对SMZ吸附的K分别为1.60 L/kg和2.65 L/kg。上述结果表明土壤表面的吸附位点、活性基团分布不均匀,添加PA6后不改变土壤的吸附机理,但对SMZ的亲和力增强。
表3 linear模型和Freundlich模型拟合参数
Table 3 Parameters for the fitted linear model and the fitted Freundlich model
样品linear模型 Freundlich模型 Kd(L/kg)R2 KF(L/kg)nR2 土壤1.60 0.9742.46 0.7611.00 土壤+PA62.65 0.9903.34 0.8620.998
2.3 其他因素的影响
吸附剂对吸附质的吸附常常处于一个复杂多变的环境下,其吸附性能可能受环境因素(如pH值、HA浓度)和吸附剂特性的影响[13, 20]。因此,根据实验方法研究了在不同PA6占比、pH值、HA浓度和PA6老化等因素下PA6对土壤吸附SMZ的影响,结果显示在所有因素条件下土壤+PA6对SMZ的吸附能力均大于土壤(图3~图6)。从图3可知,随着PA6占比增加,土壤对SMZ的吸附能力增大。当PA6分别添加0.5%、1%、2%、5%和10%时,土壤的吸附能力分别增强18.27%、29.78%、55.23%、84.56%和130.80%。从图4可知,在实验pH(3~11)下,随着pH值的增加,土壤和土壤+PA6对SMZ的吸附能力均减弱,在碱性条件(pH>7)下吸附能力急剧下降。从图5和图6可知,HA浓度(5~100 mg/L)和PA6老化(UV老化和UV+H2O2老化)均不会促进或减弱PA6的影响,但随着HA浓度的增大,土壤对SMZ的吸附能力有一定程度地提高。
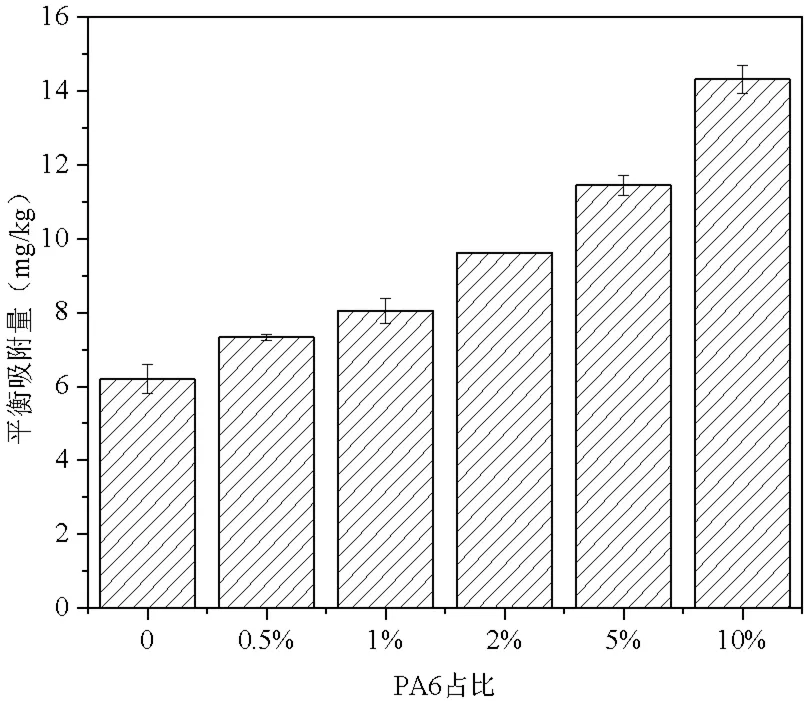
图3 PA6占比对土壤吸附SMZ的影响
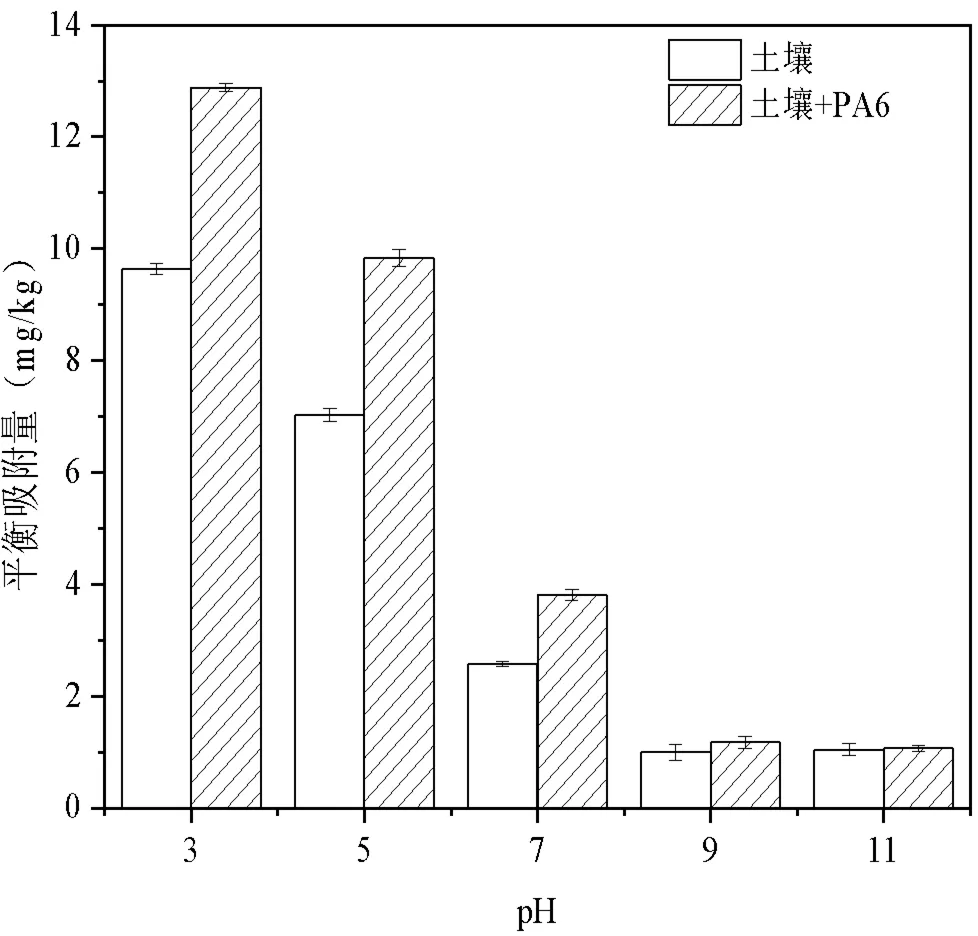
图4 pH对土壤和土壤+PA6吸附SMZ的影响

图5 HA对土壤和土壤+ PA6吸附SMZ的影响

图6 不同老化PA6+土壤吸附SMZ
3 讨论
土壤中包含有机质、矿物质和SiO2等多种组成,成分十分复杂,可以通过多种途径吸附有机污染物[20]。根据土壤和土壤+PA6对SMZ的吸附动力学和吸附等温线拟合结果(表2、表3)可知,吸附动力学数据使用双常数方程相对于Elovich方程和抛物线方程能更好地拟合,吸附等温线更符合Freundlich模型,表明其反应过程可能包括吸附、扩散、溶解和矿化等,并伴随着多种吸附机理。其它研究也发现不同质地土壤对丁草胺和五氯酚的吸附动力学数据也能用双常数方程很好地拟合,Freundlich模型能较好地描述五氯酚在土壤表面的吸附[16-17]。进一步地,Kahle和Stamm的研究表明阳离子态和分子态磺胺噻唑能够通过离子交换、氢键和范德华力与土壤中有机质相互作用[21]。
研究表明SMZ属于两性化合物,在环境中可能以阳离子态(pH < pKa1)、分子态(pKa1
HA对土壤和土壤+MPs吸附SMZ影响实验结果和Jiang等的研究结果表明(图5),HA会促进土壤吸附SMZ、抑制PA6吸附SAs和对土壤+PA6吸附SMZ无显著影响[13]。可能是由于HA在土壤吸附SMZ过程中起着架桥作用,促进土壤对SMZ的吸附;但HA会占据PA6对SMZ的吸附位点而抑制PA6对SMZ的吸附。郭欣妍等[27]也证实了土壤中有机质含量越高,对SAs的吸附能力越强。
从我们实验结果可知,土壤添加PA6后,不同环境条件下对SMZ的吸附能力均增强(图4、图5),可能是由于PA6吸附了溶液中的SMZ[12-13]。Hu等也发现MPs会提高土壤对17β-雌二醇(E2)的吸附[28],但也有其他相似研究观察到MPs对土壤的吸附抑制或无影响。如Li等[10]调查了PE对土壤吸附Zn2+和Pb2+的影响,发现PE会降低土壤对Zn2+和Pb2+的吸附能力;MPs会促进土壤中Cd2+的迁移[11],对土壤中噻虫啉的迁移无任何影响[9]。此结果的不一致可能归于土壤和MPs之间的相互作用。一方面,随着PA6占比的增大,对土壤吸附SMZ的整体影响效应(PA6导致的吸附增加量)增大,但单位影响效应(单位PA6导致的吸附增加量)减小(图3),可能是由于PA6对SMZ吸附的单位有效初始浓度随PA6的增多而减小,土壤和PA6之间的相互作用增强。另一方面,老化过程不会促进或减缓PA6对土壤吸附SMZ的影响(图6),表明PA6老化不会影响与土壤的相互作用。其他研究已证实MPs的老化能增强对土壤吸附E2的影响[28]。综上,PA6能减缓SMZ在土壤环境中的向下迁移,进而减弱对地下水的污染。
4 小结
(1)双常数方程和Freundlich模型能分别更好地拟合土壤和土壤+PA6吸附SMZ的吸附动力学和吸附等温线数据,土壤对SMZ的吸附包含多种反应过程和多种吸附机理,且PA6不改变土壤的吸附机理。
(2)随着pH的增大,土壤和土壤+PA6对SMZ的吸附能力减弱,氢键和静电作用可能是主要的吸附机理;SMZ在碱性土壤中迁移性更强,具有更大的环境风险。
(3)随着HA浓度的增大,土壤对SMZ的吸附能力增强,土壤+PA6对SMZ的吸附能力无显著变化,HA不改变PA6对土壤吸附SMZ的影响。
(4)土壤被PA6污染后对SMZ的吸附能力增强,降低SMZ在土壤环境中向下迁移的风险。
[1] Zhao L, Dong Y H, Wang H. Residues of veterinary antibiotics in manures from feedlot livestock in eight provinces of China[J]. Science of the Total Environment, 2010, 408(5): 1069-1075.
[2] Tzeng T W, Liu Y T, Deng Y, et al. Removal of sulfamethazine antibiotics using cow manure-based carbon adsorbents[J]. International journal of environmental science and technology, 2016, 13(3): 973-984.
[3] 周启星,罗义,王美娥.抗生素的环境残留, 生态毒性及抗性基因污染[J]. 生态毒理学报, 2007, 2(3): 243-251.
[4] Grenni P, Ancona V, Caracciolo A B. Ecological effects of antibiotics on natural ecosystems: A review[J]. Microchemical Journal, 2018, 136: 25-39.
[5] Jiang Y, Zhang Q, Deng X, et al. Single and competitive sorption of sulfadiazine and chlortetracycline on loess soil from Northwest China☆[J]. Environmental Pollution, 2020, 263: 114650.
[6] Wang J, Liu X, Li Y, et al. Microplastics as contaminants in the soil environment: A mini-review[J]. Science of the total environment, 2019, 691: 848-857.
[7] de Souza Machado A A, Kloas W, Zarfl C, et al. Microplastics as an emerging threat to terrestrial ecosystems[J]. Global change biology, 2018, 24(4): 1405-1416.
[8] Xu B, Liu F, Cryder Z, et al. Microplastics in the soil environment: occurrence, risks, interactions and fate–a review[J]. Critical Reviews in Environmental Science and Technology, 2020, 50(21): 2175-2222.
[9] Xu Z, Qian X, Wang C, et al. Environmentally relevant concentrations of microplastic exhibits negligible impacts on thiacloprid dissipation and enzyme activity in soil[J]. Environmental Research, 2020, 189: 109892.
[10] Li M,Wu D,Wu D,et al. Influence of polyethylene-microplastic on environmental behaviors of metals in soil[J]. Environmental Science and Pollution Research, 2021, 28(22): 28329-28336.
[11] Zhang S, Han B, Sun Y, et al. Microplastics influence the adsorption and desorption characteristics of Cd in an agricultural soil[J]. Journal of hazardous materials, 2020, 388: 121775.
[12] Guo X, Chen C, Wang J. Sorption of sulfamethoxazole onto six types of microplastics[J]. Chemosphere, 2019, 228: 300-308.
[13] Jiang Z, Huang L, Fan Y, et al. Contrasting effects of microplastic aging upon the adsorption of sulfonamides and its mechanism[J]. Chemical Engineering Journal, 2021: 132939.
[14] Pan M, Chu L M. Adsorption and degradation of five selected antibiotics in agricultural soil[J]. Science of the Total Environment, 2016, 545: 48-56.
[15] Wu L, Xiao X, Chen F, et al. New parameters for the quantitative assessment of the proliferation of antibiotic resistance genes dynamic in the environment and its application: A case of sulfonamides and sulfonamide resistance genes[J]. Science of The Total Environment, 2020, 726: 138516.
[16] 刘忠珍,何艳,吴愉萍,等.土壤中丁草胺的吸附动力学[J].中国环境科学,2007,27(4): 493~497.
[17] 卞永荣,蒋新,王代长,等. 五氯酚在酸性土壤表面的吸附-解吸特征研究[J].土壤 (Soils), 2004, 36(2): 181-186.
[18] 胡田田,仓龙,王玉军,等. 铅和铜离子在纳米羟基磷灰石上的竞争吸附动力学研究[J].环境科学,2012, 33(8):2875-2881.
[19] Wang J, Guo X. Adsorption isotherm models: Classification, physical meaning, application and solving method[J]. Chemosphere, 2020,258: 127279.
[20] 王磊,孙成,郭会琴. 土壤有机质对疏水性有机污染物的非线性吸附及其影响因素[J].土壤(Soils), 2012, 44(3): 366-373.
[21] Kahle M, Stamm C. Sorption of the veterinary antimicrobial sulfathiazole to organic materials of different origin[J]. Environmental Science & Technology, 2007, 41(1): 132-138.
[22] Yang S F, Lin C F, Lin A Y C, et al. Sorption and biodegradation of sulfonamide antibiotics by activated sludge: experimental assessment using batch data obtained under aerobic conditions[J]. Water research, 2011, 45(11): 3389-3397.
[23] Lin C E, Chang C C, Lin W C. Migration behavior and separation of sulfonamides in capillary zone electrophoresis III. Citrate buffer as a background electrolyte[J]. Journal of Chromatography A, 1997, 768(1): 105-112.
[24] 邹献中,徐建民,赵安珍,等.离子强度和 pH 对可变电荷土壤与铜离子相互作用的影响[J]. 土壤学报, 2003, 40(6): 845-851.
[25] Tušek L,Nitschke M,Werner C,et al. Surface characterisation of NH3plasma treated polyamide 6 foils[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2001, 195(1-3): 81-95.
[26] Gao J,Pedersen J A. Adsorption of sulfonamide antimicrobial agents to clay minerals[J]. Environmental science & technology, 2005, 39(24): 9509-9516.
[27] 郭欣妍,王娜,许静,等.5种磺胺类抗生素在土壤中的吸附和淋溶特性[J].环境科学学报,2013,33(11):3083-3091.
[28] Hu B,Li Y,Jiang L,et al. Influence of microplastics occurrence on the adsorption of 17β-estradiol in soil[J]. Journal of Hazardous Materials,2020,400:123325.
EFFECT OF POLYAMIDE 6 ON THE ADSORPTION OF SULFAMETHOXAZOLE IN SOIL
JIANG Zhang-song1, PENG Yan-fang2, LUO Cui-lian2, ZHOU Qi2, HUANG Liang-liang1,*ZOU Xiao-ming2
(1. College of Environmental Science and Engineering, Guilin University of Technology, Guilin, Guangxi 541004, China; 2. School of Life Sciences, Jinggangshan University, Ji’an, Jiangxi 343009, China)
Microplastics (MPs) and sulfonamide antibiotics (SAs) generally coexist in farmland soil, and they can adsorb SAs. However, the influence of MPs upon the adsorption of SAs by soil is still unclear. Therefore, in this study, farmland soil in southern red soil area was chosen to investigate the influence of polyamide 6 (PA6) upon the adsorption characteristics of sulfamethoxazole (SMZ) in soil. The results showed that the adsorption of SMZ by soil and soil+PA6 reached equilibrium within 24 h. The kinetics can be well fitted by the double constant equation (R2≥ 0.968), and the Freundlich model can describe the adsorption isotherm very well (R2≥ 0.998). Moreover, the adsorption behavior of soil for SMZ was affected by the pH values and the Humic acid (HA) concentrations in soil, and alkaline soil and low HA soil are conducive to the migration of SMZ. Furthermore, PA6 has a significant effect on the adsorption of SMZ by soil, which is manifested as the higher the proportion of PA6 in the soil, the greater its promotion effect, and it is not affected by the aging process. This study can providea scientific basis for evaluating the environmental risk of MPs and SAs in soil.
microplastics; polyamide 6; soil; sulfamethoxazole; adsorption
1674-8085(2022)04-0037-07
X53
A
10.3969/j.issn.1674-8085.2022.04.006
2021-10-25;
2022-01-12
国家自然科学基金项目(32160303, 31760165);江西省杰出青年人才资助计划项目(20192BCBL23014);江西省红壤丘陵区农业环境污染防控重点实验室开放基金项目(JXKL2021001);长江水环境教育部重点实验室开放基金项目 (YRWEF201907)
江长松(1994-),男,江西九江人,硕士生,主要从事环境污染化学研究(E-mail:jiangzhangsong1110@126.com);
*邹小明(1980-),男,江西赣州人,教授,博士,硕士生导师,主要从事环境毒理及污染控制研究(E-mail:zouxming_80@hotmail.com).
