氧化石墨烯修饰玻碳电极循环伏安法检测污水中Hg2+
2022-07-04潘雨欣雷龙文董彦杰
潘雨欣,雷龙文,董彦杰
氧化石墨烯修饰玻碳电极循环伏安法检测污水中Hg2+
潘雨欣,雷龙文,*董彦杰
(安庆师范大学化学化工学院,安徽,安庆 246013)
将氧化石墨烯修饰到玻碳电极上,并用扫描电镜对其在电极表面的结构形貌进行了表征。考察了该修饰电极对12种金属离子的选择性,对Hg2+的选择性最好,通过循环伏安法对该修饰电极与裸电极进行比较,修饰电极具有明显的化学响应。研究结果表明,对Hg2+测定的最佳实验条件为:0.10 mol/L 醋酸钠-醋酸缓冲液(pH 3.64) 2.5 mL,1.0 mol/L KNO36.5 mL。在1.0~10.0 µmol/L范围内,测定Hg2+的线性回归方程为:ΔI=2.7241CHg+9.0936(CHg的单位µmol/L),线性相关系数为0.9977,检测限(DL)为0.90 µmol/L。11次的相对标准偏差(RSD)为2.8%。回收率在99.4%~101.6%之间。我们用电感耦合等离子发射光谱仪(ICP)同时对样品进行了测定,两种方法测定结果相比较吻合性很高。
氧化石墨烯;修饰电极;循环伏安法;Hg2+
随着人类社会科技的发展和进步,工业化进程已经越发加快了脚步,人类生存的环境问题愈发显著,例如:水资源污染、土壤污染和大气污染等等。水是人们赖以生存的源泉,但由于大量工业废水的存在,给水资源造成污染,且有愈演愈烈的趋势。水污染中重金属离子的存在是造成污染的主要因素之一,重金属元素的存在非常广泛,无论是泥土、空气还是食物、水源中都存在微量的重金属元素,它们通过食物链进入人体,经长期聚集后会造成机体的慢性中毒甚至死亡,而且它们很难被生物降解。常见的重金属元素例如汞元素,对人的危害主要是影响人的中枢神经系统,从而导致对人脑的部分损伤,汞中毒会引起四肢麻木、恶心、呕吐、腹泻等[1],Hg2+在微生物存在时会甲基化,变为毒性更大的甲基汞,对人体造成的损伤更为严重[2]。
随着科技和精密仪器的进步,检测重金属元素的方法也有了巨大的进步。选择不同的仪器对于重金属元素的检测侧重点也不同,目前市面上的一些仪器除了能定性测定重金属元素外,还能对重金属元素进行定量测量。目前,痕量汞的测定方法主要有:原子吸收光谱法、分光光度法、荧光光谱分析法、电化学传感器、离子选择性电极、溶出伏安法和修饰电极法等。虽然检测重金属的方法非常多,但是由于传统方法中样品需要预处理,大型设备的缺失和检测成本过高等一系列问题造成了检测的不便。因此选用分析设备简单,样品需要量体积小、检测过程快和灵敏度高的电化学检测方法可以有效解决这些问题,并且电化学检测方法能够实现现场、持续性的检测,更有利于我们监控和处理重金属污染问题。在实际使用中,电化学分析法最低检出限可达10-12mol/L,且使用的仪器设备操作简单,检测的成本也很低。
化学修饰电极也是当下研究的热点问题之一,其原理是将具有优良的电化学性能材料修饰到原有电极上从而改变基础电极的性能,运用这种方法制备出的新电极即为化学修饰电极[3-5]。化学修饰电极的种类很多,主要有单分子层、多分子层、组合型和其他电极。单分子层电极主要利用共价键合法或者吸附法制备,多分子层电极则分为聚合物薄膜法和气相沉积法。化学修饰电极由于电极表面特殊功能基团的存在,在分离富集、测定方面取得了长足的进步[6-8]。在2011年,Qi Jaing等人通过催化化学气相沉积法将碳纳米管原位生长在预处理过的石墨电极上[9],制备出GSCNT-CME(碳纳米管化学修饰电极)。在2020年,Lydiane G. Djemmoe等人用Na2CO3(HVW-Na2CO3)化学活化的大麦粉(HVW)修饰到碳糊电极上[10],制出了溶出伏安法测定痕量Cd2+、Pb2+和Hg2+的传感器,并优化了关键实验的变量后,将传感器成功应用于实际样品中痕量金属的检测。2016年,徐旸等人分别利用羟基磷灰石、铋膜和碳酸氧铋作为修饰电极材料[11],利用循环伏安法检测了水中的铅和镉离子。该法可以精准快速的检测不同浓度的铅和镉离子,并且具有检测成本低廉的优点。所以本实验也采用了循环伏安法来检测水溶液中的金属离子。目前修饰电极用循环伏安法检测金属离子是实验时较为常用的方法之一[12-15]。
氧化石墨烯由于表面具有丰富的含氧官能团让其在水溶液以及一些极性溶液中可以稳定存在,它所具备的独特的电化学性能和较大的比表面积让其在光电领域和生物传感器等领域都有很广泛的应用。氧化石墨烯的优异电化学性能和较大比表面积[16],使它制备的修饰电极能极大地提高电极对电化学活性物质的电氧化还原信号。目前氧化石墨烯修饰电极常用制备方法主要有滴涂法[17]、真空蒸镀法和电泳沉积法[18-21]等方法。近些年,Ranjita T等人采用电还原氧化石墨烯-铋纳米粒子复合物(ErGOBi)作为电化学传感器检测抗癌药物盐酸吉西他滨(GMB),该电极在苏丹红Ⅰ上表现出良好的电化学响应[22]。Wei X B等研制了一种基于分子印迹聚合物和氧化石墨烯修饰玻碳电极的新型灵敏电化学传感器,该传感器对磺胺具有良好的亲和力和电化学响应,可以用于牛奶中磺胺的定量分析。Park D J等人通过用还原氧化石墨烯片(rGS)-金纳米颗粒(GNP)复合物修饰电极来制备电化学传感器,以测定0.1-100 μm范围内的混合物中的DA和抗坏血酸(AA)。尚未见到将氧化石墨烯用于修饰电极测定金属离子的报道。
1 材料与方法
1.1 仪器与试剂
CHI 660E型电化学工作站来自上海辰华仪器公司,并配有三电极系统,工作电极为:氧化石墨烯修饰玻碳电极;参比电极为:饱和甘汞电极;对电极为:铂丝电极[8]。实验室所用PB-10酸度计来自Sartorius(德国)。电感耦合等离子发射光谱仪(ICP)来自Perkin Elmer股份有限公司(USA)。
氧化石墨烯(GO)购自Shanghai Aladdin Biochemical Technology Co.,Ltd.(>99%)。
汞离子标准储备溶液:1.0×10-3mol/L,测定时,逐级稀释至所需浓度。
缓冲溶液:邻苯二甲酸氢钾-硝酸缓冲液(pH 2.2 ~ 3.8);磷酸氢二钠-柠檬酸缓冲液(pH 3.0 ~ 8.0);浓度为0.10 mol/L醋酸钠-醋酸缓冲液(pH 2.6 ~ 6.0)。
其他试剂:均为分析纯,实验用水为超纯水,上海默克密理博明澈D24UV超纯水机生产(18.2 MΩ)。
1.2 氧化石墨烯电极的制备
分别用0.3 μm和0.05 μm抛光粉抛光玻碳电极(GCE),然后用超纯水冲洗,抛光后的GCE放入体积比为1:1的硝酸水溶液中超声清洗1 min,取出用超纯水冲洗,再将GCE放入体积比为1:1乙醇溶液中超声清洗1 min,取出后用乙醇冲洗,静置晾干备用[8]。将氧化石墨烯粉末(GO)冷却到0℃,称量出2 mg氧化石墨烯(GO)后加入适量无水乙醇配制成2 mg/mL的醇溶液,将氧化石墨烯醇溶液超声分散均匀,然后取10 μL GO醇溶液,滴加到打磨好的GCE表面,暗处晾干后制成GO修饰玻碳电极(GO/GCE)。通过氧化石墨烯扫描电镜图谱可以清晰地看到GO在GCE上结构形貌,结果见图1。

图1 氧化石墨烯扫描电镜图谱
1.3 实验方法
用移液管向体积为10 mL的样品池中加入一定量1.0 mol/L KNO3溶液和0.10 mol/L缓冲溶液,再加入一定量1.0×10-3mol/L单一金属离子溶液,混合溶液用磁子搅拌均匀后静置备用。按照上述方法每种金属离子配制相同浓度的两份混合溶液。采用三电极工作系统,先将未修饰的裸电极(BE)插入混合溶液中,选用循环伏安扫描 (-0.2 V ~ 0.8 V)直至循环伏安曲线稳定为止,记录循环伏安(CV)曲线。取出参比电极和对电极,用超纯水冲洗后短暂静置待其表面干燥,将工作电极换成GO/GCE,采用CV (-0.2 ~ 0.8V)将GO/GCE在相同溶液中的CV曲线稳定为止,记录CV曲线[8]。
2 结果与讨论
2.1 GO/GCE对金属离子的选择性
我们用CV研究了1.0×10-3mol/L不同金属离子溶液(1.0 mol/L KNO39.0 mL,溶液酸度pH 5.02,1.0×10-3mol/L金属离子 1.0 mL)在未修饰的BE和GO/GCE上的电化学行为,计算出每种金属离子的电流峰值,GO/GCE对金属离子的选择性如图2所示。由图2结果可以看出:GO/GCE对Hg2+的选择性为最好。
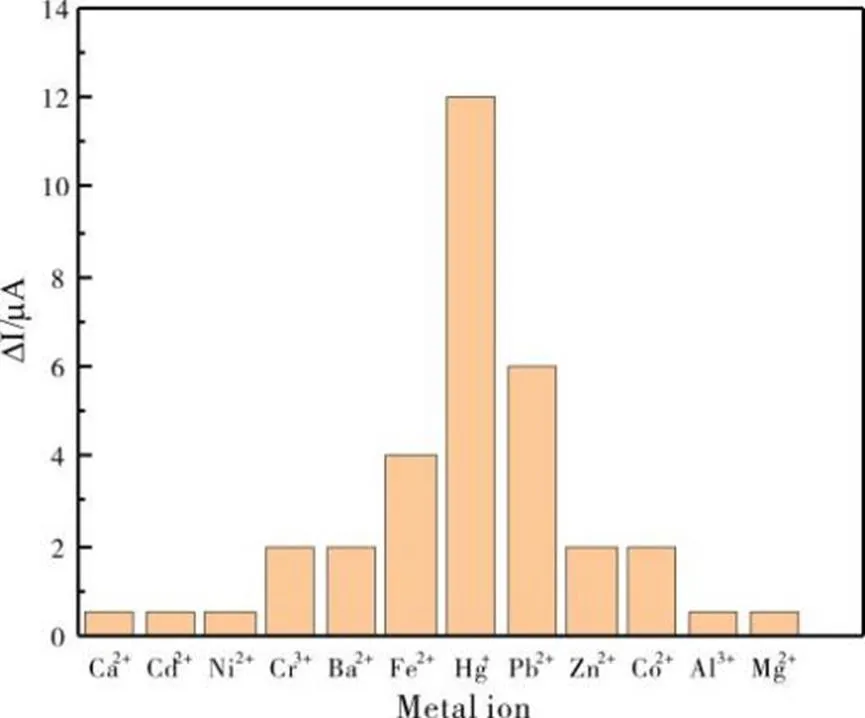
图2 GO/GCE对金属离子的选择性
2.2 Hg2+在GO/GCE上的电化学行为
我们实验用CV法研究了1.0×10-3mol/L Hg2+在GO/GCE上的电化学行为,在同样条件下,1.0×10-3mol/L Hg2+在BE上只显示出很微弱的电化学响应,这与Hg2+在GO/GCE上的电化学行为形成了明显的对比(如图3)。这是因为GO具有优异的电化学性能和较大的比表面积[8],为Hg2+在电极表面的电化学过程提供了很多的反应位点,从而使电子交换变得容易,也大大提高了测定的灵敏度。
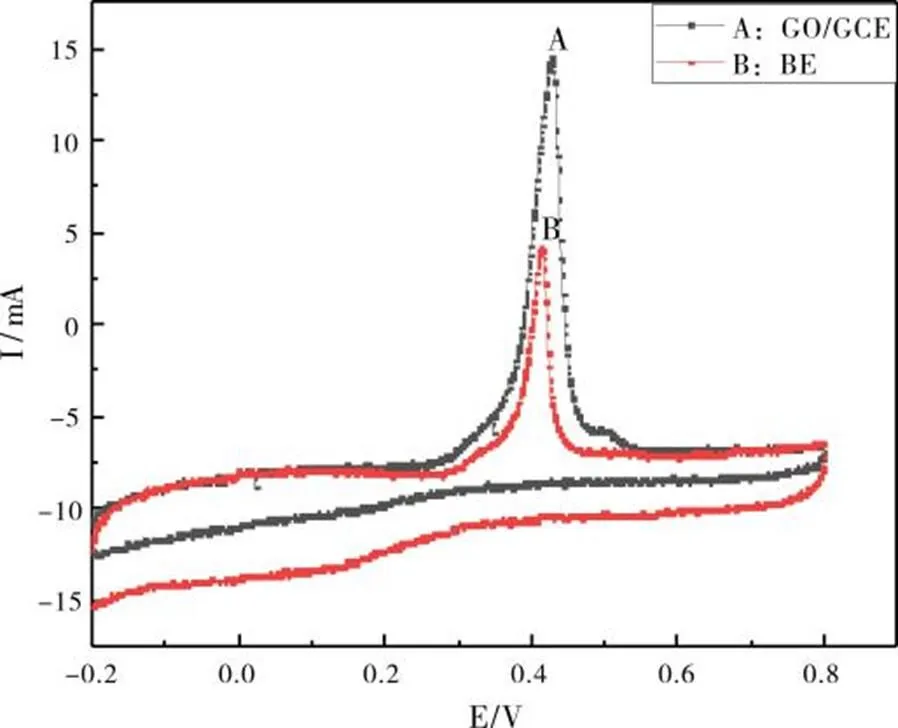
图3 GO/GCE对汞离子的CV图
2.3 基础溶液pH的调节
配置3.0 mol/L的HNO3溶液和6.0 mol/L的NaOH溶液各10 mL,用微量进样针分别取少量的HNO3和NaOH溶液,控制滴入的剂量来调节溶液(1.0 mol/L KNO39.0 mL,1.0×10-3mol/L金属离子 1.0 mL)的pH。将配置出的一系列不同pH的基础溶液利用CV检测Hg2+在电极上的电化学行为,通过对电流峰值的记录,对比得出Hg2+基础溶液的最佳pH范围为2.4 ~ 3.0之间(如图4)。

图4 基础溶液pH变化对Hg2+在GO/GCE上的电化学行为的影响
2.4 缓冲溶液组成的影响
利用CV分别研究了Hg2+在不同组分pH缓冲溶液构成的分析底液中的电化行为(缓冲溶液为1.1中所配制的溶液)。实验结果表明,在相同pH下Hg2+在醋酸钠-醋酸缓冲液中(1.0 mol / L KNO39.0 mL,溶液酸度pH 2.44,1.0×10-3mol/L Hg2+1.0 mL,缓冲溶液的体积1.0 mL)电流峰值最大,峰形较好。实验结果如图5。
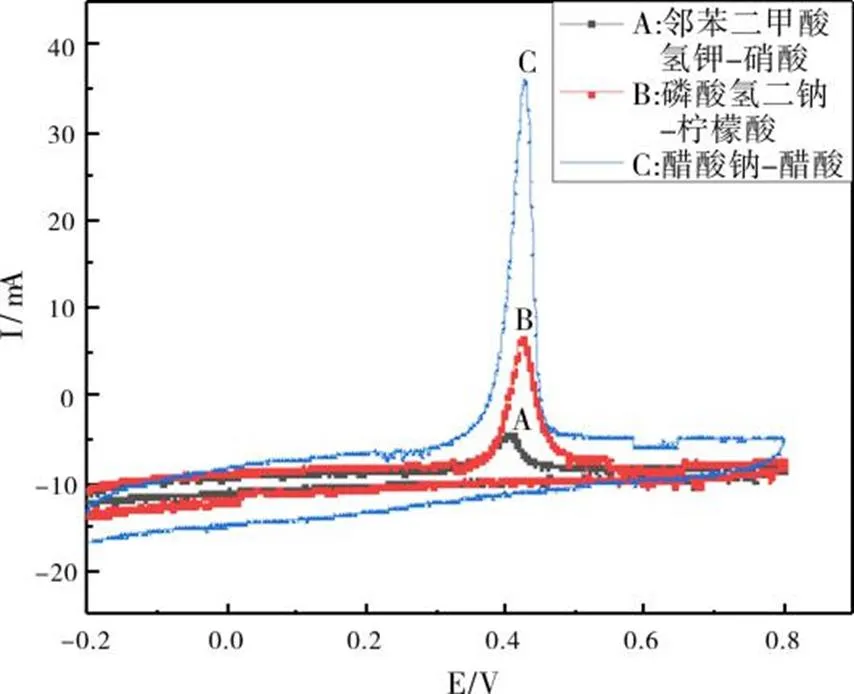
图5 GO/GCE测定汞离子缓冲溶液的选择
2.5 缓冲溶液用量的影响
在醋酸钠-醋酸作为缓冲溶液中,固定(KNO3缓冲液)的总体积不变(一定体积1.0 mol/L KNO3和一定体积0.10 mol/L缓冲溶液9.0 mL,pH = 2.44,1.0×10-3mol/L Hg2+1.0 mL),配制KNO3和缓冲液不同体积比的系列溶液,利用CV测出不同含量的缓冲液对1.0×10-3mol/L Hg2+在GO/GCE上的电化学行为的影响(如图6),发现电流峰值在缓冲液体积为2.0 mL,KNO3体积为7.0 mL的时候达到最大值。后续实验均采用此比例进行。
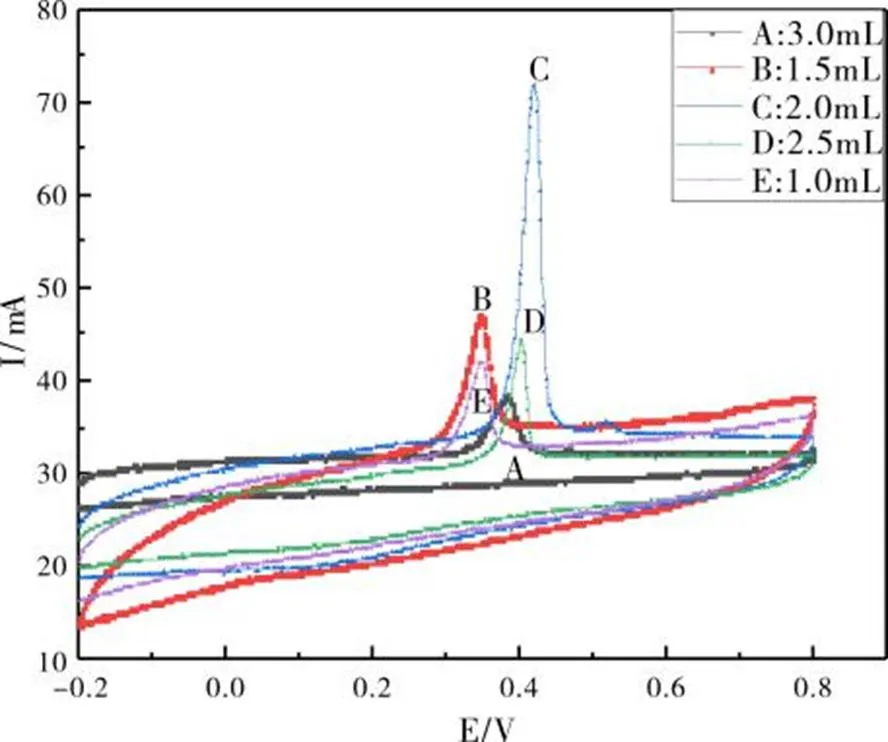
图6 GO/GCE测定汞离子缓冲溶液体积的影响
2.6 缓冲溶液pH的影响
配制不同pH值缓冲溶液,每次用量为2.0 mL,其它条件相同(1.0 mol/L KNO37.0 mL,1.0×10-3mol/L Hg2+1.0 mL,0.10 mol/L缓冲溶液2.0 mL),利用CV测出不同pH下Hg2+在GO/GCE上的电化学行为的变化(如图7),发现电流峰值在缓冲溶液pH为2.44时达到最大值。
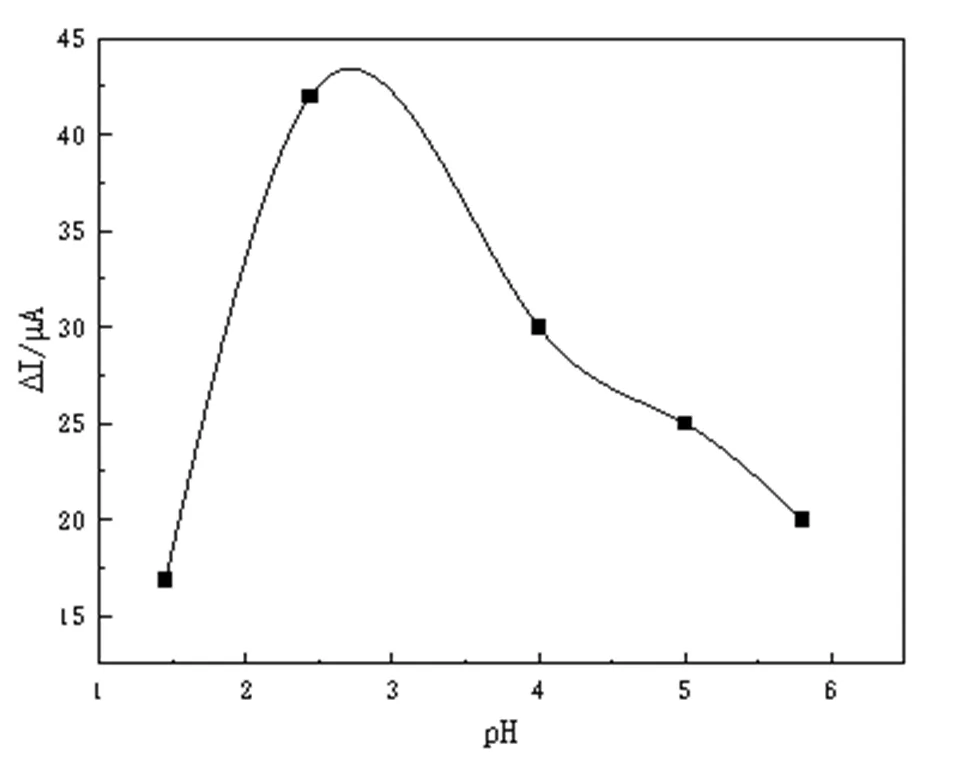
图7 GO/GCE测定汞离子缓冲溶液pH的影响
2.7 线性范围及检测限
使用1.0 mol/L KNO37.0mL,0.10 mol/L缓冲溶液2.0 mL(最优实验条件)基础液,配制系列不同浓度Hg2+标准溶液,利用CV研究了Hg2+在GO/GCE上的电化学行为,结果表明:在1.0 ~ 10.0 µmol/L范围内,Hg2+的电流峰值与浓度有良好的线性关系(如图8所示),归纳其线性回归方程为:ΔI=2.7241CHg+9.0936(CHg的单位µmol/L),线性相关系数为0.9977,检测限为0.90 µmol/L。用更新表面的电极测定2.0 µmol/L Hg2+溶液11次的相对标准偏差(RSD)为2.8%,说明了制备出的修饰电极具有较好的重现性和稳定性。
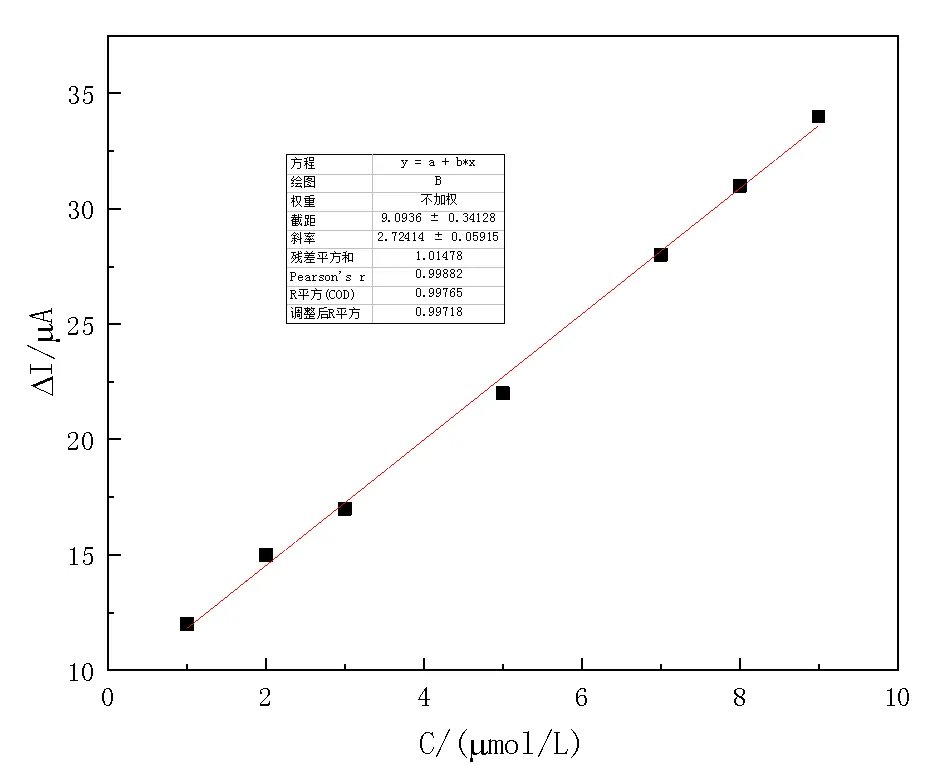
图8 Hg2+测定的线性范围
2.8 干扰实验
在优化的最佳实验条件下,测定6.0 µmol/L Hg2+溶液,并加入一定量的干扰金属离子,要求峰电流保持在±5%的范围内。常见金属离子的干扰情况如下:20000倍的K+、Na+,10倍的Cd2+、Ni2+、Cu2+、Pb2+、Ba2+、Cr3+、Zn2+、Mg2+、Fe2+、Al3+、Ca2+等不干扰汞的测定。
2.9 样品分析
准确取一定量的待测水样(视其汞量而定),加硝酸消解、蒸发至近干。加10 mL水和2滴硝酸,加热至沸腾。冷却到室温后转移至100 mL的容量瓶,加水定容,摇匀待测[8]。
在优化实验条件下,取1.0 mL安庆石塘湖废水样品,采用标准加入法测定其中Hg2+浓度,结果见表1。回收率在99.4% ~ 101.6%。用电感耦合等离子发射光谱仪(ICP)同时对样品进行测定,两种方法测定结果相比较吻合性很高。
表1 样品回收实验数据和ICP测定值对照表
Table 1 Comparison table of sample recovery experimental data and ICP determination value
序号样品量/mL加标量/µLCV测定值/µmol/LICP测定值/µmol/L回收率/% 12341.01.01.01.0-100.0200.0300.010.0019.9430.1639.9810.0520.0129.9840.01-99.4101.699.9
注:标准Hg(NO3)2溶液浓度为1.000 mol/L
3 结论
氧化石墨烯独特的电化学性能和较大的比表面积,使得用该材料制备的玻碳电极在测定Hg2+的时候表现出极佳的离子选择性。在确定了检测汞离子的缓冲体系后,通过对缓冲溶液用量、缓冲溶液pH、线性范围、重现性、检测限、和干扰离子六个实验条件的优化确定了最佳实验条件,最终实验确定修饰电极测定Hg2+的最佳实验条件为:6.5 mL的1.0 mol/L KNO3和2.5 mL的0.10 mol/L 醋酸钠-醋酸缓冲液(pH 3.64)。其中,Hg2+的线性范围为:ΔI=2.7241CHg+9.0936(CHg的单位µmol/L),线性相关系数为0.9977,检测限为0.90 µmol/L。11次的相对标准偏差(RSD)为2.8%。阳离子干扰实验中发现,20000倍的K+、Na+,10倍的Ni2+、Cd2+、Ba2+、Cr3+、Pb2+、Mg2+、Al3+、Zn2+、Ca2+、Fe2+、Cu2+等不干扰汞离子的测定,说明该修饰电极的抗干扰能力较佳。因此,通过此法可以检测水中的Hg2+浓度,为污水中的重金属离子测定提供简单可行的方法。
[1] Winefordner V. Calculation of the limit of detectability in atomic emission flame spectrometry[J].Analytical Chemistry,1964,36: 1939-1946.
[2]盛新凤,董彦杰.罗丹明6G与罗丹明6G酰肼测汞的对比研究[J].井冈山大学学报:自然科学版,2020,41(3): 19-23.
[3]王羽,王蔚港,杨向黎.基于仿生纳米导线的电化学传感器对水体重金属毒性的检测分析[J].分析化学,2021,49(1): 68-75.
[4]蔡良圣,林君,辛青. 电化学微传感器检测水中痕量铜离子[J].中国环境科学,2020,40(8): 3394-3400.
[5]于琛,韩慧滨,马红超. 氮化硼修饰碳糊电极对水中铅离子的检测[J].大连工业大学学报,2019,38(6):428-431.
[6] 耿明,董笑,朱庆仁,等.循环伏安法对邻苯二酚的测定[J]. 井冈山大学学报:自然科学版, 2021,42(4): 37-40.
[7] 林露,孙照霞,王静楠,等.双基于纳米银-二氧化钛-壳聚糖复合物修饰电极的穿心莲内酯电化学传感器及其应用研究[J].井冈山大学学报:自然科学版,2021,42(5): 14-18.
[8] 雷龙文,潘雨欣,董彦杰.钙钛矿修饰玻碳电极循环伏安法测定银离子的研究[J].鲁东大学学报:自然科学版,2021,37(1):57-61.
[9] Qi J, Yang R, Cao P. Y. Effects of the catalyst embedded conditions on the electrochemical properties of the grown in situ carbon nanotube chemically modified electrode[C]. 2011 Chinese Materials Conference,2013,2: 1399-1404.
[10] Lydiane G D, Evangeline N, Francis M M. Activated hordeum vulgare L. dust as carbon paste electrode modifier for the sensitive electrochemical detection of Cd2+,Pb2+and Hg2+ions[J].International Journal of Environmental Analytical Chemistry,2020,100(13):1429-1445.
[11] 文阁玲.新型N-RGO/MnO2复合材料的制备及其电化学检测汞的性能研究[D].芜湖:安徽工程大学,2019.
[12] 宋怡然,胡敬芳,李玥琪.基于Android的便携式水质电化学检测系统的研究[J].现代电子技术,2020,43(2): 32-36.
[13] Hu S Q, Xie Y L, Zhao S Q. Graphene/CeO2hybrid materials for the simultaneous electrochemical detection of cadmium(II), lead (II), copper(II), and mercury(II)[J]. Journal of Electroanalytical Chemistry,2015,757:235-242.
[14] De O, Paulo R, Lamy M. Mercury nanodroplets supported at biochar for electrochemical determination of zinc ions using a carbon paste electrode[J].Electrochimica Acta,2015,151: 525-530.
[15] 彭劲骥,郑红,邹义松. 基于电化学方法测定饮用水源水中的痕量铜离子[J].电化学,2019,25(6): 699-707.
[16] 徐旸,马红超,王帅.化学修饰电极在重金属离子检测中的研究与应用[D].大连:大连理工大学,2016.
[17] 简选,于浩,金君,等.聚L-组氨酸/石墨烯复合膜修饰电极对多巴胺和尿酸的同时测定[J]. 江西师范大学学报:自然科学版,2013,37(3):300-305.
[18] 许春萱,黄克靖,余萌,等.石墨烯修饰玻碳电极伏安法测定酪氨酸[J].化学研究与应用,2011,23(7): 943-946.
[19] 张娟.电化学聚合的聚合物修饰电极的改进制备及其性能研究[D].济南:山东大学,2018.
[20] 邹雪莲,王田霖,丁亚平.分析化学中的碳纳米管修饰电极[J]. 化学世界,2007,48(3): 79-182.
[21] 朱文清,蒋雪茵,张志林.有机电致发光器件中阴极界面修饰的材料、方法及分类[J].功能材料,2004,35(z1):272-275.
[22] Ranjita T, Nagappa T, Ashis S. Fabrication of the v electrochemically reduced graphene oxide-bismuth nanoparticles composite and its analytical application for an anticancer drug gemcitabine[J]. Chinese Chemical Letters,2017,28(7): 1429-1437.
Hg2+DETERMINATION IN SEWAGE BY CYCLIC VOLTAMMETRY WITH GRAPHEME OXIDE MODIFIED GLASSY CARBON ELECTRODE
PAN Yu-xin, LEI Long-wen,*DONG Yan-jie
(College of Chemistry and Chemical Engineering, Anqing Normal University, Anqing, Anhui 246013, China)
Graphene oxide was modified on glassy carbon electrode, the structure and morphology of graphene oxide on the electrode surface was characterized by scanning electron microscopy. The selectivity of the modified electrode to 12 metal ions was investigated, with the best selectivity to Hg2+. Compared the modified electrode with the bare electrode by cyclic voltammetry, the modified electrode has an obvious chemical response. The research results show that the best experimental conditions for the determination of mercury ions were: 2.5 mL sodium acetate-acetic acid buffer (0.10 mol/L, pH 3.64), 6.5 mL KNO3(1.0 mol/L). In the range of 1.0~10.0 µmol/L, the linear regression equation for measuring mercury ions is: ΔI=2.7241CHg+9.0936 (the unit of CHgis µmol/L), the linear correlation coefficient is 0.9977, and the detection limit (DL) is 0.90 µmol/L. The relative standard deviation (RSD) of 11 times was 2.8%. The recovery rate is between 99.4% and 101.6%. We have used the inductively coupled plasma emission spectrometer (ICP) to measure the samples at the same time, and the results of the two methods are quite consistent.
graphene oxide; modified electrode; cyclic voltammetry; Hg2+
1674-8085(2022)04-0015-06
O657.1
A
10.3969/j.issn.1674-8085.2022.04.003
2021-11-10;
2022-02-17
国家自然科学基金项目(21601002/B010303);安徽省高校自然科学重点项目(KJ2020A0511);省部共建煤炭高效利用与绿色化工国家重点实验室开放课题资助项目(2019-KF-31)
潘雨欣(1998-),女,安徽铜陵人,硕士生,主要从事电化学分析研究(E-mail:pyx980502@163.com);
*董彦杰(1962-),男,陕西延安人,教授,博士,硕士生导师,主要从事光、电、色谱分析研究(E-mail:dongyjaqtc@126.com).
