纤维蛋白(原)降解产物与D-二聚体最适比例可信区间的探讨*
2022-06-29黄珣钡刘超男凌莉琴
黄珣钡,刘超男,凌莉琴,廖 娟,周 静
四川大学华西医院实验医学科,四川成都 610041
纤维蛋白(原)降解产物(FDP)是纤溶酶降解纤维蛋白原和纤维蛋白形成的产物,为纤维蛋白原降解产物(FgDP)和纤维蛋白降解产物(FbDP)的统称[1-2]。D-二聚体(D-D)是纤溶酶介导的交联纤维蛋白降解的最终产物[3],由两个共价结合的纤维蛋白D结构域组成[4-5]。临床上常联合检测FDP和D-D,来判断某些由于凝血和纤溶失衡而导致的疾病,理论上D-D是FDP的一部分[2],FDP 水平应大于 D-D 水平,当出现D-D水平大于FDP水平的情况时(即FDP与D-D比例倒置),可能是由于D-D假阳性或者FDP假阴性造成,近年来已经有多篇文献报道了D-D假阳性的现象,并给出了相应的解决措施[4,6-8]。依据其生成原理,两者之间应存在某种比例关系,超出比例范围时需警惕FDP假阳性或者D-D假阴性,这种情况如何界定成为了摆在检验医师面前的一道难题,且目前尚缺乏相关的研究探索FDP/D-D的最适比例。本研究旨在通过大样本数据分析FDP/D-D的最适比例可信区间(CI),以帮助检验医师发现FDP和(或)D-D假阳(阴)性样本,并排除可能干扰FDP和(或)D-D检测的潜在影响因素,力求得到相对准确的检验结果,进一步优化临床报告质量,提高临床医生和患者满意度。
1 资料与方法
1.1一般资料 回顾性分析四川大学华西医院2019年1月至2020年12月同时进行FDP和D-D检测的报告206 879份,作为FDP/D-D最适比例CI建立组。纳入标准:FDP和D-D均在线性范围内(FDP在2.5~80 μg/mL;D-D在0.16~5.16 μg/mL FEU)。排除标准:FDP和D-D同时位于正常参考范围以内的样本,即FDP<5 μg/mL,D-D<0.5 μg/mL FEU。选取四川大学华西医院2021年3月同时进行FDP和D-D检测的样本1 022例,作为最适比例CI验证组。排除标准:FDP和D-D同时位于正常参考范围以内的样本,即FDP<5 μg/mL,D-D<0.5 μg/mL FEU。
1.2仪器与试剂 仪器为日本Sysmex公司CS5100全自动凝血分析仪,D-D检测试剂盒(INNOVANCE D-Dimer)由德国Siemens公司生产,检测原理为免疫比浊法;FDP测定试剂盒(配套试剂,Latex Test BL-2 P-FDP)购自日本BIOLINKS CO.,LTD公司,检测原理为免疫比浊法。建立组和验证组使用的D-D和FDP试剂批号有所不同,批号更换前均进行新旧批号比对,比对验证通过后方可使用;样本检测当日,D-D和FDP室内质控均在控。FDP检测试剂盒(验证试剂)换用其他厂家检测试剂,检测原理为乳胶增强免疫比浊法,样本检测当日,FDP室内质控在控。
1.3方法
1.3.1FDP/D-D最适比例CI的建立 将建立组数据按照D-D水平分为以下3组:<0.5 μg/mL FEU组、0.5~<2.5 μg/mL FEU组和≥2.5 μg/mL FEU组,建立3个组的95%CI,区间以内的样本定义为正常比值样本;区间以外的样本定义为异常比值样本,可能由于FDP和(或)D-D出现假阳(阴)性造成。
1.3.2FDP/D-D最适比例CI的验证 稀释法:对验证组中FDP≥5 μg/mL和D-D≥0.5 μg/mL FEU的样本均采用机内稀释模式进行稀释,根据FDP和D-D稀释前后结果分别计算FDP和D-D结果的偏差,偏差=(稀释后-稀释前)/稀释前×100%,偏差绝对值(|偏差|)>15%[1/2总允许误差(TEa)]则认为差异具有统计学意义。更换验证试剂法:虽然稀释前后结果|偏差|<15%,但FDP/D-D超过最适比例CI且结合临床信息高度怀疑FDP假阳性的样本,更换FDP验证试剂后重新检测。将稀释法|偏差|>15%和更换验证试剂后FDP/D-D位于最适比例CI的样本均定义为阳性样本。采用效能指标(灵敏度、特异度、阳性预测值、阴性预测值)评价本研究建立的最适比例CI在验证数据中发现阳性样本能力。
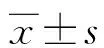
2 结 果
2.1FDP/D-D最适比例CI的建立 将建立组206 879例数据分为3组,3组数据FDP/D-D的分布及最适比例CI见表1。
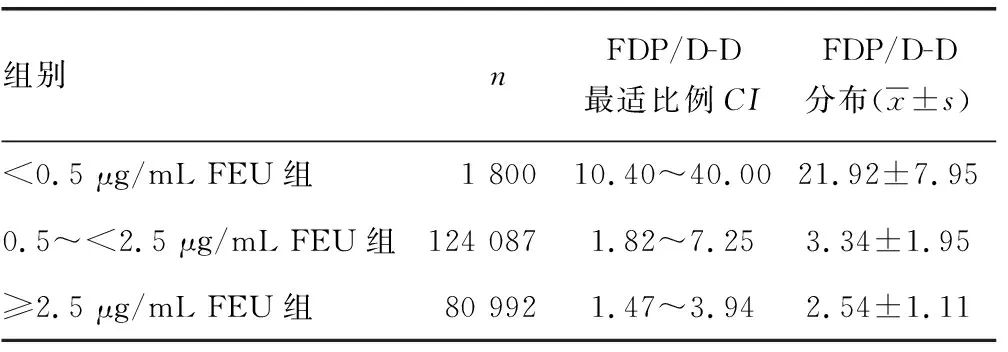
表1 各组FDP/D-D的最适比例CI
2.2验证组线性范围内样本FDP/D-D最适比例CI验证情况及效能评价 验证组中767例样本FDP、D-D均位于线性范围以内,但3个组别中分别有60.00%(3/5)、4.37%(25/572)和8.95%(17/190)样本FDP/D-D不在已建立的相应组别FDP/D-D最适比例CI。在FDP/D-D异常样本中分别有100.00%(3/3)、24.00%(6/25)和29.41%(5/17)样本为阳性样本,见表2。其中有5例样本FDP/D-D明显增高,见表3。虽然FDP稀释前后|偏差|<15%,但进一步了解患者无肝肾功能异常、无异常出血和血栓表现、无纤溶异常家族史,故更换FDP验证试剂重新检测FDP,结果明显降低。
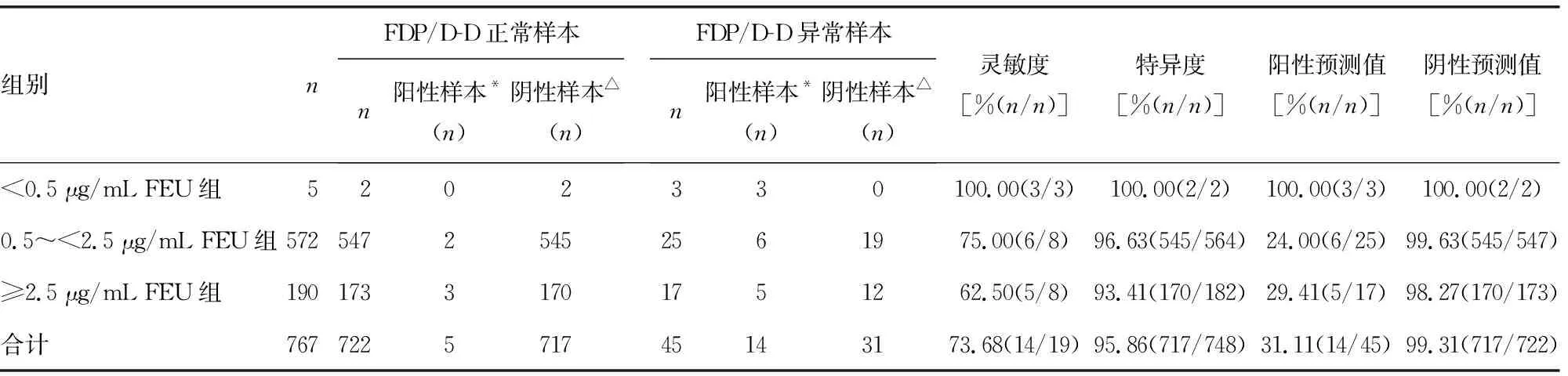
表2 线性范围内FDP/D-D最适比例CI验证情况及效能评价
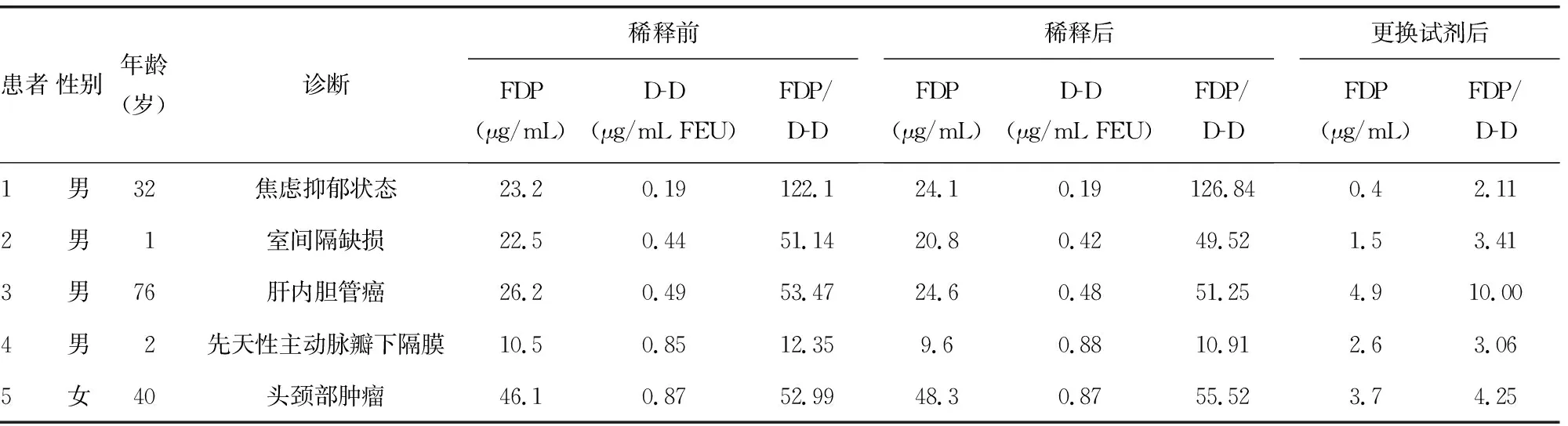
表3 FDP/D-D明显增高的5例样本情况
2.3验证组超线性范围样本FDP/D-D最适比例CI验证情况及效能评价 验证组中有255例样本超过检测范围,根据D-D≥2.5 μg/mL FEU时FDP/D-D最适比例CI,该群样本中有26.27%(67/255)样本FDP/D-D异常,异常的样本中有83.58%(56/67)的阳性样本,16.42%(11/67)的阴性样本。对于线性范围以外的结果即使FDP/D-D正常,仍有35.11%(66/188)的阳性样本漏检。采用FDP/D-D范围判断样本是否正常的灵敏度为45.90%(56/122),特异度为91.73%(122/133),阳性预测值为83.58%(56/67),阴性预测值为64.89%(122/188)。
2.4D-D和FDP检测流程图及处置建议 根据本研究,本课题组推荐使用以下流程判断和处置FDP和D-D结果,见图1。
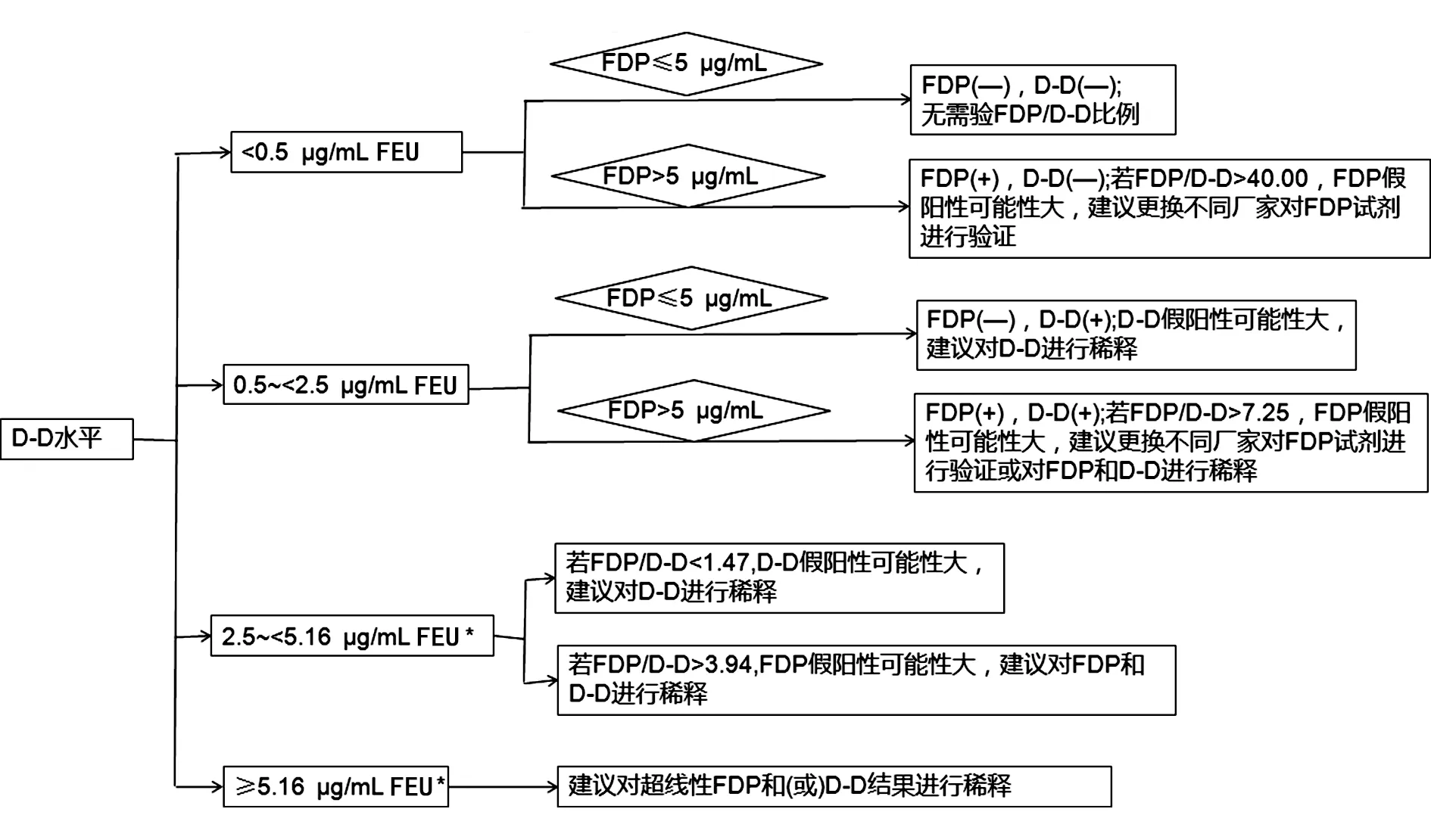
注:*D-D检测线性范围上限依据各实验室检测试剂品牌不同、批号不同自行确立。图1 D-D和FDP检测流程图及处置建议
3 讨 论
D-D是交联纤维蛋白在纤溶酶作用下的降解产物,FDP是纤维蛋白(原)的降解产物,两者联合检测有助于鉴别原发性纤溶亢进和继发性纤溶亢进,同时FDP和D-D作为纤溶标志物也用于弥散性血管内凝血(DIC)的诊断[9-10]。目前,临床上用于检测FDP和D-D的方法较多,包括乳胶凝集法、酶联免疫吸附法(ELISA)、免疫胶体金法、免疫比浊法等[11]。其中,免疫比浊法有着操作简便快速、灵敏度高、定量准确等优点,已广泛应用于多种全自动凝血分析仪[12],其检测原理基于抗原抗体反应,抗原抗体比例失调、胆红素[13]、异嗜性抗体[14]、类风湿因子[8]或其他蛋白[15]等干扰均可能影响检测准确性,导致假阳性结果,从而影响临床医生的诊断,延误患者的病情。本研究通过对大量历史数据的回顾性分析,建立了FDP/D-D最适比例CI,以帮助临床发现潜在的影响因素最终降低干扰获得相对准确的检测结果。
由于D-D水平的高低会导致FDP/D-D范围的差异较大,且D-D不同水平在国际血栓与止血学会(ISTH)的DIC诊断中积分不同[9-10],同时结合D-D在静脉血栓栓塞(VTE)疾病中的阴性排除标准D-D<0.5 μg/mL FEU,本研究分别以0.5 μg/mL FEU和2.5 μg/mL FEU的D-D水平将数据分为低、中、高3个组别建立FDP/D-D最适比例CI。
FDP和D-D的定量检测方法使其检测结果与稀释倍数呈现一定的比例关系,当存在干扰物质时,稀释可降低部分干扰因素,使其比例关系消失,稀释后结果更接近样本的真实值。本研究利用FDP和D-D稀释前后的偏差是否超过TEa的1/2(均为15%)作为评价是否存在稀释效应的标准,当稀释法无效时,再采用更换不同检测系统或检测试剂等方法解决。
对于检测结果位于线性范围以内的数据,本研究建议FDP和D-D同时位于正常参考范围以内时无须比例验证,在数据统计时亦已剔除。根据已建立的FDP/D-D区间,验证数据位于线性范围以内且FDP/D-D正常的722例样本中,仅有5例(0.69%)阳性样本被遗漏,特异度可达95.86%;比值异常的45例样本中有14例阳性标本,灵敏度为73.68%。但需要注意的是,并非所有阳性样本都可以通过稀释发现。本研究样本中,有5例样本FDP/D-D增高明显,但FDP稀释前后|偏差|<15%,根据该检测结果提示患者存在原发性纤溶亢进。经查阅患者病历,5例患者肝、肾功能均正常、无异常出血表现、无纤溶异常家族史。结合FDP检测原理,考虑到FDP包含的纤维蛋白降解片段长短不一,不同品牌试剂所包被的单克隆抗体针对的抗原靶位会存在不同,对应检出的FDP片段(X、Y、D、E等碎片)也会有所差异。当患者体内存在一些与被检物质活性相似但化学结构不同的物质时,容易造成假阳性的结果[16],此时稀释法不能有效降低此类干扰,应更换不同品牌的FDP试剂重新检测。更换检测试剂后,该5例样本的FDP结果明显降低,若仅依据线性范围来判断结果的准确性,很容易将此类FDP假性增高的样本漏检,发放不正确的报告,让临床医生做出原发性纤溶亢进的误诊结果,导致不当的诊疗。依据本研究建立的FDP/D-D最适比例CI给出以下处理建议:对于FDP和D-D均位于线性范围的样本,当D-D<0.5 μg/mL FEU,FDP/D-D>40.00时,建议更换不同厂家FDP试剂验证;当D-D为0.5~<2.5 μg/mL FEU,FDP/D-D>7.25时,FDP假阳性可能性较大,但不排除弱的干扰因素影响,此时建议更换不同厂家FDP试剂或对FDP和D-D进行稀释;当D-D为2.5~<5.16 μg/mL FEU时,若FDP/D-D<1.47则D-D假阳性可能性大,建议对D-D进行稀释;若FDP/D-D>3.94则FDP假阳性可能性较大,建议对FDP和D-D进行稀释。
由于部分实验室使用的D-D试剂线性范围较窄,临床中采用了延长D-D检测标准曲线的方法,通过人为增加D-D线性范围来减少临床稀释复检的频率,对此,本研究也进行了相关验证。在验证组中有255例样本FDP或D-D位于线性范围外,通过对上述样本进行稀释发现,比值正常的188例样本中仍有66例阳性样本漏检,但是验证组FDP和D-D位于线性范围内的767例样本中仅5例漏检,进一步提示使用延长检测标准曲线的方法获得的检测结果不准确,由此计算得到的FDP/D-D会降低发现FDP和(或)D-D结果异常的阴性预测值(由99.31%降至64.89%)。故当FDP或D-D检测结果超过标准曲线的线性范围时,应该对所有样本稀释后再进行检测,否则可造成FDP和(或)D-D假阳(阴)性,更可能导致FDP和(或)D-D的检测错误。
综上所述,联合检测FDP和D-D,同时结合FDP/D-D更有利于辨别两者检测结果的准确性。当FDP和D-D均位于线性范围以内时,可以参照不同D-D水平对应的最适比例CI发现FDP/D-D异常的样本,并采取相应处理措施,及时纠正FDP假性增高的情况;而当FDP或D-D位于线性范围以外时,利用人为增加D-D线性范围的方式获得的结果可能较真值偏差较大,建议通过稀释使其位于线性范围以内再行判断,可以较好地发现FDP和(或)D-D假阳(阴)性样本,避免由于检测结果的不准确,延误临床诊疗。
