一种眼底图像出血点的检测算法
2022-06-29周梦颖杨晓宇邱媛杨春兰刘冰
周梦颖 杨晓宇 邱媛 杨春兰 刘冰
0 引言
糖尿病视网膜病变(diabetic retinopathy,DR)是由糖尿病引起的并发症,每年因为DR引起失明的患者占失明总人口的10%左右,在我国糖尿病患者致盲率是非糖尿病患者的25倍[1],美国眼科协会视网膜专家组2008年推荐DR眼底检查的金标准是在散瞳情况下,使用传统裂隙灯联合前置镜和双目检眼镜检查周边视网膜情况,但是这种方法的敏感性和特异性主要取决于检查者的经验和接受的培训[2]。计算机辅助筛查系统是提高DR筛查效率的有力工具,而DR病变特征检测则是其中最为关键的一个步骤。出血点(hemorrhages,HA)作为DR病变主要特征之一,是早期诊断的主要依据[3]。
目前HA检测算法主要有两类:一类是先分割眼底图像关键结构,然后检测HA病变,其包括基于阈值的方法[4-6]、基于形态学的方法[7-10]等;另一类是先提取图像特征,然后使用机器学习等算法对目标分类,从而检出HA病变结构,主要有神经网络[11-13]、K均值聚类和自适应模板匹配[14]、SVM分类器[15-16]等方法。现有方法主要存在以下问题:首先是每幅眼底图像明暗不均匀,且各个图像之间整体明暗程度也不相同,HA对比度较差,给分割带来困难。其次是眼底基本结构中血管对图像分割结果的影响较大,HA和周围血管组织的灰度值存在交叉,导致算法的灵敏度降低。针对上述难点,本文对眼底图像进行灰度均匀性调整,利用HA的局部亮度灰度值特征,提出一种基于灰度检测和形态学重构的HA自动检测方法。
1 眼底图像出血点检测算法
针对HA检测的流程如图1所示。

图1 出血点检测流程Figure 1 Flowchart of HA detection
1.1 图像预处理
1.1.1 RGB通道选取
将原彩色眼底图像进行RGB通道分离,以便于观察病变特征的情况。得到3个通道的图像如图2所示。对比这3幅灰度图像可以发现G通道(图2C所示)的HA和血管在图像中较明显,因此选取G通道灰度图像作为后续处理的出发点。
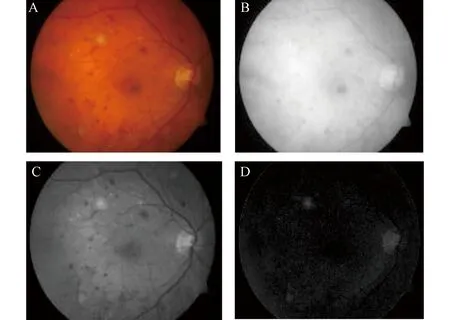
A为原始图像;B为R通道图像;C为G通道图像;D为B通道图像图2 RGB通道图像Figure 2 RGB channelimages
1.1.2 图像灰度均匀性调整
本文采用图像外围和中心灰度补偿进行图像灰度的均匀性调整。图像外围灰度补偿包含环状亮度补偿[式(1)]、线性亮度补偿[式(2)、式(3)]所示。
(1)
式中:I为原像素亮度;rmax为眼底的半径;a为补偿因子;α为指数因子。
(2)
(3)
式中:j为像素横坐标;C为截断处灰度补偿值;r1为补偿起始半径,取rmax的2/3。
图像中心亮度补偿如式(4)、式(5)所示,采用MATLAB的区域操作函数bwlabel和regionprops对图像中心最大连通区域进行环状灰度补偿。
(4)
(5)
式中:K为系数因子;C为截断处灰度补偿值;r2为补偿截止半径,取rmax的1/2;β为指数因子。灰度均匀性调整后的眼底图像如图3(B)所示:

A为G通道图像;B为灰度均匀性调整后的图像图3 基于灰度均匀性调整后的图像Figure 3 Images based on gray uniformity adjustment
1.2 基于局部灰度差异的阈值分割
1.2.1 眼底图像阈值分割
经过图像灰度均匀性调整,整幅图像中眼底组织和HA的灰度窗交叉范围变小,使用阈值分割可以更好地去除其他眼底组织,目的是缩小HA搜索范围,减少检测时的计算量,标记HA候选区域。二值化处理:
(6)
根据眼底图像HA和眼底其他关键结构的像素灰度值的分布,通过检查数据库中眼底图片,得出HA的灰度值一般在10~70之间。这里分别取最低和最高灰度值为:THlower=10,THupper=70。IBw为二值化后的像素值。阈值分割后的二值化图像如图4所示。

图4 阈值分割图像Figure 4 Image of threshold segmentation
1.2.2 出血点和血管的分割
基于图4中分割出来的出血点搜索范围,采用逐个像素搜索的方法进一步提取出血点。这里取其邻域为20×20的矩形区域,取邻域内亮度最高的像素与待判定像素进行比较,判定该像素是否可能为出血点。计算公式为:
(7)
由以上步骤检测出的血管和出血点图像如图5所示。
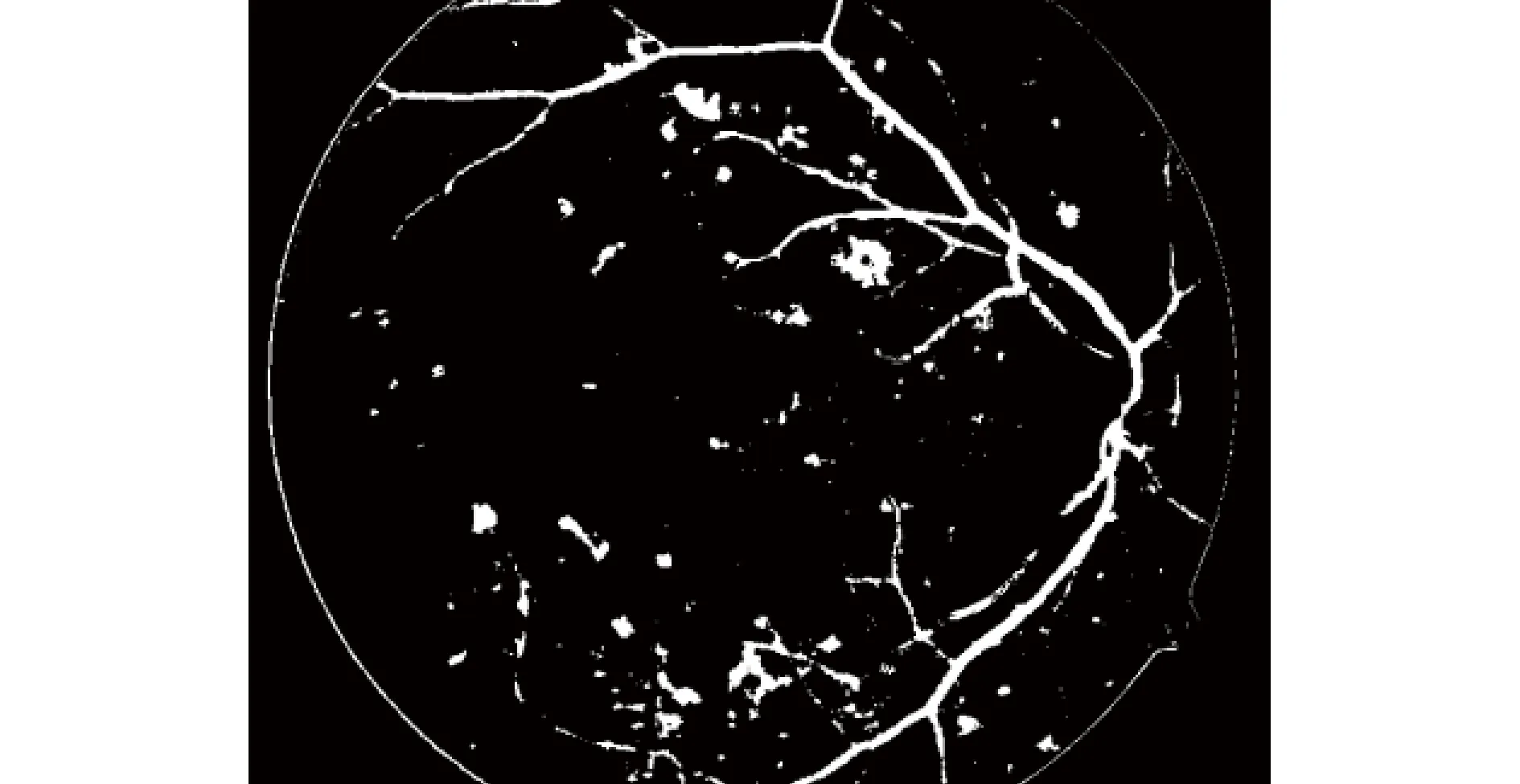
图5 局部灰度差异检测图像Figure 5 Image of local gray difference detection
1.3 血管的消除
利用形态学重构方法中的开运算和闭运算对血管的连通区域进行消除,以去除血管对HA提取的影响。血管区域的一个显著特征是形状细长,因此可以通过对区域的长度和面积的大小关系来判定其是否为血管区域。设某一连通区域中两个距离最远的像素距离为L,连通区域面积为S,当D>2时判定该区域为血管区域。图6为去除血管后的结果。

图6 血管去除后图像Figure 6 Image of blood vessel removing
(8)
1.4 基于形态学图像后处理
在出血点检测的过程中会产生一些边缘效应的负样本。为将边缘效应负样本彻底消除,本文将上一步得到的检测结果图像与原Mask形态学腐蚀操作后的二值化图像掩膜逐像素相与,来去除分割结果中有效区域外围的假阳性部分,确保整幅图像中只保留眼底区域为有效的分割区域,最终出血点检测结果如图7所示。

图7 出血点检测结果Figure 7 Image of HA detection results
2 实验结果
本文采用公开的标准数据库DIARETED1[17]进行实验。数据库包含89张眼底图像,其中5张为正常眼底图像,其余84幅病变图像主要涉及DR非增殖期的病变(比如硬性渗出物和出血点)。选取其中50幅图像(45幅具有HA病变的图像、5幅正常图像)作为实验数据。以数据库中手工标记结果作为实验检测结果评价的金标准。
在实现本文眼底图像HA检测算法的基础上,本文与两种典型算法[10,14]做了比较,结果见表1。图8展示了用本文算法得到的部分HA检测结果。在直观的图示结果中可知,本文HA检测算法与专家手工标记结果相似,具有较好的可行性、稳定性和优越性。

表1 本文算法与其他检测算法对比结果Table 1 Comparison results of other detectionalgorithms and this algorithm
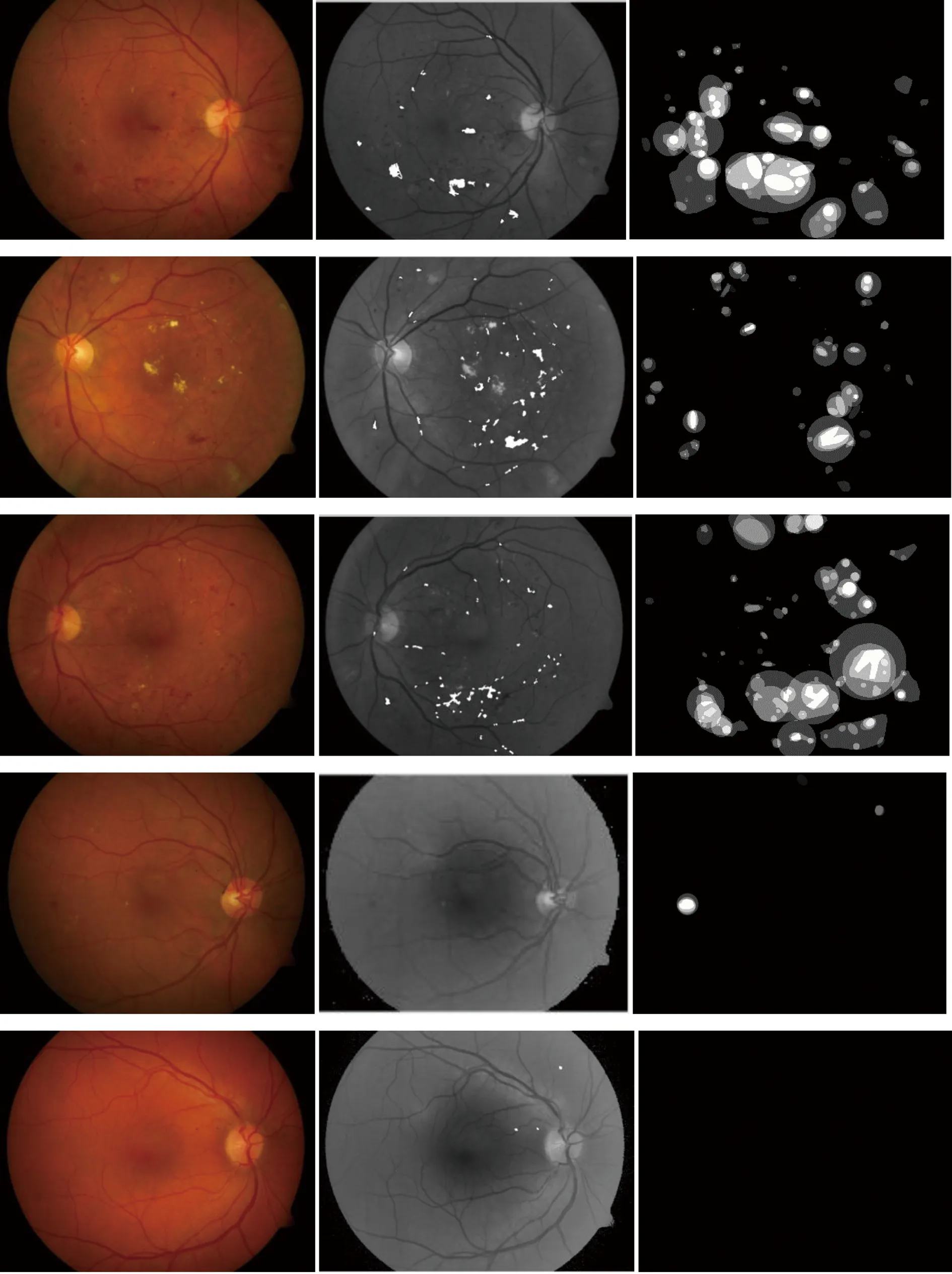
第1~4行是HA病变图像,第5行是正常图像;第1列是原始图像,第2列是本实验结果,第3列是数据库专家分割结果图8 出血点检测结果对比Figure 8 Comparison results of HA detection
3 讨论与结论
在实验中所用到的50幅眼底图像(45幅HA病变图像,5幅正常图像)中,本文正确检测HA病变图像42幅,有3张病变图像未被检测出来(例如图8第4行第2列)。正常图像5幅中,有1幅误检出了HA(图8第5行第2列)。与文献[7]、[11]、[14]比对发现,本算法灵敏度高于其他算法,而特异性与文献[14]持平,仅略低于文献[7]、[11],算法整体表现达到了目前研究中的主流水平,并在灵敏度方面有一定优势。但由于拍摄条件和个体差异,使病变区域模糊,HA的人工辨识度低,从而出现漏检,并且血管中也存在灰度不均匀,造成分割后使血管区域断裂,这些断裂的血管亮度特征与HA相似,造成一定程度的误检。
Javitta等[18]构建了DR自动筛查技术的健康准则模型,提出在患者能够保证较高检查眼底频率的情况下,自动检查的灵敏度高于60%则认为该DR检测系统有效。随着近年来DR自动诊断技术的不断发展,灵敏度和特异性不断提升。本文提出基于灰度检测和形态学重构的HA检测方法具有以下优点:减少了眼底图像质量和眼底基本组织结构对HA检测的影响,提高了检测的灵敏度。在一定程度上减少了人工成本,提高临床的筛查效率。同时满足临床中对DR病灶自动检测算法精度与速度的要求,不仅解决了眼底图像噪声干扰、光照不均匀的问题,并在灵敏度、特异性上也达到甚至部分超过了现有研究水平,为糖尿病视网膜病变辅助诊断系统奠定了基础。
