固相萃取-气相色谱法测定水中20 种酚类化合物
2022-06-28彭礼枚谭丽君蒋建军向勇
彭礼枚,谭丽君,蒋建军,向勇
[1.广电计量检测(湖南)有限公司,长沙 410000; 2.中国电建集团中南勘测研究院有限公司,长沙 410000]
环境中酚类化合物主要来源于石油化工、塑料制造、颜料合成、制药、造纸等工业污水排放沉积。酚类化合物属于毒性很强的有机污染物,大多数硝基酚有致突变作用,酚的甲基衍生物不仅致畸,而且致癌,酚类化合物的毒性随着芳环上取代程度的增加而增大。由于工业污水中酚类物质的存在,使地表水体极易受到污染[1-2],因此研究水中酚类物质的检测方法具有重要意义。目前酚类化合物的提取方法主要有溶剂萃取法、蒸馏法、衍生法、固相萃取法等[3-4],检测方法主要有气相色谱法[5]、气相色谱-质谱法[6-10]、液相色谱法[11-14]、分光光度法[15-16]等。溶剂萃取法试剂用量大,重复性差;衍生化处理,操作复杂,测量误差大;蒸馏法处理酚类化合物仅限于可挥发性酚类,可以测定的酚类化合物种类有限;固相萃取法相比前几种样品处理方法具有试剂用量少,可批量处理样品,既可富集,又能去除杂质等优点。目前现有测定水中酚类类化合物的方法中一次最多可同时测定18 种酚类物质[6],笔者建立一种固相萃取-气相色谱法测定水中酚类化合物的检测方法,该方法可同时测定20 种酚类化合物,具有快速,准确,高效,精密度好的优点,可用于地表水中酚类物质的筛查和定量。
1 实验部分
1.1 主要仪器与试剂
气相色谱仪:7890B 型,美国安捷伦科技有限公司。
固相萃取柱:HLB 柱,6 mL(1 000 mg),上海迪马科技有限公司。
电子天平:MS105 du 型,感量为0.01 mg,梅特勒-托利多国际贸易(上海)有限公司。
21 种酚类化合物混合标准溶液:苯酚、邻氯苯酚、邻甲酚、对间甲酚、邻硝基苯酚、2,4-二甲基苯酚、2,4-二氯苯酚、2,6-二氯苯酚、4-氯-3-甲酚、2,4,6-三氯苯酚、2,4,5-三氯苯酚、2,4-二硝基酚、对硝基苯酚、2,3,4,6-四氯酚、2,3,4,5-四氯酚、2,3,5,6-四氯酚、2,4-二硝基邻甲酚、五氯酚、地乐酚、消满酚、4,6-二硝基邻甲酚的质量浓度均为1 000 mg/L,编号为80011 JA,常州市坛墨质检科技股份有限公司。
正己烷、丙酮、二氯甲烷、甲醇、乙酸乙酯:均为色谱纯,美国默克试剂公司。
氮气:纯度(体积分数)为99.999%,长沙赛众特种气体有限公司。
实验用水为一级超纯水。
待测样品:东莞石马河流域地表水。
1.2 溶液配制
20 种酚类化合物混合标准使用液:苯酚、邻氯苯酚、邻甲酚、对间甲酚、邻硝基苯酚、2,4-二甲基苯酚、2,4-二氯苯酚、2,6-二氯苯酚、4-氯-3-甲酚、2,4,6-三氯苯酚、2,4,5-三氯苯酚、2,4-二硝基酚、对硝基苯酚、2,3,4,6-四氯酚、2,3,4,5-四氯酚、2,3,5,6-四氯酚、2,4-二硝基邻甲酚、五氯酚、地乐酚、消满酚的质量浓度均为100.0 mg/L,准确移取21 种酚类化合物混合标准溶液1.00 mL 于10.0 mL 容量瓶中,用甲醇定容至标线,混匀。
20 种酚类化合物系列混合标准工作溶液:分别移取0.05、0.1、0.2、0.5、1.0 mL上述20种酚类化合物混合标准使用液于5 只10.0 mL 容量瓶中,用甲醇定容至标线,配制成20 种酚类化合物的质量浓度均分别为0.5、1.0、2.0、5.0、10.0 mg/L的系列混合标准工作溶液。
1.3 色谱条件
色谱柱:HP-5柱(30 m×0.25 mm,0.25 μm,美国安捷伦科技有限公司);柱温箱升温程序:初始温度为80 ℃保持1 min,然后以10 ℃/min升温至250℃,保持10 min;载气:氦气,流量为1.0 mL/min(恒流);进样口温度:260 ℃;进样方式:不分流进样;检测器:火焰离子化检测器。
1.4 样品处理
取待测水样1 000 mL,加入3.5 g/L 的硫代硫酸钠溶液1 mL,去除余氯,加入磷酸调节pH 值为3左右。先用5 mL 甲醇活化固相萃取小柱,样品以5 mL/min 流量经过活化好的固相萃取小柱,富集过程中始终保持1 cm 液面高度,富集完成后,用5 mL乙酸乙酯洗脱,洗脱液经旋蒸浓缩,用乙酸乙酯定容至1.0 mL,待测。
2 结果与讨论
2.1 色谱条件选择
进样口温度为260 ℃时,即能保证目标化合物完全气化,又不至于因温度过高而分解,可达到最佳的气化效果,故选择进样口温度为260 ℃。
分别考察载气流量为0.8、1.0、1.2 mL/min条件下色谱峰的出峰时间和色谱峰形。结果表明,当载气流量为0.8 mL/min 时,出峰时间较长;当载气流量为1.2 mL/min 时,有部分组分没有完全分开;当载气流量为1.0 mL/min 时,各组分能较好分开,分析时间也有所缩短,故选择载气流量为1.0 mL/min。
酚类化合物属于弱极性化合物,选择HP-5 弱极性毛细管柱[6]能达到较好的分离效果。
分别考察升温速率为5、10、20 ℃/min 条件下色谱峰的分离效果。结果表明,当色谱柱升温速率为20 ℃/min 时,目标物色谱峰重叠;当升温速率为5 ℃/min 时,色谱峰形变宽,分离效果差;当升温速率为10 ℃/min 时,20 种酚类化合物能有效分离,因此选择升温速率为10 ℃/min。
在选定的1.3 色谱条件下,20 种酚类化合物混合标准溶液(10.0 mg/L)的色谱图如图1 所示。由图1 可知,在优化的仪器工作条件下,各组分均能得到充分气化,20 种酚类化合物分离效果良好。
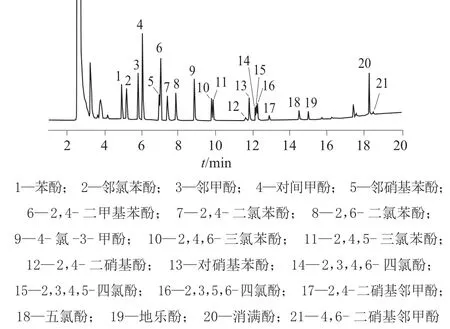
图1 酚类混合标准溶液(10.0 mg/L)色谱图
2.2 净化柱选择
分别考察PLS 柱、HLB 柱、Florisil 柱和Silica柱4 种固相萃取柱[17-19]对目标物的净化效果。将20 种酚类化合物标准溶液加入空白水样中,经不同的固相萃取柱洗脱、浓缩,用乙酸乙酯定容至1.0 mL,在1.3 色谱条件下进样测定,计算采用不同萃取小柱时各待测化合物的回收率。结果表明,采用Florisil柱时20种酚类化合物的回收率为32.4%~65.2%,Silica 柱的回收率为28.9%~67.3%,PLS 柱的回收率为56.9%~85.4%,HLB 柱属于亲水亲油平衡萃取柱,具有水可浸润性,可耐受极端pH条件,采用HLB 柱时,20 种酚类化合物的回收率均可达到90%以上,大于其它几种萃取柱,因此选择HLB 柱作为净化柱。
2.3 洗脱溶剂选择
固定其它试验条件,分别考察正己烷、乙酸乙酯、丙酮、甲醇、二氯甲烷、正己烷-二氯甲烷(体积比1∶1)[18]5 种溶剂的洗脱效率[4],计算采用不同洗脱溶剂时各待测化合物的回收率。结果表明,以正己烷为溶剂时洗脱效果最差,20 种酚类化合物的回收率为19.5%~46.7%;以丙酮为溶剂时,20 种酚类化合物的回收率为35.6%~67.5%;以正己烷-二氯甲烷(体积比1∶1)为溶剂时,20 种酚类化合物的回收率为39.6%~72.5%;以甲醇为溶剂时,20 种酚类化合物的回收率为65.8%~87.6%;以二氯甲烷为溶剂时,20 种酚类化合物的回收率为68.7%~89.6%;以乙酸乙酯为溶剂时洗脱效果最好,20 种酚类化合物的回收率均可达到91.2%以上,因此选择乙酸乙酯作为洗脱溶剂。
2.4 线性方程与检出限
在1.3 色谱条件下,对20 种酚类化合物系列混合标准工作溶液进行测定,以待测化合物的质量浓度为自变量、色谱峰面积为因变量进行线性回归,计算线性方程和相关系数。以甲醇为溶剂,对20 种酚类化合物标准溶液逐级稀释,在1.3 色谱条件下测定,以3 倍信噪比对应的质量浓度作为方法检出限,以3 倍检出限作为定量限。
20 种酚类化合物质量浓度线性范围、线性方程、相关系数、检出限及定量限见表1。

表1 20 种酚类化合物的质量浓度线性范围、线性方程、相关系数、检出限及定量限
2.5 加标回收与精密度试验
在空白样品中分别加入一定量的20 种酚类化合物混合标准溶液进行加标回收与精密度试验,每种加标水平样品按1.4方法平行处理5份样品溶液,在1.3 色谱条件下分别进行测定,加标样品色谱图如图2 所示,测定结果见表2。由表2 可知,3 种加标水平样品的平均回收率为87.0%~103.8%,测定结果的相对标准偏差为1.48%~4.89%,表明该法具有良好的准确度和精密度。

表2 20 种酚类化合物的加标回收与精密度试验结果
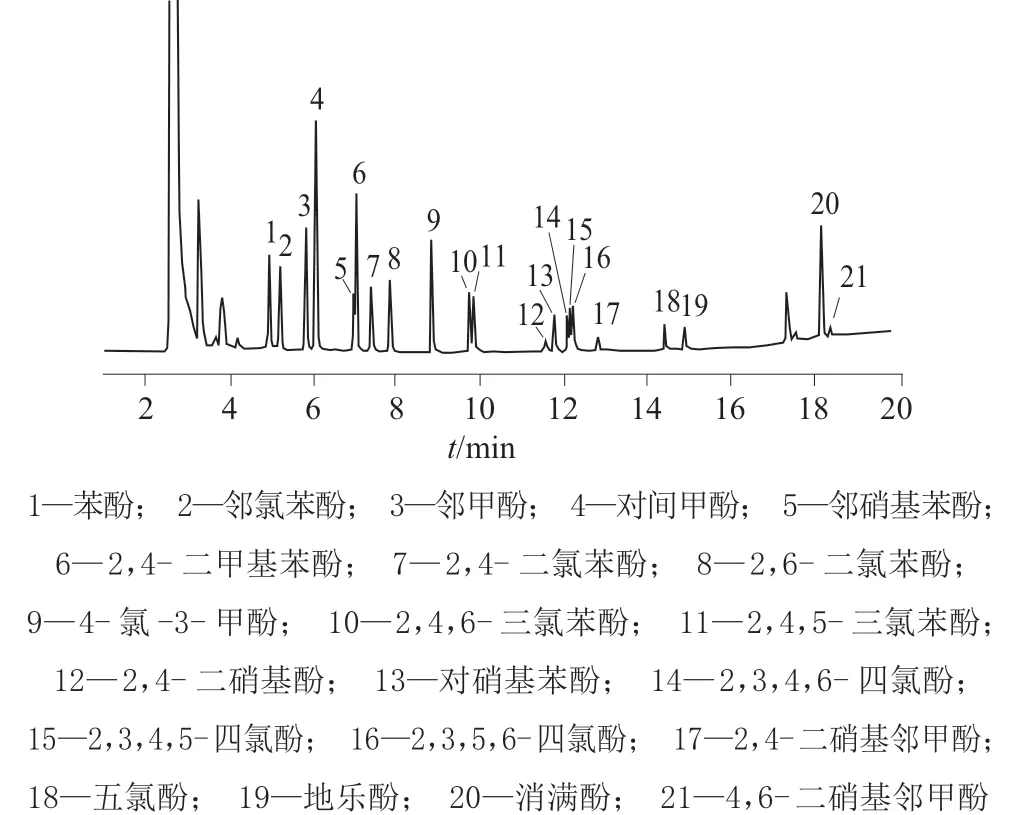
图2 加标样品溶液色谱图
3 结语
建立了测定地表水中20 种酚类化合物的气相色谱检测方法。该方法样品处理简便易行,检出限低,重复性良好,可为地表水中酚类化合物的检测提供技术参考。
