获得性免疫缺陷综合征合并神经梅毒的MRI影像表现
2022-06-27任美吉李宏军
任美吉,李 莉,赵 晶,李宏军
首都医科大学附属北京佑安医院放射科(北京 100069)
神经梅毒(neurosyphilis,NS)是由梅毒螺旋体(treponema pallidum,TP)侵犯中枢神经系统导致的疾病。NS可在梅毒初染后的几周至数年内的任何阶段发病,表现为无症状感染或神经系统功能障碍,临床症状缺乏特异性,易造成已治愈的假象[1-2]。研究表明人类免疫缺陷病毒(human immunodeficiency virus,HIV)感染和TP感染可能存在相互促进和协同的关系,HIV感染不仅改变NS的临床表现,还可能加速其发展[3],导致获得性免疫缺陷综合征(acquired immunodeficiency syndrome,AIDS)合并NS患者容易延误诊断和治疗。本文对首都医科大学附属北京佑安医院收治的32例AIDS合并NS患者的临床、病理及影像学资料进行回顾性分析,以期为临床诊断提供参考。
1 资料与方法
1.1 研究对象
回顾性收集2015年1月至2020年12月首都医科大学附属北京佑安医院经临床确诊的AIDS合并NS患者。本研究经首都医科大学附属北京佑安医院伦理委员会批准(编号:京佑科伦字〔2020〕071号)并获患者知情同意。
纳入标准:①符合《中国艾滋病诊疗指南(2021年版)》HIV诊断标准[4];②符合美国疾病预防控制中心修正的NS实验室诊断标准[5],包括1项梅毒血清学试验阳性和脑脊液性病研究实验室试验(venereal disease research laboratory test,VDRL)阳性;若脑脊液VDRL试验阴性,但有不明原因的脑脊液蛋白升高(>0.45 g/L)和(或)白细胞升高(>5 /mm3),以及原因未明的NS临床症状和体征。
排除标准:合并其他中枢神经系统感染,如合并隐球菌性脑膜脑炎、颅内结核等。
1.2 MRI检查方法
所有患者均进行MRI检查,采用Siemens Magnetom Trio Tim MRI 3.0T扫描仪,32通道头部线圈。主要序列包括:横断面T1WI、T2WI及DWI(b=1 000),横断面 T2FLAIR序列。扫描参数为:TR 1 900 ms,TE 2.52 ms,TI 900 ms,反转角8°,视野 250 mm×250 mm,矩阵256×256,层厚1 mm。其中30例行增强扫描,对比剂为Gd-DTPA,用量0.1 mmol/kg,注射流率2.0 mL/s,行横断面、冠状面和矢状面T1WI增强扫描。
所有患者的MRI影像资料均由两位经验丰富的高年资医师进行分析讨论并得出一致结果,包括发病部位和形态、各序列信号表现和增强扫描强化表现等。MRI影像学分析标准如下:①脑梗死,明确梗死部位、数目及病变范围,范围分为局限性病变和弥漫性病变;②脑炎,明确病变发生的部位、数目和范围;③脑萎缩,结合患者年龄,确定有无脑萎缩改变,并明确萎缩部位;④脑血管分析,明确是否存在狭窄血管,以及狭窄血管数目和严重程度。根据TP侵犯部位及临床表现不同,将NS分为无症状型、脑膜型、脑膜血管型、脑实质型和树胶肿型五个类型。
1.3 统计学分析
采用SPSS 23.0软件对数据进行录入与分析,计量资料以均数与标准差表示,计数治疗以例数与百分比表示,对纳入患者的主要临床症状、病灶分布位置、MRI结果等进行描述性分析。
2 结果
2.1 一般情况
根据纳排标准,最终纳入32例AIDS合并NS患者,均为男性,年龄范围为23~82岁,平均年龄34.8岁,均为性传播感染。32例患者中,6例梅毒感染在先、5例HIV感染在先,其余病例感染的顺序无法确定。32例患者的临床表现见表1。对所有患者行梅毒螺旋体特异性抗体检测(TPHA)和快速血浆反应素试验(RPR),结果均为阳性。脑脊液检测结果显示,TPHA阳性32例,VDRL和RPR阳性各31例;32例患者脑脊液白细胞数升高,以淋巴细胞为主,范围为(8~236)×106/L;蛋白含量增高(0.56~1.85 g/L);糖和氯均正常。所有患者经抗梅毒治疗后均有好转。
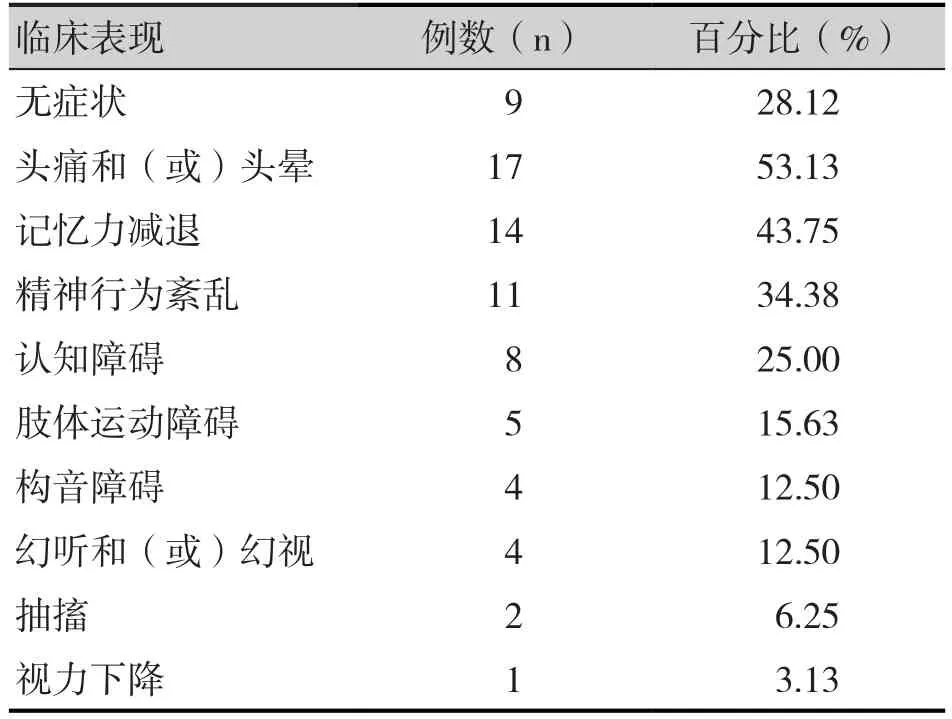
表1 32例AIDS合并NS患者的临床表现Table 1. Clinical characteristics of the 32 AIDS patients with neurosyphilis
2.2 MRI检查结果
32例患者共发现29处病灶,分布情况为颞叶7例(24.14%)、基底节6例(20.69%)、额叶6例(20.69%)、顶叶3例(10.34%)、枕叶3例(10.34%)、半卵圆中心2例(6.90%)、脑萎缩2例(6.90%)。临床分型包括无症状型9例(28.12%)、脑膜型2例(6.25%)、脑膜血管型5例(15.62%)、脑实质型15例(46.88%)和树胶肿型1例(3.13%)。
脑膜型主要表现为脑膜增厚,增强扫描呈脑回样或局限性线样强化。脑膜血管型和脑实质型均可见脑梗死,表现为脑内单发或多发的局灶性或弥漫性脑梗死灶,T1WI呈等或低信号,T2WI呈稍高或高信号,DWI呈高信号(图1)。5例脑膜血管型病例均未见明确的脑血管受累表现。脑实质型还可见脑炎和脑萎缩改变,脑炎表现为大片状脑组织肿胀,呈稍短、等或长T1、长或稍长T2信号,DWI呈等或高信号,增强扫描病灶轻度强化或明显强化;脑萎缩主要表现为脑沟、脑裂增宽、加深,脑室对称性或不对称性扩张(图2)。树胶肿型病灶位于右侧颞叶,呈结节状长T1、长T2信号,FLAIR呈高信号,增强扫描病灶不均匀强化(图3)。
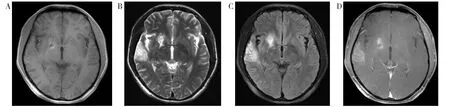
图1 脑膜血管型AIDS合并NS患者MRI影像表现Figure 1. MRI findings in meningovascular type lesions in AIDS patient with neurosyphilis
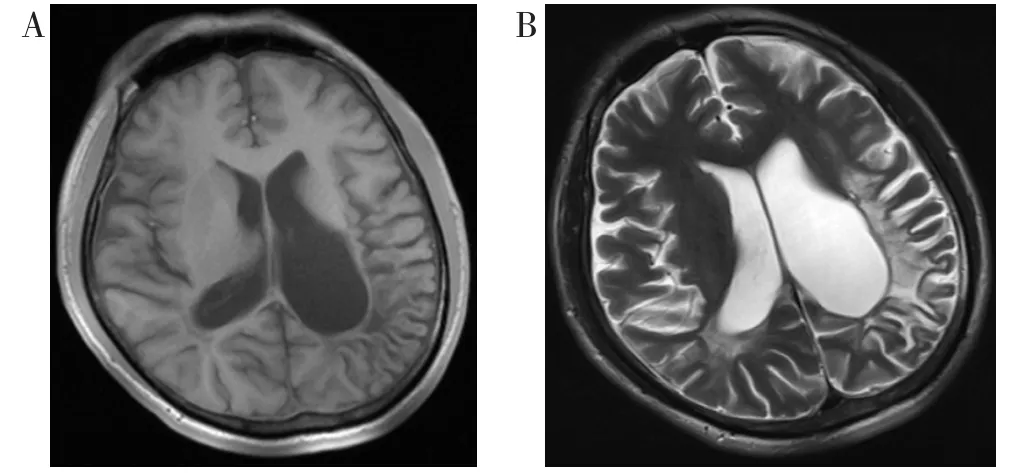
图2 脑实质型AIDS合并NS患者MRI影像表现Figure 2. MRI findings in parenchymal type lesions in AIDS patient with neurosyphilis
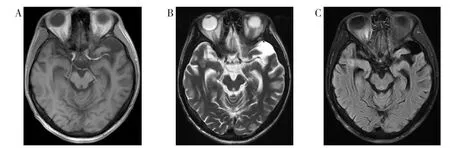
图3 树胶肿型AIDS合并NS患者MRI影像表现Figure 3. MRI findings in gumma type lesions in AIDS patient with neurosyphilis
3 讨论
研究表明,HIV感染和TP感染存在一定相互促进和协同的关系[6]。TP因HIV感染者的脑膜病变和免疫功能受抑制更易穿过血-脑脊液屏障。有研究发现在合并HIV感染的梅毒患者中NS的发生率为23.5%,显著高于未合并HIV感染的梅毒患者[7-8]。NS合并HIV感染的临床表现包括头痛头晕、共济失调、痉挛性截瘫、反应迟钝、听力丧失等,也可无任何明显症状,与未合并HIV感染的NS表现基本相似。
NS影像表现包括脑萎缩、白质病变、肉芽肿、梗死及动脉炎等,病变呈多样性,但缺乏特异性。NS病理分型往往并非独立存在,同一患者有时可同时出现多种类型。本研究32例患者中9例无症状,血清学检测均呈阳性,但无任何神经系统症状与体征,MRI检查未见明显异常。2例脑膜型,其病理改变主要为脑膜炎,且上颈段脊髓和颅神经常被累及。寇程等研究发现颅神经受累以单组受累多见[9],但也有研究报道多组颅神经同时受累的NS病例,提示NS也可引起多组颅神经受累[10-11]。脑膜型MRI影像表现为颞叶、脑膜增厚并强化。5例为脑膜血管型,该型的病理改变主要为TP造成血管损伤,最终导致脑缺血、脑梗死、脑膜炎。刘仁伟等报道,T2-FLAIR能够清晰显示脑膜血管型患者蛛网膜下腔内、软脑膜表面有含蛋白质的高信号小结节影,因此认为T2-FLAIR能有效提高MRI影像对脑膜血管型患者脑膜炎症的敏感性[12]。梅毒血管炎好发部位多在大脑中动脉、前动脉、小脑后下动脉以及脊髓前动脉供血区[13]。本研究中脑膜血管型MRI影像表现为基底节片状稍长T1、长T2信号,注射Gd-DTPA后未见强化, 伴有脑萎缩。15例为脑实质型,该型病理改变包括脑萎缩、脑室扩大、颗粒性室管膜炎等[14]。MRI影像显示病灶可位于颞叶、额叶、岛叶和胼胝体压部等,呈长T1、长T2信号。有研究表明脑实质型引起的额颞叶萎缩预示着预后不良,认为MRI影像对判断NS的预后有一定价值[15]。1例为树胶肿型,因该型可出现在病毒感染后的任何时候,被认为是NS的特异性改变,其病理改变主要为在闭塞性动脉周围炎的基础上形成的肉芽肿病变,伴有明显的微血管改变,如内膜增厚和血管周围炎症,与其他类型肉芽肿性病变有较明显的区别[16-17]。MRI影像表现为长T1长T2信号,增强扫描病灶呈结节状或环形强化。
HIV合并梅毒感染的患者需与HIV脑炎、结核性脑膜炎、单纯疱疹病毒性脑炎等疾病进行鉴别。HIV脑炎是AIDS最常见的神经系统并发症,临床表现与NS相似,影像表现亦无特异性[18],因此临床及影像表现多难以鉴别。结核性脑膜炎多于疾病早期发生在颅底,脑膜强化主要聚集于鞍上池。脑膜型NS脑室扩张,增强扫描可见脑膜线状强化。单纯疱疹病毒性脑炎起病急,常由一侧受累进展为双侧受累,发病起始部位多位于颞叶内侧并逐渐向额叶和边缘系统扩展。皮质和皮质下可出现广泛的水肿和出血点,增强扫描呈线样或脑回样强化。NS的发病过程较单纯疱疹病毒性脑炎慢,常表现为颞叶轻度萎缩伴颞角,脑实质型NS在T2WI上颞叶内侧出现异常高信号,是其特征性表现之一[19-21]。结合实验室检查和影像表现有助于二者鉴别。
综上,AIDS合并NS的临床及影像表现复杂多样,MRI检查不仅有助于本病的早期发现和诊断,还有助于临床分型,但仍需同时结合临床特征、实验室检查等综合分析,且需注意与相关疾病进行鉴别以达到早期诊断的目的。
