CT 定量指标对肺部磨玻璃结节病理侵袭性的预测价值
2022-06-23孙雅苹张娟
孙雅苹,张娟
1 天津市北辰区中医医院影像科 (天津 300400);2 北京市海淀医院健康管理中心(北京 100080)
磨玻璃结节(ground glass nodules,GGNs)作为肺部CT检查的重要影像学征象,在CT肺窗上表现为边界模糊的“云雾状”密度增高影,但病灶内的支气管和血管纹理仍可较好识别。依据结节病灶内是否有实性成分,GGNs可分为纯磨玻璃结节(pure ground glass nodules,pGGNs)和混合磨玻璃结节(mixed ground glass nodules,mGGNs)。持续存在的GGNs经随访被证实为恶性的风险会明显增加,需引起高度重视。肺部GGNs囊括了侵袭前期病变[不典型腺瘤样增生(atypical adenomatous hyperplasia,AAH)、肺原位腺癌(adenocarcinoma in situ ,AIS)]、微浸润腺癌(microinvasive adenocarcinoma,MIA)和浸润肺腺癌(invasive lung adenocarcinoma,IAC)三类,不同病理阶段的外科术式处理和预后状况存在差异,因此准确评估预测GGNs的病理侵袭性对充分了解病情、选择合适的治疗方式和预后评估尤为重要[1]。本研究旨在回顾性分析并探讨CT定量指标预测肺部GGNs病理侵袭性的应用价值,现报道如下。
1 资料和方法
1.1 一般资料
本研究为单中心回顾性分析研究,共收集2019年10月至2021年10月于天津市北辰区中医医院诊治的180例肺部GGNs 患者的临床资料和影像学资料,按照下列筛选标准筛查后共入组156例患者,剔除26例。纳入标准:临床资料和影像学资料保留完整;CT 影像学资料中有1 mm 薄层的高分辨力CT平扫图像;肺部孤立性GGNs。排除标准:相关资料残缺;CT 影像学图像质量较差;合并肺部其他病变。
156例肺部GGNs患者,男89例,女67例;年龄30~85岁,中位年龄55岁,平均年龄(54.93±8.47)岁。依据组织病理学诊断结果,将156例患者分为未浸润组(71例)和浸润组(85例)。未浸润组包括AAH、AIS各29、42例,浸润组包括MIA、IAC各46、39例。本研究得到天津市北辰区中医医院医学伦理委员会批准。
1.2 CT 影像学检查
采用Siemens 双源螺旋CT 扫描机进行胸部扫描,嘱受检者取仰卧体位,双上肢自然上举至头顶,于呼气末屏气后开始扫描,扫描范围为肺尖至肺底部。扫描参数如下:管电压120 kV,自适用调控技术设置管电流,扫描层厚5 mm,螺距0.9。采用高分辨力重建算法对图像重组,层厚和层间距均为1 mm。图像分析参数如下:肺窗窗宽1 500 HU,窗位-450 HU;纵隔窗窗宽400 HU,窗位40 HU。所得薄层图像以DICOM 格式传送至CT 后处理工作站,逐层手动勾画GGNs 的轮廓并利用工作站自带的分析软件进行CT 定量分析。
1.3 观察指标
收集未浸润组和浸润组的一般资料;由2名不知晓本研究和病理结果的影像科医师共同阅片,交流并确认GGNs 勾画位置准确,确保勾画区域避开支气管、血管或钙化层面;然后测量肺部GGNs 的最大横截面直径、面积、体积和CT 测量值,其中CT 测量值包括最大CT 值、最小CT 值、平均CT 值及与周围正常肺组织的CT 差值。上述CT 定量指标由2名医师各测量1次,取2次测量值的平均值记录。
1.4 统计学处理
采用SPSS 23.0统计软件进行数据分析,计数资料以率表示,采用χ2检验;计量资料首先进行levene 法和Kolmogorov-Smirnov(K-S) 法检验,满足正态分布和方差齐性的计量资料以±s表示,采用t检验,不满足正态分布的计量资料则用M(P25,P75)]表示,采用秩和检验;采用二元Logistic回归分析肺部GGNs 侵袭性的影响因素,并绘制ROC 曲线分析CT 定量指标对肺部GGNs 侵袭性的预测价值,用约登指数(youden index,YI)确定最佳截断值,曲线下面积(area under the curve,AUC)>0.7表示预测价值为良;P<0.05为差异有统计学意义。
2 结果
2.1 两组一般资料和CT 定量指标比较
两组肺部GGNs 的最大CT 值、平均CT 值和CT 差值比较,差异均有统计学意义(P<0.05);两组一般资料和其他CT 定量指标比较,差异均无统计学意义(P>0.05),见表1。
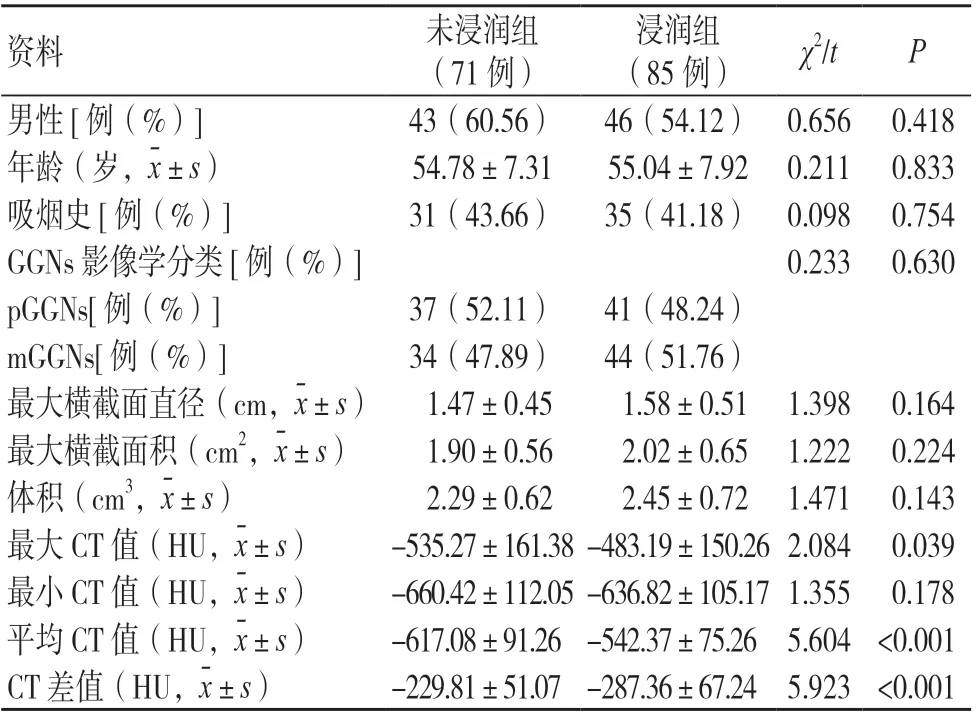
表1 两组一般资料和CT 定量指标比较
将肺部GGNs 的侵袭性作为因变量(1=浸润,0=未浸润),表1中P<0.05的指标(最大CT 值、平均CT 值和CT 差值)作为自变量,Logistic回归分析显示,平均CT 值、CT 差值是肺部GGNs 侵袭性的独立影响因素(P<0.05),而最大CT 值与肺部GGNs 的侵袭性无明显相关(P>0.05),见表2。
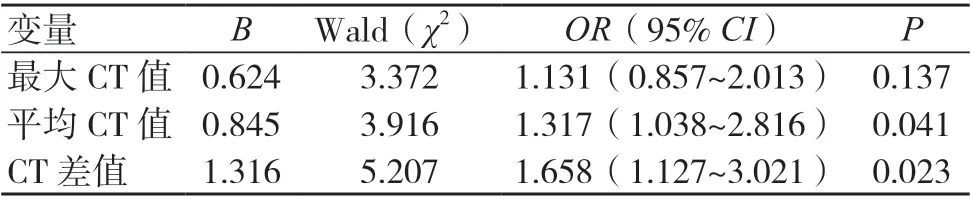
表2 肺部GGNs 侵袭性的影响因素分析
2.2 CT 定量指标预测肺部GGNs 侵袭性的ROC 曲线分析
由表2可知,肺部GGNs 的平均CT 值、CT 差值与侵袭性明显相关,故将两者作为检验变量,绘制两者单独及联合预测肺部GGNs 侵袭性的ROC曲线。状态变量:1=浸润(MIA+IAC),0=未浸润(AAH+AIS)。ROC 曲线分析显示,平均CT 值、CT 差值预测肺部GGNs 侵袭性的AUC 均>0.7,差异无统计学意义(Z=0.412,P>0.05);两者联合预测的AUC 明显大于平均CT 值单独预测,差异有统计学意义(Z=2.738,P<0.05),且联合预测的灵敏度和特异度分别为85.88%、80.28%,见图1、表3。

表3 平均CT 值、CT 差值对肺部GGNs 侵袭性的预测价值
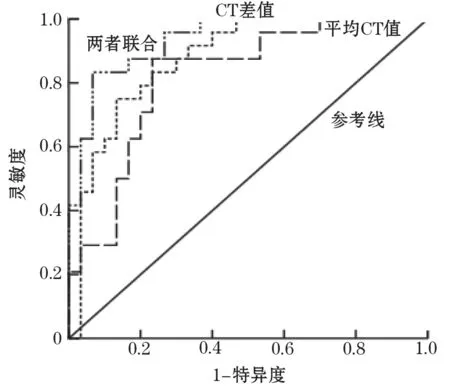
图1 平均CT 值、CT 差值预测肺部GGNs 侵袭性的ROC 曲线
3 讨论
随着CT 设备的完善和技术经验的积累,高分辨力CT 在肺癌高危人群的筛查诊断中得到广泛应用,加之人们对疾病的筛查意识增强,使得肺部GGNs 的检出率明显提高。肺部GGNs 可见于肺部良性病变和恶性病变,其良恶性判断需要定期复查胸部CT,以尽早发现恶性征兆,对于持续存在的肺部GGNs 需高度警惕恶性病变的可能。结合肿瘤生长进展的规律特点(AAH-AIS-MIA-ICA)以及不同病理阶段临床应对策略的差异性,准确评估肺部GGNs 的病理侵袭性尤为重要。既往依据肉眼观察肺部GGNs 的CT 影像学形态进行病理分级诊断,存在一定的困难和主观性,准确度偏低[2-3]。CT 定量指标可客观量化反映结节的影像学特征,尤其适合随访观察结节的变化特点,故CT 定量指标为临床预测结节的病理侵袭性提供了新的途径[4]。
本研究将入选病例分成浸润组(MIA+ICA)和未浸润组(AAH+AIS),借助高分辨力CT 测量了系列CT 定量指标,其中肺部GGNs 的最大横截面直径、最大横截面积和体积均为常规CT 定量指标,本研究未发现两组上述指标存在差异(P>0.05)。这与张宏等[5]和周围等[6]的报道相符,原因主要与结节形态的不规则性和不均匀生长有关。但结合临床实际来看,结节的大小虽然不能作为病理侵袭性的参考,但随访中若发现结节继续生长增加,尤其是体积倍增时间(volume doubling time,VDT)缩短,需怀疑结节恶性和发生浸润的可能[7]。基于CT值的密度测量是评估肺部GGNs 病理侵袭性的重要手段,随着肿瘤生长和浸润程度加重,结节内实性成分增加,CT 上可见结节密度增高,CT 值也随之增高,因此mGGNs 的恶性倾向相对较大。本研究结果显示,浸润组最大CT 值、平均CT 值均明显高于未浸润组(P<0.05),与其他研究[8-9]结论相符,也较好地说明了肺部GGNs 病理侵袭性和CT密度值之间的紧密联系。本研究创新性采用CT 差值这一指标,CT 差值可客观反映结节和周围肺组织的CT 密度差,进而反映出病灶生长浸润的肿瘤学信息[10]。本研究结果显示,浸润组和未浸润组的CT 差值也存在显著差异(P<0.05),且Logistic回归分析和ROC 曲线分析发现,平均CT 值和CT 差值是肺部GGNs 病理侵袭性的独立影响因素,两者最佳截断值分别为-571.38、-260.47 HU 时,此时AUC分别为0.819、0.875,且两者联合预测效能最大,AUC为0.935,为判断肺部GGNs 的病理侵袭性提供了阈值参考。
综上所述,肺部GGNs 的CT 定量指标可客观量化反映结节的内部情况,平均CT 值和CT 差值可作为预测其病理侵袭性的有效CT 定量指标,且两者联合预测价值更高。
