伊沙佐米治疗多发性骨髓瘤的疗效及其在SDF1/CXCR4轴机制的研究
2022-06-22路晓辉
路晓辉
多发性骨髓瘤(MM)是因骨髓内浆细胞发生克隆性异常增殖而引发的一种血液系统恶性肿瘤,患者多表现为感染、骨痛、贫血等症状,临床尚无完全治愈的手段,只能通过药物对症状进行完全或者部分缓解[1]。在过去一定时间内,临床主要采用硼替佐米等蛋白酶体抑制剂对患者化疗,其可以提高患者的无进展生存期,但化疗后患者复发概率较高,一旦复发患者很难再承受后续治疗,且易对药物产生耐药性,加大了后续治疗的难度,因此寻找一种疗效更好的药物对临床治疗具有积极的意义[2]。伊沙佐米是近年来治疗肿瘤的一线新药物,具有较强的抗肿瘤活性和浆细胞清除能力,于2018年被批准用于多发性骨髓瘤的治疗,但在我国其仍处于初期应用阶段[3]。基质细胞衍生因子(SDF)-1、趋化因子受体(CXCR)4是骨髓微环境的一类重要因子,可通过下调其表达来降低多发性骨髓瘤细胞增殖与转移。本研究通过探讨伊沙佐米治疗多发性骨髓瘤的疗效、SDF1/CXCR4轴机制和不良反应情况,为临床治疗提供依据。
1.资料与方法
1.1 一般资料 本研究选取2019年1月至2021年1月我院收治的多发性骨髓瘤患者68例为研究对象。纳入标准:①符合多发性骨髓瘤的相关诊断标准,且经病理诊断证实;②在本次治疗前至少接受过1种治疗方案,且产生耐药性。排除标准:①合并其他恶性肿瘤者;②伴有精神系统疾病者;③对本研究所用药物过敏者;④合并先天性血液疾病或免疫系统患者。本次研究经过本院医学伦理委员会同意。因医学伦理、科研经费的限制,本研究采用非随机化研究,为减少偏倚,在选择好伊沙佐米组之后根据伊沙佐米组个体的特征来选择对照组。对照组30例,其中男性18例,女性12例;年龄62~76岁,平均(63.71±1.33)岁;病程3个月~3年,平均(1.57±0.78)年;Durie-Salmon分期:Ⅰ期2例,Ⅱ期19例,Ⅲ期9例。伊沙佐米组38例,其中男性21例,女性17例;年龄60~75岁,平均(63.38±1.51)岁;病程3个月~4年,平均(1.64±0.67)年;Durie-Salmon分期:Ⅰ期4例,Ⅱ期23例,Ⅲ期11例。两组患者一般资料比较差异无统计学意义(P>0.05)。
1.2 治疗方法 对照组患者给予常规治疗,具体治疗方法为:4周为1个疗程,共治疗3个疗程,分别给予盐酸表柔比星(厂家:瀚晖制药有限公司,国药准字:H19990280,规格:10mg),静脉滴注,15mg/m2,d1-4;硫酸长春地辛(厂家:扬子江药业集团有限公司,国药准字:H20046421,规格:1mg),静脉滴注,0.8mg/m2,d1-4;地塞米松磷酸钠(厂家:天津金耀药业有限公司,国药准字H12020515,规格:1ml:5mg),静脉滴注,40mg/d,d1-4,d9-12,d17-20。伊沙佐米组患者在疗程第1、8、15天时,每周1次,每次口服枸橼酸伊沙佐米胶囊4mg(厂家:Takeda Pharma A/S,国药准字:H20180010,规格:4mg*1粒*3板/盒);第1~21天口服来那度胺胶囊25mg(厂家:Celgene International Sarl,国药准字:H20130070,规格:10mg);第1、2、8、9、15、16、22、23天口服地塞米松片20mg(厂家:广东华南药业集团有限公司,国药准字:H44024469;规格:0.75mg),28天为一个疗程,共治疗3个疗程。
1.3 观察指标 ①疗效:3个疗程完成后,对两组患者进行免疫球蛋白水平检测,根据检测结果评价两组患者的治疗疗效,血清或者尿液中免疫球蛋白水平检测阴性,骨髓中浆细胞减少不小于80%或者降至5%记为完全缓解(CR);血清或者尿液免疫球蛋白水平减少不小于90%,且1天内免疫球蛋白水平小于100mg记为非常好的部分缓解(VGPR);血清或者尿液免疫球蛋白水平减少不小于50%,且1天内免疫球蛋白水平小于200mg记为部分缓解(PR);血清或者尿液免疫球蛋白水平减少小于50%记为微小缓解(MR);治疗前后血清或者尿液免疫球蛋白平无变化记为疾病稳定(SD);治疗前后血清或者尿液免疫球蛋白水平增加记为疾病进展(PD)。疾病缓解率为CR、VGPR以及PR之和。②两组外周血SDF-1/CXCR4变化:分别在患者治疗前、治疗3个疗程后,取空腹静脉血3ml,采用BCA试剂盒进行血清蛋白含量测定,并以10μg作SDS-PAGE凝胶电泳,将蛋白分离为清晰条带,转印至NC膜,封闭90min后作一抗孵育SDF-1、CXCR4,4℃孵育过夜。清洗后再作二抗孵育,暗室显影。③不良反应:统计两组患者在治疗过程中发生的不良反应。

2.结果
2.1 两组患者3个疗程后的疗效比较 与对照组比较,伊沙佐米组患者疾病缓解率明显升高(P<0.05)。见表1。
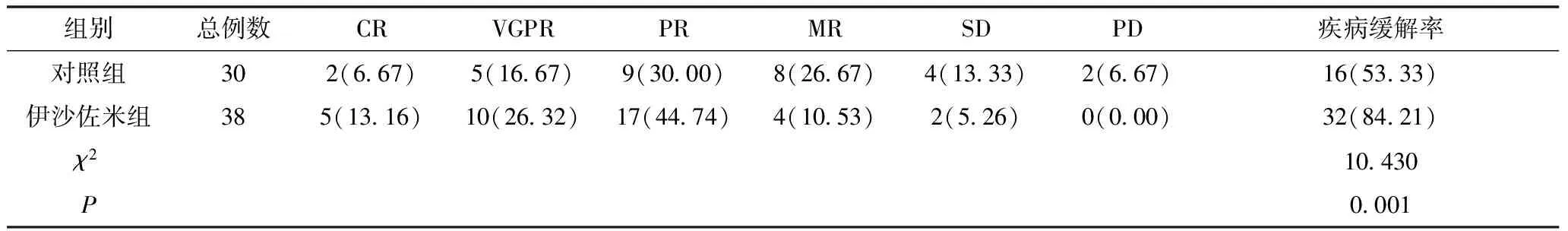
表1 两组患者3个疗程后的疗效比较 单位:例(%)
2.2 两组血清SDF-1、CXCR4比较 治疗3个疗程后,伊沙佐米组患者血清SDF-1、CXCR4水平明显降低,且显著低于对照组(P<0.05),详见表2。
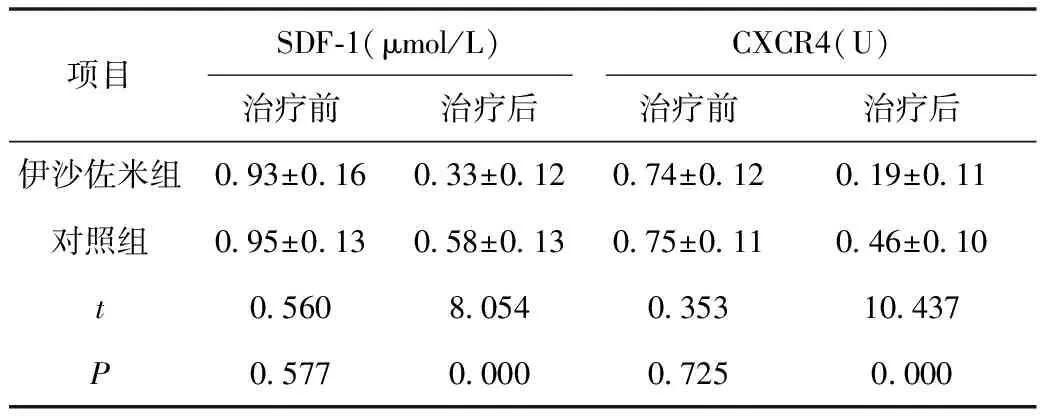
表2 两组血清SDF-1、CXCR4比较
2.3 两组患者不良反应情况 与对照组比较,伊沙佐米组感染、周围神经病变、Ⅲ级以上血液学毒性等不良反应发生率明显降低(P<0.05),而两者患者在消化道反应、乏力、心血管系统等的不良反应发生率比较差异无统计学意义(P>0.05),见表3。
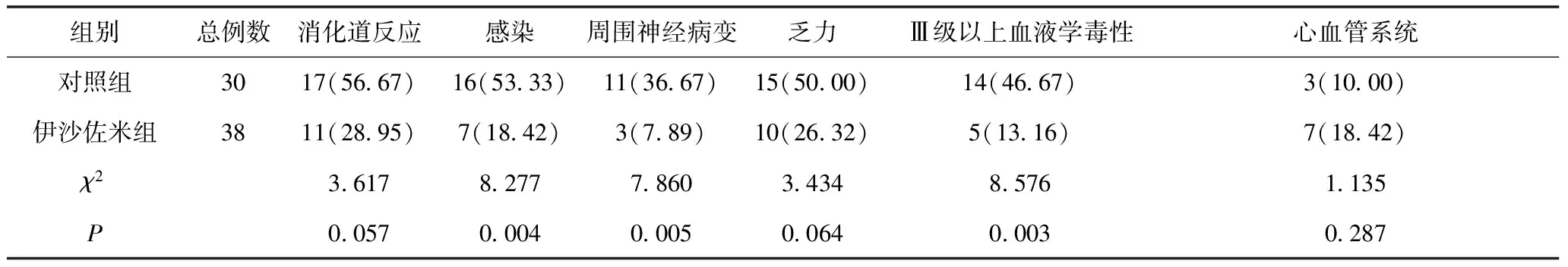
表3 两组患者不良反应情况比较 单位:例(%)
3.讨论
多发性骨髓瘤主要组织特征表现为免疫球蛋白或其片段(M蛋白)不断进行单克隆合成,并沉积于相关器官或组织内,从而对器官或组织造成损伤,因此阻止免疫球蛋白或其片段的合成是治疗多发性骨髓瘤的关键[4,5]。本研究中,以治疗前后血清或者尿液中免疫球蛋白的减少量进行疗效判定,与对照组比较,伊沙佐米组患者疾病缓解率明显升高(P<0.05),说明伊沙佐米可以有效阻止多发性骨髓瘤患者体内免疫球蛋白的合成,从而改善其沉积现象。伊沙佐米是全球首个口服用药进入临床的一类蛋白酶体抑制剂,是一种人工合成的硼酸二肽化合物,可以特异性、不可逆地抑制真核细胞中免疫球蛋白合成所需的蛋白酶体活性,从而降低免疫球蛋白或其片段的合成,进而通过多种机制使骨髓细胞增殖停留或者凋亡,起到杀死骨髓细胞的作用[6,7]。与第1代蛋白酶体抑制剂相比,新型药物伊沙佐米药物解离20S蛋白酶体的半衰期较短,解离速率亦明显比一代硼替佐米快约6倍,而更持久结合引起药物在机体循环中滞留,影响药物的抑制肿瘤活性作用。另外本研究结果显示,伊沙佐米组感染、周围神经病变、Ⅲ级以上血液学毒性等不良反应发生率明显降低,说明伊沙佐米可以降低多发性骨髓瘤患者并发症的发生概率。伊沙佐米可以通过所有类型的组织,并可以快速地被广泛代谢,肽酶代谢和环氧化物水解是其主要代谢途径,这就使得其在药物不良反应上具有较大的优势,可以迅速降解为对人体无害的物质存在于体内发挥作用,因此相比常规药物其不良反应明显降低。但有研究显示[8,9],伊沙佐米为不可逆的抑制剂,可能引发持续的氧化应激反应和内皮功能障碍,导致患者心脏毒性和心血管副作用,因此应密切关注患者心血管系统并发症的发生。本研究结果显示,虽然伊沙佐米组有7例患者发生了心血管系统相关并发症,高于对照组的心血管系统发生率,但两组比较并无差异,说明接受伊沙佐米治疗的患者心血管系统并发症发生率在可控范围内。
SDF-1最初是在小鼠骨髓基质细胞中发现的一类细胞因子,后经实验研究证实其由基质细胞分泌。SDF-1受体有CXCR4、CXCR7两种,由于目前医学界对CXCR7参与的SDF-1/CXCR7轴认识尚在初期阶段。而SDF-1/CXCR4轴已被临床研究及实验证实参与了多种肿瘤病灶增殖与转移。孙小英等在结直肠癌肝脏转移瘤动物模型实验中发现SDF-1、CXCR4可能参与结肠癌肝转移,且与SDF-1诱导癌症病灶细胞增殖、迁移有一定联系。SDF-1/CXCR4在多发性骨髓瘤细胞中大量表达,参与多发性骨髓瘤归巢以及病灶的迁移,使多发性骨髓瘤癌细胞大量克隆,骨髓组织中进而大量生成新生血管,也是多发性骨髓瘤微环境形成以及基质作用的关键调节剂[10]。这种骨髓微环境变化使多发性骨髓瘤细胞大量克隆,为多发性骨髓瘤治疗带来巨大挑战。SDF-1和CXCR4存在于多发性骨髓瘤发展各个阶段,且随疾病严重程度明显升高。目前,多发性骨髓瘤的治疗多是针对瘤细胞增殖提出抑制治疗方案,很少对骨髓瘤微环境进行治疗研究,故多发性骨髓瘤复发率极高,死亡率明显增加。通过抑制SDF-1和CXCR4表达,来抑制多发性骨髓瘤瘤细胞克隆以及转移,能够为多发性骨髓瘤提供新的治疗策略。本研究中伊沙佐米组患者在使用伊沙佐米治疗后血清SDF-1和CXCR4表达明显下降,说明伊沙佐米能改善多发性骨髓瘤患者体内微环境,抑制瘤细胞转移以及增殖克隆。
综上所述,伊沙佐米治疗多发性骨髓瘤患者可以提高疗效,提升疾病缓解率,同时可以降低感染、周围神经病变、血液学毒性等不良反应的发生,安全性较好。值得注意的是,本研究并未对伊沙佐米发挥疗效的机制进行分析,在以后的研究中需通过动物实验对相关机制进行探讨,以为伊沙佐米的治疗提供更加广泛的临床依据。
