不同载体负载的Ni基加氢催化剂对生物油加氢裂化制备芳香烃的影响研究
2022-06-22于泰莅蔡勤杰张素平
于泰莅,蔡勤杰,张素平
(华东理工大学 资源与环境工程学院,上海 200237)
0 引言
生物质农林废弃物资源化利用的一种重要方式是制取有价值的化学品[1]。木质纤维素类生物质快速热解制得的生物油是一种富氧的有机液体混合物。粗制的生物油燃料品质较差,需要通过精制过程来提升其燃料品质[2]。基于酸性分子筛催化剂的催化裂化技术能够实现生物油向芳香烃的转变,但原始生物油具有富氧缺氢的缺点,导致其裂化过程中存在脱氧效率低和催化剂易结焦失活的问题[3]。因此,有研究者提出了温和加氢-催化裂化的两段式转化过程[4],[5]。在整个转化过程中,生物油组分首先通过温和加氢提高其饱和度,随后用于催化裂化,从而提高脱氧效率并有效缓解催化剂结焦问题。
对于温和加氢-催化裂化的两段式转化过程,筛选合适的温和加氢催化剂非常关键。在生物油的主要成分中,酚类既是比醛类和酮类更难加氢的物质,又是裂化过程中极易导致催化剂失活的物质,少量的酚类掺混就能导致裂化催化剂的快速失活[6]~[8]。因此,实现高效的酚类加氢是加氢过程中的一个重要目标。Ni是一种很有发展潜力的廉价金属催化剂,当Ni负载在酸性载体上时具有较高的酚类加氢效率[9]。但是,催化剂酸性的加强也可能强化一些气化和结焦等副反应。目前,针对Ni/酸性载体催化剂的研究重点主要放在酸性载体对酚类加氢效率的提高优化以及相关机理阐述上[10],较少关注其可能引发的气化和结焦等副反应对于生物油复杂混合物体系的影响,对加氢预处理过程中气化和结焦等副反应与后续提质过程的关系更是缺乏研究。
因此,本文以生物油水相为原料,以Ni/氧化物为加氢催化剂,HZSM-5为裂化催化剂,研究两段式的生物油加氢裂化过程。在反应过程中添加甲醇作为协同反应物进行供氢,与加氢预处理起到联合供氢的作用。本文的研究目的在于理解两段式生物油加氢裂化过程中,当以Ni/氧化物作为加氢催化剂时,其酸性对于加氢阶段的加氢饱和、裂解气化以及缩合结焦等反应的催化作用,以及上述催化作用对于下游的催化裂化过程的综合影响。此外,本文考察了两种甲醇掺混比例的影响,目的在于深入理解Ni/氧化物催化加氢和甲醇供氢在整体生物油供氢上的加和关系,从而探索低甲醇掺混比例条件(即低成本)下的生物油水相有效提质途径。
1 实验部分
1.1 原料
将生物油水相与甲醇掺混的混合物(包括两个掺混质量比,分别为1∶1和2∶1)作为原料。生物油水相通过稻壳热解制得的生物油加水进行萃取获得,水油质量比为0.8。生物油水相的含水量为71.5%,相应的有机质含量为28.5%。通过气相色谱-质谱联用分析仪(GC-MS)对生物油水相的族类化合物的相对含量进行分析,可得酸类、酮类、醛类、酚类、糖类和其他的相对含量分别为26.7%,27.5%,7.9%,16.9%,13.2%和7.8%。根据各族类化合物的组成,选择乙酸作为酸类的代表化合物,羟基丙酮作为醛酮类的代表化合物,苯酚和邻苯二酚作为酚类的代表化合物,监测它们的加氢转化效率。
甲醇(分析纯)购于上海泰坦化学,硝酸镍(分析纯)购于国药集团化学试剂,HZSM-5(Si/Al=25)购于南开大学分子筛厂,纳米二氧化锆(99.9%)、纳米二氧化硅(99.5%)、二氧化铈(99.5%)和三氧化二铝(99.9%)均购于阿拉丁试剂。
1.2 催化剂制备方法
加氢阶段的Ni基催化剂(Ni/ZrO2,Ni/CeO2,Ni/Al2O3和Ni/SiO2)通过等体积浸渍法进行制备,Ni的负载量均为15%,具体方法在我们过去的研究中已有详细介绍[5]。裂化阶段使用的催化剂为HZSM-5(Si/Al=25),反应前在500℃下活化2 h。
1.3 催化剂表征方法
Ni基催化剂的NH3-TPD表征在AutochemⅡ2920化学吸附仪上进行:样品首先在550℃下预处理2 h,然后冷却至100℃,此时注入足量的NH3并在样品表面完成吸附;在100℃条件下,样品由He气流进行冲刷,以移除气相和物理吸附的NH3;最后,将样品从100℃以10℃/min的升温速率升至600℃,在升温过程中用热导检测器(TCD)监测NH3的脱附情况。
1.4 反应测试
本文采用的固定床反应系统如图1所示。该反应系统包含两个相连的管式反应器,可以实现单段的加氢和连续式的两段加氢共裂化反应。当进行加氢共裂化反应时,两个管式反应器串联,反应在100 mL/min的H2气氛下进行,压力为4 MPa。加氢段的催化剂为Ni基催化剂,裂化段的催化剂为HZSM-5,催化剂的装填量均为2 g。加氢段的反应温度为250℃,裂化段的反应温度为400℃,反应压力为4 MPa,反应物的质量空速恒定为2 h-1。加氢和加氢共裂化的反应时间均为6 h。为了监测加氢共裂化反应过程的稳定性,每1.5 h进行液体取样,计算油相产物的产率并分析组成。
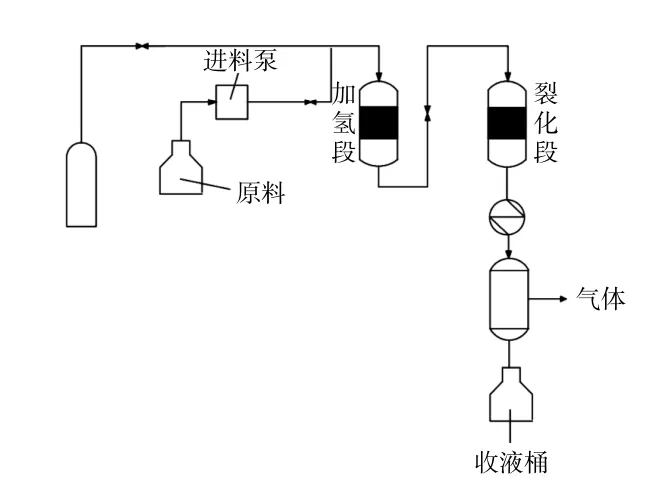
图1 固定床反应装置Fig.1 Fixed bed reactor
1 .5 产物分析
加氢反应得到的液体产物为均相,而加氢共裂化得到的是分层的水相和油相。使用Agilent 6820型气相色谱仪(GC)对加氢液体产物和原始生物油水相进行分析,色谱柱型号为HP-5,对其中的代表性族类化合物及其对应加氢产物通过外标法进行定量。GC程序:40℃下保持5 min,然后以8℃/min的升温速率升至240℃,在240℃下保持10 min。使用Clarus 500型气相色谱与质谱联用仪(GC-MS)对原始生物油水相、加氢反应得到的液体产物和加氢裂化得到的油相产物进行分析,色谱柱型号为DB-WAX,通过峰面积归一法测定其中各族类化合物的相对含量。升温程序:40℃下保持5 min,然后以8℃/min的升温速率升至240℃,在240℃下保持20 min。通过华爱9580型气相色谱仪(GC)对气体产物COx和C1-C4进行分析,毛细管柱型号为HP-AL/KCL,通过外标法进行定量,以10℃/min的升温速率将GC柱箱的温度从50℃升高到150℃。
在反应过程中形成了不同形式的固体产物:一部分固体产物沉积在加氢反应器的入口和管壁上,定义为焦;一部分含碳沉积物形成在加氢催化剂表面,定义为加氢催化积炭;一部分含碳沉积物形成在裂化催化剂表面,定义为裂化催化积炭。通过热重法对反应后的加氢催化剂和裂化催化剂表面的积炭量进行测定,以计算相应的产率。
2 结果与讨论
2.1 催化剂表征
通过NH3-TPD表征得到4种Ni基催化剂的弱、中、强酸性位的酸量如表1所示。
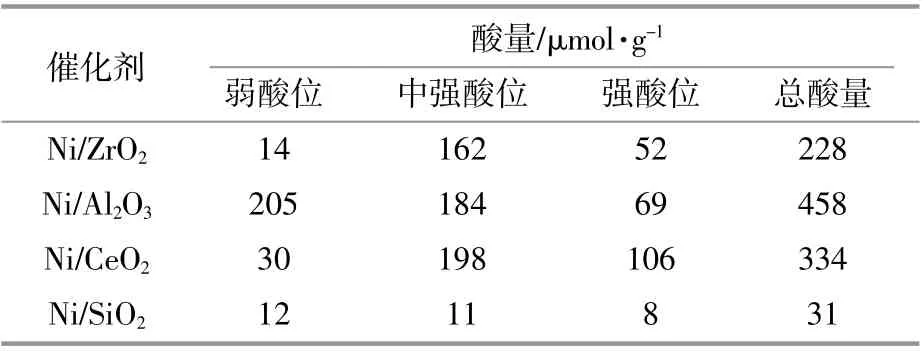
表1 4种Ni基催化剂的酸性Table 1 Acidity of four Ni-based catalysts
由表1可以看出:Ni/Al2O3的总酸量最大,其弱酸位酸量要远多于其他几种催化剂;Ni/SiO2的酸性非常弱;Ni/CeO2的强酸位酸量最多。Mortensen P M也观察到了类似的现象,他发现Ni/CeO2具有一定量的强酸位,且数量多于Ni/Al2O3和Ni/ZrO2[9]。
2.2 加氢反应
生物油水相和甲醇催化加氢的产物产率如表2所示。HT-Ni/SiO2表示以Ni/SiO2为加氢催化剂的加氢反应过程,以此类推。由表2可以看出:对于两个掺混比工况(1∶1和2∶1),以Ni/SiO2作为催化剂时,具有最高的液体产物产率,分别约为91.6%和92.2%;而使用Ni/ZrO2和Ni/CeO2作为催化剂时,液体产物产率有所降低,分别约为84.5%,85.3%和83.4%,78.2%;Ni/Al2O3作为催化剂时,液体产物产率最低,分别约为72.8%和74.2%。

表2 加氢产物产率Table 2 Hydrogenation product yield%
在气体产物产率方面,Ni/Al2O3作为催化剂时,气体产率最高;Ni/ZrO2和Ni/CeO2作为催化剂时,也有一定量的气体产物生成;而Ni/SiO2作为催化剂时,气体生成量较少。气体产物主要是一些饱和气态烃和COx,其主要来自加氢裂解过程。将Ni/SiO2和Ni/金属氧化物(金属氧化物为ZrO2,CeO2和Al2O3)的加氢结果进行对比后可以发现,只有金属Ni存在时,气化反应强度较弱;金属氧化物的引入大大强化了加氢阶段的气化反应,表明Ni和金属氧化物的酸性位对裂解气化反应起到了协同促进作用[11]。以Ni/Al2O3作为催化剂时,气化反应强度要明显高于Ni/ZrO2和Ni/CeO2作为催化剂时,其主要原因可能是Ni/Al2O3具有更高的总酸量,使它具有更多的发生裂解反应的活性中心。
在加氢阶段也发现一定量含碳沉积物的生成。这些含碳沉积物通常是复杂的含氧有机化合物,它们是不饱和含氧化合物发生多次缩合反应后形成的产物。以Ni/金属氧化物作为催化剂时,形成的含碳沉积物的量明显多于Ni/SiO2作为催化剂时,这主要是因为金属氧化物上的酸性位能够促进缩合积炭反应[9]。实验中观察到,相比于Ni/ZrO2和Ni/Al2O3,Ni/CeO2上具有更明显的结焦趋势;在掺混比为2∶1的工况下,以Ni/CeO2作为催化剂时,加氢反应末期的压力升高至4.08 MPa,说明反应器逐渐开始堵塞,而其他催化剂作用下的反应压力无明显变化。这可能是因为Ni/CeO2具有更多的强酸性位,这些强酸性位能够对含碳沉积物的形成起到更为显著的促进作用[12]。
监测的4种代表性化合物(乙酸、羟基丙酮、苯酚和邻苯二酚)及其对应的加氢产物(乙醇、1,2-丙二醇,环己醇和1,2-环己二醇)的含量如图2所示。在加氢阶段希望发生的是不饱和化合物的加氢饱和反应,因为它能产生适用于后续裂化过程的醇类化合物。在实验中观察到,在所有Ni基催化剂的作用下,醛酮类化合物的加氢活性都很高,从而形成醇类化合物,这主要与金属Ni具有较强的催化羰基加氢的能力有关[13]。乙酸的对应加氢产物—乙醇的生成量始终很低,可能是因为酯化反应是酸类的主要转化路径[14],且酸类也可能发生结焦和气化反应[15]。
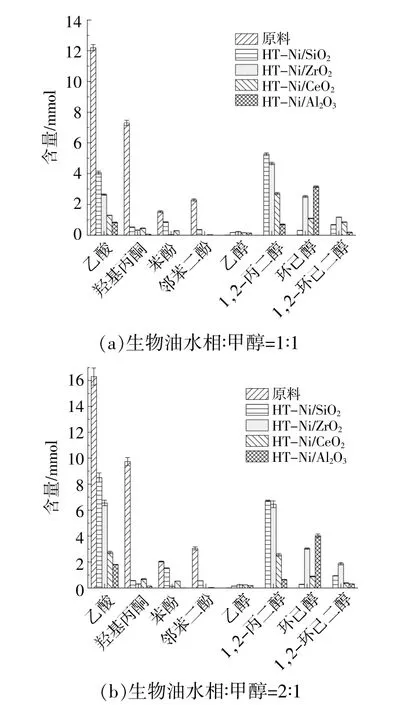
图2 代表性化合物及其加氢产物在加氢反应前后的量Fig.2 The amount of representative compounds and their hydrogenated products before and after the hydrogenation reaction
由图2可知:邻苯二酚在4种催化剂作用下的转化率均较高;以Ni/金属氧化物为催化剂时,苯酚转化率要明显高于以Ni/SiO2作为催化剂时,特别是以Ni/ZrO2和Ni/Al2O3作为催化剂时,苯酚转化率接近100%。从对应的加氢产物上看,当生物油水相∶甲醇=1∶1,以Ni/SiO2作为催化剂时,加氢生成的环己醇和环己二醇的量十分有限。Mortensen P M发现,金属氧化物中的配位不饱和金属位点(表现为酸性位)对于苯酚的O-H解离具有重要促进作用,并促使苯环活化,从而与Ni上H2解离得到的吸附氢发生反应[9]。因此,Ni和金属氧化物两种活性中心的协同作用显著促进了酚类的加氢反应。
图3为加氢反应前后族类化合物的相对含量。从图3可以看出,液体产物中仍含有较多的酚类,说明加氢反应过程可能发生了形成其他酚类衍生物的副反应。从醇类的总生成量来看,以Ni/ZrO2和Ni/Al2O3作为催化剂时,两种酚类的加氢效率都很高;而以Ni/CeO2作为催化剂时,酚类的加氢效率要低于前两者,特别是在掺混比为2∶1的工况下,酚类加氢的效率显著下降,这也反映了催化剂表面积炭和反应器堵塞对酚类加氢的消极影响。
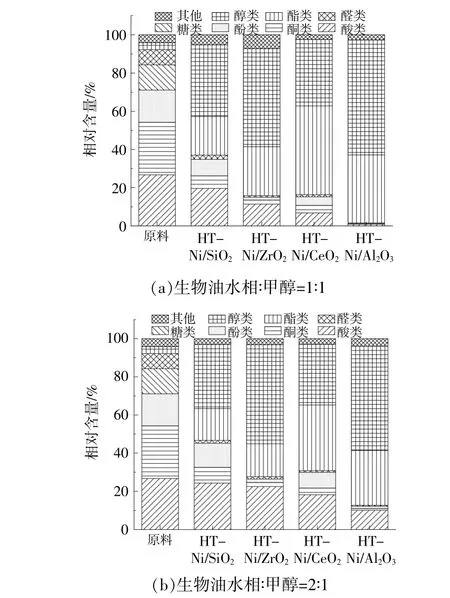
图3 加氢反应前后族类化合物的相对含量Fig.3 Relative content of chemical families before and after hydrogenation reaction
2.3 加氢共裂化反应
本文在研究加氢反应的基础上开展了加氢共裂化反应的研究,加氢共裂化反应的产物产率如表3所示。HC-Ni/SiO2表示以Ni/SiO2为加氢催化剂的加氢共裂化过程,以此类推。由表3可以看出:当生物油水相和甲醇的掺混比为1∶1时,HCNi/SiO2的油相产率与HC-Ni/ZrO2相当;而当生物油水相和甲醇的掺混比为2∶1时,HC-Ni/SiO2的油相产率甚至要低于HC-Ni/ZrO2。结合HC-Ni/ZrO2裂化催化剂表面的积炭形成量可以推断,HC-Ni/SiO2的裂化催化剂活性存在下降趋势,且在掺混比为2∶1时更为严重。HC-Ni/Al2O3的油相产率始终低于HC-Ni/ZrO2,这反映了加氢阶段的过度气化作用对于两段加氢裂化过程的不利影响。HC-Ni/CeO2的油相产率也始终低于HC-Ni/ZrO2,且在掺混比为2∶1时更为严重,这也反映出加氢阶段较强的结焦反应对油相产物生成和维持反应稳定的消极影响。

表3 加氢共裂化的产物产率Table 3 Hydrocracking product yield%
根据前面的产物产率,推断出在一些工况下裂化催化剂出现了失活。为了证明这一推断,对油相产物产率和组成进行了连续测试,结果如图4,5所示。其中,油相产物中脂肪烃含量(所有工况下均小于3%)未在图中标出。
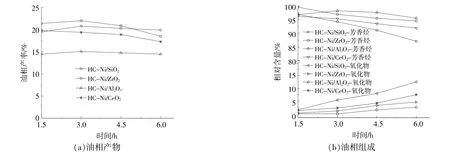
图4 生物油水相∶甲醇=1∶1时,加氢共裂化的油相产率和组成的连续监测结果Fig.4 Bio-oil water phase∶methanol=1∶1,continuous monitoring results of oil phase yield and composition of hydrocracking
从图4可以看出,HC-Ni/SiO2反应后期的油相产物产率出现了一定程度的下降,并伴随着油相产物中酚类等含氧化合物含量的提升,随着反应进行,HC-Ni/CeO2油相产物产率和品质也有一定程度的下降。
从图5可以看出:HC-Ni/SiO2和HC-Ni/CeO2油相产物产率和品质的下降趋势更为明显;HCNi/ZrO2和HC-Ni/Al2O3的反应稳定性较好,油相产物产率分别保持在20%和13%左右,且油相产物中的芳香烃(主要包括甲苯、二甲苯、三甲苯和甲基乙基苯等)含量始终在95%以上。
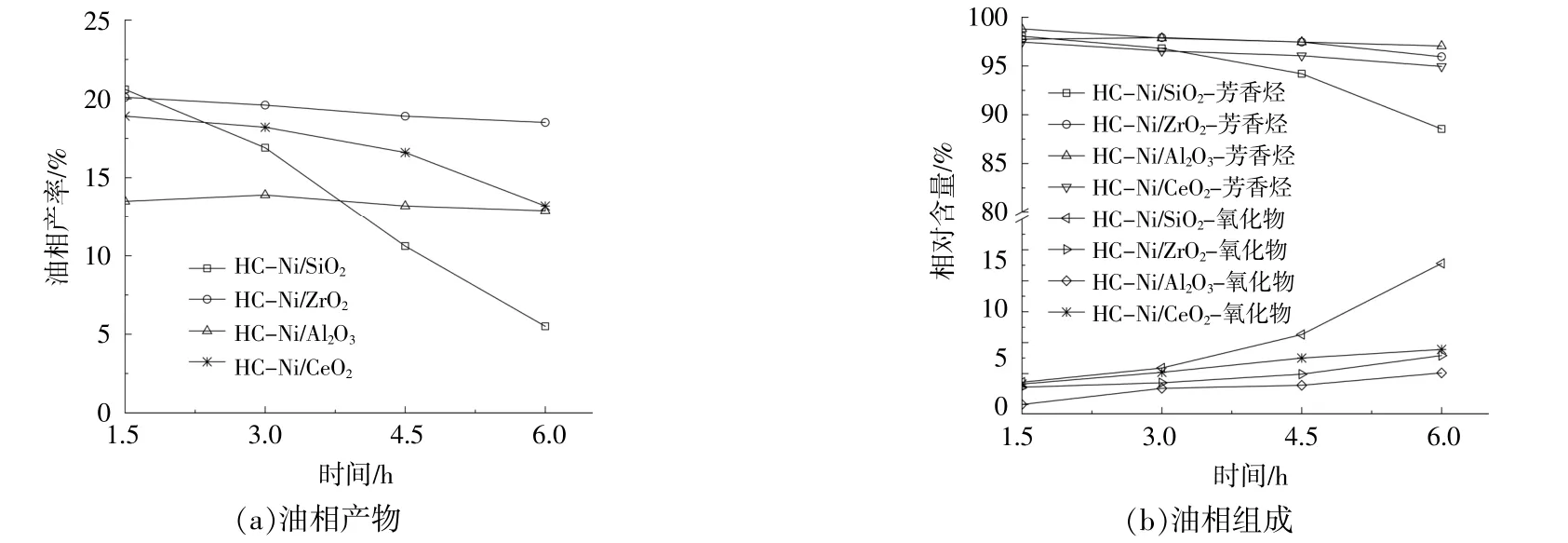
图5 生物油水相∶甲醇=2∶1时,加氢共裂化的油相产率和组成的连续监测结果Fig.5 Bio-oil water phase∶methanol=2∶1,continuous monitoring results of oil phase yield and composition of hydrocracking
我们从加氢段出口的化合物的转化行为出发,重点关注由不同加氢催化剂导致的加氢产物分布对后续裂化过程产物分布的影响,结果如图6所示。

图6 加氢催化剂对加氢产物以及裂化产物分布的影响Fig.6 The effect of hydrogenation catalyst on the distribution of hydrogenation products and cracking products
对于不饱和的化合物,如酸类、酯类和酚类,由于其富氧缺氢的特性,使其在裂化过程易发生不完全脱氧形成含氧副产物,同时易在裂化催化剂表面形成含碳沉积物。在这些化合物中,酚类极易导致催化剂失活。而富氢的醇类,在这里包括图中所示的加氢反应生成的环醇、链醇以及外加的甲醇,其自身转化为芳烃过程中生成的富余氢可借助氢转移作用促进不饱和化合物的脱氧转化[2]。同时,我们过去的研究也证实,加氢反应生成的醇类的供氢量是不足的,即外加甲醇是必需的。相关机理可以解释本文的实验结果:当生物油水相与甲醇的掺混比为1∶1时,对酚类加氢效果较差的HC-Ni/SiO2仍保持了相对较高的裂化催化剂活性,这得益于较多的外加甲醇弥补了加氢段的酚类加氢不足;而随着生物油水相与甲醇的掺混比提高至2∶1,不饱和化合物量(特别是酚类)增多,而外加甲醇量变少,整体的需氢和供氢的平衡被破坏,不仅导致了含氧副产物的生成,同时形成的含碳沉积物会导致催化剂活性的下降速度大大加快。而对于Ni/金属氧化物催化剂,特别是Ni/ZrO2和Ni/Al2O3,由于Ni和载体酸中心的协同作用促进了酚类的加氢转化,在减少需氢化合物的同时增加了供氢源,使得其能在高掺混比的条件下(2∶1)达到供氢与需氢的平衡,脱氧效率得到了较好的保持,能够稳定生成目标产物芳香烃。
加氢阶段的气体产物(包括C1-C4的烷烃和COx)在HZSM-5催化剂上的反应活性很低,其对芳香烃的形成几乎没有贡献。因此,加氢阶段的气化反应是一种不利的碳损失,这也导致了加氢阶段气化反应更强的HC-Ni/Al2O3的油相产率要始终低于HC-Ni/ZrO2。由于这些气化反应是由Ni和载体酸性位联合主导的,因此,过多的加氢催化剂的载体酸性位数量反而不利于整体加氢共裂化过程中目标产物芳香烃的形成。
加氢阶段形成的固体产物(包括焦和加氢催化剂表面的积炭)并没有进入裂化阶段,因此它也是一种碳损失。此外,加氢催化剂表面积炭的大量形成还会造成更加恶劣的结果,如掺混比为2∶1的工况下,HC-Ni/CeO2催化过程中,较多积炭形成后覆盖催化剂的活性位,不仅会降低加氢反应效率,还会强化积炭的进一步生成,最终导致反应器堵塞。结合前面加氢过程的讨论可知,Ni/金属氧化物上过多的强酸性位也会对加氢共裂化过程造成消极的影响。
综上可知,Ni/ZrO2是适用于低甲醇掺混比工况的加氢共裂化过程的加氢催化剂。这是因为Ni/ZrO2具有合适的酸性位量,能够在确保酚类高效加氢转化的基础上,尽可能地削弱加氢阶段的气化和结焦等副反应,从而提高整体过程的目标产物芳香烃产率。
3 结论
本文对生物油水相与甲醇加氢共裂化制取液体芳香烃的过程进行研究,重点考察了Ni基加氢催化剂的影响。研究发现,载体的不同会影响Ni基催化剂的酸性。Ni/SiO2的酸性很弱,使得金属Ni成为唯一的加氢活性中心,导致酚类物质的加氢转化效果较差;当生物油水相与甲醇的掺混比为2∶1时,Ni/SiO2出现了快速失活,反应过程的油相产物产率约为13.4%。
当以金属氧化物为Ni的载体时,载体上的酸性位能够与金属Ni发生协同作用而促进酚类物质的转化,使其适用于低甲醇掺混比的加氢裂化过程。Ni/Al2O3的加氢气化作用较强,导致了一定量的碳损失而降低了目标产物芳香烃的产率,当生物油水相与甲醇的掺混比为2∶1时,最终的气体产率约为15.7%,油相产物产率约为13.4%。Ni/CeO2具有较多的强酸位,这导致在该催化剂上的结焦反应较强;当生物油水相与甲醇的掺混比为2∶1时,最终油相产物产率约为16.2%,加氢阶段的焦产率约为2.3%,不仅造成了碳损失,还会导致加氢催化剂失活和反应器堵塞。Ni/ZrO2被认为是最适用于低甲醇掺混比工况的加氢裂化过程的加氢催化剂,在其作用下,酚类的加氢效率较高,气化和结焦等副反应相对较弱,所得的油相产物产率为20%左右,油相产物中的芳香烃含量在95%以上。
