信迪利单抗联合仑伐替尼二线治疗不可切除肝细胞肝癌的临床疗效及安全性
2022-06-21王俊洁徐龙袁国盛许晓明周晓元罗润齐
王俊洁 徐龙 袁国盛 许晓明 周晓元 罗润齐
1广州医科大学附属第二医院感染科(广州 510260);2南方医科大学南方医院感染科(广州 510515)
原发性肝癌(hepatocelular carcinoma,HCC)是目前我国第4 位常见恶性肿瘤及第2 位肿瘤致死病因,对我国人民的生命和健康造成了严重威胁[1]。原发性肝癌中75% ~85% 为肝细胞癌(以下简称肝癌),具有起病隐匿、进展迅速、高度侵袭性和高复发率等特点。大多数肝癌患者确诊时已是中晚期,丧失了根治机会。分子靶向药物是近年治疗中晚期肝细胞癌的方法之一,其中索拉非尼(sorafenib)[2]和仑伐替尼(lenvatinib)[3]是目前被推荐为一线治疗的靶向药物。然而,单用靶向药物治疗中晚期HCC 的客观反应率较低[4],临床上亟需更为有效的治疗选择。
近十年来,陆续有研究发现,以程序性死亡受体-1/死亡受体配体-1(programmed cell death proteinligand 1,PD-L1)为代表的免疫检查点抑制剂在肿瘤治疗方面具有显著成效[5]。但直至2018年中旬,PD-1 抑制剂Opdivo(纳武利尤单抗)和Keytruda(帕博利珠单抗)才在我国上市,由于价格昂贵而极大限制了临床应用。随着我国首个具有国际品牌的PD-1 抑制剂的研发上市,信迪利单抗将成为晚期肝癌患者可及的治疗选择之一。然而,既往研究报道发现,单用PD-1 抑制剂治疗晚期HCC 患者的客观缓解率(objective response rate,ORR)低于20%[6-8]。仑伐替尼作为一种多靶点酪氨酸激酶抑制剂,可通过抑制肿瘤微环境的血管及免疫抑制[9-10],与PD-1 抑制剂起协同增效作用。自此,PD-1/PD-L1 抑制剂联合靶向治疗开始成为新的研究热点。
目前,我国关于PD-1 抑制剂联合仑伐替尼在肝癌治疗中的研究较少。本研究对使用国产PD-1抑制剂信迪利单抗联合仑伐替尼二线治疗不可切除肝细胞肝癌患者的临床数据进行回顾性分析,初步探索两药联合治疗方案在我国肝癌人群中的疗效及安全性。
1 对象与方法
1.1 研究对象 回顾性收集2019年2月至2021年12月在广州医科大学附属第二医院、南方医科大学南方医院共两家单位收治的采用信迪利单抗联合仑伐替尼及仑伐替尼单药治疗不可切除肝细胞肝癌患者的临床资料,进行电话随访并收集病例资料。
1.2 病例纳入与排除标准 患者在接受治疗前已被充分告知临床获益及不良反应。纳入标准:(1)依照《原发性肝癌诊疗规范(2019年版)》[11]确诊为HCC;(2)参照巴塞罗那(BCLC)临床肝癌分期体系属于中晚期(B/C 期);(3)Child-Pugh 分级为A 级或者B 级;(4)在使用标准一线方案治疗期间,疾病出现进展,改为信迪利单抗联合仑伐替尼作为二线治疗方案;(5)ECOG 评分低于2 分;(6)依照mRECIST 评价标准,影像学表现为可见到一个以上可测量病灶,用于实体瘤评价;(7)临床资料完整。排除标准:(1)存在其他类型的原发性恶性肿瘤;(2)联用其他具有抗肿瘤作用的药物;(3)合并严重的基础性疾病,如严重肾功能不全、严重心功能不全、重度感染等;(4)30 d 内接受大手术或出现消化道出血者;(5)难以控制的高血压;(6)妊娠。见图1。
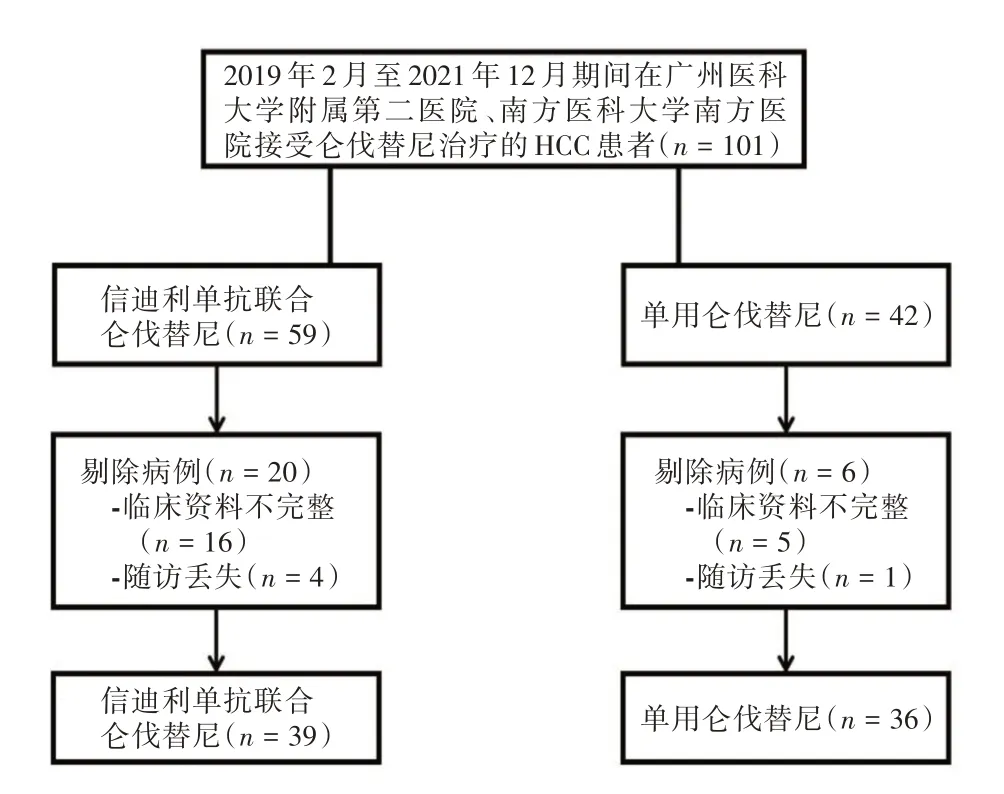
图1 患者筛选流程图Fig.1 Flow chart of patient screening
1.3 给药方法 根据患者体质量予以仑伐替尼(乐卫玛,日本卫材(Eisai)公司生产),对于体质量<60 kg的患者,本品推荐日剂量为8 mg(2 粒4 mg 胶囊),每日一次;对于体质量≥60 kg 的患者,本品推荐日剂量为12 mg(3 粒4 mg 胶囊),每日一次。信迪利单抗(达伯舒,信达生物制药(苏州)有限公司生产),200 mg,每3 周给一次。
1.4 观察指标与疗效评估 每6 ~8 周复查血常规、肝功能、肾功能、凝血功能等指标及甲胎蛋白(AFP)、上腹部增强电子计算机断层扫描(CT)/增强磁共振成像(MRI),随访截止时间为2022年1月31日。(1)根据mRECIST 标准[12],以肿瘤增强显影范围评价肿瘤的控制情况:①完全缓解(complete response,CR):所有靶病灶均未见动脉期增强;②部分缓解(partial response,PR):靶病灶增强扫描动脉期的直径总和减少超过30% ;③疾病进展(progressive disease,PD):靶病灶增强扫描动脉期,直径比原始水平至少增大20%,或出现新发病灶;④疾病稳定(stable disease,SD):靶病灶的缩小程度既未达到PR 标准,增大程度也未达到PD 标准。(2)客观缓解率(objective response rate,ORR)=(CR+PR)(/CR+PR+SD+PD)×100%。(3)疾病控制率(disease control rate,DCR)=(CR+PR+SD)(/CR+PR+SD+PD)×100% 。(4)无疾病进展(progressionfree survival,PFS)时间是指患者从治疗开始直到肿瘤出现进展或随访丢失或死亡的时间。(5)生存期(overall survival,OS)是指患者从治疗开始直到末次随访或死亡的时间。(6)不良反应评价:根据常见不良反应事件评价标准(CTCAE 5.0)将不良反应分为1 至5 级。治疗期间严密观察患者的生命体征、血常规、肝功能、肾功能、尿常规、大便常规等指标,出院后通过电话、微信及门诊复查等多种方式进行。及时评价并记录其他不良反应。
1.5 统计学方法 应用SPSS 25.0统计软件处理数据,正态分布计量资料用均数±标准差表示,比较采用t检验,计数资料用例(%)表示,比较采用χ2检验;非正态分布资料用M(P25,P75)表示,两组间比较采用曼-惠特尼U检验;采用Kaplan-Meier 法绘制相应生存曲线。P<0.05为差异有统计学意义。
2 结果
2.1 一般资料 随访截止时,本项研究共纳入患者75 例,其中男性57 例,女性18 例;年龄28 ~77 岁,平均(50.2 ± 5.7)岁;Child-Pugh 分级,A 级51 例(68%),B 级24 例(32%);BCLC 分期,B 期25 例(33.3%),C 期50 例(66.7%),两组基线资料比较差异无统计学意义。见表1。
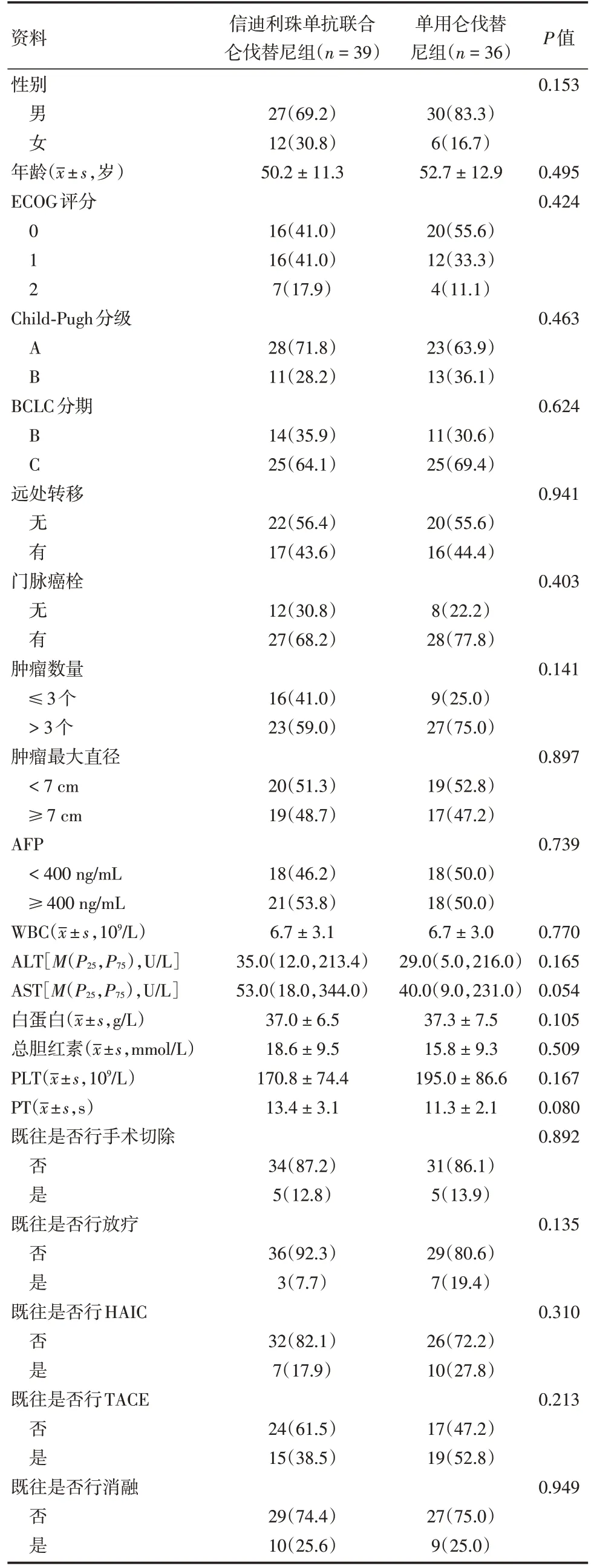
表1 两组患者的基线特征分析Tab.1 Baseline characteristics of two groups 例(%)
2.2 患者肿瘤控制情况 两组患者均无病例获得CR。39 例患者接受信迪利单抗联合仑伐替尼治疗后,15 例(38.4%)例获得PR,14 例(35.9%)获得SD,10例(25.8%)进展;ORR为38.5%;DCR为74.4%。36 例患者单用仑伐替尼治疗后,6 例(16.7%)例获得PR,14 例(35.8%)获得SD,10 例(25.8%)进展;ORR 为38.5%;DCR 为74.4%。见表2。
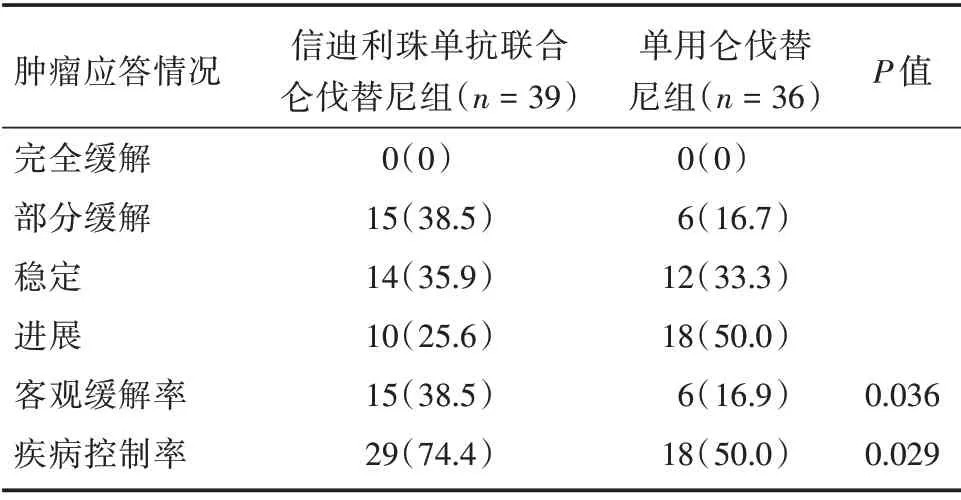
表2 两组患者接受治疗后的mRESIST 评价结果Tab.2 MRESIST evaluation results of two groupsafter therapy例(%)
2.3 生存曲线分析 联合治疗组中位PFS 时间为9.1 个月(95%CI:7.5 ~10.7),仑伐替尼单药组中位PFS 时间为5.9 个月(95%CI:4.7 ~7.1);两组PFS比较差异有统计学意义(P<0.001),见图2。联合治疗组中位OS 时间为18.4 个月(95%CI:16.5 ~20.3),仑伐替尼单药组中位OS 时间为11.6 个月(95% CI:7.2 ~16.0);两组间OS 比较差异有统计学意义(P=0.016),见图3。
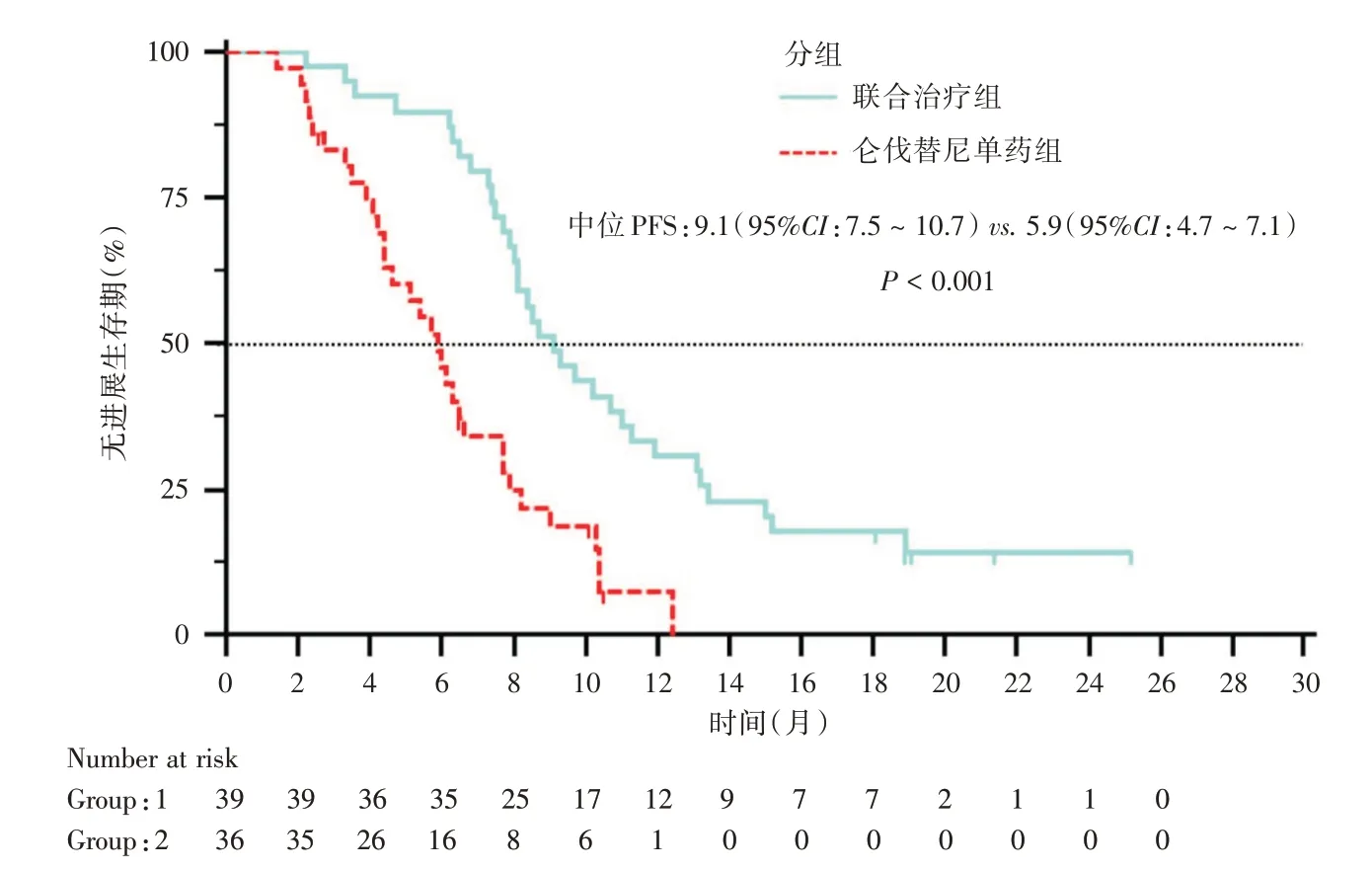
图2 两组患者接受治疗后的无疾病进展时间分析Fig.2 Disease-free time of two groupsafter therapy
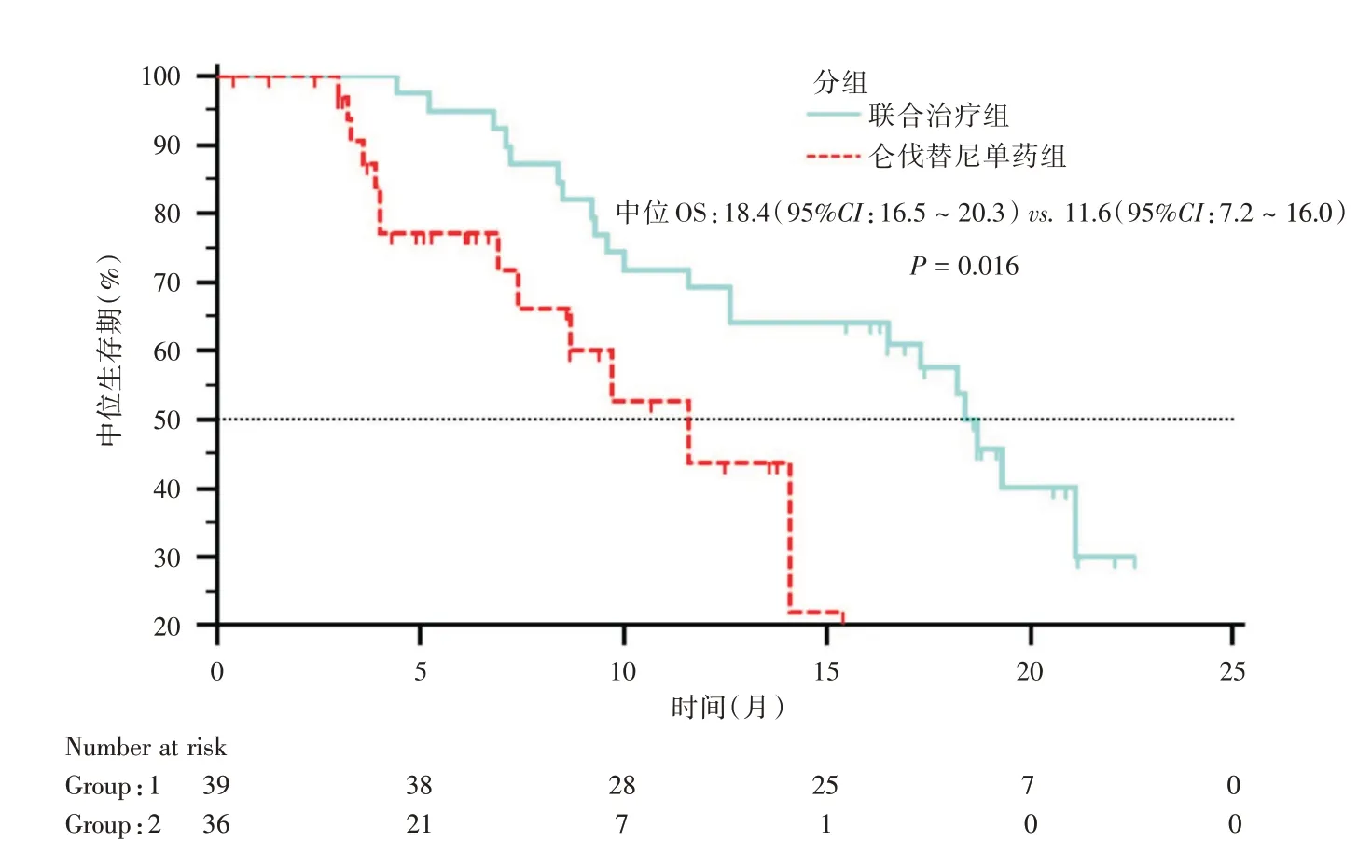
图3 两组患者接受治疗后的生存曲线分析Fig.3 Survival curve analysis of two groupsafter therapy
2.4 不良反应 随访截止时,发生率超过10%的不良事件及≥3 级的不良事件见表3。上述不良反应均得到有效控制。两组间不良反应发生率差异无统计学意义。
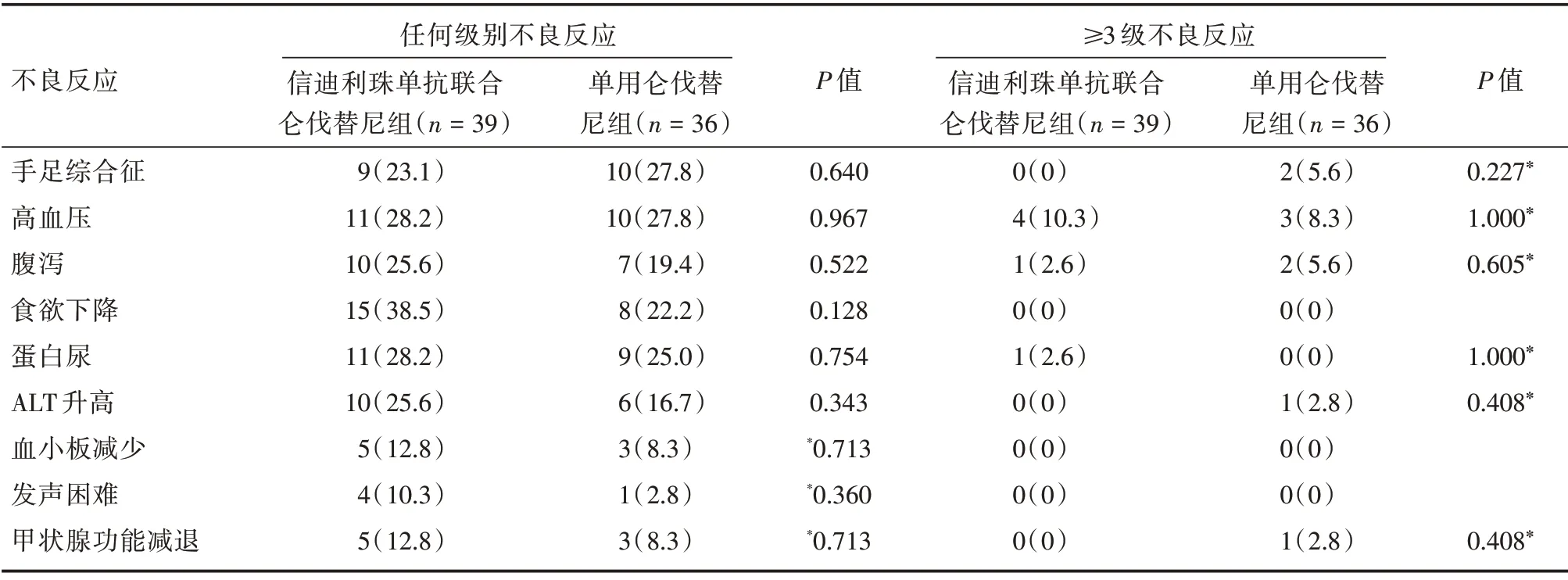
表3 两组患者随访过程中的不良事件分析Tab.3 Adverse events of two groups during follow-up 例(%)
3 讨论
研究结果发现[13],目前我国仅有不到30%的HCC 患者能够被及早发现、诊断和并获得治疗,提示多数患者在确诊时已处于疾病中晚期,无法得到根治机会。以往,对于不可切除的HCC 患者的一线治疗药物仅有索拉非尼,但该药不良反应较多,且肿瘤应答率低,无法显著提高乙型肝炎病毒(hepatitis B virus,HBV)阳性相关肝癌患者的总生存率[14]。而在中国,HBV 慢性感染是HCC 的主要发病原因。近年来,仑伐替尼(lenvatinib)对于HBV相关的HCC 取得了良好的疗效[3]。2018年8月仑伐替尼被推荐用于不可切除HCC 的一线治疗,为晚期肝癌患者带来了新的希望。
以免疫检查点抑制剂为代表的肿瘤免疫治疗已成为继手术、化疗、放疗和靶向治疗后的第五大肿瘤治疗手段[15],其中PD-1 抑制剂相关研究进展迅速,陆续在多种恶性肿瘤的治疗领域大放异彩。KEY-NOTE224 研究[16]表明,PD-1 抑制剂帕博利珠单抗治疗晚期肝癌的ORR 达17%,DCR 可达61%。虽然PD-1 抑制剂给肝癌治疗带来了新的希望,但临床效果有限。抗血管内皮生长因子/血管内皮生长因子受体治疗可减弱肿瘤微环境中的免疫抑制,与PD-1 抑制剂具备协同增效作用。前期临床研究[10]证实,仑伐替尼联合帕博利珠单抗治疗晚期肝癌的DCR 可达85%,仑伐替尼联合帕博利珠单抗的Ⅲ期临床试验(LEAP-002)正在进行中。近期,我国有学者[17-19]研究了7 例接受信迪利单抗联合仑伐替尼治疗的晚期肝癌患者,结果提示PR 4 例,SD 1 例,PD 2 例。由于样本量较小,且基线资料不匹配,无法进行统计学比较。
联合免疫治疗为晚期肝癌患者带来临床获益,也展示良好的安全性。本研究回顾性分析了两家单位共39 例信迪利单抗联合仑伐替尼、36 例单用仑伐替尼二线治疗不可切除肝细胞肝癌患者的初步疗效及不良反应,结果表明相较于单用仑伐替尼,信迪利单抗联合仑伐替尼治疗可提高患者无疾病进展时间及中位OS 时间。
与仑伐替尼单药组比较,本项研究中并无患者死于信迪利单抗联合仑伐替尼联合治疗相关的严重不良反应,最常见的药物相关不良反应包括食欲下降、高血压、蛋白尿、ALT 升高、腹泻、手足综合征等,与既往研究类似[20]。大多数不良反应为1 ~2 级,通过减少剂量或者对症治疗可减少毒性作用产生。
综上,本研究初步显示对于二线治疗不可切除肝细胞肝癌患者,信迪利单抗联合仑伐替尼具有较好的疗效和安全性,但因是回顾性研究、样本量小、随访时间短,期待更多的探索性研究,随着研究的深入,信迪利单抗联合仑伐替尼将在晚期原发性肝癌中展现更为广阔的治疗前景,肝癌患者总生存率及生存质量将不断提升。
