漫射光相关断层成像在乳腺肿瘤检测中的应用
2022-06-15耿晓濛张晓娟桂志国
耿晓濛, 张晓娟, 桂志国, 尚 禹
(中北大学 信息与通信工程学院, 山西 太原 030051)
0 引 言
乳腺癌发病率位居女性恶性肿瘤之首, 按照发展阶段分为Ⅰ级~Ⅳ级, 其中晚期乳腺癌(Ⅲ级和Ⅳ级)的致死率很高[1]. 乳腺肿瘤的早期诊断有助于降低疾病风险. 目前, 临床上乳腺肿瘤的影像学诊断方法主要有四类: 第一类是乳腺彩色超声影像, 通过肿瘤与健康组织的软硬度差异进行诊断, 不容易区分初期肿瘤, 诊断结果存在主观性[2]; 第二类是磁共振影像, 可以检测到离散的多灶肿瘤, 然而该方法敏感度过高, 导致特异性不足[3]; 第三类是乳腺钼靶, 与磁共振相反, 该方法特异性高, 但敏感性欠缺[4], 并且具有放射性; 第四类是乳腺热成像, 热度信号大多来自乳腺表面, 不易探测组织深层[5].
乳腺肿瘤表现有微血管无规则增生、 局部血氧代谢病态旺盛、 血流量异常升高等. 因此, 准确的微血管血流状态对肿瘤的早期检测有重要价值. 但是, 临床上最常用的超声多普勒血流只能测量大血管的血流, 而乳腺肿瘤影响的是微血管的血流[6], 无法用多普勒技术测出. 此外, 灌注磁共振技术可以得到较高空间分辨率的血流影像, 但是其价格昂贵, 不易用于早期检测. 近红外漫射光断层成像技术(DCT)是一种新型的无创血流成像技术, 该技术根据光场的时间自相关函数g1(τ)与微血管系统内红细胞运动的关系来直接测量深层组织的血流信息, 具有轻便、 快速和低成本等优势, 因此发展很快, 也逐步应用于生理和临床研究中[7].
在DCT发展的早期阶段, 光源和探测器的光纤阵列是通过同一个镜片和准直系统来聚焦被测组织的表面[8]. 受镜头面积的限制, DCT技术多数在小鼠头部进行小视野成像. 随着技术的进步, 光源和探测器使用独立的聚焦镜片, 但是必须通过线形扫描的方式来实现大视野的成像, 严重地增加了测量时间, 也容易给图像带来运动伪影.
为了克服上述问题, 本文设计了阵列式光开关来分时共享光源和探测器, 在降低成本的同时实现大视野的血流成像. 此外, 通过结合迭代线性算法和Bregman-TV算法的混合算法来重建血流图像[9], 其中迭代线性算法结合了g1(τ)的积分形式与N阶泰勒多项式(称为N阶线性算法), 并充分考虑了不规则被测目标的组织异质性; Bregman-TV算法是一种混合的图像重建算法, 其中, Bregman算法为不可微方程提供了解决方案[10], TV算法可以使非边缘区域更加均匀, 同时很好地保留边缘[11]. 通过优化光源-探测器光纤在被测组织表面位置的分布, 降低了图像重建线性方程组的病态性. 在上述算法的基础上, 设计了适用于乳腺肿瘤的蒙特卡洛仿真实验[11], 从而得到在乳腺组织中的光子路径, 把光子路径嵌入至迭代线性算法和重建算法, 使得算法能够精确处理乳腺血流数据. 另外, 设计了适用于本研究的集重建、 计算、 存储于一体的自动化程序, 实现了批量处理多个病例数据.
作为初步的临床验证, 对1例肿瘤患者和1例乳腺钙化患者进行了DCT血流成像, 并进行了图像分析, 从图像特征的角度来验证DCT技术对于诊断乳腺肿瘤的有效性.
1 血流测量原理
根据近红外光测量血流的原理如图 1 所示, 激光器发出785 nm的近红外漫射光(相干长度>5 m), 经多模光纤传输进入乳腺组织, 组织内的光子在经过一系列的吸收和散射后, 最终一部分光子从距离源光纤几厘米远的组织表面逸出, 并由单模探测器光纤收集; 采集到的光子经由单模光纤被单光子探测器计数, 最终输出的光子被一个8通道数字相关器接收; 相关器对光强做自相关运算最终得到非归一化的光强时间自相关函数g2(τ), 其与光场时间自相关函数g1(τ)满足Siegert关系. 归一化的光场时间自相关函数满足扩散相关方程. 在不规则边界的条件下, 从扩散相关方程中, 通过N阶线性算法提取乳腺血流指数值(Blood Flow Index, BFI)[9].
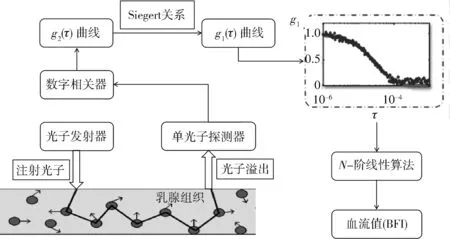
图1 血流测量原理图
2 血流提取与成像算法
N阶线性算法需要已知光子在组织内部的传输路径和能量权重, 这可以通过光子的蒙特卡罗仿真(Monte Carlo simulation, MC)获得. 利用MC仿真软件(MCVM)模拟光子在乳腺组织中的传输轨迹, 进而得到每个光源-探测器(Source-Detector, S-D)组合检测的光子能量权重和光子传输路径[12]. 适用于乳腺组织的光子MC仿真参数设置如表 1 所示.

(1)

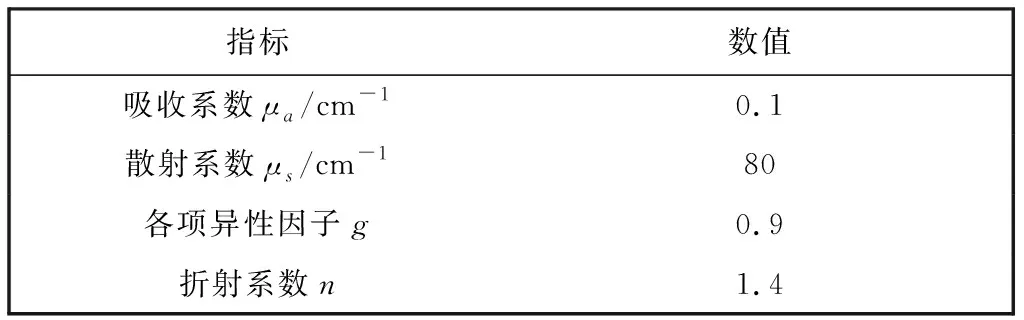
表 1 MC仿真参数设置表
自从近红外光组织测量技术发展起来后, 各个研究组开发了多种图像重建算法, 比较成熟的是解析方法和有限元方法. 但是, 解析方法要求被测组织具有简单且理想的几何特性, 显然这并不符合生物组织形状不规则的情况; 有限元方法不能充分利用采集的光子自相关数据, 带来很大的成像噪声. 本文改进的N阶线性算法与Bregman-TV混合算法可用于任意形态的生物组织, 并且能够充分利用被测数据, 提高成像质量.
利用N阶线性算法从g1(τ)曲线中精确提取血流值, 与传统的解析方法和有限元方法相比, 该算法不寻求扩散相关方程的解析解, 而是结合积分形式与N阶泰勒多项式, 通过光子轨迹信息提取血流值(BFI), 并且充分考虑了组织异质性和不规则性.
N阶线性算法的求解使用的是混合的Bregman-TV算法, 其详细步骤见文献[4]的描述, 具体形式如下:
当延迟时间τ足够小时, 一阶(N=1)和N阶(N>1)离散近似解的形式如式(2)和式(3)所示.

(2)

(3)
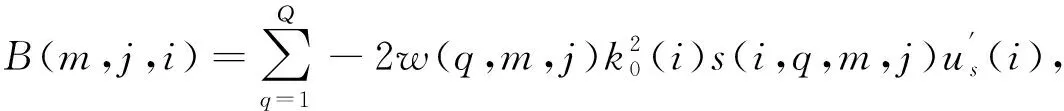
(4)
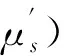
当N=1时, 未知变量αDB仅出现在式(2)的右侧.该项是τ和g1(m,j,τ)-1之间线性回归的斜率.一旦斜率Sl确定, 采用适当的图像重建算法, 就可以根据式(5)计算未知量(αDB(1)).
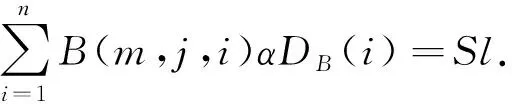
(5)
当N>1时, 未知变量αDB出现在式(3)的两侧.因此, 血流值αDB的重构通过式(3)和式(5)在迭代过程中实现.
此外, 为了评价N阶线性算法和有限元方法的血流图像重建质量, 通过计算机仿真实验比对了两种方法重建图像的对比度[13]. 当异常血流值(代表病变区域)设定从正常血流值(代表健康组织)的2倍增加至6倍时, 有限元方法重建出的血流图像对比度涨幅为99%, 而N阶线性算法重建图像对比度涨幅为108%; 此外,N阶线性算法耗时仅为有限元方法的48%, 大大提高了重建速率[14]. 结果表明, 在相同的光源-探测器阵列和三维空间体素条件下,N阶线性算法优于有限元方法.
3 乳腺血流成像探头
本研究自主设计了适用于乳腺成像的光纤探头来采集受试者的乳腺血流数据, 探头外形为倒置的碗状腔体, 如图2(a)所示, 并且增加内陷15°的弧面设计, 使探头更加贴合乳腺; 探头内有设计好的光纤阵列, 探头的分体结构如图2(b)所示. 光纤探头平面映射的光源-探测器如图 3 所示, 共有8个光源和48个探测器(每个光源周围围绕6个探测器), 此阵列中, 光源-探测器的分布方式既覆盖了不同的深度信息, 也平衡了不同位置单元的光子信息, 很大程度上降低了图像重建线性方程组的病态性.

(a) 乳腺探头实物图
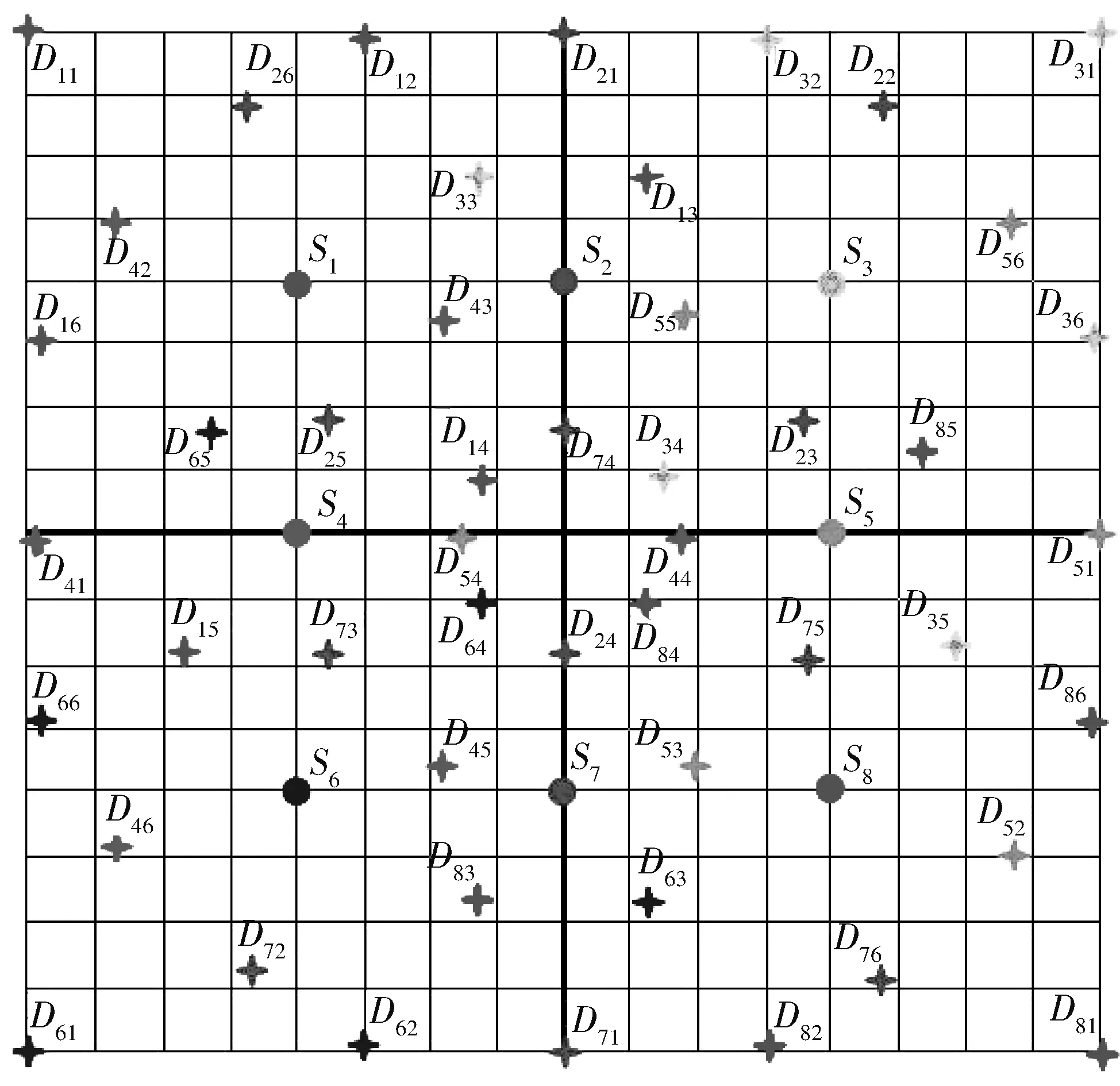
图 3 光源-探测器阵列图
图 3 中,Si代表第i个光源的位置;Dij代表与第i个光源对应的第j个探测器.
4 临床试验与结果
经中北大学和浙江嘉兴市第一医院生物与医学伦理委员会批准后, 将DCT技术应用到乳腺肿瘤临床试验中, 共测量了2例成年乳腺肿瘤患者的DCT数据, 两位受试者是从嘉兴市第一医院乳腺外科门诊和住院部招募的, 年龄分别为 53岁和47岁, 并且排除中风、 高血压和白血病等其他病症. 受试者已被告知所有的研究细节, 并签署了知情同意书. 受试者在2 h内先后完成DCT检查、 乳腺超声检查以及活检穿刺取样, 从而保证三项检查中, 受试者的身体状态相同.
4.1 乳腺血流检测过程
受试者平躺, 全身放松, 双手上举放于头部两侧, 充分暴露乳腺区域; 使用酒精擦拭待测乳腺进行消毒; 测试时, 将定制的乳腺探头垂直覆盖于被测乳腺, 关闭室内所有光源, 开启DCT检测系统采集数据, 单个乳腺采集时长10 min. 分别采集2位受试者的左右侧乳腺血流数据.
完成DCT检查之后, 受试者也进行了临床检查(包括乳腺彩色超声检查和活检穿刺), 与DCT技术获得的血流影像进行对比验证.
4.2 数据处理与分析
乳腺DCT血流检测采用的组织模型大小为16 cm×16 cm×6 cm, 一共1 536个体素, 每个体素的大小为1 cm×1 cm×1 cm.
在得到乳腺血流数据之后, 通过N阶线性算法得到48条乳腺血流的自相关函数曲线, 曲线的斜率即代表血流值(BFI). 原始的血流数据以16×16×6 的三维数值矩阵表示, 通过SPSS 26.0软件包提取每一个血流值矩阵的统计学特征, 包括均值、 标准差、 最大值等. 考虑到受试者的血流状态各不相同, 对同一受试者的左右两侧乳腺血流状态进行了对比.
采用Bregman-TV重建算法得到乳腺血流图像, 为了提高图像分辨率, 对16×16×6的原始数据进行线性插值处理, 得到160×160×60的血流重建图像, 并通过Paraview软件包进行显示. 通过与彩超诊断报告和病理检查结果做对比, 分析血流重建图像与真实病情的相似度, 以及诊断乳腺肿瘤的准确率.
4.3 临床案例分析
受试者A的临床检查结果显示右乳下方见低回声区, 右乳有结节伴钙化, BI-RADS分级为4B类, 病理结果诊断为右乳患有浸润性癌; 左乳的临床检查结果均为健康.
该受试者的双侧乳腺血流重建图像如图 4 所示, 图4(a)为左侧乳腺血流重建图像, 图4(b)为右侧乳腺血流重建图像.
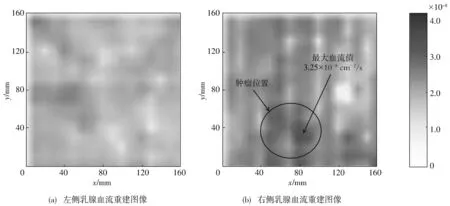
图 4 受试者A的乳腺血流重建图像
从由 4 和表 2 可以看出, 右侧乳腺整体血流值明显高于左侧, 右侧血流指数(BFI)均值为1.85×10-8cm2/s, 左侧血流均值为1.18×10-8cm2/s, 均值比值为1.57倍. 与右乳相比较, 左乳血流值波动幅度较小, 分布明显更加均匀, 标准差是0.19×10-8, 仅为右乳血流值标准差的38%. 由图4(b)可以看出, 右乳的右上方存在低血流值区域, 最小值为6.58×10-8cm2/s, 疑似钙化灶导致的血流不畅. 另外, 右乳血流最大值3.25×10-8cm2/s定位于乳腺下方, 提示该区域存在肿瘤, 使得血供增加, 与该患者的彩超和病理检查结果相同, 并且能够定位出肿瘤存在的位置. 此外, 左乳的均值、 标准差、 最大值均低于右乳, 表示左乳血流均匀稳定, 三项检查结果均表明左乳为健康的正常乳腺.
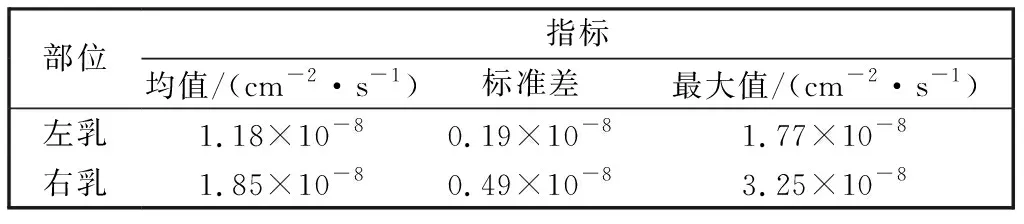
表 2 受试者A的BFI统计指标值
受试者B的临床检查结果显示左乳上方见导管扩张, 下方见低回声区, 左腋下皮质增厚, 左乳有结节伴钙化, 导管扩张伴多发弱回声, 病理结果为乳腺增生症伴潴留囊肿形成, 囊周慢性化脓性肉芽肿性炎伴局灶钙化, 小灶区导管上皮普通型增生. 右乳彩超所见为下方存在结节, BI-RADS分级为3类.
该受试者的双侧乳腺血流重建图像如图 5 所示, 图5(a)为左侧乳腺血流重建图像, 图5(b)是右侧乳腺血流重建图像.

图 5 受试者B的乳腺血流重建图像
由图 5 和表 3 可以看出, 左右侧乳腺均存在结节引起的血流不均匀区域, 但是左乳整体的血流值均匀度不如右乳, 右乳血流标准差为左乳的78%. 左乳上方存在一高血流区, 最大血流值为3.81×10-8cm2/s, 表示导管扩张使得乳腺血供增加. 此外, 左乳整体血流值略低于右乳, 血流值均值相差9%, 左乳下方存在多个低血流区域, 最小血流值为1.28×10-8cm2/s, 提示乳腺钙化结节阻碍血管通畅, 降低血流水平. 右乳下方高血流区域的最大血流值为2.40×10-8cm2/s, 由BI-RADS分级为3类的非钙化结节导致, 位置信息与彩超检查结果一致.
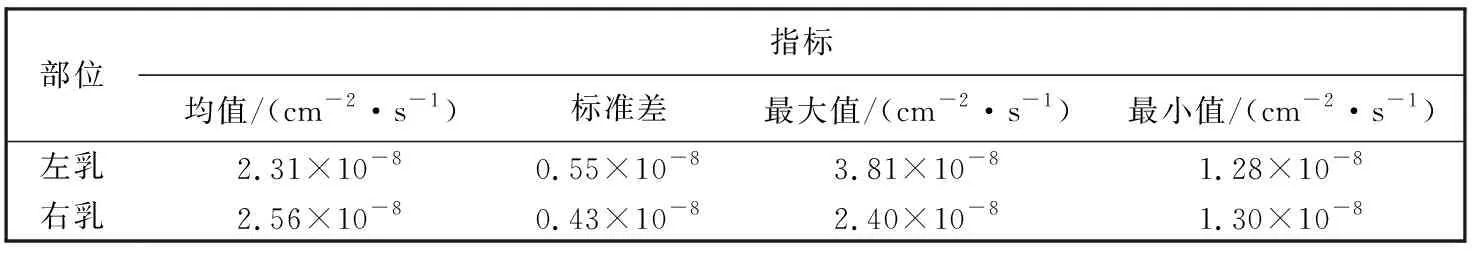
表 3 受试者B的BFI统计指标值
5 结 论
本研究开发了结合迭代线性算法和Bregman-TV的DCT血流重建算法, 通过光开关实现了光源和探测器的分时共享, 降低了设备成本. 此外, 设计了适合于乳腺的碗状光纤探头, 并优化了光源-探测器光纤在组织表面的配置, 从而提高了图像重建的精度. 初步的临床试验表明, 本研究开发的DCT成像系统和算法可以探测到乳腺肿瘤以及钙化引起的血流的变化, 具体表现在含有肿瘤的乳腺的血流值高于对侧, 钙化组织的血流低于对侧. 当左右侧乳腺血流严重不对称时, 提示乳腺患病概率增加. 除此之外, DCT也可以对肿瘤或钙化等异常组织进行定位. 初步的临床试验证实了DCT系统在乳腺癌筛查方面有潜在的应用价值, 更多的病例正在测量和分析, 以便获得有统计意义的临床结论.
