酸法地浸采铀硫酸稀释放热应用研究
2022-06-14王亚安闻振乾苏学斌姚益轩胥国龙
王亚安,闻振乾,苏学斌,姚益轩,胥国龙,张 翀
(1.核工业北京化工冶金研究院,北京 101149;2.中国铀业有限公司,北京 100010)
天然铀是重要的战略资源和能源矿产,扮演着“军工基石、核电粮仓”的关键角色。砂岩型铀矿是我国主要的天然铀资源类型,原地浸出采铀(以下简称“地浸采铀”)则是砂岩型铀矿开发的首选工艺[1-2]。地浸采铀是指用化学溶液,通过钻孔从天然埋藏条件下具有一定渗透性能的砂岩铀矿体中,选择性提取和回收铀金属的一种铀矿采冶工艺。该工艺需将浸出剂从注液孔注入地下,沿矿层渗流,浸出矿石中的铀,形成浸出液并从抽液孔提升至地表,再经过水冶处理以分离、回收浸出液中的金属铀[3-6],具有投资节省、建设周期短、生产效率高、产品成本低、环境友好等显著优点。自2014年起,地浸采铀所获铀产量已占我国天然铀年总产量的50%以上,并呈逐年提升态势。
根据矿石类型选择不同浸出剂,将地浸采铀工艺分为酸法浸出、碱法浸出和中性浸出三种[1-2,4-5]。在酸法浸出工艺中,硫酸因具有价格低廉、性质稳定及对矿石中铀浸出率高等优点成为配制浸出剂首选的化工原料[7]。 工业浓硫酸质量浓度为92.5%(实验室内硫酸试剂浓度为98%),在国内外酸法地浸矿山中,浓硫酸通常是通过管道直接加入露天配液池,与吸附尾液混合配制成硫酸浓度为5~30 g/L[8-9]的浸出剂,再由化工泵经地表管道输送至各个注液钻孔注入地下矿体。由于浸出剂中硫酸浓度低,且在露天环境中热量消耗快及温度变化不明显,因此国内外酸法地浸采铀矿山对硫酸稀释放热的现象及利用没有引起足够重视,这也造成了热能的浪费。
事实上,浓硫酸稀释放热包括两个过程:一个过程是硫酸分子的扩散和电离,该过程为吸收热量;另一过程为氢离子和硫酸根离子的水合,该过程伴随着放热。硫酸根离子和水分子能结合成非常稳定的水合离子,相较于吸热过程而言,会放出大量的热,所以总体上浓硫酸稀释为放热过程[10-11]。欧列[12]曾对硫酸稀释热的原理及公式进行了综述,总结并推荐了不同条件下硫酸稀释热的计算表格;RÜTTEN等[13]测量了不同硫酸/水摩尔比体系下的温度升高范围;许宗伟等[14]将硫酸稀释热用于复合肥生产环节,结果表明可大大减少用电成本;伏双才[15]则分析了硫酸装置低温热回收系统中蒸汽产量存在偏差的原因,并计算了各负荷状态下低温热回收系统的热能利用率。由此可见,硫酸稀释放热技术在一些行业已得到应用。
在酸法地浸采铀“淋萃流程”[16-17]中,浸出液从抽液孔提升至地表,通常要经过过滤、离子交换(树脂吸附浸出液中的铀,浸出液变为吸附尾液,再与浓硫酸配制成新的浸出剂)、淋洗树脂(形成萃原液)、萃取(对萃原液进行铀富集,形成饱和有机相)、反萃取(对饱和有机相再次进行铀富集,形成合格液)、沉淀(部分沉淀母液去蒸发池)、压滤,最终形成产品“黄饼”[18-19]。其中,反萃取工艺是将铀从有机相萃取至水相,以便于后续沉淀工序的进行,其受温度的影响大,稳定运行温度需保持在20 ℃以上。国内地浸铀矿山大多处于北方地区,冬季寒冷漫长,需消耗大量煤炭或电能供暖以保证水冶环节的正常运行。此外,铀的浸出和溶液运移发生在含矿含水层中,为了控制溶浸范围,要求井场抽液量大于注液量一定比例,《核工业铀矿冶工程设计规范》(GB 50521—2009)规定抽液量与注液量基本平衡,抽液量大于注液量0.3%~1.0%,使得浸出区域内形成地下水降落漏斗[20],从而可有效控制溶浸液扩散。鉴于此,国内地浸矿山基本都建造了依靠自然蒸发的蒸发池,以容纳和蒸发多抽出的0.3%~1.0%废液及后续工艺产生的废水,依据待处理的废水量,蒸发池面积可达几亩(1)1亩=666.67 m2。甚至几十亩。然而,受气温影响,废水蒸发速度较慢,而且建设蒸发池一方面需要大面积动土,退役治理地表恢复难度大;另一方面大面积的蒸发池也需要投入征地、租地、建设和维护等方面的成本,所以须予以重点关注。
基于此,本文通过分析计算和试验,将硫酸稀释热用于前述酸法地浸采铀工艺流程的相关环节,以改善低温环境下“淋萃流程”的反萃取效果,加快蒸发池内废液蒸发速度,取得了实质性效果。本文研究减轻了酸法地浸采铀工艺中的热浪费现象,加深了对硫酸稀释放热的认识,可为同类型行业提供借鉴。
1 硫酸稀释放热介绍及室内试验验证
根据《硫酸工艺设计手册》[10-11],在一定温度下,将质量浓度为w1的1 mol硫酸加水稀释至质量浓度为w2的1 mol硫酸,其放出的稀释热计算见式(1)。
Q2-Q1=

(1)
式中:Q2-Q1为1 mol硫酸稀释后放出的热量,J/mol;n1为质量浓度为w1时1 mol硫酸所含有的水摩尔数;n2为质量浓度为w2时1 mol硫酸所含有的水摩尔数;c(H2O)为水的比热容,取4.161 8 kJ/kg·℃。
假设将体积V(H2SO4)=200 mL质量浓度为w1(H2SO4)=98%的硫酸加入V(H2O)=1 000 mL水中,则稀释后的硫酸浓度计算见式(2)。
w2(H2SO4)=

(2)
式中:ρ为密度,g/cm3;ρ(H2SO4)为1.84 g/cm3;ρ(H2O)为1 g/cm3。
于是,浓度为w1(H2SO4)=98%硫酸含有的水摩尔数计算见式(3)。
n1=
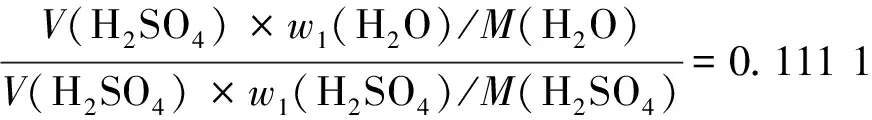
(3)
式中:w1(H2O)=1-w1(H2SO4)=2%;M为物质的摩尔质量,g/mol;M(H2O)为18 g/mol;M(H2SO4)为98 g/mol。
同理,浓度w2(H2SO4)=26.9%硫酸含有的水摩尔数计算见式(4)。
n2=
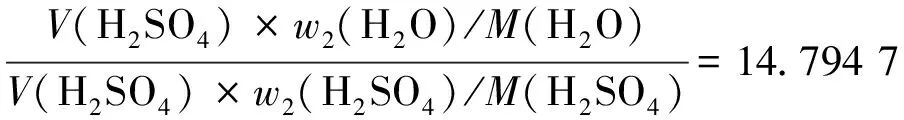
(4)
将式(3)和式(4)带入式(1)求得1 mol硫酸放出的热量为:Q2-Q1=62 320.886 8 J/mol≈62.321 9 kJ/mol。由于本文研究中硫酸物质的量为3.755 1 mol(质量/物质摩尔质量),所以总共放出的热量为234.025 0 kJ。若将热量进一步转换成温度变化量,则根据式(5)进行计算。
Q2-Q1=c(H2SO4)m(H2SO4+H2O)ΔT
(5)
式中:c(H2SO4)为不同温度、不同浓度硫酸对应的比热容,具体数值参照文献[10]和文献[11],当温度为20 ℃时,w2(H2SO4)=26.9%的比热容为3.383 0 kJ/kg·℃;m(H2SO4+H2O)为稀释后的体系质量,kg;ΔT为体系稀释前后温度变化量,℃。据此求得:ΔT=50.567 0 ℃。 此外,还可得到不同硫酸-水体积比下的稀释热理论温度差,如图1所示。
由式(1)和图1可知,随着硫酸-水体积比的增大,尽管放出的热量逐渐增大,但稀释热温度理论升高值呈现出先增大后减小的趋势,即存在一个最佳的硫酸-水体积比使溶液体系温度升高最大,这是因为当稀释过量后,体系中多余的水分吸收了部分热量。为了验证计算值, 采用室内试验的方法, 取200 mL浓硫酸分别倒入装有不同体积(1 000 mL、800 mL、600 mL、400 mL、200 mL、100 mL)自来水的烧杯中,烧杯体积为2 000 mL,并将温度计置于液面以下。在倒入浓硫酸的同时,用玻璃棒不停搅拌,使溶液温度分布均匀,硫酸稀释放热迅速,观察温度计读数并记录最高温度(室温为20 ℃),如图2所示,试验数据见图1。试验值的变化趋势验证了硫酸稀释放热的理论值,但数值略低,这可能是由于敞口试验过程中有一部分热量损失所导致。
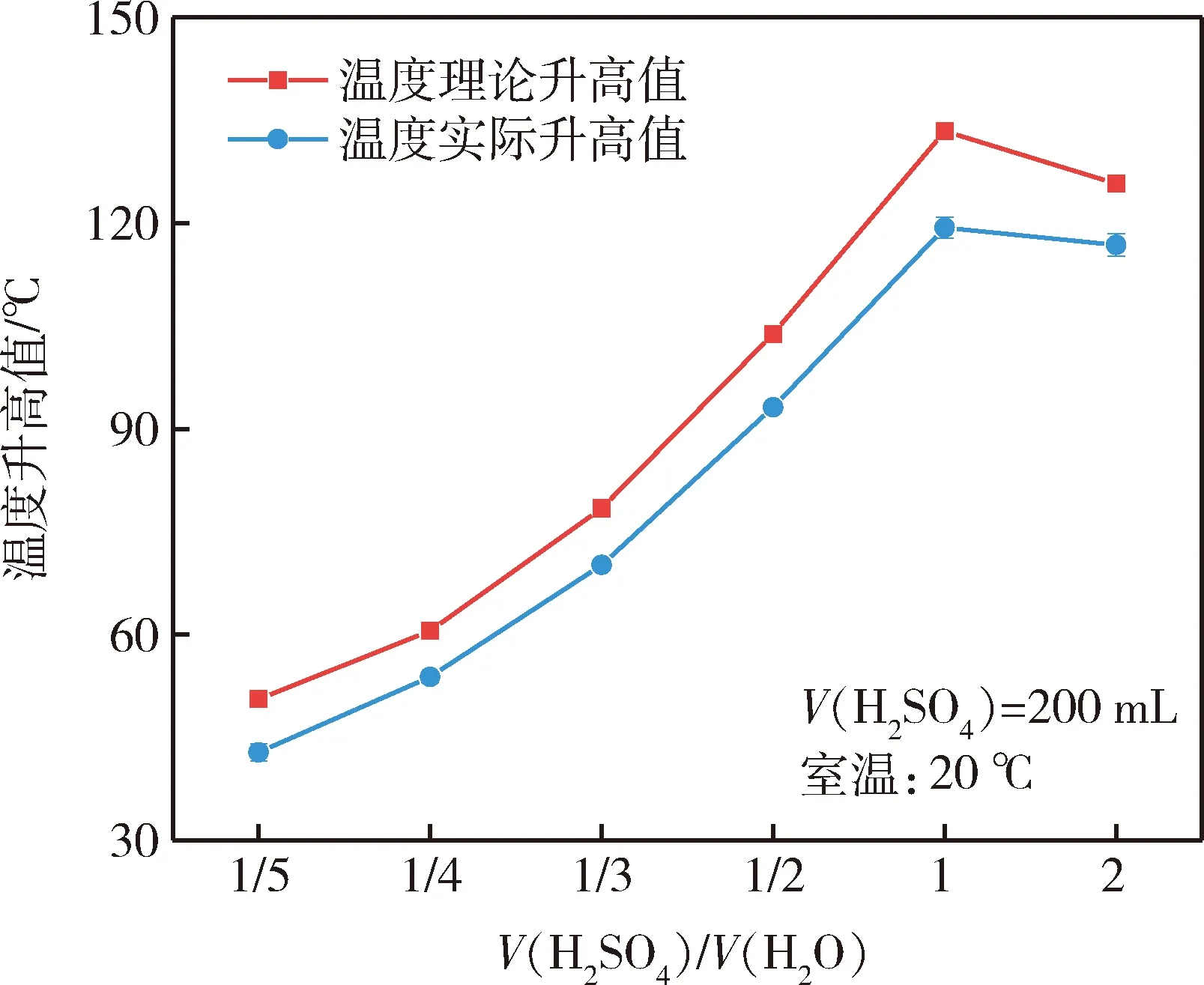
图1 不同硫酸-水体积比下的稀释热温度理论升高值Fig.1 Theoretical increase value of dilution heattemperature under different sulfuric acid-watervolume ratio

图2 不同硫酸-水体积比下的稀释热温度测量Fig.2 Measurement of dilution heat temperature atdifferent volume ratios of sulfuric acid to water
2 硫酸稀释热应用及讨论
2.1 硫酸稀释热用于反萃取工艺
2.1.1 背景介绍
某铀矿床地处内蒙古锡林郭勒盟苏尼特左旗,当地冰冻期从每年10月至次年4月,期间平均气温-18.6 ℃,极端气温-42.8 ℃。冬季运行期间,反萃取工序所处水冶车间空间大,暖气供热对温度提升效果一般,而低温运行导致有机相与水相分相速度慢、乳化现象明显,且贫有机相夹带反萃取剂严重[21-22],未加热时合格液出口分相情况如图3所示,严重影响水冶环节的运行和后续工序的开展。

图3 合格液出口有机相-水相分相情况Fig.3 Organic-water phase separation condition inqualified liquid export
2.1.2 试验方案及流程
鉴于石墨稀释器具有传热效率高、结构强度高、使用寿命长等特点[23],特选用石墨稀释器作为硫酸稀释放热的装置;同时,经过调研,四氟沉浸式热交换器具有耐腐蚀能力强、抗结垢性好、传热性能好等优点[24],选用四氟沉浸式热交换器作为热量回收设备,并将其与反萃取工艺连接,试验流程见图4。具体地,经树脂离子交换后的吸附尾液与工业浓硫酸以一定比例混合进入石墨稀释器释放热量,萃取剂萃取淋洗液后形成饱和有机相并进入反萃取环节,前述四氟沉浸式热交换器置于饱和有机相储槽内,循环清水则作为传热媒介在进入石墨稀释器获取热量后返回给饱和有机相加热,以此实现升温的目的。为记录温度值变化,在稀释器出口及饱和有机相储槽设置了温度变送器。
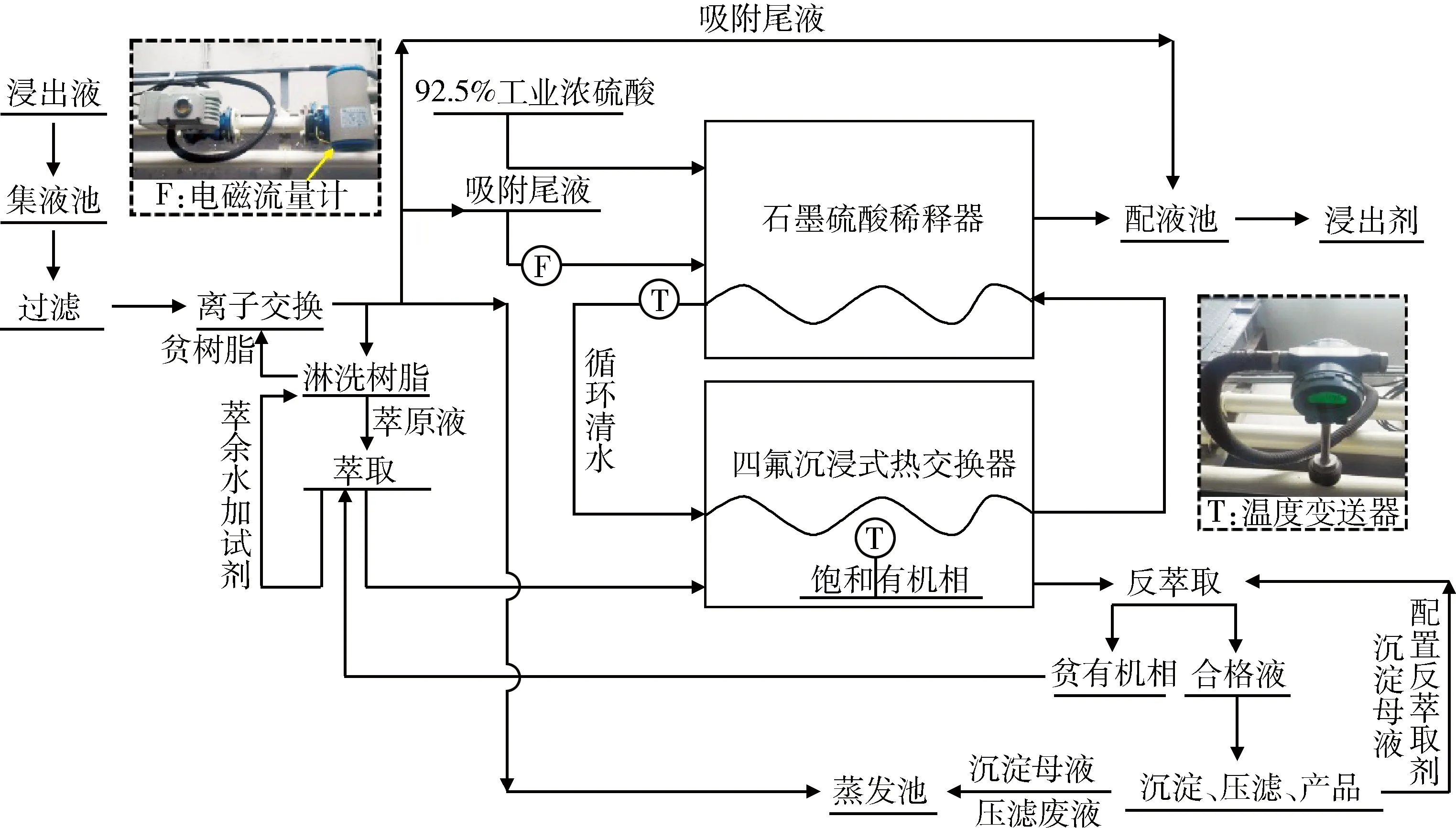
图4 某铀矿山浸出液处理流程及反萃取环节加热示意Fig.4 Process flow of leaching solution in a uranium mine and heating diagram of reverse-extraction
根据现有工艺,浓硫酸流量为Q(H2SO4)=1.40 m3/h,饱和有机相主要成分为含铀磺化煤油,其流量为Q(有机相)=5.85 m3/h,比热容为c(有机相)=2.1 kJ/kg·℃,密度为ρ(有机相)=800 kg/m3;反萃取装置为一中空长方体,其长、宽、高分别为1.78 m、1.23 m、7.22 m;为保证有机相温度至少达到20 ℃,经试算,水-酸流量比不得大于12,考虑到热量损失,以及吸附尾液流量不能太小,否则无法完全稀释放热,最终结合给水泵的额定流量设定Q(H2O)/Q(H2SO4)的范围为3.5~9.0。另外,为尽可能吸收、传递温度,循环清水的流速是很重要的因素,本文结合《热交换器设计手册》的推荐确定循环清水流速为0.5 m/s。
进一步,为评价饱和有机相的热量利用率,根据式(6)进行计算。

(6)
2.1.3 结果与讨论
测量的循环清水出水温度以及饱和有机相温度结果见图5。由图5可知,随着水-酸流量比的增加,二者温度相应降低,这与前述提及的体系水量增多后热量消耗增大有关,但饱和有机相温度大于20 ℃,现场试验达到了预期效果。

图5 循环水、饱和有机相温度以及热量利用率Fig.5 Temperature of circulating water,saturated organicphase and heat utilization efficiency
利用式(6)计算饱和有机相的热量利用率,结果见图5。由图5可知,在试验范围内,最高热量利用率超过60%,随着水-酸流量比的增加,数值相应降低。同时,欲使热量利用率大于40%且饱和有机相温度大于20 ℃,并结合石墨稀释器最佳运行状态为保持循环水出水温度在50 ℃以下(否则会将石墨氧化),得到最佳水-酸流量比的范围为:4.5≤Q(H2O)/Q(H2SO4)≤8.0。
此外,从合格液出口的有机相-水相分相情况亦可展示体系升温后的效果(图6),在对饱和有机相加热后,基本消除了乳化现象,这对后续产品的制备具有重要意义。

图6 加热后合格液出口有机相-水相分相情况Fig.6 Organic-water phase separation condition inqualified liquid export after been heated
事实上,当温度升高时,溶液体系黏度降低且表面张力增大,有利于加快油-水分相并减少乳化现象[21]。进一步可知,温度升高有利于提高铀的反萃取率,试验分析了加热前、加热后50 d内的贫有机相及萃余水中铀浓度大小,如图7所示。结果表明,加热反萃取环节可有效降低贫有机相中的铀浓度,同时也使铀浓度分布曲线变得均匀。因有机相在萃取-反萃取系统中循环使用,贫有机相含铀浓度的降低会进一步提高贫有机相的萃取效率,进而降低萃取环节萃余水中的铀浓度,使整个萃取-反萃取系统在良性循环中稳定运行。 但水-酸比对贫有机相及萃余水中铀浓度的影响不大,说明只需将温度维持在20 ℃以上,就可实现萃取-反萃取系统的高效运行。

图7 加热前后萃余水与贫有机相中铀浓度变化趋势Fig.7 Variation trend of uranium concentration inraffinate and lean organic phase before andafter heating
2.2 硫酸稀释热用于蒸发池工艺
2.2.1 背景介绍
在地浸采铀工艺中建造蒸发池的目的,一方面是为容纳抽液孔多抽出的液体,另一方面则是为收集水冶环节产生的废液,再通过自然蒸发处理。该铀矿床所在地的年平均蒸发量为1.679 m,前期基于工艺参数测算,矿区设计、采用了4个体积一致的蒸发池串联的方式进行废液蒸发,蒸发池长、宽、高分别是100 m、 60 m、 1.20 m,为防止废水渗透污染地下水,在蒸发池池底、池壁进行防渗漏处理,并在周边堆高约1 m的围堰,以防降水量突然增大,蒸发池中废水溢出。蒸发池占地面积大,征地、租地成本相对较高,同时由于气温低,废液蒸发速度也较慢。
2.2.2 试验流程及结果
本文针对加快废液蒸发速度的试验是探索性的,由于所建蒸发池的面积足以容纳该矿区产生的废液,为不影响正常的蒸发流程,蒸发池1、蒸发池2、蒸发池3依旧用作自然蒸发,并将与蒸发池4相连的管路阀门关闭,令其作为加热池,露天场合进行试验。鉴于矿区处理水量大,该试验未采取中间传热媒介,而是直接将池内水循环于石墨硫酸稀释器与蒸发池之间,通过一段时间后测量水位的降深,并折算成年蒸发量以评价硫酸稀释加热对蒸发工艺的效果,具体流程见图8[25]。
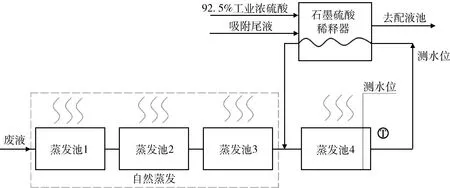
图8 某铀矿山地浸采铀蒸发流程及废液蒸发环节加热示意Fig.8 Evaporation process of in-situ leaching uranium mining and heating diagram of discard solution evaporation
工业浓硫酸流量设置为Q(H2SO4)=1.4 m3/h,同时为保持高热量利用率,令水-酸流量比为4.5;选用耐酸化工泵作为动力源,并控制蒸发池内废水循环流速为0.5 m/s。另外,设置蒸发池4内的初始水位高度为0.2 m,需指出,该数值的确定过程为:先令石墨稀释器处于待工状态,即不通入浓硫酸与吸附尾液,只令蒸发池内废水循环于稀释器与蒸发池之间,再用水位仪测定原始水位高度。
通入工业浓硫酸和吸附尾液进行不间断试验,待循环15 d后测量水位降深,其数值约为76 mm,此时池内温度约为35 ℃。需指出,由于蒸发池面积大,温度分布不合理,故本文研究是在蒸发池出口管路测量的温度。
根据水位降深可知,采用加热法蒸发废液,在其他条件相同的前提下(不考虑其他诸多因素),其年平均蒸发量为1.849 m,相较于该地的年平均蒸发量,蒸发速度提升10.13%;同理,若以现在所建蒸发池的体积为基准,该试验工况对应的蒸发池体积则减小10.13%,有效减少了占地用量。
2.2.3 思考
事实上,当液体自身温度升高时,分子热运动加剧,蒸发量自然提升,虽然与环境温度、湿度、液体分压等因素相关,但从经济性角度来看,对蒸发池进行加热,配套的设备仅有稀释器、液泵及相应管道,额外的费用则为液泵产生的电费及可能的维修费。相比于大面积征地、租地而言,提高蒸发池温度以加快蒸发速度,以此实现减小蒸发池面积并节省征地、租地的费用是合理可行的。
综上,尽管硫酸稀释放热原理简单且实现方法简易,但以往并没有引起足够的重视,这造成了大量的热量浪费。比如,矿区生活用暖主要为烧煤锅炉或电热锅炉取暖,若将硫酸稀释热用于矿区生活采暖未尝不是一种降低成本、减小大气污染的措施。
3 结 论
地浸采铀工艺流程中存在大量热浪费的现象,同时又存在需要加热的环节。利用试验的方法,将配制浸出剂时的硫酸稀释热用于地浸采铀相关环节,取得了一定效果,得到如下结论。
1) 硫酸稀释放热可使体系温度升高,随水-酸体积比的减小,温度值呈现出先增大后减小的趋势,即存在一个最佳的水-酸体积比使溶液体系温度升高最大,这是因为当稀释过量后,体系中多余的水分吸收了部分热量。
2) 硫酸稀释放热可改善地浸采铀工艺水冶环节“淋萃流程”的反萃取效果,试验表明,水-酸流量比控制在4.5~8.0之间,可使饱和有机相的溶液温度大于20 ℃且热量利用率达到40%。
3) 当饱和有机相温度升高时,体系黏度减小,表面张力增大,可加快油-水分相时间,同时消除乳化现象;另外,经过取样分析发现,将硫酸稀释热用于“淋萃流程”可有效降低贫有机相和萃余水中的铀浓度,进而提高产品质量。
4) 硫酸稀释放热可提高地浸采铀工艺蒸发池内的废液蒸发速度,试验表明,在本文研究中,当水-酸流量比控制为4.5时可使蒸发速度提升10.13%;蒸发速度的提升意味着在处理相同量的废水时可减小蒸发池面积,降低成本。
