对甲苯磺酸耦合碱性过氧化氢预处理对不同木质纤维素生物转化的影响
2022-06-14管舒仪蔡晓丹陈欣玥杨明琰
管舒仪,窦 妍,2,蔡晓丹,陈欣玥,张 笑,杨明琰,2
(1长安大学 水利与环境学院,陕西 西安 710054;2旱区地下水文与生态效应教育部重点实验室,陕西 西安 710054)
随着社会的飞速发展,化石燃料消耗所带来的能源短缺和环境污染问题日益严重,以纤维素等可再生资源为原料发展生物燃料成为解决该问题的重要途径[1]。我国农林废弃物资源丰富,仅林业加工剩余物、农作物秸秆等农林废弃物年产量就达8亿t,但实际利用量仅为2.2亿t左右,可利用的潜在资源数量巨大[2]。农林废弃物是木质纤维素类生物质的重要来源,主要由纤维素、半纤维素和木质素(简称“三素”)组成,其中纤维素含量占30%~60%,是自然界含量最丰富的可再生资源,其可以通过酶解糖化及生物发酵制备生物乙醇、生物丁醇、生物柴油等生物燃料[3]。但是纤维素、半纤维素和木质素之间通过酯键和醚键等共价键、氢键和范德华力等分子间作用力形成了十分复杂的网状结构,具有较强的机械强度,可抵抗外界微生物侵蚀以及化学试剂渗透[4],必须经过适当的预处理,脱除其中的木质素和半纤维素,降低纤维素的聚合度,才能改善酶对纤维素的可及性,提高酶解糖化效率。农林废弃物传统的预处理方法有酸、碱、有机溶剂法等,但这些方法存在处理温度较高、能耗较大、化学试剂难以回收、污染严重等问题[5]。
酸基助水溶剂对甲苯磺酸(p-toluenesulfonic acid,p-TsOH)是一种类表面活性剂,在水中溶解度较高,具有较强的酸性,因此可以利用其酸性和表面活性选择性溶解木质纤维素中的半纤维素和木质素而保留纤维素,使得3种大分子得到分级分离。由于p-TsOH水溶液可在≤80 ℃条件下快速分离木质纤维素的3种大分子,使用条件温和,分离效率高,且其自身可以低温结晶回收后循环使用,在木质纤维素的快速分离、纤维素的生物转化[6]、糠醛等戊糖的生产[7]以及木质纤维素纳米材料的制备[8]等方面显示出广阔的应用前景。如Chen等[9]研究发现,p-TsOH水溶液(80 ℃,处理时间小于20 min),对杨木中木质素的脱除率与传统碱法(150 ℃处理2 h)相当;Yang等[6]于2019年发现,在80 ℃条件下利用p-TsOH预处理农作物废弃物20 min,纤维素、半纤维素和木质素3种组分得到了高效分离,同时p-TsOH可以循环使用,且处理效果不减。虽然p-TsOH可以选择性脱除木质纤维素中的木质素和半纤维素,但其预处理后的原料中仍然保留了10%以上的木质素和10%以上的半纤维素,对后续酶解糖化及生物乙醇发酵仍然存在一定的限制。此外,不同原料中的木质素含量及构成木质素分子的单体类型与数量均不同,木质素的分子量、化学结构有较大的差异,这对预处理的效果也有很大的影响[10],而预处理方法的普适性是全面评价其应用价值的一个重要因素,因此有必要就其对不同种类原料的预处理效果进行综合研究。
小麦秸秆是重要的农业废弃物,其中含有丰富的纤维素,对其进行资源化利用具有广阔的应用前景。芒草具有生物量和纤维素含量高、多年生、对环境适应性强等特性,被认为是最具潜力的能源植物之一。杨木适应性广,生长速度快,资源丰富,在我国南北方均有广泛种植。本研究以农业废弃物小麦秸秆、芒草秆及阔叶木杨木为原料,采用p-TsOH耦合碱性过氧化氢(alkaline hydrogen peroxide,AHP)的方法对其进行预处理,研究酸碱耦合处理对3种原料化学组成、结构形态、酶解率以及乙醇产率的影响,以期为农林废弃物生物转化制备可发酵糖及生物燃料提供理论依据。
1 材料与方法
1.1 材料与试剂
小麦秸秆,取自陕西省西安市;芒草秆,购于湖南省怀化市;杨木,购于山东省。用植物粉碎机将上述木质纤维素粉碎,过孔径0.833 mm筛,放入自封袋中备用。纤维素酶Cellic®CTec2,由Novozymes诺维信中国公司提供,酶活性为147 FPU/mL。乙醇发酵菌种,为高活性干酵母,由安琪酵母股份有限公司生产;p-TsOH、氢氧化钠、过氧化氢等均为国产分析纯级试剂。
1.2 预处理方法
p-TsOH处理[6]:取芒草秆、小麦秸秆和杨木各10 g(绝干质量),加100 g质量分数为70%的p-TsOH溶液,在恒温水浴锅中预热至80 ℃,将两者混合并连续搅拌反应20 min后,加入133 mL的去离子水终止反应,真空抽滤,固体残渣用去离子水洗至中性,测定固体产率及纤维素、半纤维素和木质素含量。每个样品重复3次,计算标准差。
p-TsOH耦合AHP处理[11]:取5 g(绝干质量)经p-TsOH处理的样品,与100 mL、体积分数2% H2O2溶液以1∶20体积比混合,用5 mol/L NaOH溶液调节pH至11.5,置于50 ℃、120 r/min 恒温振荡器中振摇12 h,真空抽滤,将固体残渣用去离子水冲洗至中性,测定固体产率及纤维素、半纤维素和木质素含量。每个样品重复3次,计算标准差。
1.3 纤维素酶添加量对酶解率的影响
取1 g(绝干质量)p-TsOH耦合AHP两步处理(以下简称两步处理)后的样品于具塞三角瓶中,加入pH为5.6的50 mmol/L的醋酸-醋酸钠缓冲溶液,使底物质量浓度为20 g/L,分别加入不同体积的纤维素酶,使其最终添加量分别为5,10,15 FPU/g(以纤维素的质量计算,下同),之后置于50 ℃、180 r/min的恒温振荡器中酶解,分别在酶解4,8,12,24,48,72 h取样,用SBA-40E生物传感分析仪测定葡萄糖质量浓度,计算酶解率(substrate enzymatic digestibility,SED)。每个样品重复3次,计算标准差。
1.4 不同发酵工艺对乙醇产率的影响
分步糖化发酵(separate hydrolysis fermentation,SHF):取2 g(绝干质量)p-TsOH耦合AHP处理后的样品,加入pH 5.6的50 mmol/L的醋酸-醋酸钠缓冲溶液,使底物质量浓度为130 g/L,再加入10 FPU/g纤维素酶,置于50 ℃、180 r/min的恒温振荡器中酶解72 h,离心去除沉淀,将上清液在121 ℃灭菌30 min后,接种干酵母,接种量为底物质量的6%,于32 ℃、170 r/min条件下振荡发酵,分别在发酵4,8,12,24,48,72,96 h取样,测定发酵液中乙醇和葡萄糖的质量浓度,计算乙醇的产率。每个样品重复3次,计算标准差。
同步糖化发酵(simultaneous saccharification and fermentation,SSF):称取2 g(绝干质量)p-TsOH耦合AHP处理后的样品,121 ℃灭菌30 min后,加入pH 5.6的50 mmol/L 的醋酸-醋酸钠缓冲溶液,使底物质量浓度为130 g/L,再加入10 FPU/g 纤维素酶,接种底物质量6%的干酵母,于32 ℃、170 r/min条件下振荡发酵,分别于发酵4,8,12,24,48,72,96 h取样,测定发酵液中乙醇和葡萄糖的质量浓度,计算乙醇产率。每个样品重复3次,计算标准差。
1.5 测定指标及方法
1.5.1 固体产率及三素含量 测定处理后样品的绝干质量。计算固体产率公式为:
S=W1/W2×100%。
式中:S为固体产率,%;W1为处理后样品的绝干质量,g;W2为木质纤维素原料的绝干质量,g。
小麦秸秆、芒草秆、杨木原料及预处理样品木质纤维素中纤维素、半纤维素和木质素含量分析采用美国能源部可再生能源实验室(NREL)的方法[12]进行测定。计算半纤维素、木质素的脱除率及纤维素保留率:
式中:X为半纤维素的脱除率,%;S为固体产率,%;A1、A0分别为处理后样品、木质纤维素原料的半纤维素含量,%;Y为木质素的脱除率,%;B1、B0分别为处理后样品、木质纤维素原料的木质素含量,%;Z为纤维素的保留率,C1、C0分别为处理后样品、木质纤维素原料的纤维素含量,%。
1.5.2 样品的表征 (1)微观形貌的扫描电镜(SEM)分析。样品的微观形貌采用扫描电镜(Hitachi S-4800,日本)进行观察。
(2)吸收特性的傅里叶变换红外光谱(FT-IR)分析。样品的红外光谱分析采用德国布鲁克的TENSOR Ⅱ傅里叶红外光谱仪,测试波长为500~2 000 cm-1,分辨率为4 cm-1。
(3)晶体结构的X-射线衍射分析(XRD)。使用X-射线衍射仪(D8 ADVANCE,布鲁克,德国)测定样品的衍射峰强度,计算结晶度[13],具体计算公式如下:
CrI=(I002-Iam)/I002×100%。
式中:CrI为结晶度,I002为结晶区域2θ角接近22.5°的衍射峰强度,Iam为非结晶区域2θ角接近18°的衍射峰强度。
(4)保水值。采用离心法测定纤维的保水值(water retention value,WRV)[14]。取不同预处理后的木质纤维素,用孔径0.037 mm尼龙网布包裹,于4 000 r/min离心20 min,对离心后样品称质量,记为W1,然后将其于105 ℃条件下干燥至质量恒定,并称质量,记为W2。计算WRV:
WRV=(W1-W2)/W2×100%。
式中:W1为离心后湿样品的质量,g;W2为干燥后样品的质量,g。
1.5.3 酶解率 酶解液中葡萄糖质量浓度参考文献[15]的方法测定。计算酶解率(SED):
式中:Cglu是酶解液中葡萄糖的质量浓度,g/L;V是酶解液的体积,L;0.9是葡萄糖和纤维素之间的转换系数;M是样品的绝干质量,g;Ccel是样品的纤维素含量,%。
1.5.4 乙醇产率 发酵液中葡萄糖质量浓度参考文献[15]的方法测定,乙醇质量浓度参考文献[16]的方法测定。计算乙醇产率(y):
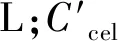
2 结果与分析
2.1 不同预处理方法对木质纤维素固体产率及化学组分含量的影响
经过p-TsOH处理、p-TsOH耦合AHP两步处理的芒草秆、小麦秸秆和杨木的固体产率及化学组分含量如图1所示。由图1可知,经过p-TsOH处理,芒草秆、小麦秸秆和杨木原料的固体产率分别为49%,48%和56%,损失部分为脱除的木质素和半纤维素,3种原料中杨木的固体产率较高,说明p-TsOH对其处理效率相对较低。经p-TsOH耦合AHP两步处理后,芒草秆、小麦秸秆和杨木的固体产率分别降为39%,36%和46%,说明两步预处理进一步脱除了3种原料中的木质素和半纤维素。经过p-TsOH处理,芒草秆中半纤维素和木质素含量分别从原料的29.05%和25.03%降为14.83%和15.00%,纤维素含量从原料的34.10%提高至64.96%;小麦秸秆半纤维素和木质素含量分别从原料的24.96%和23.04%降为13.33%和11.22%,纤维素含量从原料的34.10%提高至69.02%;杨木半纤维素和木质素含量分别从原料的16.60%和25.91%降为7.22%和18.57%,纤维素含量从原料的39.32%提高至68.15%。结果表明,经过p-TsOH预处理后,3种原料的纤维素得到了明显的富集,但样品中木质素和半纤维素含量总体高于10%(杨木半纤维素含量低于10%),这对进一步的酶解糖化和乙醇发酵会产生不利的影响。将p-TsOH处理得到的固体残渣进一步用AHP处理后,芒草秆、小麦秸秆和杨木样品中纤维素、半纤维素、木质素含量分别为76.56%、12.97%、1.91%,81.78%、11.14%、2.20%和77.43%、6.79%、3.26%。计算可知,经p-TsOH耦合AHP两步处理后,芒草秆、小麦秸秆和杨木的纤维素保留率分别为87.97%,87.85%和90.53%,半纤维素脱除率分别为82.50%,84.21%和81.19%,木质素脱除率分别为97.01%,96.50%和94.01%。可知两步预处理后3种原料中的木质素脱除率均达到94%以上,半纤维素脱除率均达到80%以上,而纤维素的损失均低于15%,说明两步预处理可以选择性地脱除半纤维素和木质素,最大程度地保留纤维素。
2.2 不同预处理方法对木质纤维素结构形态的影响
2.2.1 扫描电镜(SEM)结果 从图2可以看出,未进行预处理的原料样品表面光滑,纤维排列紧密整齐。经过p-TsOH处理后的木质纤维素,原本致密的结构遭到了破坏,表面粗糙,孔隙增多;进一步经过AHP处理后木质纤维素结构破坏更为严重,结构变得疏松不规则,比表面积增大。这主要是因为大部分半纤维素和木质素被脱除后,木质纤维素结构变得松散,孔隙增大,纤维素对酶的可及性增加,对之后的酶解有积极的作用。
2.2.2 FT-IR分析结果 897,1 050和1 160 cm-1处的吸收峰分别为纤维素β-糖苷键的不对称伸缩振动、纤维素和部分半纤维素内C-O键的伸缩和纤维素C-O-C的不对称伸缩振动的吸收峰[17]。由图3可知,经过两步处理后,3种原料样品在897,1 050,1 160 cm-1处的吸收峰强度均明显增强,说明样品中纤维素得到了富集。1 510和1 600 cm-1处的吸收峰均与木质素苯环的芳香骨架振动有关,1 250 cm-1处的峰由木质素酚醚键C-O-C伸缩振动所致。经p-TsOH处理后,样品在1 250,1 510和1 600 cm-1处的吸收峰强度减弱,表明p-TsOH处理脱除了一部分木质素;之后进一步经过AHP处理,这3处的吸收峰强度变得更弱甚至消失,表明大量的木质素已被除去。1 736 cm-1处的峰为半纤维素与木质素之间酯键的吸收峰[18]。经过不同预处理,3种原料在1 736 cm-1处的吸收峰几乎消失,说明原料中的半纤维素与木质素得到了较好的脱除。
2.2.3 X-射线衍射分析结果 由图4-A可知,所有样品在2θ角为16°和22°附近均有明显的衍射峰,这是纤维素Ⅰ的典型结构特征[19],说明预处理过程没有破坏纤维素固有的晶体结构。从图4-B可以看出,经p-TsOH预处理后,3种样品的结晶度均比原料高,这是因为p-TsOH预处理可以脱除原料中无定形态的木质素和半纤维素,以及纤维素的无定形区域,使得样品中无定形区破坏而结晶区保留,导致样品结晶度增高;之后再经过AHP处理,进一步脱除了样品中残留的木质素和半纤维素,样品的结晶度进一步增大。
2.2.4 不同预处理方法对木质纤维素保水值的影响 保水值是表征纤维水化润胀程度的指标,与纤维的表面积和总孔隙率有关[20]。从图5可以看出,3种原料经过不同方法预处理后保水值均明显增大。这是因为原料中的木质素和半纤维素得到了脱除,使得纤维素的孔隙率与比表面积增大,导致样品保水值增大。
此外,两步处理后3种材料的保水值高于p-TsOH处理样品,这主要是由于p-TsOH处理后样品中还含有10%以上的木质素,阻碍了纤维素分子中游离羟基与水分子的结合,从而降低了纤维的润胀程度;而两步处理进一步脱除了样品中的木质素和半纤维素,使得样品保水值进一步增加。3种原料中,杨木原料的两步处理与p-TsOH处理的保水值差异比其他2种材料大,其原因主要是因为p-TsOH处理后,杨木材料中的木质素含量仍然较高,因而其保水值低于另外2种材料;而两步处理后,由于杨木中木质素的大量脱除和纤维素的富集,其保水值明显提高,致使p-TsOH处理与两步处理样品的保水值差异较大。
2.3 纤维素酶添加量对两步处理木质纤维素酶解率的影响
预处理的目的是脱除木质纤维素类生物质中的木质素和半纤维素,降低纤维素的聚合度,提高原料的孔隙率及纤维素对酶的可及性,从而能够用较低的酶量达到较高的酶解率。以两步预处理的芒草秆、小麦秸秆和杨木为纤维素原料,研究纤维素酶添加量对酶解率的影响,结果如图6所示。图6显示,随着纤维素酶添加量的增加和酶解时间的延长,3种材料的酶解率均表现出相似的规律,即酶解前期酶解率迅速增大,之后趋于平稳。3种材料相比,杨木的酶解率相对较低,当纤维素酶添加量为5 FPU/g、酶解72 h时,芒草秆和小麦秸秆的酶解率均超过90%,而杨木的酶解率为78%。当纤维素酶添加量为15 FPU/g、酶解12 h时,芒草秆、小麦秸秆的酶解率均达到100%,而杨木的酶解率为73%。由2.1节内容可知,两步处理杨木的木质素含量比小麦秸秆和芒草秆高,而木质素会对纤维素的酶解产生不利的影响,因而造成杨木的酶解效率低于其他2种材料,这与文献[21]的结果一致。当纤维素酶添加量为10 FPU/g、酶解24 h时,芒草秆、小麦秸秆和杨木的酶解率均达到95%以上。考虑到纤维素酶的成本,故选择纤维素酶添加量为10 FPU/g、处理24 h作为最佳酶解条件。
2.4 不同发酵工艺对乙醇产率的影响
不同发酵工艺对发酵液中的葡萄糖和乙醇质量浓度及乙醇产率的影响如图7所示。
图7显示,2种发酵工艺条件下,发酵初期乙醇质量浓度及产率均随着发酵时间的延长迅速增加,之后趋于稳定。SHF工艺中,发酵初期葡萄糖质量浓度随着发酵时间的延长迅速降低,之后趋于稳定;SSF工艺中,葡萄糖质量浓度随着发酵时间的延长始终维持在较低的水平。SHF工艺中,因为酶解和发酵分开进行,故发酵前12 h,葡萄糖被迅速消耗,其质量浓度迅速降低,乙醇质量浓度迅速上升,此时3种原料乙醇质量浓度及产率均高于SSF发酵工艺;至24 h时,芒草秆、小麦秸秆和杨木3种原料葡萄糖质量浓度已分别降至0.56,0.52和0.41 g/L,乙醇质量浓度分别上升至55,57和45 g/L,说明SHF发酵在24 h时,葡萄糖已基本耗尽,因而此后乙醇质量浓度和产率基本保持不变。SSF工艺中,因为酶解和发酵同时进行,酶解产生的葡萄糖立即被酵母利用,因此在整个发酵过程中,葡萄糖质量浓度始终维持在较低的水平;发酵0~48 h,乙醇质量浓度和产率一直在升高,48 h之后趋于稳定,且乙醇质量浓度及产率均超过了SHF工艺。发酵96 h时,芒草秆、小麦秸秆和杨木SSF发酵的乙醇质量浓度分别为59.5,61.5和51.5 g/L,乙醇产率分别为92.63%,90.07%和88.00%;其SHF发酵的乙醇质量浓度分别为55.5,57.5和45.7 g/L,乙醇产率分别为86.40%,84.21%和78.09%。由此可知,SSF的发酵效果明显优于SHF。
3 讨 论
木质纤维素由于具有复杂致密的结构,故具有很强的顽抗性,木质纤维原料未经预处理时其纤维素酶酶解率通常低于20%,且降解速度非常缓慢,没有应用价值[22],因此必须通过预处理提高其酶解率。传统的酸、碱预处理方法主要通过增加预处理强度来提高处理效率,如提高酸、碱浓度、温度、压力及处理时间,但这些方式均会增加能耗和经济成本,同时造成木质纤维素各有效组分的损失,使其工业化生产受限[23]。近年来,物理、化学及生物方法联合的预处理方法因协同效应明显,且具有处理强度低、效率高的优点,引起了广泛的关注。Gao等[24]采用蒸汽爆破和优化的绿液预处理1年生竹子,可以有效降低木质纤维素的顽抗性,使纤维素完全糖化;Lee等[25]采用超声结合低共熔溶剂的方法预处理油棕榈空果束以强化纤维素的酶解糖化,结果使还原糖产率明显提高,说明超声波与低共熔溶剂具有协同效应。此外,近年来更多的研究聚焦在木质纤维素全组分的资源化利用方面,因此在预处理方法中,除了要考虑纤维素和半纤维素的降解效率外,木质素的易回收性及结构完整性也是评价预处理方法一个关键因素[26]。基于以上几点,理想的预处理策略应具有能耗低、处理方式绿色无污染、各组分易回收且结构完整、稳定等特点。
助水溶剂(hydrotrope,HP)是指一些短链烷基取代的苯甲酸或苯磺酸盐等小分子两亲化合物,其结构类似于表面活性剂,但疏水性较小,具有较好的水溶性。当溶液中的HP浓度超过其临界缔合浓度时,即可以通过分子间非共价键的形式发生自我缔合,形成类似胶束的聚集体,疏水有机物可以通过包裹在这类聚集体内而溶解在水溶液中,从而增加有机物的水溶性;当HP浓度低于最低助溶浓度(minimal hydrotrope concentration,MHC)时,聚集体解聚释放不溶物,从而使不溶物易于回收。p-TsOH除了具有助水溶剂的特性,可以在水溶液中选择性溶解木质素外,由于其具有较强的酸性,还可以选择性溶解半纤维素,在木质纤维素预处理中可以利用其酸性和助水溶性快速、高效、选择性地溶解木质纤维素中的半纤维素和木质素而保留纤维素,并通过稀释助水溶剂使其浓度 ≤ MHC以回收结构稳定的木质素,因而p-TsOH处理是一种极具前景的木质纤维素生物精炼方法[9,27]。研究发现,经过p-TsOH处理的木质纤维素中仍保留有10%以上的木质素和一定量的半纤维素,二者仍是纤维素利用的物理障碍[21],其会对纤维素酶造成无效吸附,降低纤维素对酶的可及性及酶解效率,从而增加纤维素酶的用量,提高生产成本。Ji等[28]采用p-TsOH结合物理超声的方法处理杨木,以促进木质素的提取,提高纤维素的酶解效率及乙醇的产率,最终得到的乙醇质量浓度为40.08 g/L,产率为81.87%。
AHP处理是一种常用的木质纤维素预处理方法,氢氧根离子能催化木质素-半纤维素之间酯键的皂化反应,促进木质素及半纤维素的溶解;此外,过氧化氢作为氧化剂可以降解木质素和半纤维素,提高纤维素对酶的可及性。AHP预处理条件温和,所需碱量较少,常用来处理木质纤维素原料,以脱除木质素及半纤维素,从而获得富含纤维素的原料。但单一AHP处理效率较低且时间长,通常需要24 h以上才能达到较好的效果。苗林平等[29]采用AHP处理小麦秸秆,于30 ℃处理24 h后,木质素脱除率为48.66%,半纤维素脱除率为41.81%,纤维素保留率为89.52%。近年来,很多研究将AHP处理与其他方法相结合,以缩短处理时间,提高处理效率。如徐忠等[30]采用超声波辅助AHP处理玉米皮,在优化条件下,使半纤维素和木质素得到了有效去除,纤维素含量增加至83.34%;Zhang等[31]采用球磨机辅助AHP处理,从玉米秸秆中生产功能性低聚木糖和可发酵糖,在优化条件下,木质素脱除率为84.29%,葡萄糖产率达到68.94%。
本研究选用p-TsOH耦合AHP两步处理,在温和条件下分步脱除芒草秆、小麦秸秆和杨木3种原料中的木质素和半纤维素,得到富含纤维素的原料,其半纤维素脱除率分别为82.50%,84.21%和81.19%,木质素的脱除率分别为97.01%,96.50%和94.01%,纤维素保留率分别为87.97%,87.85%和90.53%,达到了预期目的。Fu等[32]采用AHP处理芒草,于30 ℃处理24 h后,木质素和半纤维素的脱除率分别为70.7%和17%,纤维素保留率为99.8%;Yuan等[33]将小麦秸秆先采用体积分数50%乙醇于160 ℃处理50 min后,再用质量分数11%碳酸钠于75 ℃处理50 min,木质素和半纤维素的脱除率分别为69.3%和74.8%,纤维素保留率为87.3%;周敏姑等[3]采用体积分数1%硫酸协同氯化胆碱/乳酸低共熔溶剂预处理杨木1 h,木质素和半纤维素的脱除率分别为55.3%和90.7%,纤维素保留率为64.6%。与以上研究相比,本研究采用的p-TsOH耦合AHP两步处理可以高效脱除木质纤维素中的半纤维素和木质素而保留纤维素,且处理条件温和,对不同的原料普适性较好,是一种十分有前景的生物质精炼方法。
p-TsOH耦合AHP两步处理对芒草秆、小麦秸秆和杨木3种原料的微观形态、结构、结晶度及保水值也产生了一定的影响。这主要是因为两步法处理后原料中木质素和半纤维素被大量脱除,其致密完整的结构遭到破坏,变得疏松,孔隙度增加,这种变化有利于后续的酶解糖化作用的进行。两步处理方法没有改变3种原料纤维素的晶型,但由于无定形成分的大量脱除,使纤维素的结晶度和保水值得到了提高。预处理后材料的结构表征结果与成分分析结果一致。
4 结 论
1)采用p-TsOH耦合AHP两步处理,在水溶液的温和处理条件下,芒草秆、小麦秸秆和杨木木质纤维素中的木质素和半纤维素的脱除率分别为97.01%和82.50%,96.50%和84.21%,94.01%和81.19%,纤维素的保留率分别为87.97%,87.85%和90.53%,说明该方法可以选择性脱除原料中的木质素和半纤维素,得到富含纤维素的原料,且该方法对不同原料的适用性较好,具有较高的应用价值。
2)当纤维素酶添加量为10 FPU/g、底物质量浓度为130 g/L时,p-TsOH耦合AHP两步处理芒草秆、小麦秸秆和杨木原料采用同步糖化发酵工艺时乙醇质量浓度分别为59.5,61.5和51.5 g/L,乙醇产率分别为92.63%,90.07%和88.00%。
