麦角酸二乙基酰胺人工抗原的制备与初步应用
2022-06-11伍丽贤袁强梁飞敏曹斯婷
伍丽贤,袁强,梁飞敏,曹斯婷
·论著·
麦角酸二乙基酰胺人工抗原的制备与初步应用
伍丽贤,袁强,梁飞敏,曹斯婷
通过化学方法制备麦角酸二乙基酰胺人工抗原并初步应用到胶体金试剂条上。利用碳二亚胺法把化学修饰后的麦角酸二乙基酰胺与载体蛋白连接成为完全抗原,使用质谱法和紫外全波长扫描法验证制备效果,并作为包被原应用于胶体金检测试剂条上。经过 330 例临床样本测试、60 种常用药物交叉反应测试、尿 pH 和尿比重干扰测试,该抗原能与麦角酸二乙基酰胺抗体在胶体金试剂条上表现出良好的特异性与敏感性。其灵敏度在 10 ng/ml,特异性为99.06%,敏感性为100%,可在 5 min 内实现现场尿液快速检测。该方法制备的麦角酸二乙基酰胺人工抗原可用于麦角酸二乙基酰胺胶体金免疫检测方法中。
麦角酸二乙基酰胺; 人工抗原; 胶体金免疫层析法; 现场快速检测
麦角酸二乙基酰胺(lysergic acid diethylamine,LSD),又称麦角二乙酰胺,化学名 9,10-二去氢-N,N-二乙基-6-甲基麦角灵-8β-酰胺,是世界上最强烈的致幻剂之一[1],口服 10 μg 即可产生精神作用[2],服食超过 200 μg 可引致猝死[3-4],属于国家管制的精神药物。1938 年,LSD 由瑞士化学家阿尔伯特·霍夫曼首次制备。因其具有强大的精神活性,20 世纪 50 年代曾作为治疗情绪障碍及成瘾心理治疗辅助剂,60 ~ 80 年代经黑市流入美国地区,成为当地最流行的毒品之一[5-8]。2021年美国国家药物滥用研究所公布数据显示在美国 12 岁以上人群中约有 710 万人在过去一年曾滥用过致幻剂[9]。自 2016 年起新型毒品LSD 在中国悄悄兴起,国内警方已破获数十起 LSD 走私案件。这些被浸迹过 LSD 的药纸带有邮票和纹身花纹,特别受国内 00 后青年吸毒者欢迎,所以也被称之为“邮票”。
LSD 在口服 24 小时内有 13% 代谢为 2-氧代-3-羟基-LSD(O-H-LSD),1% 以原药形式排到尿液中。由于 O-H-LSD 由细胞色素 P450 酶形成,不具有药理学活性,检测仍以样本中的 LSD 原药形式作为 LSD 滥用标志物[10-12]。LSD 是最难检测的毒品之一,原因是当生物样本中的 LSD 暴露于光、热和碱性条件下,极其容易水解[13]。目前尿液中 LSD 的检测方法以 GC-MS/MS 和LC-MS/MS 为主,这种方法虽然灵敏度高,但样本需要经过复杂的前处理并且需要配合大型仪器,所以此类方法只适合于实验室[14-16]。胶体金免疫层析法使用胶体金颗粒作为示踪剂,利用免疫学中抗原抗体能特异性结合的原理,在层析过程中形成肉眼可见条带的一种免疫学检测方法,它具有检测速度快,可肉眼观测结果,操作简便的特点,非常适合现场快速筛查及路边执法[17]。国内外关于胶体金免疫层析法检测尿液中 LSD 的报道较少,本文用化学方法制备 LSD 半抗原,并连接于牛血清白蛋白(BSA)得到 LSD 完全抗原,并将其作为包被原应用于 LSD 胶体金免疫层析试剂中,建立了 LSD 胶体金免疫层析半定量分析方法,可实现 5 min 现场快速检测。
1 材料与方法
1.1 材料
1.1.1 主要仪器设备 XYZ 大平台三维感应划膜喷金仪 HM3260 购自上海金标生物科技有限公司;HGS510-1 喷金标机购自杭州峰航科技有限公司;MCE 1202S-2CCN-0 精密电子天平购自德国Sartorius公司;C-MAG HS7 数显加热恒温磁力搅拌器购自德国 IKA 公司;Milli-Q Advantage A10 超纯水仪购自美国 Millipore 公司;傅立叶变换红外光谱仪Traffinity-1S、液相三重四级杆色谱质谱仪 LCMS-8045 和气相色谱质谱联用仪 GCMS-7890A-5975C 均购自日本岛津公司;气相色谱仪 Clarus 680 购自美国 PerkinElmer 公司;ST16R 高速冷冻离心机和 Nanodrop 2000C 微量紫外-可见分光光度计均购自美国 Thermo Fisher 公司。
1.1.2 主要试剂与耗材 麦角酸二乙酰胺及其同系物等标准品为Cerilliant公司产品;麦角酸二乙基酰胺单克隆抗体为美国Eastcoast Bio 公司产品;牛血清白蛋白为美国Sigma 公司产品;羊抗鼠 IgG购自隆基生物;100 nm 金溶胶溶液为广州万孚生物技术股份有限公司产品;其他试剂均为分析纯;硝酸纤维素膜购自Sartorius 公司;金标结合垫、样品垫、吸水纸及 PVC 底板购自上海杰一生物技术有限公司。
1.2 方法
1.2.1 半抗原的制备 称取麦角酸二乙基酰胺 323 mg(1 mmol)溶于 16 ml 乙腈,甲酸酸化至pH 5.0,分批加入 12 ml 新制 2 mol/L KMnO4溶液,每次 4 ml,室温下密封搅拌反应 15 h。过滤取滤液调pH 至 7.0。用乙酸乙酯洗涤上述滤液 3 次,每次 7 ml。无水硫酸钠干燥有机相后,旋转蒸发得到红棕色油状物,为中间产物 A(295 mg)。
中间产物 A 加入 K2CO3414 mg,TBAB 23 mg,KI 23 mg,4-溴丁酸乙酯 295 mg,12 ml (C2H5)3N,氦气保护下于 50 ℃搅拌反应 20 h。待温度降至室温后加入 20 ml 水,用乙酸乙酯洗涤上述产物3 次,每次 7 ml,无水硫酸钠干燥有机相后,旋转蒸发得到黄色油状物,为化合物 B(234 mg)。
化合物 B 加入 95% 乙醇 12 ml 和饱和 LiOH 6 ml,40 ℃搅拌反应 4 h;冰浴下边搅拌边加入去离子水 10 ml,用 1 mol/L HCl 酸化至pH 3.0,用乙酸乙酯洗涤上述产物 3 次,每次 7 ml,无水硫酸钠干燥有机相后,旋转蒸发得到173 mg 黄色油状物,制备路线如图 1。
1.2.2 全抗原的制备 使用碳二亚胺法把 LSD 半抗原与 BSA 连接。取 0.05 mmol(19 mg)LSD 半抗原溶于 1 ml N,N-二甲基酰胺(DMF)中,分别加入 19 mg EDC和 19 mg NHS,室温搅拌反应4 h,反应液置于 1.5 ml 离心管 10 000 r/min 离心 10 min,取上清液备用。
50 mg BSA 溶于 4 ℃预冷的 4 ml 0.05 mol/L pH 7.4 PBS 中,缓慢滴入上述上清液 0.8 ml,4 ℃反应 4 h,0.01 mol/ml pH 7.4 PBS 透析48 h,分装后冻干备用。
1.2.3 LSD 全抗原的鉴定 采用紫外光谱法鉴定LSD 全抗原制备效果。在 200 ~ 800 nm 范围内,分子中价电子经紫外光或可见光激发,吸收能量后从低能级跃迁到高能级,形成特征吸收光谱,其吸收强度和波长由分子所含生色团和助色团以及共轭情况决定[18-20]。BSA 在 280 nm 处有一个特征吸收峰,因此,可对比同一浓度下的 BSA 与 LSD 全抗原在 280 nm 处紫外光谱特征吸收峰,若 LSD 全抗原在 280 nm 峰值发生平移或叠加,可初步判断 LSD 半抗原已偶联到 BSA 上[21]。
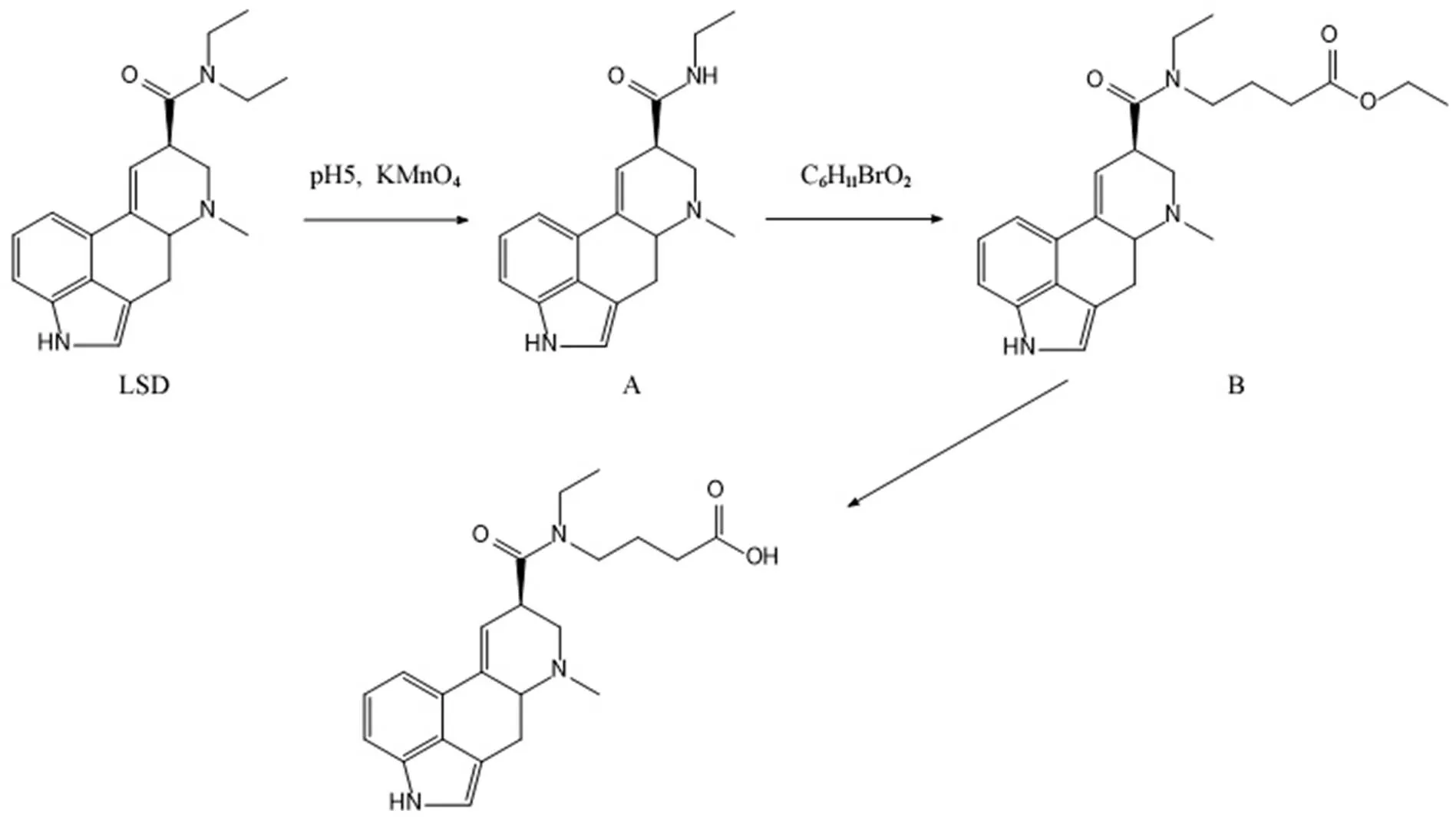
图1 LSD 半抗原制备路线图
Figure 1 Synthetic route of LSD hapten
1.2.4 LSD 胶体金免疫层析试剂条性能评价
1.2.4.1 试剂条的组装 PVC 底板贴上 NC 膜后,LSD 全抗原用 0.01 mol/L pH 7.4 PBS 稀释至0.2 mg/ml,用划膜喷金仪喷于 NC 膜 T 线位置,羊抗鼠IgG 稀释至0.4 mg/ml,喷于 NC 膜C 线位置,50 ℃烘干 24 h。NC 膜 T 线端依次贴上胶体金标记 LSD 抗体的喷金结合垫、样品垫,NC 膜 C 线端贴上吸水垫,裁切成 4.0 mm的试剂条。
1.2.4.2 灵敏度及同系物 cutoff 值的确定 用 LSD 试剂条对阴性尿液及不同浓度的 LSD 尿液进行检测,加样 5 min 后观察 T 线和 C 线位置是否出现紫红色线,若观察到 T 线和 C 线均出现紫红色线,结果为阴性,若只有 C 线显色,T 线不显色,结果为阳性,阳性的最低检出限为该试剂条的cutoff 值。
在阴性尿液中分别加入 LSD 代谢物 2-氧代- 3-羟基-LSD(O-H-LSD)及麦角酸 N,N-甲基丙胺(LAMPA)配置成不同浓度的尿液,用 LSD 试剂条对每个浓度尿液进行检测,加样 5 min 后记录结果,确定试剂条的 O-H-LSD 及LAMPA 检测cutoff 值。
1.2.4.3 抗交叉能力测试 对 60 种常见药物(100 μg/ml)进行检测,测试其抗药物干扰能力。
1.2.4.4 尿液pH 值测试 把阴性尿液、–50% cutoff 及 +50% cutoff 的阳性尿液分别用 0.1 mol/mlNaOH 和 0.1 mol/ml HCl 溶液调pH 至 4.0、5.0、6.0、7.0、8.0、9.0,用 LSD 试剂条分别对以上尿液进行检测,每个尿样做 10 次重复测试,检测其抗尿液pH 干扰能力。
1.2.4.5 尿液比重测试 把 15 份不同尿液比重 SG(范围 1.003 ~ 1.040)的尿样分别配制成–50% cutoff 及 +50% cutoff 的阳性尿液,用 LSD 试剂条分别对以上阴性尿液及配置的–50% cutoff 及 +50% cutoff 的阳性尿液进行检测,每个尿样做10 次重复测试,检测其抗尿比重干扰能力。
1.2.4.6 性能的临床评价 对 330 例经 LC-MS/MS 确证的临床尿液样本进行测试,测试其敏感性与特异性。

2 结果
2.1 LSD 半抗原的鉴定
LSD 半抗原经 ESI-MS 分析(图 2),结构为 4-((9R)-N-乙基-7-甲基-4,6,6a,7,8,9-六氢吲哚[4,3- fg]喹啉-9-甲酰胺)丁酸。
2.2 LSD 全抗原的鉴定
LSD 半抗原、全抗原和 BSA 在 0.5 mg/ml 浓度下的紫外光谱扫描图如图 3 所示,可见 LSD 半抗原、LSD 完全抗原和 BSA 的最大吸收峰值分别在288 nm、282 nm、280 nm,与 BSA 紫外曲线相比,LSD 完全抗原的最大吸收峰发生往右上方红移并带有增色效应,所以可初步判断 LSD 半抗原已成功连到 BSA 上。
2.3 LSD 试剂条性能鉴定
2.3.1 试剂条的灵敏度测试结果 LSD 胶体金试剂条采用的是竞争性免疫层析法,阴性尿液中分别配置成如图 4 所示浓度的 LSD 阳性尿液,用试剂条进行检测,5 min 肉眼观察结果。当 LSD 浓度为 10 ng/ml 时,试剂条 T 线刚好消失,因此可定义该浓度为试剂条的阳性 cutoff 值,检测 +50% cutoff(5 ng/ml)浓度为阳性结果,检测 –50% cutoff(15 ng/ml)浓度T 线有微弱显色,为阴性结果。
同理检出代谢物 O-H-LSD 和同系物 LAMPA 的cutoff 值分别为2000 ng/ml 和 20 ng/ml(图 5)。
2.3.2 试剂条的抗药物干扰测试结果 LSD 试剂条检测 60 种常用药物,结果如表 1所示,均没有交叉情况,特异性良好。
2.3.3 试剂条的抗尿液 pH 干扰结果 LSD 试剂条检测 pH 4.0 ~ 9.0 尿液,检测结果未受尿液 pH 值干扰,未出现假阳性和假阴性结果。
2.3.4 试剂条的抗尿液比重干扰结果 LSD 试剂条检测尿比重 1.003 ~ 1.040 的尿液,检测结果未受尿液比重值干扰,未出现假阳性和假阴性结果。
2.3.5 试剂条性能的临床评价结果 检测 330 例来自圣地亚哥研发中心收集的经定性定量确认的尿液样本(表 2),LSD 试剂条的特异性为99.06%,敏感性为100%,有 2 例临界值样本,这两例样本其 LSD 浓度分别为 8.093 ng/ml、9.214 ng/ml,浓度处于检测 cutoff 值附近,是曾经少量服食过LSD 的吸毒人员样本。
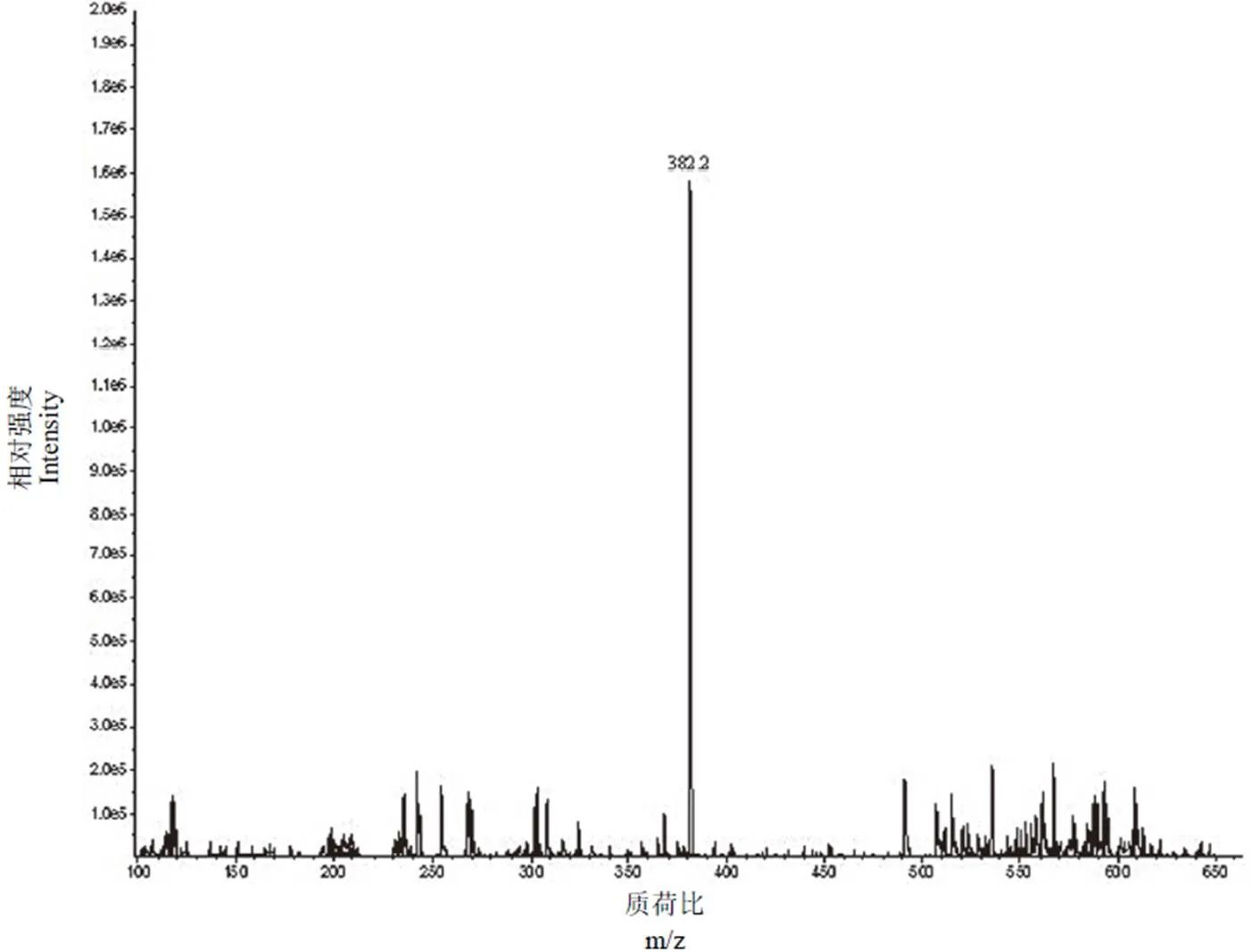
图2 4-((9R)-N-乙基-7-甲基-4,6,6A,7,8,9-六氢吲哚[4,3-FG]喹啉-9-甲酰胺)丁酸 ESI-MS 分析
Figure 2 4-((9R)-N-ethyl-7-methyl-4,6,6A,7,8,9-hexahydroindolo[4,3-FG]quinoline-9-carboxamido)butanoic acid ESI-MS analysis
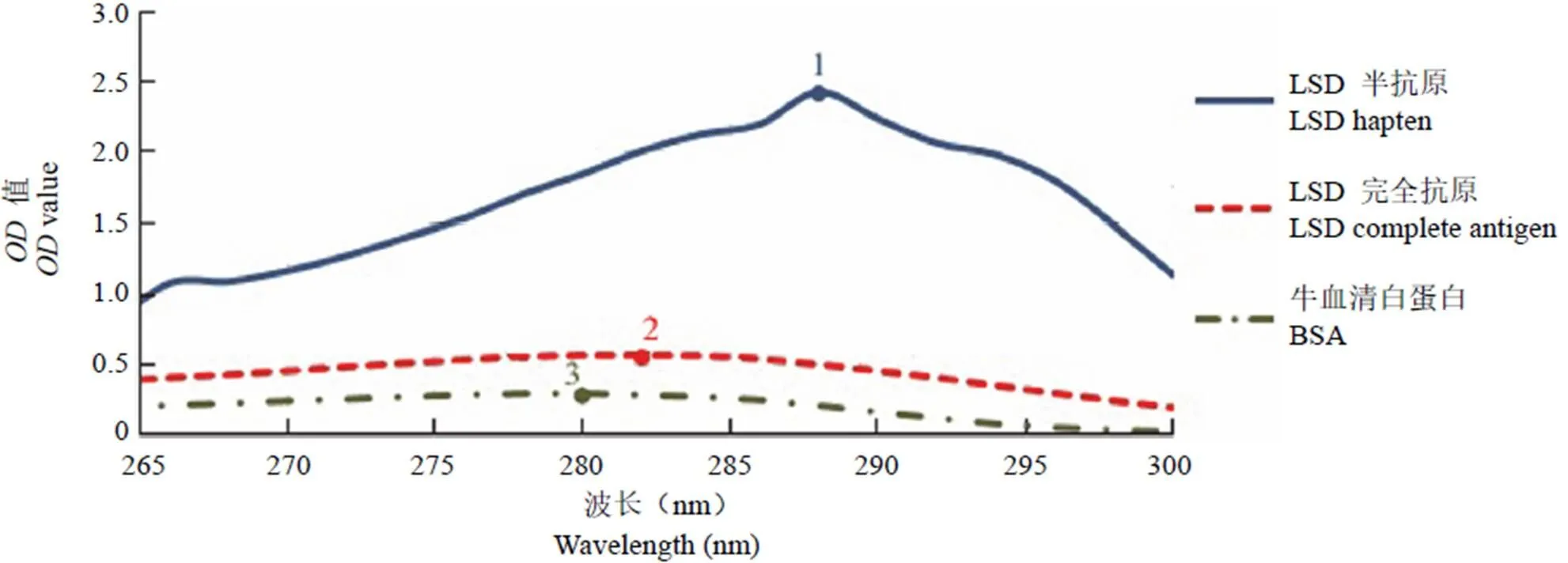
图3 LSD 半抗原、全抗原和 BSA 紫外光谱图[1:LSD 半抗原峰值(288,2.42);2:LSD 完全抗原峰值(282,0.564);3:BSA 峰值(280,0.292)]
Figure 3 Ultraviolet spectra of LSD hapten, complete antigen and BSA [1: Peak of LSD hapten (288, 2.42); 2: Peak of LSD complete antigen (282, 0.564); 3: Peak of BSA (280, 0.292)]

图4 LSD 灵敏度测试结果
Figure 4 Sensitivity test result of LSD reagent strip
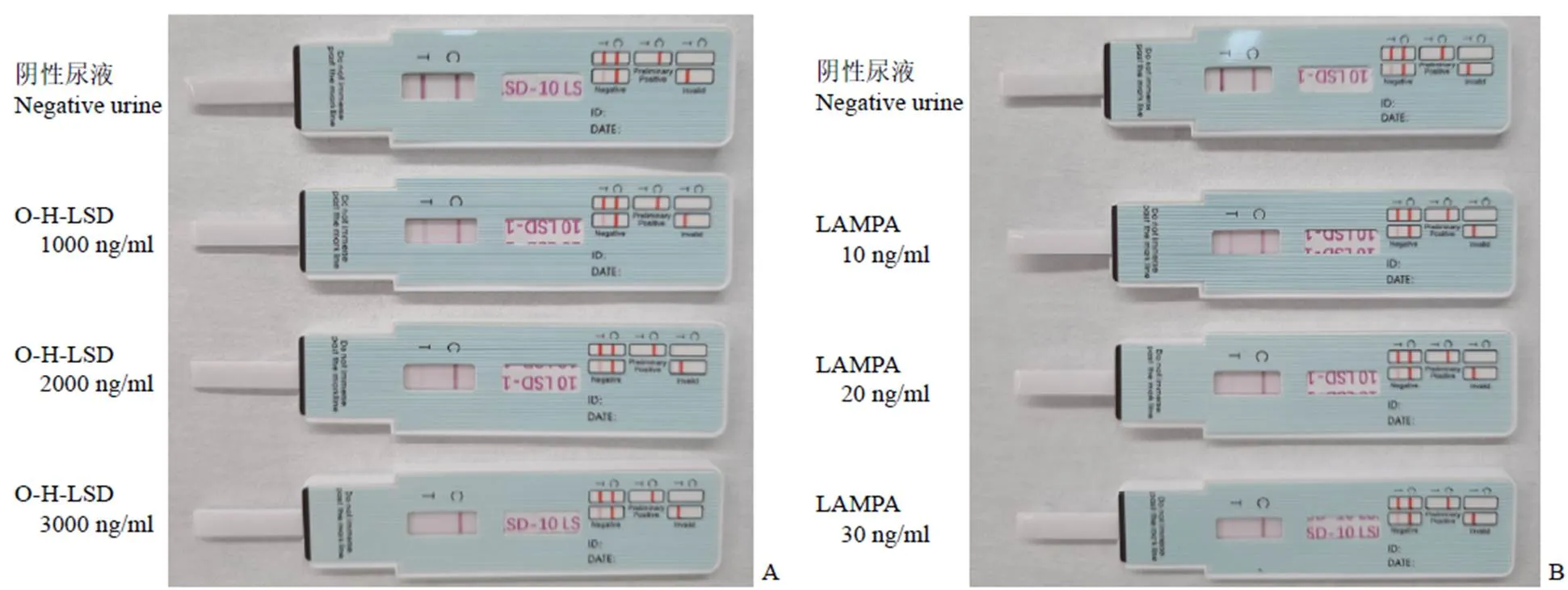
图5 LSD 同系物的检出结果(A:O-H-LSD 不同浓度检测结果;B:LAMPA 不同浓度检测结果)
Figure 5 Test results of LSD homologues (A: Test results of different concentration of O-H-LSD; B: Test results of different concentration of LAMPA)
表1 60种常用药物干扰实验结果
Table 1 Results of cross experiments on commonly used drugs
药名Drugs结果Result药名Drugs结果Result药名Drugs结果Result 阿司匹林 Aspirin-氯雷他定 Loratadine-吗啡 Morphine- 对乙酰氨基酚 Acetaminophen-左炔诺孕酮 Levonorgestrel-盐酸摇头丸 MDMA- 多潘立酮 Domperidone-盐酸伪麻黄碱Pseudoephedrine hydrochloride-盐酸甲基安非他命Methamphetamine hydrochloride- 布洛芬 Ibuprofen-氨茶碱 Aminophylline-甲基苯丙胺 Methylamphetamine- 卡马西平 Carbamazepine-孟鲁司特 Montelukast-咖啡因 Caffeine- 拉莫三嗪 Lamotrigine-福尔可定 Pholcodine-克拉霉素 Clarithromycin- 加巴喷丁 Gabapentin-磷酸可待因 Codeine phosphate-地红霉素 Dirithromycin- 氯硝西泮 Clonazepam-乙酰可待因 Acetyl codeine-阿昔洛韦 Acyclovir- 盐酸氯丙嗪Chlorpromazine hydrochloride-那可丁 Narcotine-利福平 Rifampicin- 氟哌啶醇 Haloperidol-氢溴酸右美沙芬Dextromethorphan hydrobromide-酮康唑 Ketoconazole- 奋乃静 Perphenazine-盐酸麻黄碱 Ephedrine hydrochloride-左氧氟沙星 Levofloxacin- 帕利哌酮 Paliperidone-盐酸普鲁卡因 Procaine hydrochloride-环丙沙星 Ciprofloxacin- 利培酮 Risperidone-盐酸可卡因 Cocaine hydrochloride-青霉素V钾 Penicillin V potassium- 盐酸哌替啶 Pethidine hydrochloride-盐酸利多卡因 Lidocaine hydrochloride-氨苄西林 Ampicillin- 罂粟碱 Papaverine 氯胺酮 Ketamine-阿莫西林 Amoxicillin- 美沙酮 Adanon-硝西泮 Nitrazepam-四环素 Tetracycline- 萘磺酸右丙氧芬Naphthalene sulfonate dextropropoxyphene-奥沙西泮 Oxazepam-头孢克洛 Cefaclor- 盐酸曲马多 Tramadol hydrochloride-巴比妥 Barbital-头孢拉定 Cefradine- 氨酚羟考酮 Oxycodone-盐酸纳洛酮 Naloxone hydrochloride-氢氯噻嗪 Hydrochlorothiazide- 安非他命 Amphetamine-盐酸纳曲酮 Naltrexone hydrochloride-头孢氨苄 Cefalexin-
表2 临床样本测试结果
Table 2 Test results of clinical sample
LSD 胶体金试剂条Colloidal gold reagent strip of LSDLC-MS/MS总数Total results 阳性 Positive阴性 Negative 阳性 Positive120 2122 阴性 Negative 0208208 总数 Total results120210330
3 讨论
抗原抗体材料是构建免疫层析试剂的关键,半抗原分子结构中修饰位点的选择与连接臂长度的设计是影响人工抗原性能的重要因素。LSD 分子量为 267,需经化学修饰接上连接臂才能与大分子载体结合,用于免疫检测方法上。有报道指出,连接臂接入位点的不同会令半抗原的空间结构发生变化,所合成的完全抗原会暴露出不同的抗原决定簇,因此其与抗体结合的亲和力和特异性也是大不相同的[22]。LSD 左侧的杂环结构为 LSD 的特征结构,是较强的抗原决定簇。本研究保留此特征结构,先把 LSD 上二乙酰胺脱去乙基,再接入末端带有羧基的四碳脂肪族碳链连接臂,连接臂的分子量小而结构简单,有效降低因连接臂带来的非特异性结合,并可充分暴露而不被载体蛋白遮挡,从而使 LSD 抗原能更好地与 LSD 抗体结合[23]。
连接臂的碳链长度一般多为 3 ~ 6 个,使用不同碳链长度的连接臂可影响人工抗原的稳定性。本研究中使用 4 个碳的连接臂会比 6 个碳连接臂的 LSD 抗原在 4 ℃环境下溶液的稳定性以及其在 NC 膜上固定干燥后的稳定性更好。原因分析有二:一是当其连接臂较长时,氢键、疏水作用或其他作用力使连接臂折叠而导致半抗原包裹到载体蛋白中,部分抗原决定簇被载体蛋白遮挡而导致抗原部分失效的现象[24];二是连接臂的增长会显著增加半抗原的偶联率[25]。蛋白载体表面连有大量半抗原时,表面的疏水作用增强使 LSD 抗原在保存溶液或包被稀释液中容易发生沉淀析出,从而影响其稳定性。所以在半抗原的修饰设计时,连接臂的碳链长度也是一个关键的考虑因素。
本研究制备的 LSD 人工抗原成功应用于 LSD 免疫胶体金尿液试剂上,结合《中华人民共和国禁毒法》和《戒毒条例》可为缉毒禁毒工作提供快速、准确的判断依据,便于管理机构对吸毒和戒毒人员的长期跟踪及管理。
[1] Nichols DE. Hallucinogens. Pharmacol Ther, 2004, 101(2):131-181.
[2] Holze F, Liechti ME, Hutten NRPW, et al. Pharmacokinetics and pharmacodynamics of lysergic acid diethylamide microdoses in healthy participants. Clin Pharmacol Ther, 2021, 109(3):658-666.
[3] Aakerøy R, Brede WR, Stølen SB, et al.Severe neurological sequelae after a recreational dose of LSD. J Anal Oxicol, 2021, 45(7):e1-e3.
[4] Nichols DE, Grob CS. Is LSD toxic? Forensic Sci Int, 2018, 284: 141-145.
[5] Nichols DE. Dark classics in chemical neuroscience: lysergic acid diethylamide (LSD). ACS Chem Neurosci, 2018, 9(10):2331-2343.
[6] Begola MJ, Schillerstrom JE. Hallucinogens and their therapeutic use: a literature review. J Psychiatry Clin Pract, 2019, 25(5):334-346.
[7] Fuentes JJ, Fonseca F, Elices M, et al. Therapeutic use of LSD in psychiatry: a systematic review of randomized-controlled clinical trials. Front Psychiatry, 2020, 10:943.
[8] Li ZX. Lessons learned from the abuse of LSD in the United States in the 20th century: implications for the control of new psychoactive substances (NPS) in China. J Yunnan Police Coll, 2019, (3):7-11. (in Chinese)
李振辛.二十世纪美国LSD的滥用经验教训对我国新精神活性物质(NPS)管控的启示. 云南警官学院学报, 2019, (3):7-11.
[9] National Institute on Drug Abuse. Hallucinogens and dissociative drugs research report. (2015-02) [2022-05-20]. https://nida.nih.gov/ download/1199/hallucinogens-dissociative-drugs-research-report.pdf?v=2076fc6330f762e0da6767921f96d6ce.
[10] Dolder PC, Schmid Y, Steuer AE, et al. Pharmacokinetics and pharmacodynamics of lysergic acid diethylamide in healthy subjects. Clin Pharmacokinet, 2017, 56(10):1219-1230.
[11] Marta RFLO. Metabolism of lysergic acid diethylamide (LSD): an update. Drug Metab Rev, 2019, 51(3):378-387.
[12] Luethi D, Hoener MC, Krähenbühl S, et al. Cytochrome P450 enzymes contribute to the metabolism of LSD to nor-LSD and 2-oxo-3-hydroxy-LSD: Implications for clinical LSD use. Biochem Pharmacol, 2019, 164:129-138.
[13] Baselt R. Disposition of toxic drugs and chemicals in man. 8th ed. Foster City, CA: Biomedical Publications, 2008:871-874.
[14] Tanaka R, Maiko K, Takashi H, et al. Identification and analysis of lsd derivatives in illegal products as paper sheet. Yakugaku Zasshi, 2020, 140(5):739-750.
[15] Tang S, Li CX, Zhang YG. Advances in determination of LSD and its metabolites in physiological specimens. Chin J Forensic Sci, 2020, (4):31-38. (in Chinese)
汤珊, 李春晓, 张运阁. 生物样品中麦角酰二乙胺检测方法研究进展. 中国司法鉴定, 2020, (4):31-38.
[16] Jiang HP. The analytical research of lysergic acid diethylamide and the metabolite in the urine. J Sichuan Police Coll, 2006, 18(5):56-59. (in Chinese)
蒋和平. 论尿液中麦角酰二乙胺及其代谢物的分析研究. 四川警官高等专科学校学报, 2006, 18(5):56-59.
[17] Xu JL, Liu BB, Wang YL, et al. Lateral flow assay for determination of tebuconazole in agricultural products. Chin J Anal Chem, 2019, 47(11):1823-1831. (in Chinese)
许俊丽, 刘贝贝, 王玉龙, 等. 胶体金免疫层析试纸法检测农产品中戊唑醇残留. 分析化学, 2019, 47(11):1823-1831.
[18] Cao HH. Application of ultraviolet spectroscopy in structural analysis of compounds. Inner Mongolia Petrochemical Industry, 2013, (8):34-36. (in Chinese)
曹海华. 紫外光谱在化合物结构分析中的应用. 内蒙古石油化工, 2013, (8):34-36.
[19] Zhou J, Jin WJ, Du LM. Study of derivatization reaction of sparfloxacin and its UV spectrum. J Anal Sci, 2002, 18(6):472-474. (in Chinese)
周静, 晋卫军, 杜黎明. 司帕沙星衍生化反应及其紫外光谱性质研究. 分析科学学报, 2002, 18(6):472-474.
[20] Zhang FR, Ma H, Chen L, et al.Interference effects of determination of gastrodin in geb using UV spectra. Guangzhou Chem Industry, 2015, 43(15):131-133.
[21] Yang AG, Mao JF, Yao LB.Experimental techniques in biochemistry and molecular biology. Beijing: Higher Education Press, 2001: 250-251. (in Chinese)
杨安钢, 毛积芳, 药立波. 生物化学与分子生物学实验技术. 北京: 高等教育出版社, 2001:250-251.
[22] Kim YJ, Cho YA, Lee HS, et al. Investigation of the effect of hapten heterology on immunoassay sensitivity and development of an enzyme-linked immunosorbent assay for the organophosphorus insecticide fenthion. Anal Chim Acta, 2003, 494(1-2):29-40.
[23] Yin XM, Wang XL, Yu HT. Synthesis and identification of hapten and artificial antigen of free thyroxine. Chin J Anal Chem, 2013, 41(6): 936-939. (in Chinese)
印晓梅, 王小龙, 于海涛. 游离甲状腺素半抗原及人工抗原的合成及鉴定. 分析化学, 2013, 41(6):936-939.
[24] Song J, Wang RM, Wang YQ, et al.Hapten design, modification and preparation of artificial antigens. Chin J Anal Chem, 2010, 38(8): 1211-1218. (in Chinese)
宋娟, 王榕妹, 王悦秋, 等. 半抗原的设计、修饰及人工抗原的制备. 分析化学, 2010, 38(8):1211-1218.
[25] Shi HY, Wang MH. Effect of hapten space arm length on immune recognition. Chin J Pesticide Sci, 2008, 10(2):172-177. (in Chinese)
施海燕, 王鸣华. 半抗原的间隔臂长度对免疫识别的影响. 农药学学报, 2008, 10(2):172-177.
Synthesis and application of artificial lysergic acid diethylamine antigen
WU Li-xian, YUAN Qiang, LIANG Fei-min, CAO Si-ting
We aim to synthesize an artificial lysergic acid diethylamine (LSD) antigen by chemical method and apply it to colloidal gold reagent strip.Carbodimide method was used to link chemically modified lysergic acid diethylamine with carrier protein to form complete antigen. The synthesis effectwas verified by electrospray mass spectrometry and UV full-wavelength scanning, and the complete lysergic acid diethylamine antigen was used as a coating on the reagent strip for colloidal gold detection.Data of 330 clinical sample tests and 60 common drug cross-reaction tests, anti-urine pH and anti-urine specific gravity interference tests revealed that the antigen could show good specificity and sensitivity with LSD antibody on colloidal gold reagent strip.The artificial antigen synthesized by this chemical method can be used in the colloidal gold immunoassay of LSD, which can enable rapid point-of-care testing of urine samples within 5 minutes, with the sensitivity of 10 ng/ml, the specificity of 99.06% and the sensitivity of 100%.
lysergic acid diethylamine; artificial antigen; colloidal gold immunochromatography; point-of-care test
National Local Joint Engineering Laboratory for Self Inspection Rapid Diagnosis, Guangzhou Wondfo Biotech Co., Ltd, Guangzhou 510663, China
WU Li-xian, Email: lillian7040@126.com
10.3969/j.issn.1673-713X.2022.03.003
510663 广州万孚生物技术股份有限公司自检型快速诊断国家地方联合工程实验室
伍丽贤,Email:lillian7040@126.com
2021-12-02
