HPLC 法测定替格瑞洛原料药和替格瑞洛片的含量
2022-06-08蔡丽朋周琪
蔡丽朋,周琪
江西青峰药业有限公司,江西 赣州 341000
替格瑞洛是英国阿斯利康(Astra Zeneca)公司研发的一种新型选择性小分子抗凝血药物[1],与阿司匹林合用治疗急性冠状动脉综合征(ACS),降低心肌梗死和卒中的发生率[2],相比已有的小分子抗凝血药物更安全[3]。江西青峰药业有限公司研发生产的替格瑞洛原料药及片剂需要控制13个杂质,含量测定方法需要考虑替格瑞洛与这13个杂质的分离。文献[4]提到了替格瑞洛原料药含量测定的方法,但是其方法仅考虑了替格瑞洛与两个杂质之间的分离度,方法适用性差。本研究建立了同时适用于替格瑞洛原料药与替格瑞洛片含量测定的方法,并参照《中国药典》2020 年版四部通则9101[5]和人用药品注册技术要求国际协调会(ICH)Q2[6]要求进行了方法学验证,为产品的质量控制提供有效的手段。
1 仪器与材料
1.1 仪器
XS105DU 型电子天平(瑞典Mettler Toledo 公司);KQ-300DE 型台式数控超声波清洗器(东莞市科桥超声波设备有限公司);Waters e2695-2489型高效液相色谱仪(美国Waters 公司)。
1.2 试药
替格瑞洛对照品[江西青峰药业有限公司(以下简称自制),含量99.6%];替格瑞洛原料药(自制,含量99.8%);替格瑞洛片(自制,规格:90 mg,含量97.0%);杂质A 对照品(自制,含量99.32%);杂质B 对照品(自制,含量98.85%);杂质C 对照品(自制,含量98.84%);杂质D 对照品(自制,含量98.86%);杂质E 对照品(自制,含量99.36%);杂质F 对照品(自制,含量98.69%);杂质G 对照品(自制,含量97.73%);杂质H 对照品(自制,含量98.93%);杂质I 对照品(自制,含量98.77%);杂质J 对照品(自制,含量99.07%);杂质K 对照品(自制,含量99.58%);杂质L 对照品(烟台普里医药技术有限公司,含量99.69%);杂质M 对照品(自制,含量98.65%);乙腈为色谱纯,磷酸二氢钠一水合物,磷酸二氢钠二水合物,磷酸等其他试剂均为分析纯。
2 方法与结果
2.1 色谱条件
磷酸盐缓冲液配制:称取磷酸二氢钠一水合物138 g 或磷酸二氢钠二水合物156 g,加水1 000 mL溶解,用稀磷酸调pH 值至3.0,得1.0 mol/L 的磷酸二氢钠溶液;取1.0 mol/L 磷酸二氢钠溶液10 mL,加水至480 mL,摇匀。色谱柱为Aglient Zorbax SB C18 mm(150 mm×4.6 mm,1.8 μm),流动相A:乙腈,流动相B:磷酸盐缓冲液,梯度洗脱;流速:1.0 mL/min;柱温:55 ℃;检测波长:242 nm;进样体积:5 μL。梯度洗脱表见表1。

表1 梯度洗脱表
2.2 溶液配制
(1)空白溶剂:35%乙腈。(2)原料药供试品溶液配制:取替格瑞洛原料药适量,精密称定,加空白溶剂溶解并定量稀释制成每1 mL 含替格瑞洛0.5 mg 的溶液。(3)片剂供试品溶液配制:取替格瑞洛片5 片,置100 mL 量瓶中,加空白溶剂约50 mL,超声15 min,放冷,用空白溶剂稀释至刻度,摇匀,过滤,取续滤液1.0 mL 置10 mL 量瓶中,用空白溶剂稀释至刻度,摇匀。(4)替格瑞洛片空白辅料溶液配制:取处方量的空白辅料1 050 mg,置100 mL 量瓶中,其余操作同替格瑞洛片供试品溶液配制。(5)对照品溶液配制:取替格瑞洛对照品适量,精密称定,加空白溶剂溶解并定量稀释制成每1 mL含替格瑞洛0.5 mg 的溶液。(6)系统适用性溶液配制:取替格瑞洛有关物质方法项下控制的杂质A、杂质B、杂质C、杂质D、杂质E、杂质F、杂质G、杂质H、杂质I、杂质J、杂质K、杂质L、杂质M对照品,替格瑞洛对照品各适量,精密称定,加空白溶剂溶解并逐步定量稀释制成每1 mL 含杂质A至杂质M 各0.75 μg,替格瑞洛0.5 mg 的溶液。
2.3 专属性
分别进样空白辅料溶液、替格瑞洛对照品溶液、替格瑞洛原料药供试品溶液、替格瑞洛片供试品溶液色谱图及系统适用性实验考查,各溶液色谱图见图1~5。
图1 空白辅料溶液色谱图
从图中可知,空白辅料溶液、有关物质项下控制的杂质A~杂质M 不干扰替格瑞洛的测定,替格瑞洛的保留时间为6.232 min,最小分离度为3.4,系统适用性良好,专属性强。
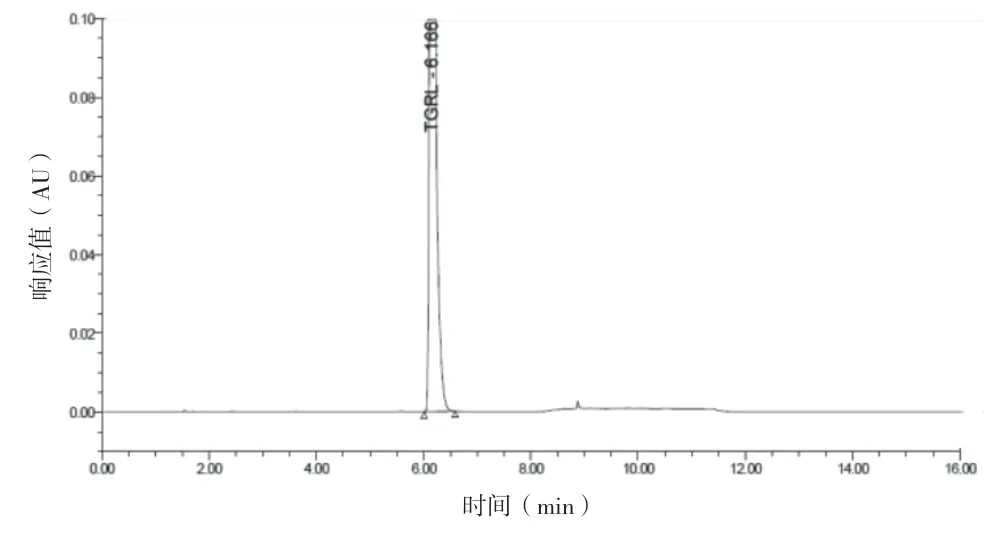
图2 替格瑞洛对照品溶液色谱图

图3 原料药供试品溶液色谱图

图4 片剂供试品溶液色谱图

图5 系统适用性溶液色谱图
2.4 精密度试验
取对照品溶液,依法连续进样6 次,替格瑞洛的保留时间RSD 为0.04%,峰面积RSD 为0.11%。结果表明仪器进样精密度良好。
2.5 线性与范围
取替格瑞洛对照品适量,精密称定,加空白溶剂溶解并稀释成系列标准溶液,按“2.1”项下色谱条件测定,结果在101.417~811.334 μg/mL 浓度范围内,峰面积(A)与替格瑞洛浓度(C)有良好的线性关系,回归方程为A=5 907.6C+28 789,r=0.999 9。
2.6 重复性试验
2.6.1 原料药的重复性试验由实验员A 配制6 份供试品溶液,依“2.1”项下色谱方法测定;由实验员B 在不同的时间配制6 份供试品溶液,采用不同的仪器,依“2.1”项下色谱方法测定,比较12 份样品的检测结果:实验人员A 测定6 份供试品溶液含量均值为100.2%,RSD 为0.48%;实验人员B 测定6 份供试品溶液含量均值为99.5%,RSD 为0.18%;12 份供试品溶液含量RSD 为0.44%。
2.6.2 片剂的重复性试验由实验员A 配制6 份供试品溶液,依“2.1”项下色谱方法测定;由实验员B 在不同的时间配制6 份供试品溶液,采用不同的仪器,依“2.3”项下色谱方法测定,比较12 份样品的检测结果:实验人员A 测定6 份供试品溶液含量均值为97.0%,RSD 为0.35%;实验人员B 测定6 份供试品溶液含量均值为97.6%,RSD 为0.42%;12 份供试品溶液含量RSD 为0.48%。
2.7 回收率试验
2.7.1 原料药回收率取替格瑞洛对照品适量,精密称定,配制成进样浓度80%、100%、120%的3 种浓度的样品溶液,每个浓度平行3 份,依法进样检测,9份供试品溶液的平均回收率为99.9%,RSD为0.89%。
2.7.2 片剂回收率取替格瑞洛对照品适量和处方量的辅料,精密称定,配制成进样浓度80%、100%、120%的3 种浓度的样品溶液,每个浓度各3 份,依法进样检测,9 份供试品溶液的平均回收率为100.3%,RSD 为0.41%。
2.8 溶液稳定性
依法配制原料药供试品溶液、片剂供试品溶液与对照品溶液,分别于0 h、2 h、4 h、12 h、24 h、32 h、40 h、48 h 进样,考察稳定性。对照品溶液在48 h 内,主峰峰面积RSD 为1.10%,保留时间RSD 为0.68%;原料药供试品溶液在48 h 内,主峰峰面积RSD 为1.24%,保留时间RSD 为0.69%;片供试品溶液在48 h 内,主峰峰面积RSD 为0.68%,保留时间RSD 为0.10%。结果表明原料药供试品溶液、片剂供试品溶液及对照品溶液在室温条件下放置,至少48 h 内稳定。
2.9 耐用性
依法配制空白溶剂、空白辅料溶液、原料药供试品溶液、片剂供试品溶液、对照品溶液及系统适用性溶液,微小改变色谱条件,依法检测,考察方法耐用性。各个测试条件下,空白溶剂、空白辅料及有关物质项下控制的其他杂质对替格瑞洛检测均无干扰,结果见表2。
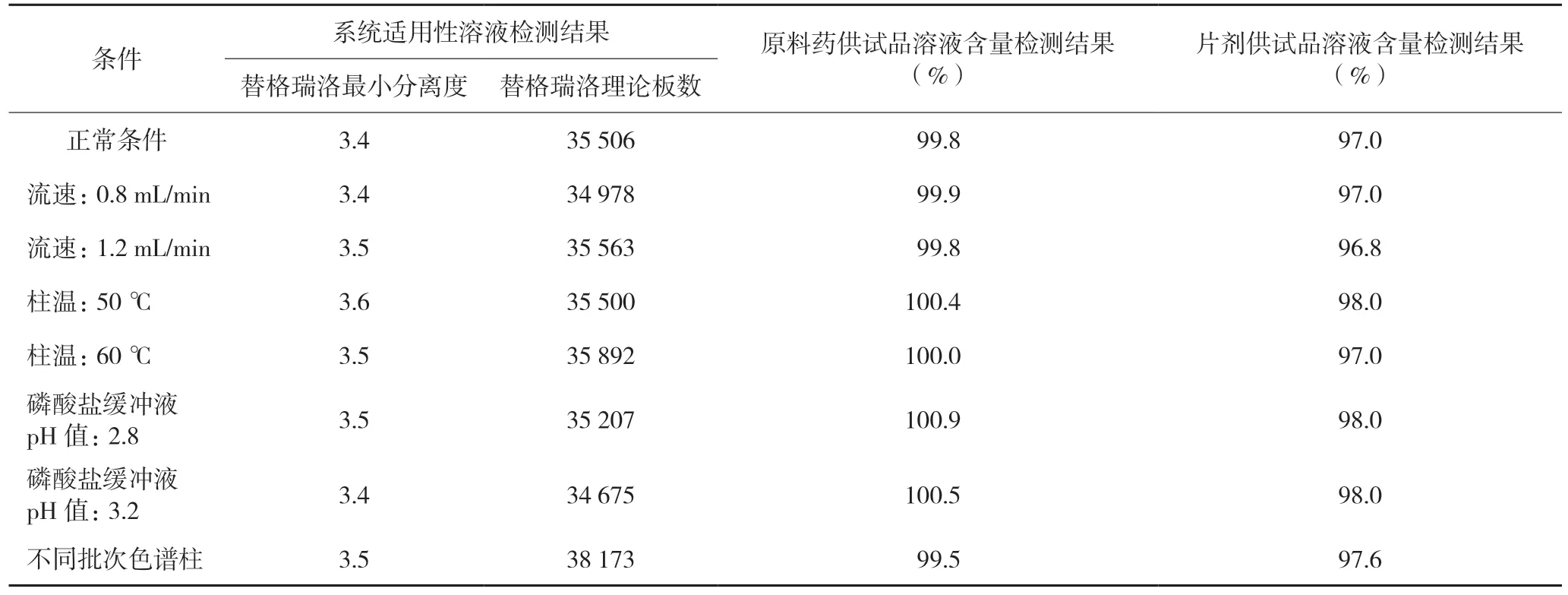
表2 耐用性考察结果
结果表明:微小改变流速、柱温、流动相水相pH 值及使用不同批次色谱柱,不会对检测结果造成影响,方法的耐用性良好。
2.10 样品测定
分别取替格瑞洛原料药和替格瑞洛片,按“2.2”项下分别配制供试品溶液,依“2.1”项下色谱条件测定。计算结果见表3。

表3 样品的测定结果
3 结论
本研究建立了同时适用于替格瑞洛原料药与替格瑞洛片含量测定的方法,本法精密度好,准确度高、分析时间短、稳定性良好,能够同时满足替格瑞洛原料药和替格瑞洛片商业化生产中替格瑞洛含量的检测要求,以便更好地控制产品的质量。
